【2026版三维高考设计高中化学人教版培优课时训练word电子版第47讲沉淀溶解平衡
 47讲沉淀溶解平衡
47讲沉淀溶解平衡
一、选择题(本题包括9小题,每小题只有一个选项符合题意)
1.牙齿表面存在如下平衡:Ca5(PO4)3OH(s)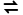 5C
5C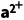 (aq)+3P
(aq)+3P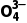 (aq)+OH-(aq)Ksp=6.8×10-37,Ca5(PO4)3F的Ksp=2.8×10-61。下列说法错误的是()
(aq)+OH-(aq)Ksp=6.8×10-37,Ca5(PO4)3F的Ksp=2.8×10-61。下列说法错误的是()
A.在牙膏中添加适量的磷酸盐,能起到保护牙齿的作用
B.口腔中的食物残渣能产生有机酸,容易导致龋齿,使Ksp增大
C.正常口腔的pH接近中性,有利于牙齿健康
D.使用含氟牙膏,当Ca5(PO4)3OH(s)与Ca5(PO4)3F(s)共存时,≈2.4×1024
2.下列有关BaSO3沉淀溶解平衡的说法中错误的是()
A.BaSO3的溶度积常数表达式Ksp(BaSO3)=c(Ba2+)·c(S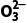 )
)
B.BaSO3难溶于水,溶液中没有Ba2+和S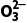
C.升高温度,BaSO3的溶解度增大
D.向BaSO3悬浊液中加入Na2SO3固体,BaSO3溶解的量减少
3.探究Mg(OH)2的沉淀溶解平衡时,利用下表三种试剂进行实验,下列说法不正确的是()
|
编号 |
① |
② |
③ |
|
分散质 |
Mg(OH)2 |
HCl |
NH4Cl |
|
备注 |
悬浊液 |
1 mol·L-1 |
1 mol·L-1 |
A.向①中滴加几滴酚酞溶液后,溶液显红色,说明Mg(OH)2是一种弱电解质
B.为了使悬浊液中Mg(OH)2溶解得更快,加入过量NH4Cl浓溶液并充分振荡,效果更好
C.①、③混合后发生反应:Mg(OH)2(s)+2N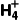 (aq)
(aq)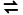 M
M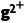 (aq)+2NH3·H2O(aq)
(aq)+2NH3·H2O(aq)
D.向少量Mg(HCO3)2溶液中加入足量NaOH溶液,反应的离子方程式是M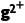 +2HC
+2HC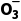 +4OH-
+4OH- Mg(OH)2↓+2C
Mg(OH)2↓+2C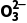 +2H2O
+2H2O
4.(2024·信阳模拟)已知Ksp(CaSO4)=5×10-5,Ksp(CaCO3)=3×10-9。按下列图示进行实验,下列说法正确的是()
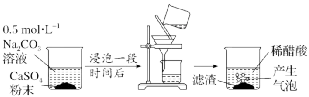
A.0.5 mol·L-1 Na2CO3溶液中存在:c(OH-)-c(H+)=c(HC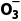 )+c(H2CO3)
)+c(H2CO3)
B.反应CaSO4+C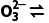 CaCO3+S
CaCO3+S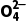 正向进行,需满足
正向进行,需满足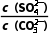 >
>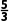 ×104
×104
C.过滤后所得清液中一定存在:c(Ca2+)=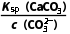
D.滤渣中加入醋酸发生反应的离子方程式:CaCO3+2H+ Ca2++CO2↑+H2O
Ca2++CO2↑+H2O
5.(2024·柳州模拟)下表是五种银盐的溶度积常数(25 ℃):
|
化学式 |
AgCl |
Ag2SO4 |
Ag2S |
AgBr |
AgI |
|
溶度积 |
1.8×10-10 |
1.4×10-5 |
6.3×10-50 |
7.7×10-13 |
8.51×10-16 |
下列说法错误的是()
A.因AgI难溶于水,故其为弱电解质
B.五种物质在常温下溶解度最小的是Ag2S
C.在c(Cl-)=c(Br-)=c(I-)=0.01 mol·L-1的混合溶液中,逐滴滴加硝酸银溶液,依次产生AgI、AgBr、AgCl沉淀
D.AgCl沉淀中加入NaBr溶液,可能会转化为AgBr沉淀
6.已知室温时Ksp(CaCO3)=3.36×10-9,Ksp(CaF2)=3.45×10-11。下列关于CaCO3和CaF2两悬浊液说法错误的是()
A.CaCO3和CaF2两悬浊液中,前者的c(Ca2+)较小
B.分别滴加稀硫酸,CaCO3与CaF2的溶度积常数均增大
C.分别加入0.1 mol·L-1的CaCl2溶液,c(C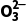 )和c(F-)均减小
)和c(F-)均减小
D.CaCO3和CaF2共存的饱和溶液中,的值约为97.4
7.(2024·佛山模拟)探究Mg(OH)2沉淀溶解平衡的形成及移动情况,实验过程中溶液pH变化情况如图所示。下列说法错误的是()
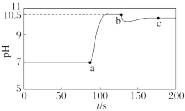
A.a点表示蒸馏水中加入过量Mg(OH)2固体
B.加入少量蒸馏水,可实现b~c段变化
C.饱和Mg(OH)2溶液中,c(OH-)=10-3.5 mol·L-1
D.常用Mg(OH)2处理废水中的Cu2+,可推测Ksp[Mg(OH)2]>Ksp[Cu(OH)2]
8.(2024·台州模拟)已知:(ⅰ)2Cu2++4I-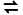 2CuI↓+I2;
2CuI↓+I2;
(ⅱ)CuI为白色沉淀,CuOH为橙色沉淀,Ksp[Cu(OH)2]=10-19.66。
现进行如下实验:
①将0.2 mol·L-1 CuSO4溶液与0.4 mol·L-1 KI溶液等体积混合,充分反应后过滤,测得滤液pH=2;
②向滤液中滴加1滴稀NaOH溶液,出现白色沉淀;
③继续滴加NaOH溶液,数滴后又出现蓝色沉淀。
对该实验的解释不正确的是()
A.①充分反应后可观察到白色沉淀和棕黄色溶液
B.②中未生成蓝色沉淀,说明Ksp[Cu(OH)2]>Ksp(CuI)
C.③中出现蓝色沉淀时,反应(ⅰ)中的平衡可能逆向移动
D.无论②还是③,随着NaOH溶液的加入,c(I2)始终降低
9.分析化学中以K2CrO4为指示剂,用AgNO3标准溶液滴定溶液中的Cl-,测定c(Cl-)。
已知:ⅰ.K2CrO4溶液中存在平衡:2Cr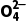 +2H+
+2H+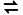 Cr2
Cr2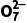 +H2O;
+H2O;
ⅱ.25 ℃时,Ksp(Ag2CrO4)=2.0×10-12(砖红色),Ksp(AgCl)=1.8×10-10(白色)。
下列分析不正确的是()
A.实验中先产生白色沉淀,滴定终点时产生砖红色沉淀
B.产生白色沉淀时,存在AgCl(s)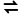 Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)
C.当产生砖红色沉淀时,如果c(Cr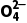 )=5.0×10-3 mol·L-1,Cl-已沉淀完全
)=5.0×10-3 mol·L-1,Cl-已沉淀完全
D.滴定时应控制溶液pH在合适范围内,若pH过低,会导致测定结果偏低
二、非选择题(本题包括2小题)
10.我国《生活饮用水卫生标准》中规定生活用水中镉的排放量不超过0.005 mg·L-1。处理含镉废水可采用化学沉淀法。
(1)写出磷酸镉[Cd3(PO4)2]沉淀溶解平衡常数的表达式:Ksp[Cd3(PO4)2]=。
(2)一定温度下,CdCO3的Ksp=4.0×10-12,Cd(OH)2的Ksp=3.2×10-14,该温度下[填“CdCO3”或“Cd(OH)2”]的饱和溶液中Cd2+浓度较大。
(3)向某含镉废水中加入Na2S,当S2-浓度达到7.9×10-8 mol·L-1时,废水中Cd2+的浓度为mol·L-1[已知Ksp(CdS)=7.9×10-27],此时(填“符合”或“不符合”)《生活饮用水卫生标准》。
(4)要将等体积的4×10-3 mol·L-1的AgNO3溶液和4×10-3 mol·L-1的K2CrO4溶液混合,是否能析出Ag2CrO4沉淀[列式计算,不考虑溶液体积的变化,已知Ksp(Ag2CrO4)=2×10-12]。
11.(1)向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时溶液中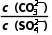 =(结果保留两位有效数字)。已知Ksp(BaCO3)=2.6×10-9,Ksp(BaSO4)=1.1×10-10。
=(结果保留两位有效数字)。已知Ksp(BaCO3)=2.6×10-9,Ksp(BaSO4)=1.1×10-10。
(2)若FeCl2与MgCl2混合溶液中c(Mg2+)=0.02 mol·L-1,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1.0×10-5 mol·L-1,此时是否有Mg3(PO4)2沉淀生成?
。
[列式计算,FePO4、Mg3(PO4)2的Ksp分别为1.3×10-22、1.0×10-24]。
(3)已知:Sn与Si同族,25 ℃时相关的溶度积见表。
|
化学式 |
Sn(OH)4(或SnO2·2H2O) |
Fe(OH)3 |
Cu(OH)2 |
|
溶度积 |
1.0×10-56 |
4×10-38 |
2.5×10-20 |
①滤液中Fe3+和Cu2+的浓度相近,加入NaOH溶液,先得到的沉淀是。②25 ℃时,为了使Cu2+沉淀完全,需调节溶液H+浓度不大于mol·L-1。
通过网盘分享的文件:word讲义
链接: https://pan.baidu.com/s/136tUpK67Q1V3PV2VsUIuPw?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风




