作为临床医生或科研人员,你是否也曾被以下场景困扰:
面对一份 NGS(二代测序)报告中满屏的 VUS(临床意义未明变异),翻遍数据库也找不到确凿证据? 面对入排标准复杂如“天书”的临床试验,只能眼睁睁看着潜在符合条件的患者流失? 面对堆积如山的影像、病理和电子病历数据,感叹人类的大脑已无法处理这种“多模态”的复杂关联?
2026 年 2 月,精准肿瘤学领域的重量级综述 《生成式人工智能在精准肿瘤学中的应用:安全性、治理与意义》正式发表于 Journal of Hematology & Oncology。
这篇文章由日本国立癌症研究中心(National Cancer Center)的 Ryuji Hamamoto 教授团队领衔,联合多家顶尖机构撰写。它不仅梳理了 AI 的演进史,更犀利地指出了 GenAI(生成式人工智能)如何作为“数字辅助者”,桥接文献、指南、临床试验与个体数据,将精准肿瘤学从“靶向药 × 单一生物标志物”推向 “学习型肿瘤学(Learning Oncology)” 的新范式。
机制进化:从“死记硬背”到“开卷考试”
要理解生成式 AI,我们先要跳出传统算法的“回归方程”。
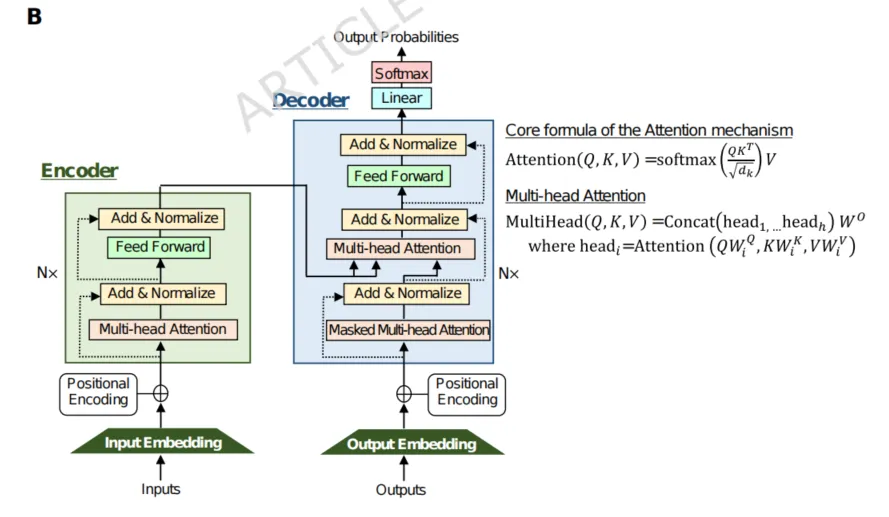
如果说早期的 RBM(受限玻尔兹曼机) 或 DBN(深度信念网络) 是在试图摸索数据的底层概率分布(像是在黑盒里摸象),那么 2017 年诞生的 Transformer 架构则彻底改变了游戏规则。
1. 为什么是 Transformer?
Transformer 引入了 Self-Attention(自注意力机制)。简单来说,它不再死记硬背,而是学会了理解上下文。在分析基因序列或临床病历时,它能自动识别哪些词或哪些变异位点是“关键点”。
2. RAG:给 AI 配一个“数字图书馆”
大家最担心的 AI 问题就是 Hallucination(幻觉)——它会一本正经地编造不存在的指南。为了解决这个问题,综述提出了 RAG(检索增强生成) 架构。
传统模型:靠训练时的记忆回答(类似闭卷考试,知识会过时)。 RAG 架构:在回答前,先去权威数据库(如 PubMed, OncoKB, CIVIC)里检索最新的证据,再结合这些证据生成回答(类似开卷考试,有据可查)。
[Transformer 架构示意图]解读:展示自注意力机制如何处理输入序列,这是目前 GPT, Gemini 等大模型的核心灵魂。
诊疗标准现状:传统精准医疗 vs. AI 增强模式
精准医疗发展二十载,我们正处于一个十字路口。下表总结了当前临床实践与 AI 介入后的变革对比:
| 变异解读 | RAG 驱动 | |
| 临床试验匹配 | TrialGPT | |
| 报告撰写 | VLM(视觉语言模型) | |
| 数据利用 | Ambient AI | |
| 决策逻辑 | 学习型肿瘤学 |
突破与变革:三大核心轴心的“范式转移”
综述明确指出,生成式 AI 在精准肿瘤学中有三大“杀手锏”级应用场景:
1. 基因变异的“深度翻译官”
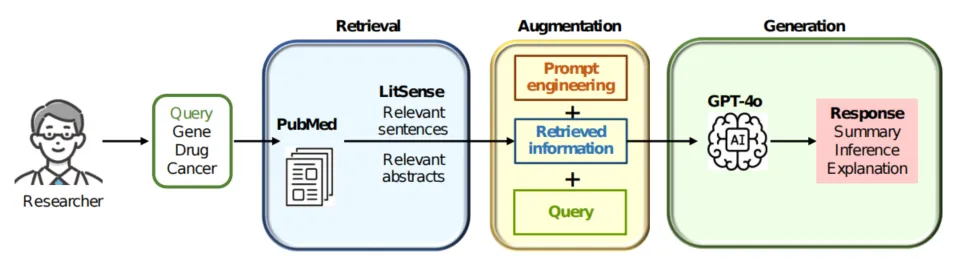
面对 NGS 产出的海量数据,GenAI 不仅仅是分类器。研究显示,GPT-4o 在区分疾病相关变异与 VUS 时的准确率已达到 0.73 以上。更重要的是,像 GeneRxGPT 这样的工具可以构建泛癌种的药-金相互作用网络,甚至能发现如 CTNNB1 突变对索拉非尼敏感性影响等潜在治疗策略。
[药物-基因关系推理流程图]解读:展示从 PubMed 检索、知识扩展到最终生成推理结论的自动化闭环。
2. 临床试验匹配的“超级导航”
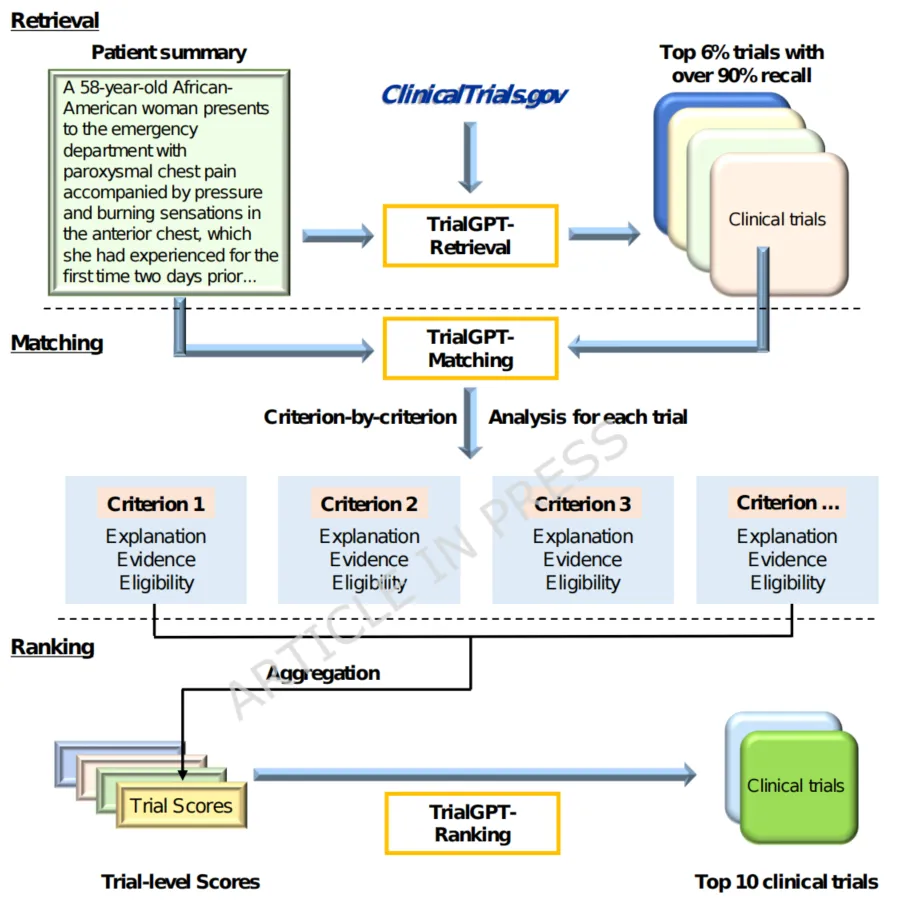
传统的临床试验招募往往面临“信息不对称”。TrialGPT 架构通过三个模块(检索、匹配、排序)解决了这一痛点。在测试中,它召回了超过 90% 的相关试验,且减少了临床医生约 42.6% 的工作量。这意味着,原本需要数小时的患者筛选,现在可以在分钟级完成,极大提升了 入组率。
[TrialGPT 运行机制图]解读:重点展示其如何逐项(Criterion-by-criterion)分析患者病历与试验要求的逻辑关联。
3. 多模态“肿瘤表型”计算
这是最前沿的领域。通过 VLM(视觉语言模型) 和病理基础模型(如 Prov-GigaPath),AI 可以直接从 H&E 染色切片或放射影像中“预估”分子特征(即分子代理估算)。
Flamingo-CXR 等模型在放射影像报告生成中,已被证明在 94% 的正常病例中表现优于或等同于人类。 这种“影像/病理 + 基因 + EHR(电子健康档案)”的全深度融合,让 计算肿瘤表型成为可能。
争议与反思:华丽外表下的“灰色地带”
作为严谨的医学综述,作者并未一味吹捧,而是犀利地指出了目前 AI 落地的几大“暗礁”:
1. 知识的“保质期”
肿瘤学指南更新极快(如 ASCO Living Guidelines)。如果 AI 训练数据停留在去年,它可能会给出已经过时的治疗建议,甚至漏掉上个月刚获批的重磅药物。
对策:必须实施 RAG 和持续监控机制,而不是依赖“离线”的预训练权重。
2. 算法偏见与公平性
AI 可能会学习到训练数据中的人口统计学偏差。如果在欠发达地区数据缺失,AI 可能会在这些人群的治疗建议上表现不佳,从而加剧 医疗不平等(Health Disparities)。
3. “幻觉”下的法律责任
如果 AI 给出了错误的推荐,谁来担责?
核心原则:必须坚持 HITL(人机协同) 模式。AI 的输出应视为“医生审阅的草稿”而非“最终裁决”。在 EU AI Act(欧盟 AI 法案) 的框架下,医疗 AI 被归类为高风险类别,必须具备严格的可审计性(Audit Trails)。
临床决策建议:构建“安全底座”
如何安全地在你的科室部署 GenAI?作者给出了一个 “安全设计” 的建议路径图:
数据标准化:采用 OMOP, mCODE, FHIR 等标准,打破院内数据孤岛。 检索增强:所有决策支持系统必须强制开启 RAG,并显示证据来源。 合成数据策略:在科研开发阶段,利用 Differential Privacy(差分隐私) 技术生成合成 EHR,保护患者隐私。 人机回路:建立明确的 SOP(标准操作程序),确保重要决策(如分子肿瘤委员会讨论)必须有专家二次确认。
未来风向标:从“医生工具”到“学习型系统”
综述在结尾提出了一个宏伟蓝图:学习型肿瘤学。
这不仅仅是部署一个聊天机器人,而是建立一个能够自我迭代的生态系统。在这个系统中,每一例临床决策、每一份 RWD、每一次治疗反馈,都会通过标准化的多模态链路实时反馈给模型。模型在受控环境下进行版本更新,从而实现诊疗策略的持续优化。
预测未来 3-5 年:
多模态融合将成为标配:医生看到的不再是孤立的报告,而是 AI 整合后的、具备预测概率的肿瘤全景视图。 监管范式的转变:监管机构(如 FDA)将从“静态审批”转向对“生命周期控制计划(PCCP)”的监管,允许模型在监控下安全迭代。
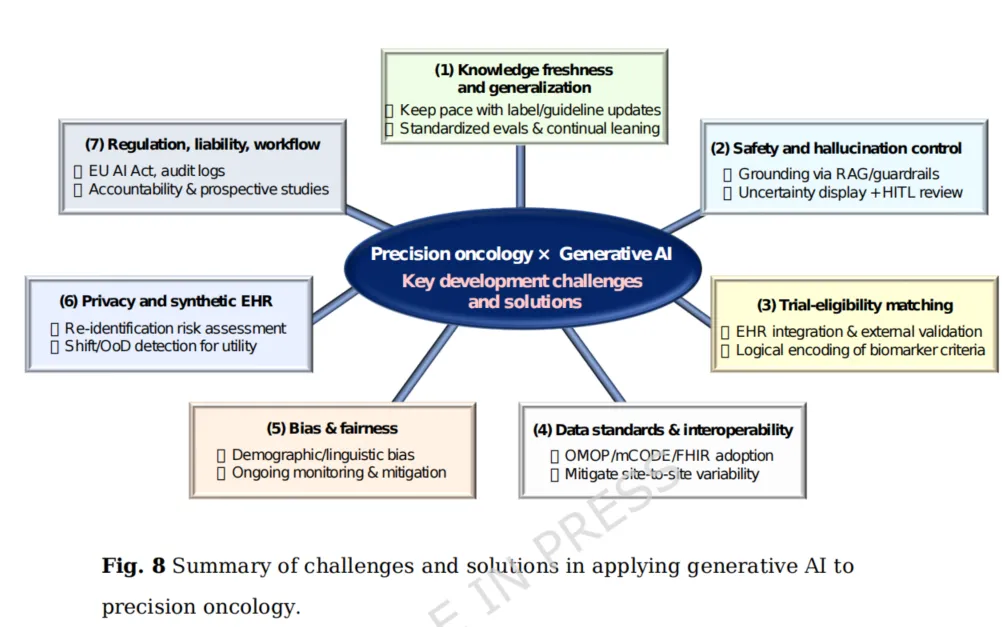
[ 挑战与解决方案全景图]
如果说前沿模型是“引擎”,那么这篇综述总结的挑战与解决方案全景图 就是确保这台赛车不脱轨的“导航仪” 。作者系统性地梳理了 GenAI 在精准肿瘤学落地的 7 大轴心挑战,并给出了针锋相对的破局方案 。
轴心一:知识“保鲜期”与跨中心泛化
挑战:肿瘤学知识迭代极快,模型极易产生“知识陈旧” 。同时,不同医院的测序面板和病历格式各异,导致模型“水土不服” 。
方案:强制引入 RAG(检索增强生成) 架构,让 AI 在回答前先查阅最新的说明书和指南 。通过多中心外部验证和持续学习,保持模型的“进化”状态 。
轴心二:消灭“幻觉”与安全红线
挑战:AI 可能会编造看似合理的突变解读或用药证据,这在决策中是致命的 。
方案:通过 RAG 架构实现输出内容的证据溯源(Grounding) 。同时,系统必须具备不确定性显示功能,并强制医生进行 HITL(人机协同) 审核 。
轴心三:破解临床试验的“逻辑迷宫”
挑战:临床试验的入排标准不仅复杂,而且往往涉及多生物标志物组合的复杂逻辑 。
方案:利用大模型对生物标志物标准进行逻辑编码,实现自动化的精准匹配 。
轴心四:打破数据“巴别塔”
挑战:各医院术语不一、格式不均,是限制 AI 发挥的最大瓶颈 。
方案:全面拥抱 OMOP、mCODE 和 FHIR 等国际标准数据模型,将非结构化数据转化为 AI 可读的“通用语言” 。
轴心五:偏见监测与算法公平
挑战:如果训练数据缺乏特定族群信息,AI 可能给出带有歧视性或偏差的偏见建议 。
方案:建立持续监控机制,对 AI 建议进行分层审计,确保精准医疗不因算法而产生新的不平等 。
轴心六:隐私护航与合成数据
挑战:肿瘤基因数据具有极高的唯一性,传统脱敏手段仍有“再识别”风险 。
方案:利用 Differential Privacy(差分隐私) 技术生成“合成病历”,既能供 AI 训练使用,又从物理层面杜绝了隐私泄露的可能性 。
轴心七:监管合规与法律责任
挑战:高风险医疗 AI 的责任边界在哪里?如何满足欧盟 AI 法案等严苛监管?
方案:建立详尽的审计日志(Audit logs),实现决策全过程的可追溯 。明确医生作为最终决策者的法律地位,通过 SOP 将 AI 深度嵌入现有工作流 。
互动话题
作为临床一线医生或癌症研究者,你最希望 GenAI 帮你分担哪部分工作?是写病历,还是解读 NGS 报告?亦或是寻找临床试验?
在图 8 总结的这 7 大挑战中,你认为目前在我国临床落地最大的“拦路虎”是哪一个?是数据标准不统一,还是法律责任界定?
欢迎在评论区分享你的看法。
参考文献
Ryuji Hamamoto, Takafumi Koyama, Satoshi Takahashi, et al. Implementing generative artificial intelligence in precision oncology: safety, governance, and significance. J Hematol Oncol (2026).
 夜雨聆风
夜雨聆风