
导语
临床试验是药物从实验室走向临床的必经之路,也是验证药物安全有效的 “金标准”。但长期以来,行业始终被几大痛点困扰:招募慢、成本高、周期长、数据乱、成功率低。全球86%的临床试验无法按期完成招募,50%的临床数据存在质量缺陷,单个新药研发成本逼近26亿美元,而最终上市成功率不足12%。
近年来,以机器学习、深度学习、自然语言处理(NLP)和大语言模型(LLM)为代表的人工智能(AI)技术,正在以不可逆转的态势渗透临床试验全流程。本文基于多篇国际权威期刊文章的观点,系统阐述AI 在临床试验中的全场景应用、核心局限、落地痛点以及未来走向,为从业者提供可落地、可参考、可决策的专业判断。
一、AI在临床试验中的全流程落地:从试验设计到上市后监测
1、 临床试验设计阶段:从 “经验驱动” 转向 “数据驱动”
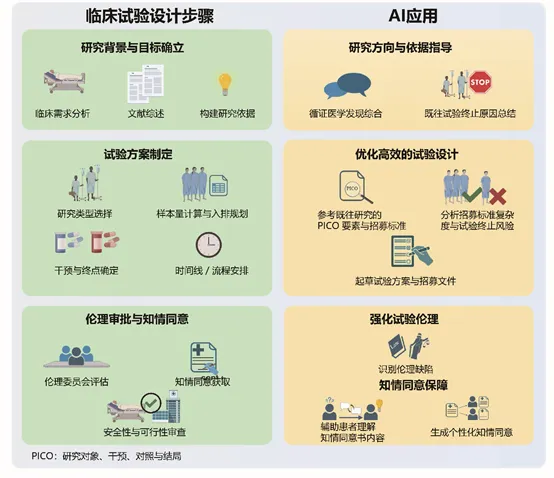
1.1.方案科学化与 PICO 自动提取。AI 可自动读取海量文献与历史试验,提取 PICO 要素(人群、干预、对照、结局),辅助构建科学假设,减少方案设计的主观性与漏洞。
1.2. 入排标准智能优化。自动分析数万份方案,识别与 “试验失败” 强相关的严苛条款;平衡科学性与招募可行性,降低不合理的排除率;自动生成标准化、结构化、可检索的入排标准。
1.3. 研究中心智能选择。通过机器学习评估:疾病人群分布;交通可及性;研究者历史绩效;竞争试验情况;从而提升入组速度,降低中心启动失败率。
1.4. 伦理与知情同意自动化生成与简化。自动识别伦理风险点;将专业版知情同意书简化至中学阅读水平;支持多语言、多文化背景适配;提升患者理解率与知情质量。
2、患者招募与筛选:AI 最成熟、价值最显著的环节
2.1. 患者–试验自动匹配。NLP与大模型直接读取电子病历;自动判断患者是否符合入排标准;匹配效率提升65%,准确率可达78%–90%。
2.2.高通量虚拟筛选。突破地域限制,实现去中心化筛选;智能聊天机器人完成预筛与宣教;单患者筛选时间从小时级压缩至分钟级。
2.3. 提升人群多样性与公平性。AI 可识别少数族裔、低收入、偏远地区等被低估人群,减少算法偏见,提高试验人群代表性,增强结果外推性。
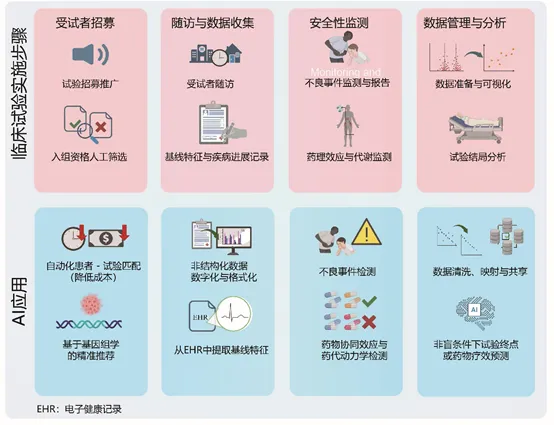
3、数据采集、清洗、管理与标准化:AI 的 “硬核基建能力”
3.1. 多模态数据自动抽取。结构化数据、检验检查、自由文本、影像报告、可穿戴设备数据统一接入与解析。
3.2. 智能数据清洗。自动识别缺失、异常、逻辑错误;清洗时间缩短60%–80%;减少人工质疑(Query)数量。
3.3. 术语标准化与数据映射。自动映射 ICD、LOINC、SNOMED、UMLS、OMOP CDM;实现跨中心、跨系统数据互通。
4、风险监测与安全性管理:从事后补救到实时预警
4.1. 不良事件(AE)实时监测。数字生物标志物 + AI 可穿戴监测灵敏度达90%;24–48小时内识别异常,远快于传统 4–6 周;自动提取 AE、编码、判断严重性与相关性。
4.2. 基于风险的监查(Risk-Based Monitoring)。AI自动识别高风险中心、高风险数据、方案偏离,实现资源精准投放,降低 30%–40%监查成本。
4.3. 药物相互作用(DDI)预警。大模型与机器学习可从文献、说明书、病历中自动识别潜在相互作用,提升用药安全。
5、试验结局预测与自适应设计:提升成功率的关键
5.1. 试验成败提前预测。预测模型准确率可达85%,帮助企业提前终止无效试验,节约数亿成本。
5.2. 患者分层与精准获益预测。识别最可能获益的亚组,支持精准临床试验。
5.3. 自适应设计优化。AI 支持样本量重新估算、随机化比例调整、剂量调整、早期终止,让试验更灵活、更高效、更伦理。
三、AI在临床试验中的现实短板与风险:从业者必须清醒认知
1、大模型 “幻觉问题”:医疗场景致命风险。LLM可能编造:不存在的检验指标;虚假的医学结论;错误的入排判断;编造文献与数据。在医疗与临床试验中,幻觉=安全风险,必须严格控制。
2、算法偏见与数据偏差。训练数据以白人、城市人群为主;少数族裔、老年、儿童、罕见病数据不足;模型可能 “歧视” 医疗可及性差的群体;导致结果不具普适性。
3、黑箱不可解释。监管与临床难以接受。深度学习、大模型通常被视为 “黑箱”:医生无法信任无法解释的判断;伦理委员会难以接受;监管机构要求可追溯、可解释。
4、数据隐私与合规风险。EHR、基因组数据高度敏感;GDPR、HIPAA、国内个人信息保护法要求严格;数据出境、集中训练、第三方处理均存在合规风险。
5、落地成本高、集成难度大。单医院系统对接成本可达25万–50万美元;老旧系统不兼容;数据格式不统一;需要大量定制化与术语适配。
6、监管框架仍不明确。全球范围内尚无统一的 AI 临床试验审批标准;模型验证、更新、质控体系不健全;算法作为 “医疗决策工具” 的责任界定不清晰。
7、泛化能力不足。在某一疾病、某一中心训练的模型,换到另一中心可能效果骤降,难以规模化复制。
四、AI 落地临床试验的关键路径:从技术到合规的完整框架
AI要真正安全、合规、高效落地,必须建立分层实施框架。
1、优先落地:低风险、高收益场景:
①文献分析、方案信息提取;
②招募策略优化、中心可行性预测;
③数据清洗、格式标准化;
④非介入性监测、趋势分析。这些场景不直接影响患者安全,适合作为 AI 切入点。
2、严格管控:中高风险场景:
①患者 eligibility 判断;
②不良事件自动判定;
③剂量建议、治疗分组。
必须满足:
①AI 输出仅供参考;
②医生/研究者最终审核;
③全程留痕、可追溯;
④高风险场景禁止全自动替代人工。
3、技术解决方案:行业共识方向。检索增强生成(RAG):外接知识库、说明书、试验数据,减少幻觉。可解释 AI(XAI):每一步判断给出理由,满足临床与监管。联邦学习:数据不出院,模型多中心协同训练,保护隐私。混合模型:规则引擎 + 机器学习 + 大模型,兼顾灵活与稳定。提示工程:标准化提示词,减少输出波动。
4、合规与质控体系。模型需验证、校准、持续监控性能;建立偏见监测机制;输出留痕、可审计;明确责任主体:研究者/机构对决策负责。
五、未来展望: AI 将如何彻底改变临床试验?
未来临床试验将呈现七大趋势:
1、全流程AI化:AI成为临床试验 “操作系统”。从方案设计→招募→数据→监查→统计→报告→发表,全流程 AI 辅助。
2、去中心化试验(DCT)成为主流。AI+可穿戴+远程监查+数字生物标志物,让试验 “去医院化”,更高效、更普惠。
3、大模型+检索增强生成(RAG)成为标配。幻觉问题被显著抑制,准确性接近人工专家。
4、可解释 AI(XAI)成为准入门槛。监管将强制要求:AI 决策必须可解释、可追溯、可复核。
5、全球统一监管框架逐步形成。FDA、EMA、NMPA未来有望推出 AI 临床试验指南,行业进入规范化时代。
6、精准临床试验成为常态。基于AI的患者分层、生物标志物筛选、自适应设计,让每一项试验更高效、更伦理、更成功。
7、罕见病、肿瘤、儿科等领域有望最先突破。这些领域患者少、筛选难、数据稀,AI 最具潜力。
给临床试验从业者的启示与建议
1、拥抱趋势,但保持专业判断。AI 是工具,不是替代者。医学判断、伦理责任、科学严谨性仍由人掌控。
2、从 “单点工具” 开始落地。不必追求一步到位,可从数据清洗、招募筛选、文献整理切入。
3、建立 AI 质控与合规意识。所有 AI 输出必须可追溯、可复核、可验证。
4、关注数据质量与数据安全。高质量、标准化、合规的数据,是AI有效的前提。
5、提升数字素养。未来的 CRC、CRA、医学/项目经理、统计师、研究者,都必须具备基本的 AI 认知能力。
总结
AI在临床试验中已从技术探索走向效率革命,能够大幅优化方案设计、患者招募、数据处理与风险监控等环节,显著缩短周期、降低成本、提升数据质量与试验成功率,为全流程智能化奠定坚实基础。然而,要实现稳健合规落地,仍面临算法幻觉、数据偏见、模型可解释性不足、隐私保护压力大、系统集成成本高等关键问题。未来,我们需在技术可控、伦理合规、可解释性与标准化体系上持续突破,才能真正安全、规模化地赋能临床试验高质量发展。
参考文献
1. Olawade DB, et al. Artificial intelligence in clinical trials: A comprehensive review of opportunities, challenges, and future directions. Int J Med Inform. 2026 Feb;206:106141.
2. Chen H, et al. Enhancing Patient-Trial Matching With Large Language Models: A Scoping Review of Emerging Applications and Approaches. JCO Clin Cancer Inform. 2025 Jun;9:e2500071.
3. Lin A, et al. Large language models in clinical trials: applications, technical advances, and future directions. BMC Med. 2025 Oct 14;23(1):563.
4. Chopra H, et al. Revolutionizing clinical trials: the role of AI in accelerating medical breakthroughs. Int J Surg. 2023 Dec 1;109(12):4211-4220.
医学部
CLIN-NOV

医学科学团队100%由临床医生组成,36%具有博士学位,涉及各热门治疗领域。拥有丰富的临床经验及较高的科学素养,并具有丰富的临床研究项目经验。致力于为申办方设计制定合理的产品临床开发策略及临床研究方案,提供优质的医学监查服务。配以撰写经验丰富的医学写作团队,为产品临床开发提供全流程文件输出,为临床研究的开展及产品注册申报保驾护航。

 夜雨聆风
夜雨聆风