
2026年04月27日,辽宁省药监局发布了对3家医疗器械生产企业的飞行检查公告,沈阳恒源药业、沈阳太平洋医疗用品、医普生物科技(辽宁)被查出问题。看完通报发现一个规律:没有大案要案,全是小毛病——但飞检恰恰就爱抓这些小毛病。
文件与记录:写得出来做不到,或者做到了没写
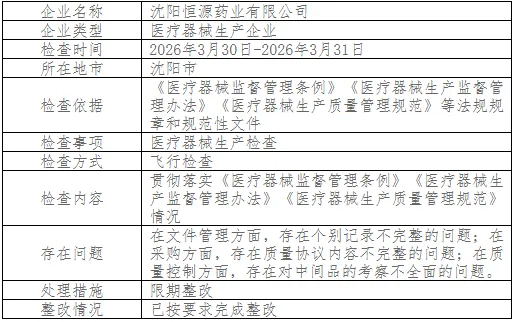
三家企业在记录和文件管理上都有缺陷。
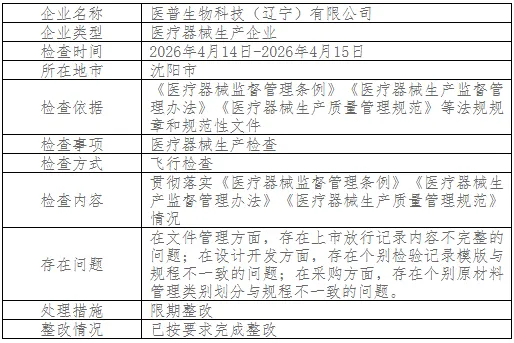
恒源药业是个别记录不完整,医普生物是上市放行记录内容不完整,太平洋医疗是制水系统运行记录不完整。
飞检的逻辑是:记录就是证据。 你说设备运行正常,记录呢?你说产品放行了,放行记录签全了吗?你说制水系统没问题,运行参数谁记的、什么时候记的、有没有异常?记录一缺,就等于没做,或者做了但没法证明。
更隐蔽的是医普生物那条检验记录模版与规程不一致。模版是实际操作的依据,规程是体系文件的要求,两者对不上,说明文件体系本身在打架,员工现场填记录时,到底按哪个来?
采购与外协:协议和评价流于形式
三家企业在采购环节都栽了。
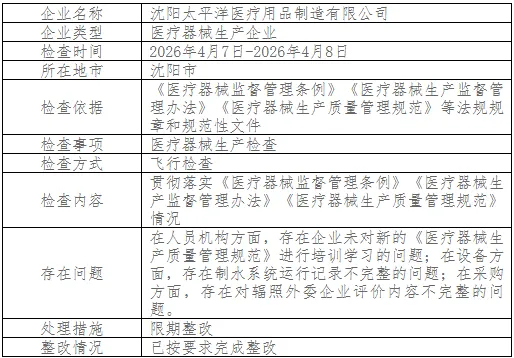
恒源药业质量协议内容不完整,太平洋医疗对辐照外委企业评价内容不完整,医普生物原材料管理类别划分与规程不一致。
医疗器械生产对外协过程(比如辐照灭菌)的控制要求很严。你说外协企业合格,评价报告里评了什么?资质?现场审计?历史质量数据?还是只填了个表?质量协议也一样,签是签了,关键质量条款、验收标准、变更通知机制写进去了吗?
医普生物那条原材料管理类别划分与规程不一致更要命。原材料按什么标准分级管理(A类、B类还是关键/非关键)?如果现场划分和文件规定不一致,说明来料管控的口子松了,关键原材料和非关键原材料可能混管。
人员与培训:规范更新了,人还没跟上
太平洋医疗被点的一条很有代表性:未对新的《医疗器械生产质量管理规范》进行培训学习。
规范更新了,企业体系文件可能也更新了,但员工没培训,等于新规范只停留在纸上。飞检查这个,不是看有没有培训计划,是看培训有没有覆盖到最新法规要求,以及培训后有没有考核、有没有记录。
飞检的底层逻辑
查的不是有没有问题,是体系能不能自洽。
这3家企业的问题,单看都不严重,没有产品不合格、没有生产造假。但飞检的视角是:如果你的记录不完整、文件和实际操作不一致、新规培训没跟上,说明你的质量管理体系在空转。
对医疗器械生产企业来说,现在可以对照自查三件事:
1、记录完整性抽查:随机抽5份批生产记录、放行记录、设备运行记录,看关键字段(时间、参数、签名、复核)有没有空白。
2、文件一致性核对:把现场使用的记录模版、操作流程,和质量手册、程序文件逐条比对,看有没有现场一套、文件一套。
3、外协与采购档案:把主要原材料供应商、外协服务商(辐照、灭菌、检测等)的质量协议和评价报告翻出来,看内容是否完整、是否在有效期内。
飞检不提前打招呼,查的就是日常管理是不是真干而不是假写。记录写全了、文件对上了、培训到位了,小问题自然少。
供稿:中食药集团
编辑:王不留行

 夜雨聆风
夜雨聆风