文档内容
专练 18 硫及其化合物
授课提示:对应学生用书35页
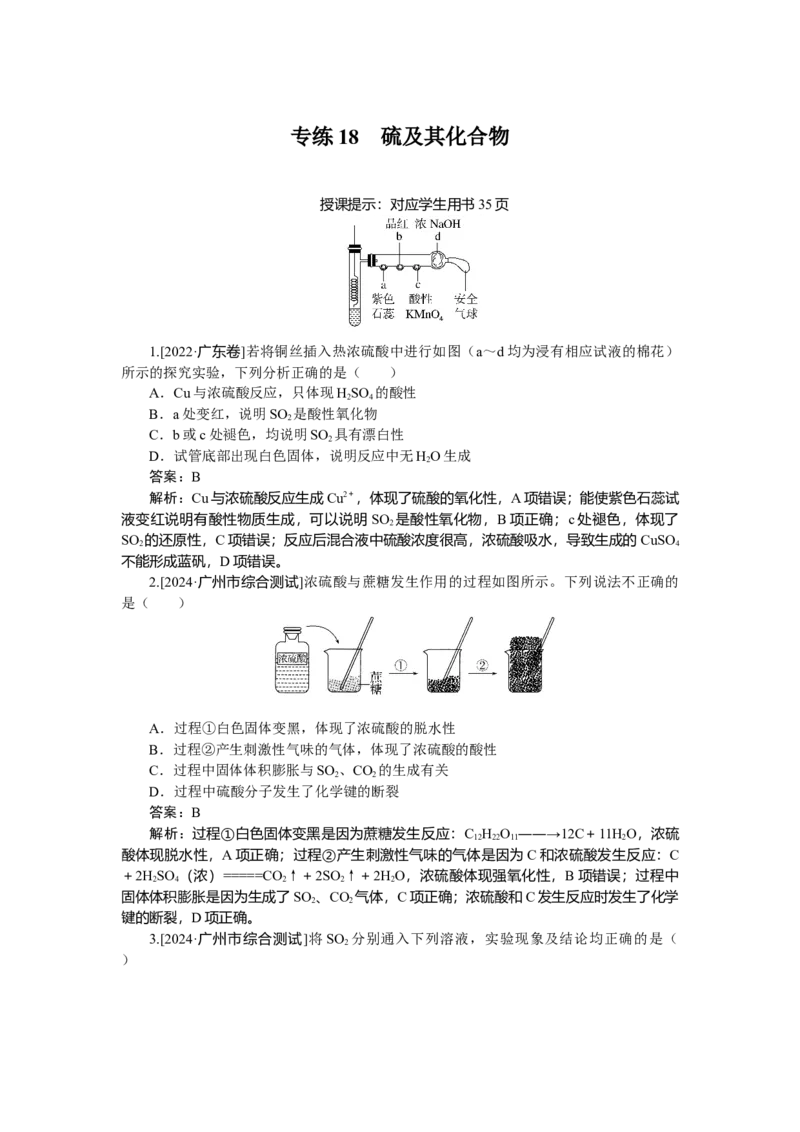
1.[2022·广东卷]若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)
所示的探究实验,下列分析正确的是( )
A.Cu与浓硫酸反应,只体现HSO 的酸性
2 4
B.a处变红,说明SO 是酸性氧化物
2
C.b或c处褪色,均说明SO 具有漂白性
2
D.试管底部出现白色固体,说明反应中无HO生成
2
答案:B
解析:Cu与浓硫酸反应生成Cu2+,体现了硫酸的氧化性,A项错误;能使紫色石蕊试
液变红说明有酸性物质生成,可以说明SO 是酸性氧化物,B项正确;c处褪色,体现了
2
SO 的还原性,C项错误;反应后混合液中硫酸浓度很高,浓硫酸吸水,导致生成的CuSO
2 4
不能形成蓝矾,D项错误。
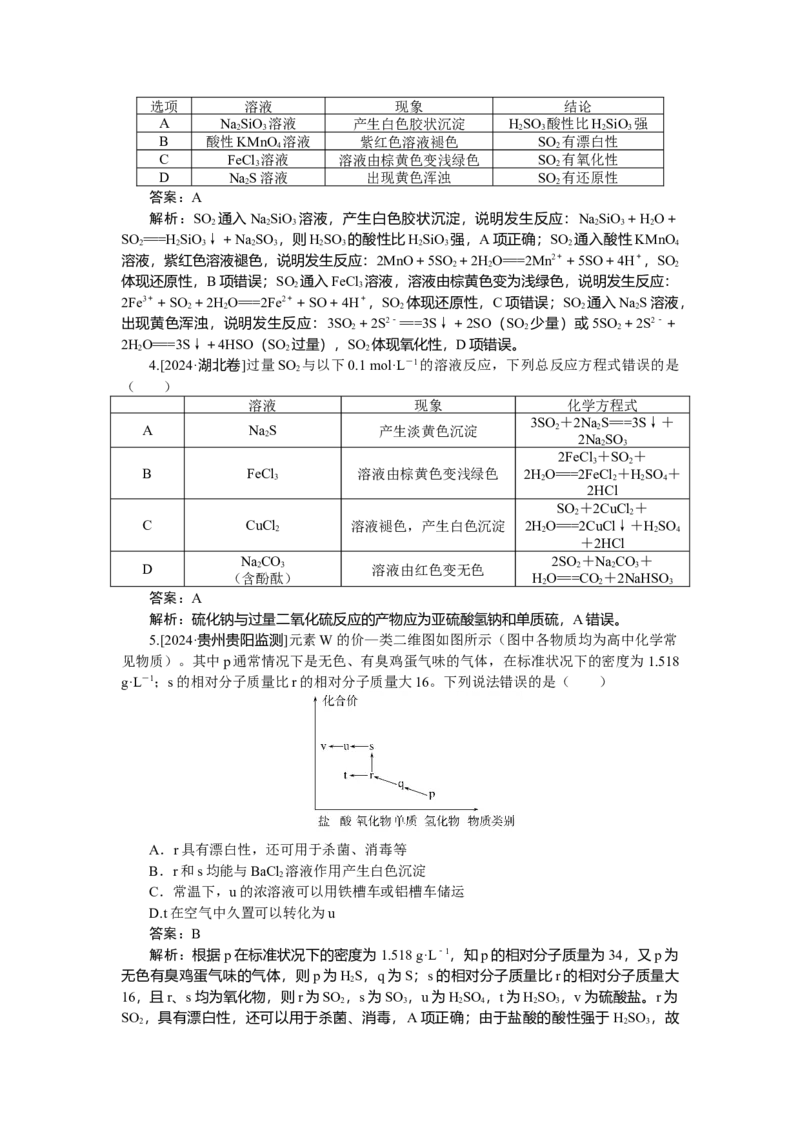
2.[2024·广州市综合测试]浓硫酸与蔗糖发生作用的过程如图所示。下列说法不正确的
是( )
A.过程①白色固体变黑,体现了浓硫酸的脱水性
B.过程②产生刺激性气味的气体,体现了浓硫酸的酸性
C.过程中固体体积膨胀与SO 、CO 的生成有关
2 2
D.过程中硫酸分子发生了化学键的断裂
答案:B
解析:过程①白色固体变黑是因为蔗糖发生反应:C H O ――→12C+11HO,浓硫
12 22 11 2
酸体现脱水性,A项正确;过程②产生刺激性气味的气体是因为C和浓硫酸发生反应:C
+2HSO (浓)=====CO↑+2SO ↑+2HO,浓硫酸体现强氧化性,B项错误;过程中
2 4 2 2 2
固体体积膨胀是因为生成了SO 、CO 气体,C项正确;浓硫酸和C发生反应时发生了化学
2 2
键的断裂,D项正确。
3.[2024·广州市综合测试]将SO 分别通入下列溶液,实验现象及结论均正确的是(
2
)选项 溶液 现象 结论
A NaSiO 溶液 产生白色胶状沉淀 HSO 酸性比HSiO 强
2 3 2 3 2 3
B 酸性KMnO 溶液 紫红色溶液褪色 SO 有漂白性
4 2
C FeCl 溶液 溶液由棕黄色变浅绿色 SO 有氧化性
3 2
D NaS溶液 出现黄色浑浊 SO 有还原性
2 2
答案:A
解析:SO 通入NaSiO 溶液,产生白色胶状沉淀,说明发生反应:NaSiO +HO+
2 2 3 2 3 2
SO ===H SiO↓+NaSO ,则HSO 的酸性比HSiO 强,A项正确;SO 通入酸性KMnO
2 2 3 2 3 2 3 2 3 2 4
溶液,紫红色溶液褪色,说明发生反应:2MnO+5SO +2HO===2Mn2++5SO+4H+,SO
2 2 2
体现还原性,B项错误;SO 通入FeCl 溶液,溶液由棕黄色变为浅绿色,说明发生反应:
2 3
2Fe3++SO +2HO===2Fe2++SO+4H+,SO 体现还原性,C项错误;SO 通入NaS溶液,
2 2 2 2 2
出现黄色浑浊,说明发生反应:3SO +2S2-===3S↓+2SO(SO 少量)或5SO +2S2-+
2 2 2
2HO===3S↓+4HSO(SO 过量),SO 体现氧化性,D项错误。
2 2 2
4.[2024·湖北卷]过量SO 与以下0.1 mol·L-1的溶液反应,下列总反应方程式错误的是
2
( )
溶液 现象 化学方程式
3SO +2NaS===3S↓+
A NaS 产生淡黄色沉淀 2 2
2 2NaSO
2 3
2FeCl +SO +
3 2
B FeCl 溶液由棕黄色变浅绿色 2HO===2FeCl +HSO +
3 2 2 2 4
2HCl
SO +2CuCl +
2 2
C CuCl 溶液褪色,产生白色沉淀 2HO===2CuCl↓+HSO
2 2 2 4
+2HCl
NaCO 2SO +NaCO+
D 2 3 溶液由红色变无色 2 2 3
(含酚酞) HO===CO +2NaHSO
2 2 3
答案:A
解析:硫化钠与过量二氧化硫反应的产物应为亚硫酸氢钠和单质硫,A错误。
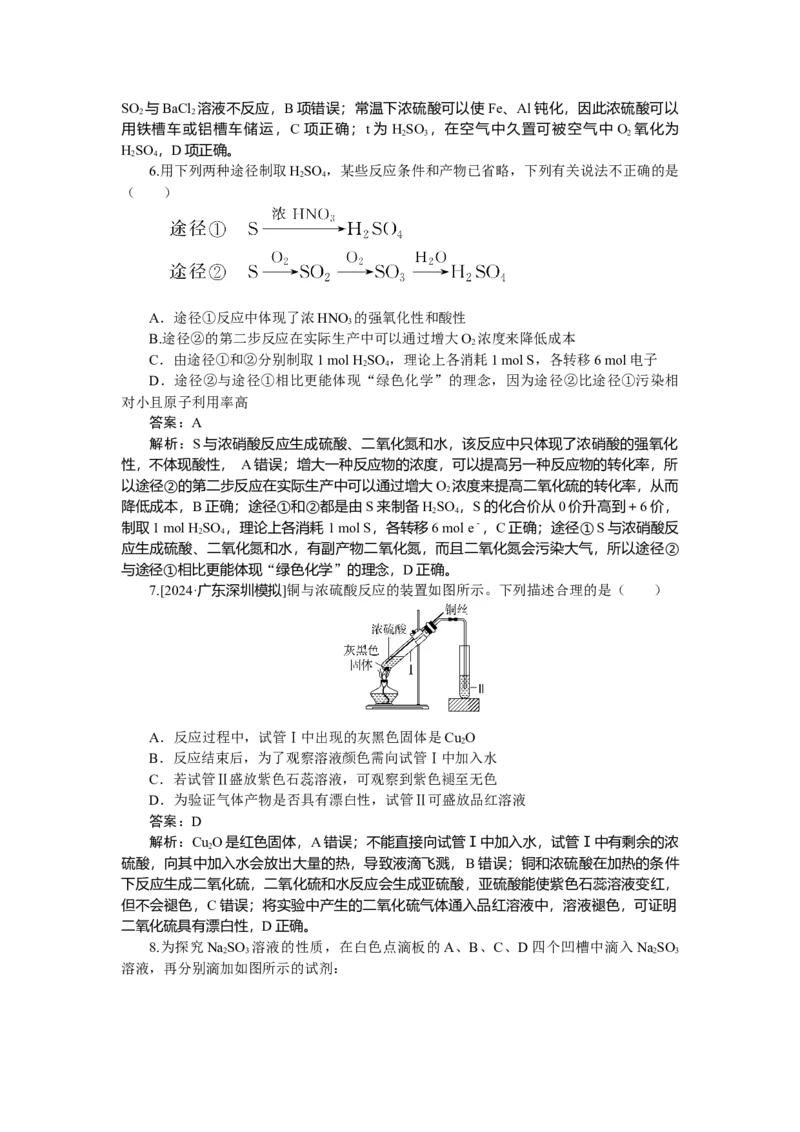
5.[2024·贵州贵阳监测]元素W的价—类二维图如图所示(图中各物质均为高中化学常
见物质)。其中p通常情况下是无色、有臭鸡蛋气味的气体,在标准状况下的密度为1.518
g·L-1;s的相对分子质量比r的相对分子质量大16。下列说法错误的是( )
A.r具有漂白性,还可用于杀菌、消毒等
B.r和s均能与BaCl 溶液作用产生白色沉淀
2
C.常温下,u的浓溶液可以用铁槽车或铝槽车储运
D.t在空气中久置可以转化为u
答案:B
解析:根据p在标准状况下的密度为1.518 g·L-1,知p的相对分子质量为34,又p为
无色有臭鸡蛋气味的气体,则p为HS,q为S;s的相对分子质量比r的相对分子质量大
2
16,且r、s均为氧化物,则r为SO ,s为SO ,u为HSO ,t为HSO ,v为硫酸盐。r为
2 3 2 4 2 3
SO ,具有漂白性,还可以用于杀菌、消毒,A项正确;由于盐酸的酸性强于 HSO ,故
2 2 3SO 与BaCl 溶液不反应,B项错误;常温下浓硫酸可以使Fe、Al钝化,因此浓硫酸可以
2 2
用铁槽车或铝槽车储运,C 项正确;t 为 HSO ,在空气中久置可被空气中 O 氧化为
2 3 2
HSO ,D项正确。
2 4
6.用下列两种途径制取HSO ,某些反应条件和产物已省略,下列有关说法不正确的是
2 4
( )
A.途径①反应中体现了浓HNO 的强氧化性和酸性
3
B.途径②的第二步反应在实际生产中可以通过增大O 浓度来降低成本
2
C.由途径①和②分别制取1 mol H SO ,理论上各消耗1 mol S,各转移6 mol电子
2 4
D.途径②与途径①相比更能体现“绿色化学”的理念,因为途径②比途径①污染相
对小且原子利用率高
答案:A
解析:S与浓硝酸反应生成硫酸、二氧化氮和水,该反应中只体现了浓硝酸的强氧化
性,不体现酸性, A错误;增大一种反应物的浓度,可以提高另一种反应物的转化率,所
以途径②的第二步反应在实际生产中可以通过增大O 浓度来提高二氧化硫的转化率,从而
2
降低成本,B正确;途径①和②都是由S来制备HSO ,S的化合价从0价升高到+6价,
2 4
制取1 mol H SO ,理论上各消耗1 mol S,各转移6 mol e-,C正确;途径①S与浓硝酸反
2 4
应生成硫酸、二氧化氮和水,有副产物二氧化氮,而且二氧化氮会污染大气,所以途径②
与途径①相比更能体现“绿色化学”的理念,D正确。
7.[2024·广东深圳模拟]铜与浓硫酸反应的装置如图所示。下列描述合理的是( )
A.反应过程中,试管Ⅰ中出现的灰黑色固体是Cu O
2
B.反应结束后,为了观察溶液颜色需向试管Ⅰ中加入水
C.若试管Ⅱ盛放紫色石蕊溶液,可观察到紫色褪至无色
D.为验证气体产物是否具有漂白性,试管Ⅱ可盛放品红溶液
答案:D
解析:Cu O是红色固体,A错误;不能直接向试管Ⅰ中加入水,试管Ⅰ中有剩余的浓
2
硫酸,向其中加入水会放出大量的热,导致液滴飞溅,B错误;铜和浓硫酸在加热的条件
下反应生成二氧化硫,二氧化硫和水反应会生成亚硫酸,亚硫酸能使紫色石蕊溶液变红,
但不会褪色,C错误;将实验中产生的二氧化硫气体通入品红溶液中,溶液褪色,可证明
二氧化硫具有漂白性,D正确。
8.为探究NaSO 溶液的性质,在白色点滴板的A、B、C、D四个凹槽中滴入NaSO
2 3 2 3
溶液,再分别滴加如图所示的试剂:对应实验现象的“解释或结论”正确的是( )
选项 实验现象 解释或结论
A 溶液褪色 还原性:SOH CO ,
2 2 3 2 3 3 2 2 3 2 3
A正确; SO 溶于水显酸性,H+与NO结合成HNO,HNO 会氧化SO生成SO,B错误;
2 3 3
C项发生反应:SO +2HS===3S↓+2HO,SO 作氧化剂,具有氧化性,C错误; KMnO
2 2 2 2 4
具有强氧化性,可以氧化SO 生成SO,SO 表现还原性,D错误。
2 2
12.[2024·兰州市高三诊断考试]某小组同学探究SO 与新制Cu(OH) 悬浊液反应的实
2 2
验装置如图所示:
下列说法不正确的是( )
A.配制70%硫酸溶液需要用到的仪器有烧杯、量筒、玻璃棒、胶头滴管
B.装置B的作用是监控SO 流速,其中试剂可以用饱和NaHSO 溶液
2 3
C.反应开始时C中出现砖红色沉淀,氧化剂和还原剂的物质的量之比为2∶1
D.反应后向C的溶液中加入稀盐酸酸化后,再滴加BaCl 溶液,有白色沉淀生成,证
2
明反应中SO 作还原剂
2
答案:D
解析:配制70%硫酸溶液需使用量筒和胶头滴管量取浓硫酸,需在烧杯中进行稀释,
且稀释时需用玻璃棒搅拌,A项正确;装置B的作用是监控SO 流速,由于SO 在饱和
2 2
NaHSO 溶液中的溶解度较小,故其中的试剂可以用饱和NaHSO 溶液,B项正确;反应开
3 3
始时C中出现砖红色沉淀,说明发生反应:SO +2Cu(OH) ===Cu O+HSO +HO,其
2 2 2 2 4 2
中SO 为还原剂,Cu(OH) 为氧化剂,则氧化剂和还原剂的物质的量之比为2∶1,C项
2 2
正确;由于CuSO 溶液能与稀盐酸酸化的BaCl 溶液反应生成BaSO 白色沉淀,故无法证
4 2 4
明反应中SO 作还原剂,D项错误。
2