文档内容
专练 64 实验综合应用(二)
授课提示:对应学生用书127页
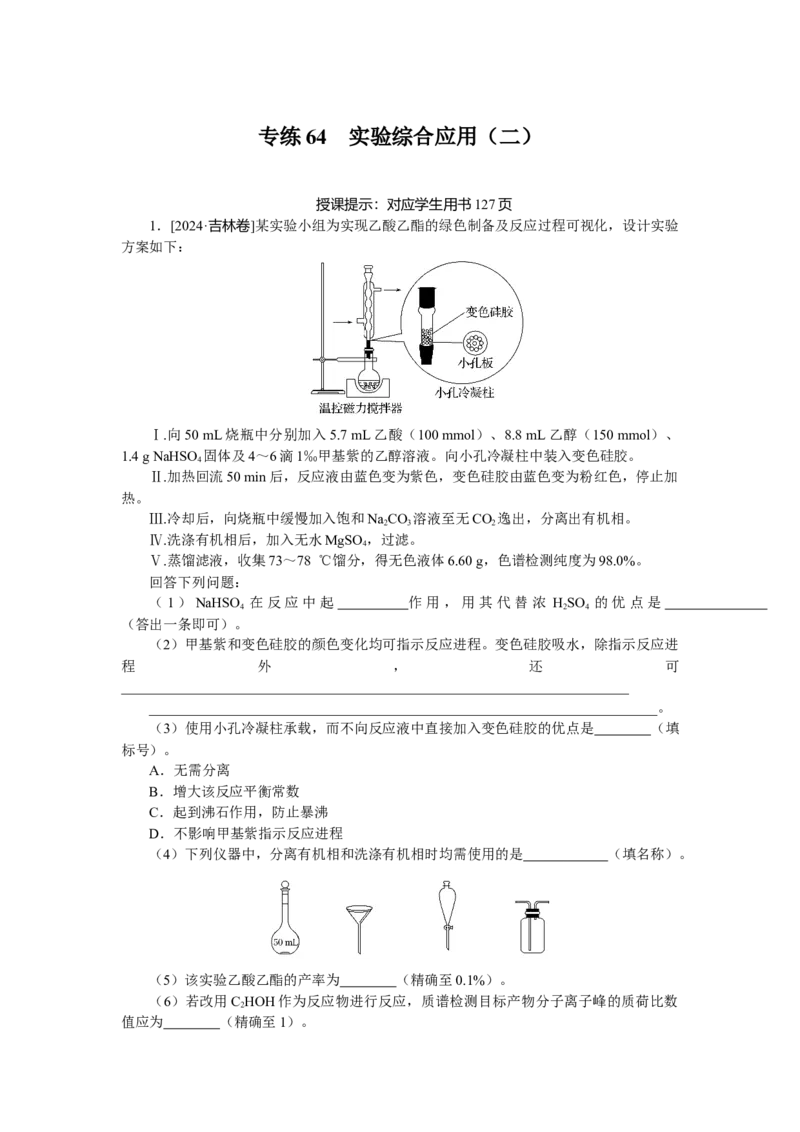
1.[2024·吉林卷]某实验小组为实现乙酸乙酯的绿色制备及反应过程可视化,设计实验
方案如下:
Ⅰ.向50 mL烧瓶中分别加入5.7 mL乙酸(100 mmol)、8.8 mL乙醇(150 mmol)、
1.4 g NaHSO 固体及4~6滴1‰甲基紫的乙醇溶液。向小孔冷凝柱中装入变色硅胶。
4
Ⅱ.加热回流50 min后,反应液由蓝色变为紫色,变色硅胶由蓝色变为粉红色,停止加
热。
Ⅲ.冷却后,向烧瓶中缓慢加入饱和NaCO 溶液至无CO 逸出,分离出有机相。
2 3 2
Ⅳ.洗涤有机相后,加入无水MgSO ,过滤。
4
Ⅴ.蒸馏滤液,收集73~78 ℃馏分,得无色液体6.60 g,色谱检测纯度为98.0%。
回答下列问题:
(1)NaHSO 在反应中起 作用,用其代替浓 HSO 的优点是
4 2 4
(答出一条即可)。
(2)甲基紫和变色硅胶的颜色变化均可指示反应进程。变色硅胶吸水,除指示反应进
程 外 , 还 可
________________________________________________________________________
________________________________________________________________________。
(3)使用小孔冷凝柱承载,而不向反应液中直接加入变色硅胶的优点是 (填
标号)。
A.无需分离
B.增大该反应平衡常数
C.起到沸石作用,防止暴沸
D.不影响甲基紫指示反应进程
(4)下列仪器中,分离有机相和洗涤有机相时均需使用的是 (填名称)。
(5)该实验乙酸乙酯的产率为 (精确至0.1%)。
(6)若改用C HOH作为反应物进行反应,质谱检测目标产物分子离子峰的质荷比数
2
值应为 (精确至1)。答案:(1)催化剂 NaHSO 无腐蚀性,操作安全;副产物少,无有毒气体 SO 产生
4 2
(答出一条即可)
(2)促进反应正向进行,提高乙酸乙酯的产率
(3)AD (4)分液漏斗 (5)73.5% (6)90
解析:(1)乙酸和乙醇在浓硫酸催化和加热条件下发生酯化反应生成乙酸乙酯和水,
该实验中用NaHSO4代替浓H2SO4,起催化剂作用。NaHSO4无腐蚀性,实验操作更安全;
浓H2SO4具有强氧化性,可与乙醇反应生成SO2等副产物,用NaHSO4代替浓H2SO4,
减少副产物的产生。(2)变色硅胶吸水,除指示反应进程外,还可使酯化反应正向进行,
提高乙酸乙酯产率。(3)变色硅胶在小孔板上方,无需分离,A项正确;平衡常数只与温
度有关,故B项错误;变色硅胶没有加入溶液中,不能防止暴沸,C项错误;根据反应液
由蓝色变为紫色、变色硅胶由蓝色变为粉红色,知变色硅胶与甲基紫不接触才不影响甲基
紫指示反应进程,D项正确。(4)分离和洗涤有机相均需用到的仪器为分液漏斗。(5)
由于乙醇过量,故根据乙酸的量计算乙酸乙酯的理论产量为 100×10-3 mol×88 g·mol-1=
8.8 g,则乙酸乙酯的产率为×100%=73.5%。(6)若改用C HOH作为反应物进行反应,根
2
据“酸脱羟基醇脱氢”知,生成的乙酸乙酯为CHCO18OC H ,其相对分子质量为90,则
3 2 5
质谱检测目标产物分子离子峰的质荷比数值为90。
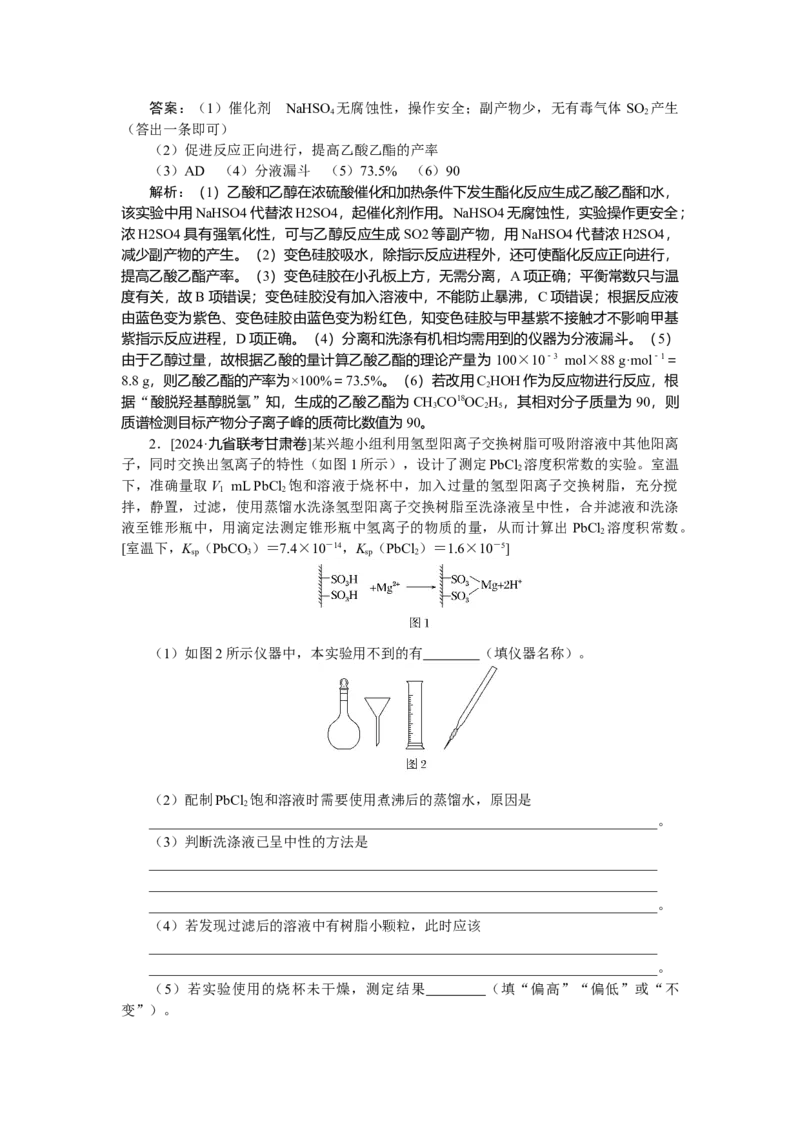
2.[2024·九省联考甘肃卷]某兴趣小组利用氢型阳离子交换树脂可吸附溶液中其他阳离
子,同时交换出氢离子的特性(如图1所示),设计了测定PbCl 溶度积常数的实验。室温
2
下,准确量取V mL PbCl 饱和溶液于烧杯中,加入过量的氢型阳离子交换树脂,充分搅
1 2
拌,静置,过滤,使用蒸馏水洗涤氢型阳离子交换树脂至洗涤液呈中性,合并滤液和洗涤
液至锥形瓶中,用滴定法测定锥形瓶中氢离子的物质的量,从而计算出 PbCl 溶度积常数。
2
[室温下,K (PbCO )=7.4×10-14,K (PbCl )=1.6×10-5]
sp 3 sp 2
(1)如图2所示仪器中,本实验用不到的有 (填仪器名称)。
(2)配制PbCl 饱和溶液时需要使用煮沸后的蒸馏水,原因是
2
________________________________________________________________________。
(3)判断洗涤液已呈中性的方法是
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(4)若发现过滤后的溶液中有树脂小颗粒,此时应该
________________________________________________________________________
________________________________________________________________________。
(5)若实验使用的烧杯未干燥,测定结果 (填“偏高”“偏低”或“不
变”)。(6)为了测定锥形瓶中氢离子的物质的量,使用浓度为 c mol·L-1的NaOH标准溶液
进行滴定,可选用 为指示剂,滴定终点的现象为
。达到滴定终点时,消耗V mL NaOH标准溶液,则K (PbCl )= (用含c、
2 sp 2
V、V 的式子表示)。
1 2
(7)该兴趣小组对实验进行讨论,某同学提出可以利用该方法测定FeF 的K ,该方
2 sp
法 (填“可行”或“不可行”),原因是
________________________________________________________________________
________________________________________________________________________。
答案:(1)量筒、容量瓶 (2)除去溶解在水中的CO (3)取一小片pH试纸于
2
表面皿中央,用玻璃棒蘸取最后一次洗涤液于pH试纸的中央,显色稳定后迅速与标准比
色卡对照,直至pH=7 (4)重新过滤,并洗涤树脂小颗粒,合并滤液、洗涤液至锥形瓶
中 (5)不变 (6)酚酞溶液 当滴入最后半滴NaOH标准溶液后,锥形瓶中溶液由无
色变为粉红色且半分钟内不恢复原色 (7)不可行 FeF 中的F-可能会与氢型阳离子
2
交换树脂中—SO H中的H+形成弱酸HF,使得氢型阳离子交换树脂释放出更多的氢离子,
3
导致实验产生误差
解析:(1)该实验中涉及准确量取V mL PbCl 饱和溶液(需要使用移液管,而不是
1 2
量筒),搅拌,静置,过滤,洗涤氢型阳离子交换树脂,合并滤液和洗涤液至锥形瓶中,
用氢氧化钠标准溶液进行滴定,从而测定氢离子的物质的量,故图中仪器用到的有漏斗、
碱式滴定管,用不到的有量筒、容量瓶。(2)由题干信息可知,K (PbCO )