文档内容
《化学》三色速记手册
【考点七】氮及其化合物
(一)氮气的性质及用途
1.化学性质
常温下,N 的化学性质很不活泼,可代替稀有气体做保护气,但在高温、放电、点燃等条件
2
下,N2能与 H、O、ⅡA 族的 Mg、Ca 等发生化学反应。
2 2
2.氮气的用途
合成氨;制硝酸;用作保护气,保护农副产品;液氮可作冷冻剂。
3.氮气的工业制法
工业上从液态空气中,利用液态氮的沸点比液态氧的沸点低加以分离而制得氮气
(二)氮的氧化物
1.氮氧化合物的种类
氮有+1、+2、+3、+4、+5 五种正化合价,可形成 N2O、NO、NO、NO、NO、NO 六种氧化
2 3 2 2 4 2 5
物,其中 NO 和NO 分别是 HNO 和 HNO 的酸酐。
2 3 2 5 2 3
2.NO和NO 的性质
2
(1)物理性质
NO:无色、无味的气体,有毒,微溶于水。
NO:红棕色有刺激性气味的有毒气体。
2
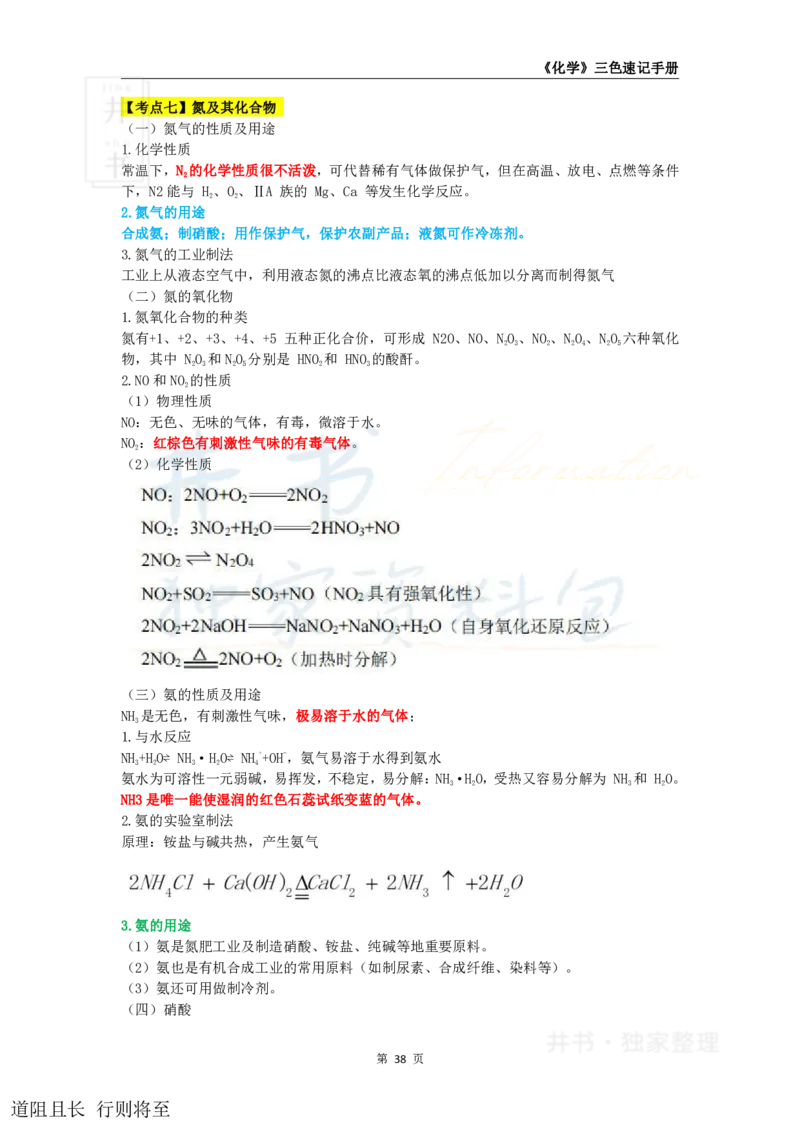
(2)化学性质
(三)氨的性质及用途
NH 是无色,有刺激性气味,极易溶于水的气体;
3
1.与水反应
NH+HO⇌ NH·HO⇌ NH++OH-,氨气易溶于水得到氨水
3 2 3 2 4
氨水为可溶性一元弱碱,易挥发,不稳定,易分解:NH·HO,受热又容易分解为 NH 和 HO。
3 2 3 2
NH3是唯一能使湿润的红色石蕊试纸变蓝的气体。
2.氨的实验室制法
原理:铵盐与碱共热,产生氨气
3.氨的用途
(1)氨是氮肥工业及制造硝酸、铵盐、纯碱等地重要原料。
(2)氨也是有机合成工业的常用原料(如制尿素、合成纤维、染料等)。
(3)氨还可用做制冷剂。
(四)硝酸
第 38 页《化学》三色速记手册
1.物理性质
(1)纯硝酸为无色、有刺激性气味的液体。
(2)硝酸沸点(83℃)低,易挥发,在空气中遇水蒸气呈白雾状。
(3)质量分数为 69%以上的硝酸称为浓硝酸。
2.化学性质
(1)强酸性
能与碱、CuO 等碱性氧化物、BaCO3等盐反应。稀硝酸使紫色石蕊试液变红,浓硝酸使石蕊
试液先变红(H+作用),加热后褪色(强氧化作用,即漂白作用)。用此可以证明浓硝酸的
氧化性比稀硝酸强。
(2)不稳定性
硝酸不稳定,见光或受热易分解,其反应方程式为:
存放:HNO 应盛放在棕色试剂瓶里,并存放在黑暗阴凉处。浓硝酸常呈黄色是因为 HNO 分
3 3
解产生的 NO2溶解于硝酸中,去掉硝酸中黄色的方法是通入少量O,发生的反应为:
2
4NO+O+2HO=4HNO
2 2 2 3
(3)强氧化性
①与金属的反应(大部分金属能与硝酸反应)
Cu+4HNO(浓)=Cu(NO)+2NO↑+2HO
3 3 2 2 2
3Cu+8HNO(稀)=3Cu(NO)+2NO↑+4HO
3 3 2 2
常温下,铁、铝遇冷的浓 HNO3 能发生钝化,原因是浓 HNO3使 Fe、Al表面生成一层致密
的氧化物薄膜,阻止了酸与内层金属的进一步反应,故常温下可用铁、铝容器盛装冷的浓
HNO。
3
②与非金属(木炭)的反应
③硝酸还能与其他还原剂,如 H2S、SO2、Na2SO3、FeSO4、KI、NaBr等发生氧化还原反应
3Fe2++4H++NO-=3Fe3++NO↑+2HO
3 2
6I-+8H++2NO-=3I+2NO↑+4HO
3 2 2
④王水
浓硝酸和浓盐酸按体积比 1:3 混合即为王水,它的氧化性更强,能溶解Pt、Au 等金属。
3.用途
制炸药、染料、塑料、硝酸盐。
第五章 有机化合物
【考点一】有机化合物定义
碳氢化合物及其衍生物
CO2-、CO、CO、CN-等
3 2
由于其性质与无机物相似,习惯上仍列为无机物
【考点二】有机化合物结构特点
1.数目庞大
2.结构复杂,种类繁多
(1)碳都是四价
(2)碳与其它原子以共价键结合
第 39 页《化学》三色速记手册
(3)原子按一定次序和方式相连
(4)同分异构
【考点三】有机化合物性质的特点
1.容易燃烧
大多数有机物都能燃烧(如汽油、棉花、酒精),大多数无机物都不能着火。(CCl 不但不
4
燃烧,反而能灭火)
有机物燃烧时炭化变黑,最终生成CO 和HO。
2 2
利用燃烧法可区别有机物和无机物。
2.熔、沸点较低
许多有机物在常温是气体、液体,即使常温为固体的有机物,熔点一般也很低,一般不超过
400℃。
固体无机物的熔点都在千度左右,如NaCl的熔点为808℃,氧化铝的熔点为2050℃。
3.难溶于水易溶于有机溶剂
一般有机物难溶于水而易溶于有机溶剂。
根据相似相溶原理,极性强的无机化合物易溶于极性强的水,极性弱的有机化合物易溶于极
性弱的有机溶剂。
一些极性较强的有机化合物(低级醇、羧酸、磺酸等)也溶于水。
4.稳定性差
多数有机物不如无机物稳定。例如维生素C
5.反应速度慢
无机物的离子反应,反应迅速,瞬息间即可完成。有机物的反应,多数是分子间的反应,往
往需要一定的能量,因此反应速度较慢,需要时间长,往往用加热、加催化剂、或光照等手
段来加速反应。
6.反应产物复杂
一个有机化合物在同样的反应条件下可以同时进行若干不同的反应,得到许多不同的产物。
一般把这个化合物主要进行的一个反应叫做主反应,其他的叫做副反应。
反应产物往往是混合物,有机反应产率达80%相当可观,有40%的产率就有合成价值。
【考点四】有机化合物分类
一、烷烃
(一)定义
只含有碳、氢两种元素的化合物称为碳氢化合物,简称烃
在烃类分子中,碳原子皆以单键(C-C)相连的称为烷烃。
(二)烷烃的同系列和通式
烷是饱和的意思。烃分子中碳原子之间以单键连接碳原子的其余化合价完全为氢原子所饱和。
CH 甲烷
4
CHCH 乙烷
3 3
CHCHCH 丙烷
3 2 3
CHCHCHCH 丁烷
3 2 2 3
通式:CH
n 2n+2
同系列:结构相似,组成上相差一个或多个CH 并具有同一通式的一系列化合物称为同系列。
2
同系物:同系列中的各个化合物之间互称为同系物。
同系列的系差:相差一个或若干个CH 原子团。
2
(三)烷烃的命名
通常把烷烃称为“某烷”,“某”是指烷烃中碳原子的数目。由一到十用甲、乙、丙、丁、
第 40 页《化学》三色速记手册
戊、己、庚、辛、壬、癸表示。如:C H ,叫十一烷。
11 24
(四)烷烃的物理性质
1.物态:
在常温下,C~C 的烷烃是气体,C~C 为液体C 以上为固体。直链烷烃随分子量增大而发
1 4 5 17 18
生物态变化。
2.(1)分子结构相似(同系列中的同系物)随分子量的增大(或C原子增多);分子间作
用力增大,熔沸点增高。
(2)分子式相同的烃,支链越多,熔沸点越低(如戊烷的3种同分异构体的沸点:正戊烷>
异戊烷>新戊烷)C原子5个以上的烷烃唯独新戊烷为气态
(五)烷烃的化学性质
1.取代反应
烷烃能与卤素在高温或光照条件下发生取代反应。
2.氧化反应(加氧去氢)
氧化:在有机分子中加入氧或去氢。
还原:在有机分子中加入氢或去掉氧。
①完全氧化:
CH+2O→CO+HO
4 2 2 2
应用:烷烃因为燃烧相对缓和,而常被用作燃料。
②不完全氧化
3.热裂反应
热裂反应:在高温及没有氧气的条件下发生键断裂的反应。
烷烃在800-1100°C的热裂产物主要是乙烯,其次为丙烯,丁烯,丁二烯和氢。
热裂反应相当复杂,热裂的同时,还有转变为较大分子的反应。
(六)甲烷
1.存在形式
甲烷是天然气、沼气、油田气和煤矿坑道气的主要成分。海底存在的“可燃冰”主要是天然
气水合物(CH4·nH2O)
2.甲烷的用途
是一种重要的燃料和化工原料(是合成氨和合成甲醇、汽油等工业的原料),甲烷分解生成
的炭黑是橡胶工业的原料。
3.甲烷的物理性质
是一种没有颜色、没有气味的气体,密度是0.717g/L(标准状况),极难溶于水。
4.甲烷的分子结构
第 41 页《化学》三色速记手册
二、不饱和烃
分子中含有碳碳双键或碳碳三键的开链烃,称为不饱和开链烃。不饱和开链烃分为烯烃和炔
烃。
(一)烯烃
1.烯烃定义
分子中含有碳碳双键的链烃称为烯烃,简称烯
通式:CH
n 2n
官能团:碳碳双键(C=C)
2.烯烃的理化性质
(1)物理性质
①沸点:直链α-烯烃的沸点随着分子中碳原子数的增多而升高。
②相对密度:都小于1,随着分子中碳原子数的增多,直链α-烯烃的相对密度逐渐增大。
③不溶于水,能溶解于非极性和弱极性的有机溶剂(相似相溶原理)
(3)化学性质
由于烯烃分子中的碳碳双键含有不稳定、易断裂的π键,因而化学性质都比较活泼,容易发
生加成、氧化、聚合等化学反应。
①加成反应
有机化合物分子中的双键中的π键断裂,加入其他原子或原子团的反应
②氧化反应
可燃性:易燃,并放出热量,燃烧时火焰明亮,并产生黑烟(乙烯燃烧不完全);
常温下容易被氧化剂氧化,如将乙烯通入酸性KMnO4溶液,溶液的紫色很快褪去
③加聚反应
(4)乙烯
乙烯是最重要的石油化工产品之一,乙烯的产量可以用来衡量一个国家石油化工发展水平的
标志。乙烯是无色、稍有气味的气体,难溶于水,标准状况下的密度为1.25g/L,比空气的
密度略小。
(二)炔烃
1.炔烃定义
分子中含有碳碳三键的链烃称为烯烃,简称炔
通式:CnH
2n-2
第 42 页《化学》三色速记手册
官能团:碳碳双键(CH≡CH)
2.炔烃的物理性质
(1)常温下乙炔、丙炔和1-丁炔为气体,含5-18个碳的炔烃为液体。
(2)炔烃难溶于水,易溶于极性小的丙酮、石油醚、四氯化碳及苯等有机溶剂。
(3)炔烃的熔沸点比相应的烷烃、烯烃高。
3.化学性质
由于炔烃分子中的碳碳三键含有不稳定、易断裂的π键,因而化学性质活泼,容易发生加成、
氧化、聚合等化学反应
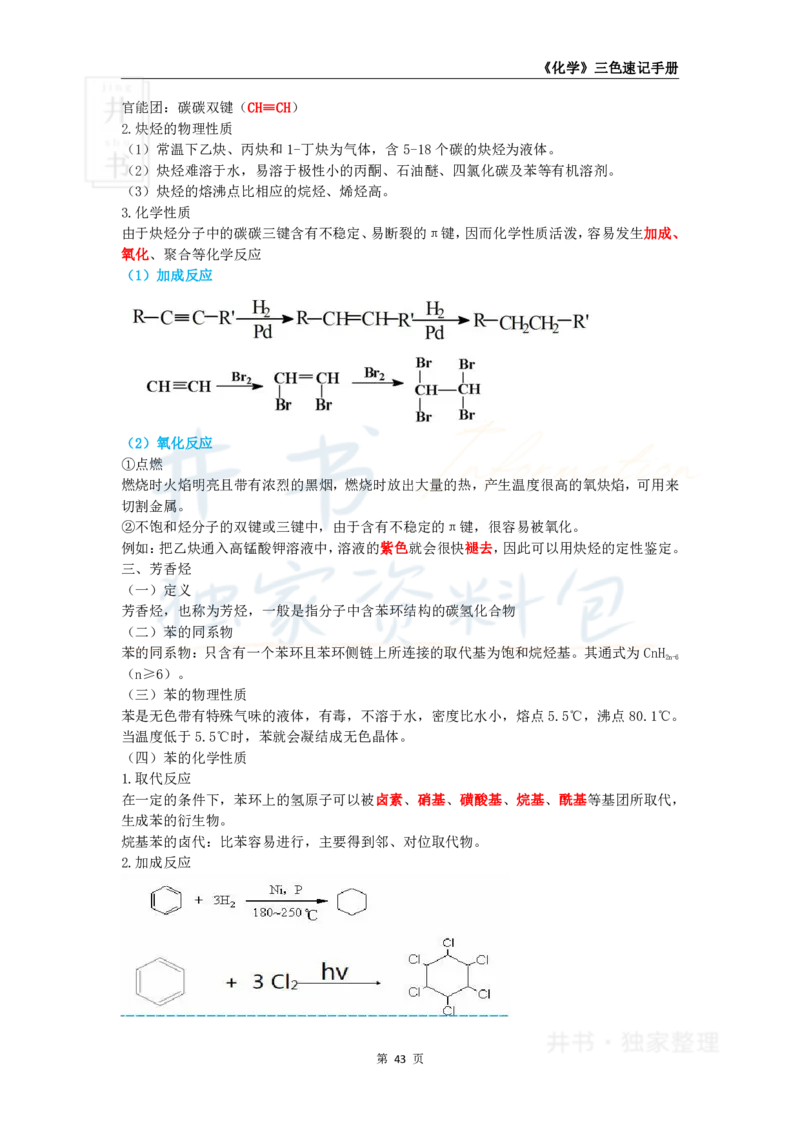
(1)加成反应
(2)氧化反应
①点燃
燃烧时火焰明亮且带有浓烈的黑烟,燃烧时放出大量的热,产生温度很高的氧炔焰,可用来
切割金属。
②不饱和烃分子的双键或三键中,由于含有不稳定的π键,很容易被氧化。
例如:把乙炔通入高锰酸钾溶液中,溶液的紫色就会很快褪去,因此可以用炔烃的定性鉴定。
三、芳香烃
(一)定义
芳香烃,也称为芳烃,一般是指分子中含苯环结构的碳氢化合物
(二)苯的同系物
苯的同系物:只含有一个苯环且苯环侧链上所连接的取代基为饱和烷烃基。其通式为CnH
2n-6
(n≥6)。
(三)苯的物理性质
苯是无色带有特殊气味的液体,有毒,不溶于水,密度比水小,熔点5.5℃,沸点80.1℃。
当温度低于5.5℃时,苯就会凝结成无色晶体。
(四)苯的化学性质
1.取代反应
在一定的条件下,苯环上的氢原子可以被卤素、硝基、磺酸基、烷基、酰基等基团所取代,
生成苯的衍生物。
烷基苯的卤代:比苯容易进行,主要得到邻、对位取代物。
2.加成反应
第 43 页