文档内容
《化学》三色速记手册
(五)铝的其他化合物及铝合金
1.明矾
化学式:KAl(SO)·12HO
4 2 2
属类:复盐(由两种不同的金属阳离子和一种酸根阴离子构成的化合物)。
明矾净水原理:
KAl(SO)·12HO溶解于水后发生反应
4 2 2
Al3++3HO ⇋ Al(OH)(胶体)+3H+
2 3
形成的Al(OH) 胶体吸附能力强
3
2.铝合金及其制品
(1)合金指的是由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的
物质。
(2)合金有比它的成分金属更优良的性质。
如:
①合金的熔点一般比它的各成分金属的低;
②合金的硬度一般比它的各成分金属的大;
③合金的化学性质也因成分金属的不同而不同。
3.金属铝与镁、铜、硅等金属或非金属熔合形成铝合金。铝合金具有密度小、强度高、塑性
好、易于成型、制造工艺简单、成本低廉等特点,并且有一定的抗腐蚀能力。铝合金可用于
建筑业、容器、包装业、交通运输、电子行业,并广泛用于制造飞机构件等。
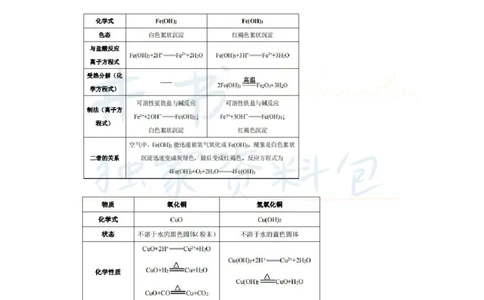
【考点三】铁、铜及其化合物
(一)铁、铜的物理性质
铁元素在周期表中位于第四周期第Ⅷ族,属于过渡金属。铁的粉末为黑色,纯净的铁块是银
白色金属,不仅有金属的通性(良好的导热性、延展性),而且易被磁铁吸引,也可被磁化。
铜元素在周期表中的位置是第四周期第IB族,属于过渡金属。铜是一种有金属光泽的紫红
色金属,质软,具有良好的导电导热性(仅次于银)、延展性。铜属于重金属、有色金属、
常见金属、不能被磁铁吸引
(二)铁、铜的化学性质
1.铁的化学性质
当铁与弱氧化剂(如盐酸、硫酸铜溶液等)反应时,只能失去2个电子形成Fe2+,当铁与强
氧化剂(如氯气、硝酸等)反应时,失去3个电子而形成Fe3+
(1)与非金属反应
第 31 页《化学》三色速记手册
由此可比较非金属单质的氧化性强弱:Cl、O 的氧化性比S强。
2 2
(2)与水蒸气反应(与冷、热水均不反应)
(3)与酸反应
与非氧化性酸:Fe+2H+=Fe2++H↑
2
与氧化性酸:
①在冷的浓HNO 或浓HSO 中钝化
3 2 4
②反应时,酸过量的产物为Fe3+
Fe+4HNO(稀)= Fe(NO)+NO↑+2HO
3 3 3 2
(4)与盐反应
Fe与CuSO 溶液反应的离子方程式:Fe+Cu2+ =Cu+Fe2+
4
Fe与FeCl 溶液反应的离子方程式:Fe+2Fe3+= 3Fe2+
3
2.铜的化学性质
(1)与非金属单质反应
(2)通入O 时,能与盐酸、硫酸反应
2
(3)与强氧化性酸(浓HSO、硝酸)反应
2 4
(4)与盐溶液反应
3.铁、铜常见化合物
氧化物 氧化亚铁(FeO) 氧化铁(FeO) 四氧化三铁(FeO)
2 3 3 4
第 32 页《化学》三色速记手册
俗名 — 铁红 磁性氧化铁
色态 黑色粉末 红棕色粉末 黑色晶体
铁元素
+2 +3 +2、+3
价态
与盐酸 + 2+ + 3+ + 2+ 3+
FeO+2H=Fe +HO FeO+6H=2Fe +3HO FeO+8H=Fe +2Fe +4HO
反应 2 2 3 2 3 4 2
与CO
的反应
炼铁、作铝热剂,
用途 色素 炼铁
作油漆的颜料
【考点四】碳、硅及其化合物
(一)碳、硅的结构、物理性质与用途
碳 硅
单质 金刚石、石墨、C 等 晶体硅和无定形硅
60
存在形式 既有游离态,又有化合态 仅有化合态
结构 金刚石:空间网状 晶体硅:与金刚石类似的空间网状结构
第 33 页《化学》三色速记手册
石墨:层状结构
金刚石熔点高、硬度大,石 晶体硅为灰黑色固体,有金属光泽、硬度大、
物理性质
墨熔点高,质软,有滑腻感 熔点高
金刚石用作切割刀具,石墨 晶体硅用作半导体材料、硅芯片和硅太阳能电
用途
用作电极、铅笔芯 池
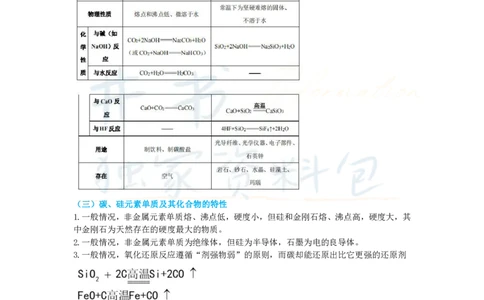
(二)碳、硅的氧化物
(三)碳、硅元素单质及其化合物的特性
1.一般情况,非金属元素单质熔、沸点低,硬度小,但硅和金刚石熔、沸点高,硬度大,其
中金刚石为天然存在的硬度最大的物质。
2.一般情况,非金属元素单质为绝缘体,但硅为半导体,石墨为电的良导体。
3.一般情况,氧化还原反应遵循“剂强物弱”的原则,而碳却能还原出比它更强的还原剂
4.非金属单质一般不能生成H2,但C、Si均可:
5.一般情况,较活泼金属+酸 = 盐+氢气,然而Si是非金属,却能与氢氟酸发生反应:
6.一般情况,酸性氧化物+碱 = 盐+水,SiO 是酸性氧化物,却能与氢氟酸反应
2
SiO+4HF =SiF↑+2HO
2 4 2
第 34 页《化学》三色速记手册
7.无机酸一般能溶于水,而HSiO 却难溶于水。
2 3
8.HCO 的酸性强于HSiO 且生成的硅酸为沉淀,所以有 NaSiO+CO+HO=HSiO↓+NaCO,
2 3 2 3 2 3 2 2 2 3 2 3
【考点五】氯、溴、碘及其化合物
(一)氯气的性质和用途
1.物理性质
通常氯气为黄绿色、有刺激性气味,密度比空气大的有毒气体,易液化。
25 ℃时,1体积水约溶解 2 体积氯气,其水溶液俗称氯水,为淡黄绿色。
2.化学性质
氯气的化学性质很活泼,是一种活泼的非金属单质,是强氧化剂
(1)与金属反应(与变价金属反应,将金属氧化至高价态)
(2)与非金属反应
(3)与水反应
(4)与碱反应
Cl+2NaOH=NaCl+NaClO+HO
2 2
2Cl+2Ca(OH)=CaCl+Ca(ClO)+2HO
2 2 2 2 2
(5)与还原性物质反应
Cl+SO+2HO=HSO+2HCl
2 2 2 2 4
2KI+Cl=2KCl+I
2 2
2FeCl+Cl=2FeCl
2 2 3
(二)氯气的制备
1.氯气的实验室制法
用强氧化性物质(如 MnO、KMnO、KClO 等)和浓盐酸反应。
2 4 3
2.氯气工业制法
第 35 页《化学》三色速记手册
电解饱和食盐水
(三)氯离子的检验
在用AgNO 溶液检验Cl-时,一般先在被检测的溶液中滴入少量稀硝酸使其酸化,以排除干
3
扰离子。
(四)氯气的用途
制漂白粉,消毒,制盐酸、农药、氯仿等。
(五)卤素中某些特性及相关应用
1.氟
(1)无正价和含氧酸,非金属性最强
(2)与H 反应在暗处即爆炸
2
(3)HF是弱酸,能腐蚀玻璃,有毒,在HX中沸点最高
2.溴
(1)溴是深红棕色液体,易挥发
(2)溴易溶于有机溶剂
(3)盛溴的试剂瓶加水,进行水封,保存液溴不能用橡胶塞
(4)AgBr作为感光材料用于照相(在AgX中,除了AgF外,均具有感光性)
3.碘
(1)I 遇淀粉变蓝色
2
(2)I 加热时易升华
2
(3)I 易溶于有机溶剂
2
(4)食盐中加入KIO 可防止甲状腺肿大
3
【考点六】氧、硫及其化合物
(一)硫的性质和用途
硫(俗称硫黄)是一种淡黄色晶体,质脆,易研成粉末。
硫不溶于水,微溶于酒精,易溶于CS。
2
硫是一种生命元素,组成某些蛋白质时离不开它,这也正是石油、天然气、煤等化石燃料中
经常含硫的原因。
(二)化学性质
1.与非金属单质反应
现象:硫在空气中燃烧发出淡蓝色火焰,在纯氧中燃烧发出蓝紫色火焰。
2.与金属单质反应
3.与强氧化性酸反应
4.与强碱反应
第 36 页《化学》三色速记手册
(三)二氧化硫
二氧化硫对环境的污染及治理
(1)二氧化硫的污染:SO 是污染大气的主要有害物质之一,对人体的直接危害是引起呼
2
吸道疾病,严重时致人死亡。
(2)酸雨的形成和危害:大气中 SO 和 NO 溶于水后形成酸性溶液,随雨水下降,就可能
2 2
形成酸雨,酸雨的 pH 小于 5.6。酸雨能直接破坏农作物、森林、草原,使土壤、湖泊酸化、
还会加速建筑物、工业设备和名胜古迹的腐蚀。
(3)治理方法:空气中的二氧化硫主要来自化石燃料(煤和石油)的燃烧,以及含硫矿石
的冶炼和硫肥、磷肥、纸浆生产等产生的工业废气。消除污染的主要方法之一是减少SO 的
2
排放。
(四)硫酸的性质和用途
1.物理性质
无色油状液体,难挥发,密度比水大;类属于二元强酸,稀硫酸具有酸的通性。
2.硫酸稀释方法
将浓硫酸沿器壁慢慢注入水中,并不断搅拌。
3.硫酸的特性
(1)强氧化性
(2)吸水性:浓硫酸常做干燥剂,但不能干燥 NH、HS、HI 等
3 2
(3)脱水性:将有机物质中氢、氧元素的原子按 2:1 脱成水,如使蔗糖变黑
(4)浓硫酸与金属的反应
①钝化:常温下,冷浓硫酸对 Al、Fe 有“钝化”作用,可用铝槽车装运
②活泼金属(如 Zn)
开始产生 SO,浓度变小后产生 H。
2 2
③不活泼金属(如 Cu)
开始产生 SO(加热),浓度变小后,稀硫酸不再与 Cu 反应。
2
第 37 页