文档内容
考点 51 物质的制备
本考点试题常以制备某无机物或某有机物为背景进行设计。考查常见仪器的正确使用、物质间的反应、
物质分离、提纯的基本操作、实验方案的评价与设计、实验安全及事故处理方法等。涉及装置的选择、仪
器的连接顺序、物质的纯化、尾气的处理等等。试题涉及知识面广,形式灵活多变。旨在考查考生化学实
验与探究的能力及科学探究与创新意识的核心素养。
预测2023年考查的角度有仪器的识别与应用、物质的制备、除杂与分离、物质的性质探究与验证、实
验现象的分析与描述、实验结论的评价与计算。
一、无机物的制备
二、有机物的制备
无机物的制备
1.气体的制备
发生
装置
搭配仪器的顺序:从下往上,从左往右
净化
装置
净化装置:“长”进“短”出量气装置:“短”进“长”出
干燥管:“粗”进“细”出
收集
装置
尾气
处理
装置
①制备在空气中易吸水、潮解、变质以及水解的物质(如Al S 、AlCl
2 2 3
等),往往在装置末端再接一个干燥装置,以防止空气中水蒸气的进入。
特殊 ②用液体吸收气体,若气体溶解度较大,要加防倒吸装置。
实验 ③若制备物易与空气中的O、CO 等反应,应加排空气装置。
2 2
装置 ④使用可燃性气体如H 、CO、CH 等,先用原料气赶走系统内的空气,
2 4
分析 再点燃酒精灯加热,以防止爆炸。
⑤制备一些易与空气中的成分发生反应的物质(如H 还原CuO的实验),
2
反应结束时,应先熄灭酒精灯,继续通原料气至试管冷却
2.实验条件的控制
常见的操作 思考方向
加过量试剂 使反应完全进行(或增大产率、转化率)
加氧化剂(如HO) 氧化还原性物质,生成目标产物或除去某种离子
2 2
通入N 或其他惰性气体 除去装置中的空气,排除氧气的干扰
2
末端放置干燥管 防止空气中的水蒸气干扰实验
①调节溶液的酸碱性,抑制水解(或使其中某些金属离子形成氢
氧化物沉淀) ②“酸作用”还可除去氧化物(膜) ③“碱作用”
调节溶液的pH
还可除去油污,除去铝片氧化膜,溶解铝、二氧化硅等④特定
的氧化还原反应需要的酸性条件(或碱性条件)
①防止副反应的发生②使化学平衡移动;控制化学反应的方向
③控制固体的溶解与结晶(如趁热过滤能防止某物质降温时析
控制温度 出)④控制反应速率;使催化剂达到最大活性⑤升温:促进溶液
中的气体逸出,使某物质达到沸点挥发⑥加热煮沸:促进水
(水浴、冰浴、油浴)
解,聚沉后利于过滤分离⑦趁热过滤:减少因降温而析出的溶
质的量⑧降温:防止物质高温分解或挥发;降温(或减压)可以
减少能源成本,降低对设备的要求
①水洗:通常是为了除去晶体表面水溶性的杂质②“冰水洗
涤”:能洗去晶体表面的杂质离子,且防止晶体在洗涤过程中
的溶解损耗③用特定有机试剂清洗晶体:洗去晶体表面的杂
洗涤晶体
质,降低晶体的溶解度、有利于析出,减少损耗等④洗涤沉淀
方法:往漏斗中加入蒸馏水至浸没沉淀,待水自然流下后,重
复以上操作2~3次
分离、提纯 过滤、蒸发、萃取、分液、蒸馏等。从溶液中得到晶体的方法:蒸发浓缩→冷却结晶→过滤→洗涤→干燥
3.常用的计算方法
实验题中涉及的计算主要有:样品的质量分数或纯度的计算,物质的转化率或产率、物质的量浓度、
物质的质量的计算。
(1)计算公式:n=,n=,n=cV(aq);物质的质量分数(或纯度)=×100%; 产品产率=×100%;物质的
转化率=×100%
(2)计算方法:关系式法常应用于一步反应或分多步进行的连续反应中,利用该法可以节省不必要的中
间运算过程,避免计算错误,并能迅速准确地获得结果。一步反应中可以直接找出反应物与目标产物的关
系;在多步反应中,若第一步反应的产物是下一步反应的反应物,可以根据化学方程式将某中间物质作为
“中介”,找出已知物质和所求物质之间量的关系。
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)用碳酸钠粉末可以制备CO( )
2
(2)用铁片和稀HSO 反应制取H 时,为加快产生H 的速率可改用浓HSO ( )
2 4 2 2 2 4
(3)加热分解NH HCO 固体,将所得的气体进行适当处理可获得NH ( )
4 3 3
(4)用KMnO 固体和用KClO 固体制备O 的装置完全相同( )
4 3 2
(5)由MgCl 溶液制备无水MgCl :将MgCl 溶液加热蒸干( )
2 2 2
(6)用向上排空气法收集铜粉和稀硝酸反应产生的NO( )
(7)排水法收集KMnO 分解产生的O:先熄灭酒精灯,后移出导管( )
4 2
(8)浓盐酸与MnO 反应制备纯净Cl:气体产物先通过浓硫酸,后通过饱和食盐水( )
2 2
【典例】
例1 (2022•全国甲卷)硫化钠可广泛用于染料、医药行业。工业生产的硫化钠粗品中常含有一定量的
煤灰及重金属硫化物等杂质。硫化钠易溶于热乙醇,重金属硫化物难溶于乙醇。实验室中常用95%乙醇重
结晶纯化硫化钠粗品。回答下列问题:
(1)工业上常用芒硝(Na SO ·10H O)和煤粉在高温下生产硫化钠,同时生成CO,该反应的化学方程式
2 4 2
为_______。
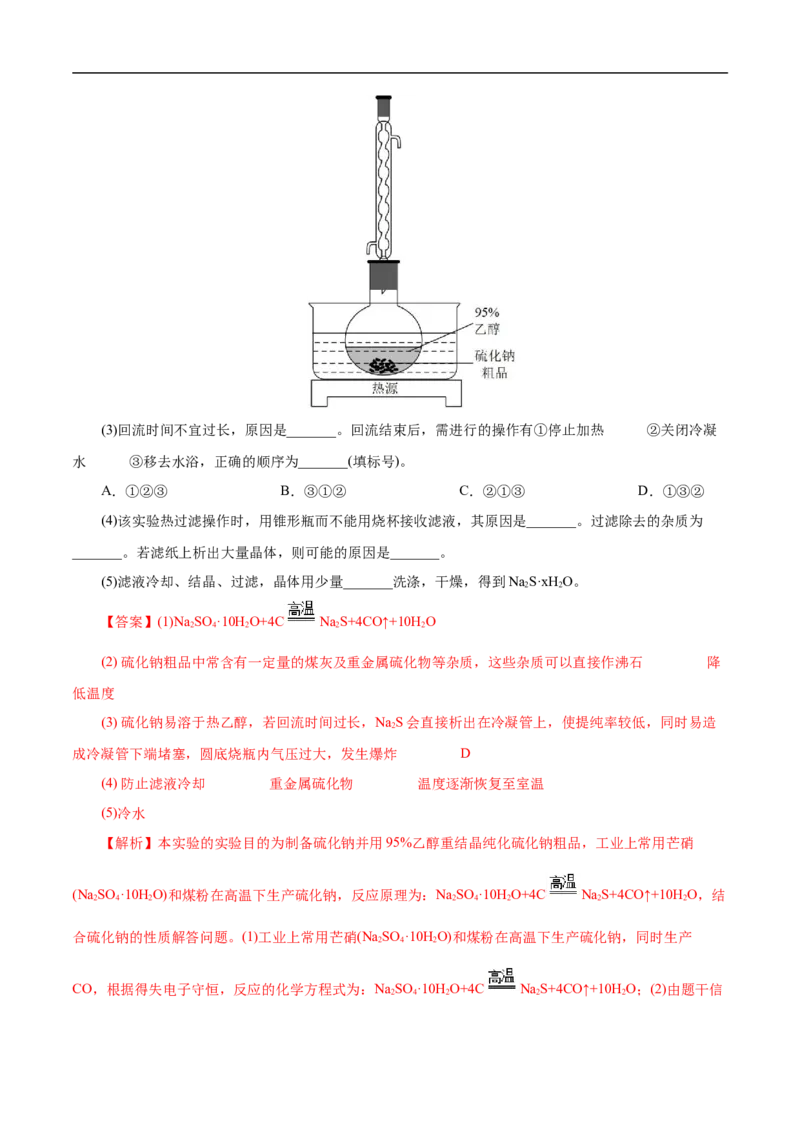
(2)溶解回流装置如图所示,回流前无需加入沸石,其原因是_______。回流时,烧瓶内气雾上升高度
不宜超过冷凝管高度的1/3.若气雾上升过高,可采取的措施是_______。(3)回流时间不宜过长,原因是_______。回流结束后,需进行的操作有①停止加热 ②关闭冷凝
水 ③移去水浴,正确的顺序为_______(填标号)。
A.①②③ B.③①② C.②①③ D.①③②
(4)该实验热过滤操作时,用锥形瓶而不能用烧杯接收滤液,其原因是_______。过滤除去的杂质为
_______。若滤纸上析出大量晶体,则可能的原因是_______。
(5)滤液冷却、结晶、过滤,晶体用少量_______洗涤,干燥,得到NaS·xHO。
2 2
【答案】(1)Na SO ·10H O+4C NaS+4CO↑+10H O
2 4 2 2 2
(2) 硫化钠粗品中常含有一定量的煤灰及重金属硫化物等杂质,这些杂质可以直接作沸石 降
低温度
(3) 硫化钠易溶于热乙醇,若回流时间过长,NaS会直接析出在冷凝管上,使提纯率较低,同时易造
2
成冷凝管下端堵塞,圆底烧瓶内气压过大,发生爆炸 D
(4) 防止滤液冷却 重金属硫化物 温度逐渐恢复至室温
(5)冷水
【解析】本实验的实验目的为制备硫化钠并用95%乙醇重结晶纯化硫化钠粗品,工业上常用芒硝
(Na SO ·10H O)和煤粉在高温下生产硫化钠,反应原理为:NaSO ·10H O+4C NaS+4CO↑+10H O,结
2 4 2 2 4 2 2 2
合硫化钠的性质解答问题。(1)工业上常用芒硝(Na SO ·10H O)和煤粉在高温下生产硫化钠,同时生产
2 4 2
CO,根据得失电子守恒,反应的化学方程式为:NaSO ·10H O+4C NaS+4CO↑+10H O;(2)由题干信
2 4 2 2 2息,生产的硫化钠粗品中常含有一定量的煤灰及重金属硫化物等杂质,这些杂质可以直接作沸石,因此回
流前无需加入沸石,若气流上升过高,可直接降低降低温度,使气压降低;(3)硫化钠易溶于热乙醇,若回
流时间过长,NaS会直接析出在冷凝管上,使提纯率较低,同时易造成冷凝管下端堵塞,圆底烧瓶内气压
2
过大,发生爆炸;回流结束后,先停止加热,再移去水浴后再关闭冷凝水,故正确的顺序为①③②,故选
D。(4)硫化钠易溶于热乙醇,使用锥形瓶可有效防止滤液冷却,重金属硫化物难溶于乙醇,故过滤除去的
杂质为重金属硫化物,由于硫化钠易溶于热乙醇,过滤后温度逐渐恢复至室温,滤纸上便会析出大量晶体;
(5)乙醇与水互溶,硫化钠易溶于热乙醇,因此将滤液冷却、结晶、过滤后,晶体可用少量冷水洗涤,再干
燥,即可得到NaS·xHO。
2 2
例2 (2022•海南省选择性考试)胆矾(CuSO ·5H O)是一种重要化工原料,某研究小组以生锈的铜屑为
4 2
原料[主要成分是Cu,含有少量的油污、CuO、CuCO、Cu(OH) ]制备胆矾。流程如下。
3 2
回答问题:
(1)步骤①的目的是_______。
(2)步骤②中,若仅用浓HSO 溶解固体B,将生成_______(填化学式)污染环境。
2 4
(3)步骤②中,在HO 存在下Cu溶于稀HSO ,反应的化学方程式为_______。
2 2 2 4
(4)经步骤④得到的胆矾,不能用水洗涤的主要原因是_______。
(5)实验证明,滤液D能将I-氧化为I。
2
ⅰ.甲同学认为不可能是步骤②中过量HO 将I-氧化为I,理由是_______。
2 2 2
ⅱ.乙同学通过实验证实,只能是Cu2+将I-氧化为I,写出乙同学的实验方案及结果_______(不要求写具
2
体操作过程)。
【答案】(1)除油污 (2)SO
2
(3) Cu+ H O+ H SO =CuSO+2H O
2 2 2 4 4 2
(4)胆矾晶体易溶于水
(5) 溶液 C 经步骤③加热浓缩后双氧水已完全分解 取滤液,向其中加入适量硫化钠,使铜
离子恰好完全沉淀,再加入I-,不能被氧化
【解析】由流程中的信息可知,原料经碳酸钠溶液浸洗后过滤,可以除去原料表面的油污;滤渣固体
B与过量的稀硫酸、双氧水反应,其中的CuO、CuCO、Cu(OH) 均转化为CuSO ,溶液C为硫酸铜溶液
3 2 4
和稀硫酸的混合液,加热浓缩、冷却结晶、过滤后得到胆矾。(1)原料表面含有少量的油污,NaCO 溶液呈
2 3
碱性,可以除去原料表面的油污,因此,步骤①的目的是:除去原料表面的油污。(2)在加热的条件下,铜可以与浓硫酸发生反应生成CuSO 、SO 和HO,二氧化硫是一种大气污染物,步骤②中,若仅用浓HSO
4 2 2 2 4
溶解固体B,将生成SO 污染环境。(3)步骤②中,在HO 存在下Cu溶于稀HSO ,生成CuSO 和HO,
2 2 2 2 4 4 2
该反应的化学方程式为Cu+ HO+ H SO =CuSO+2H O。(4)胆矾是一种易溶于水的晶体,因此,经步骤④
2 2 2 4 4 2
得到的胆矾,不能用水洗涤的主要原因是:胆矾晶体易溶于水,用水洗涤会导致胆矾的产率降低。(5)ⅰ.
HO 常温下即能发生分解反应,在加热的条件下,其分解更快,因此,甲同学认为不可能是步骤②中过量
2 2
HO 将I-氧化为I,理由是:溶液C经步骤③加热浓缩后HO 已完全分解。ⅱ. I-氧化为I 时溶液的颜色会
2 2 2 2 2 2
发生变化;滤液D中含有CuSO 和HSO ,乙同学通过实验证实,只能是Cu2+将I-氧化为I,较简单的方案
4 2 4 2
是除去溶液中的Cu2+,然后再向其中加入含有I-的溶液,观察溶液是否变色;除去溶液中的Cu2+的方法有
多种,可以加入适当的沉淀剂将其转化为难溶物,如加入NaS将其转化为CuS沉淀,因此,乙同学的实
2
验方案为取少量滤液D,向其中加入适量NaS溶液,直至不再有沉淀生成,静置后向上层清液中加入少量
2
KⅠ溶液;实验结果为:上层清液不变色,证明I-不能被除去Cu2+的溶液氧化,故只能是Cu2+将I-氧化为
I。
2
【对点提升】
对点1 (2021•全国乙卷)氧化石墨烯具有稳定的网状结构,在能源、材料等领域有着重要的应用前景,
通过氧化剥离石墨制备氧化石墨烯的一种方法如下(转置如图所示):
Ⅰ.将浓HSO 、NaNO 、石墨粉末在c中混合,置于冰水浴中,剧烈搅拌下,分批缓慢加入KMnO 粉
2 4 3 4
末,塞好瓶口。
Ⅱ.转至油浴中,35℃搅拌1小时,缓慢滴加一定量的蒸馏水。升温至98℃并保持1小时。
Ⅲ.转移至大烧杯中,静置冷却至室温。加入大量蒸馏水,而后滴加HO 至悬浊液由紫色变为土黄色。
2 2
Ⅳ.离心分离,稀盐酸洗涤沉淀。
Ⅴ.蒸馏水洗涤沉淀。
Ⅵ.冷冻干燥,得到土黄色的氧化石墨烯。回答下列问题:
(1)装置图中,仪器a、c的名称分别是_______、_______,仪器b的进水口是_______(填字母)。
(2)步骤Ⅰ中,需分批缓慢加入KMnO 粉末并使用冰水浴,原因是_______。
4
(3)步骤Ⅱ中的加热方式采用油浴,不使用热水浴,原因是_______。
(4)步骤Ⅲ中,HO 的作用是_______(以离子方程式表示)。
2 2
(5)步骤Ⅳ中,洗涤是否完成,可通过检测洗出液中是否存在SO 2-来判断。检测的方法是_______。
4
(6)步骤Ⅴ可用pH试纸检测来判断Cl-是否洗净,其理由是_______。
对点2 硫酸亚铁晶体FeSO ·7H O 在医药上作补血剂。工业上用废铁生产FeSO ·7H O 的一种流程如
4 2 4 2
下图所示:
(1)步骤 I 中除铁和硫酸、铁锈和硫酸反应外, 还有一个反应的化学方程式为_______:步骤 I 加入
稀硫酸的量不能过量的原因是_______;步骤 II 加入稀硫酸的目的是_______。
(2)证明步骤 (1)滤液中只含有Fe2+ 的方法: 取样, 先滴加 KSCN 溶液, 无明显现象, 再滴加
_______; 该过程的现象为:_______。
(3)步骤 III 从硫酸亚铁溶液中获得硫酸亚铁晶体 (FeSO ·7H O) 的实验操作为_______、_______、过
4 2
滤、冰水洗涤、烘干。烘干操作需在低温条件下进行, 原因是_______。
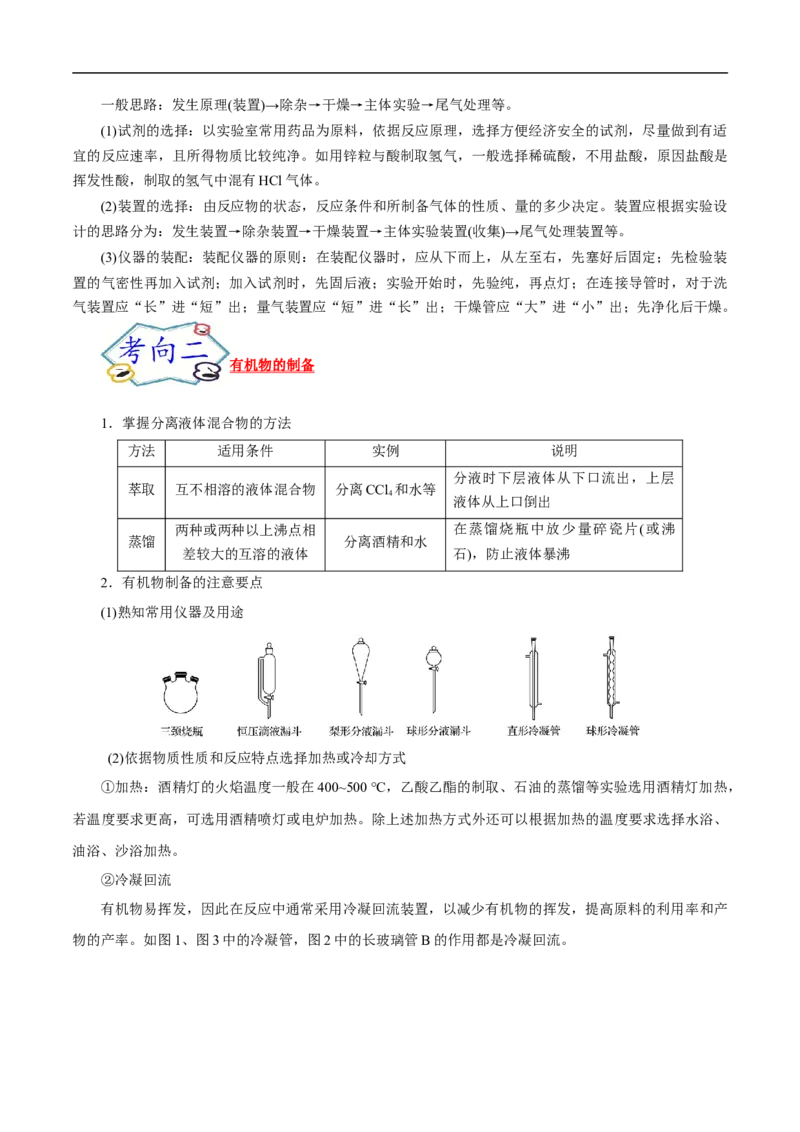
(4)取27.8gFeSO·7H O隔绝空气加热至不同温度, 剩余固体的质量变化如下图所示。
4 2
分析数据, 写出 残留物的化学式_______; 时固体物质发生反应的化学方程式是_______,做出这一判断的依据是_______。
【答案】(1) Fe+Fe (SO )=3 FeSO 确保生成物全部都是硫酸亚铁; 防止亚铁离子水解;
2 4 3 4
(2) 氯水; 溶液变成血红色;
(3) 蒸发浓缩; 冷却结晶 防止FeSO ·7H O分解失去部分结晶水
4 2
(4) FeSO ·H O 2 FeSO Fe O+SO↑+SO↑ FeSO ·7H O为0.1mol,加热分解到C点后
4 2 4 2 3 2 3 4 2
质量不再变化,C为铁的氧化物。剩余固体是8g,铁元素的质量为5.6g,则氧元素的质量为2.4g,可得出
氧化物中铁和氧原子个数比为2:3,故为Fe O。根据氧化还原反应规律推断铁元素化合价升高,必有元
2 3
素化合价降低,则有生成SO ,由质量守恒定律得出化学反应为:2 FeSO Fe O+SO↑+SO↑。
2 4 2 3 2 3
【解析】根据题中信息知废铁中含有铁、铁锈和不溶性杂质。步骤I加稀硫酸,铁和铁锈与硫酸,生
成的硫酸铁也会和铁反应生成硫酸亚铁,过滤后可除去不溶性杂质;在步骤II加稀硫酸是为了抑制亚铁离
子水解,得到的硫酸亚铁溶液经过步骤III:蒸发浓缩、冷却结晶可得到FeSO ·7H O晶体。(1)铁锈与硫酸
4 2
反应生成硫酸铁,硫酸铁能够继续与铁反应生成硫酸亚铁,化学方程式为:Fe+Fe (SO )=3 FeSO ;在步骤
2 4 3 4
I加稀硫酸不能过量,是为了确保生成物全部是硫酸亚铁,得到的产物更纯净,不用后续除杂;在步骤II
加稀硫酸是为了抑制亚铁离子水解,防止得到的晶体中有杂质;(2)检验亚铁离子,先加KSCN溶液无现象,
再加氯水将亚铁离子氧化成铁离子,若出现血红色,则有亚铁离子。故加入的试剂为氯水,现象为溶液变
成血红色;(3)要得到带结晶水的晶体,通常采用蒸发浓缩、冷却结晶的方法。硫酸亚铁溶液经过蒸发浓缩、
冷却结晶可得到FeSO ·7H O晶体;FeSO ·7H O受热易失去结晶水,因此低温烘干是为了防止FeSO ·7H O
4 2 4 2 4 2
晶体失去结晶水;(4)27.8g FeSO ·7H O的物质的量为0.1mol,结晶水完全失去时剩下固体的质量为:
4 2
,由图可知B( )完全失去结晶水,成分为FeSO ,对比B( )和A(
4
)点,两者质量差为 ,即A比B多一个结晶水,A点成分为:FeSO ·H O;自始至终,
4 2
铁元素质量守恒,FeSO ·7H O为0.1mol,加热分解到C( )点后质量不再变化,C点成分为铁的氧化
4 2
物。剩余固体是8g,铁元素的质量为5.6g,则氧元素的质量为2.4g,可得出氧化物中铁和氧原子个数比为
2:3,故为Fe O。根据氧化还原反应规律推断铁元素化合价升高,必有元素化合价降低,则有生成SO ,
2 3 2
由质量守恒定律得出化学反应为:2 FeSO Fe O+SO↑+SO↑。
4 2 3 2 3
【巧学妙记】
基本流程:根据目标产物→确定可能原理→设计可能实验方案→优化实验方案→选择原料→设计反应
装置(方法、仪器等)→实施实验(步骤、操作要点、控制反应条件等)→分离提纯产品。一般思路:发生原理(装置)→除杂→干燥→主体实验→尾气处理等。
(1)试剂的选择:以实验室常用药品为原料,依据反应原理,选择方便经济安全的试剂,尽量做到有适
宜的反应速率,且所得物质比较纯净。如用锌粒与酸制取氢气,一般选择稀硫酸,不用盐酸,原因盐酸是
挥发性酸,制取的氢气中混有HCl气体。
(2)装置的选择:由反应物的状态,反应条件和所制备气体的性质、量的多少决定。装置应根据实验设
计的思路分为:发生装置→除杂装置→干燥装置→主体实验装置(收集)→尾气处理装置等。
(3)仪器的装配:装配仪器的原则:在装配仪器时,应从下而上,从左至右,先塞好后固定;先检验装
置的气密性再加入试剂;加入试剂时,先固后液;实验开始时,先验纯,再点灯;在连接导管时,对于洗
气装置应“长”进“短”出;量气装置应“短”进“长”出;干燥管应“大”进“小”出;先净化后干燥。
有机物的制备
1.掌握分离液体混合物的方法
方法 适用条件 实例 说明
分液时下层液体从下口流出,上层
萃取 互不相溶的液体混合物 分离CCl 和水等
4
液体从上口倒出
两种或两种以上沸点相 在蒸馏烧瓶中放少量碎瓷片(或沸
蒸馏 分离酒精和水
差较大的互溶的液体 石),防止液体暴沸
2.有机物制备的注意要点
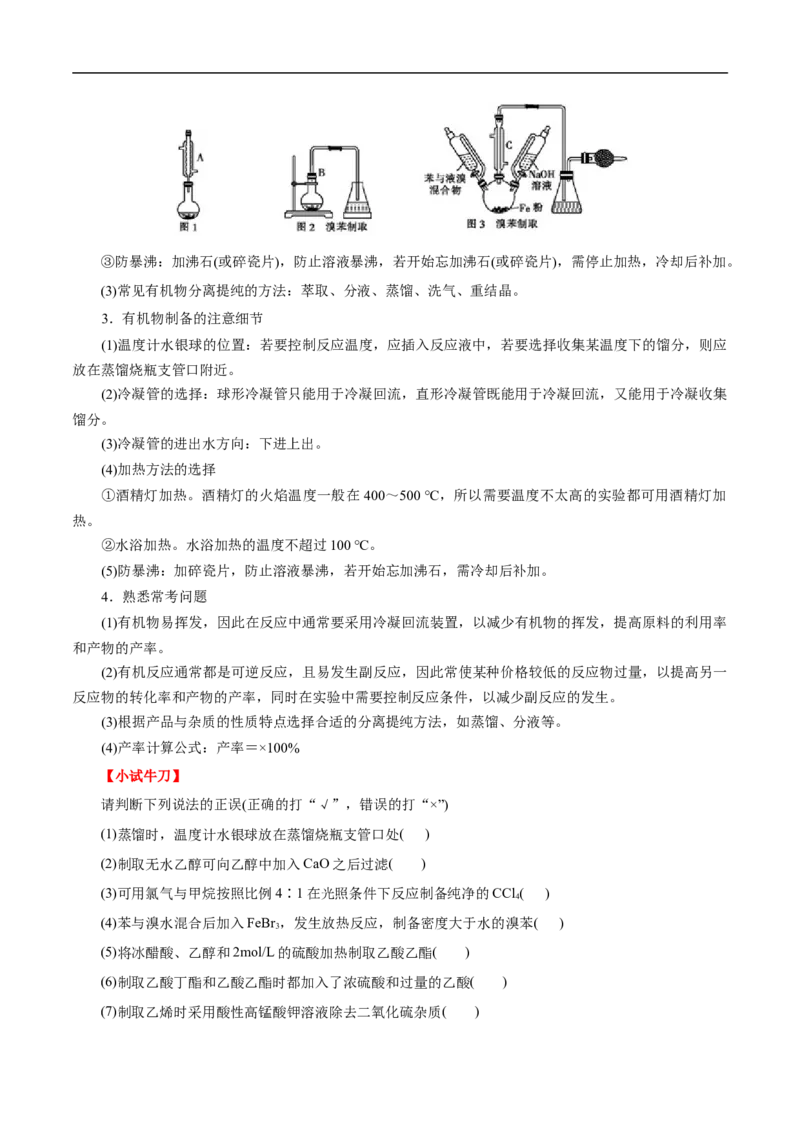
(1)熟知常用仪器及用途
(2)依据物质性质和反应特点选择加热或冷却方式
①加热:酒精灯的火焰温度一般在400~500 ℃,乙酸乙酯的制取、石油的蒸馏等实验选用酒精灯加热,
若温度要求更高,可选用酒精喷灯或电炉加热。除上述加热方式外还可以根据加热的温度要求选择水浴、
油浴、沙浴加热。
②冷凝回流
有机物易挥发,因此在反应中通常采用冷凝回流装置,以减少有机物的挥发,提高原料的利用率和产
物的产率。如图1、图3中的冷凝管,图2中的长玻璃管B的作用都是冷凝回流。③防暴沸:加沸石(或碎瓷片),防止溶液暴沸,若开始忘加沸石(或碎瓷片),需停止加热,冷却后补加。
(3)常见有机物分离提纯的方法:萃取、分液、蒸馏、洗气、重结晶。
3.有机物制备的注意细节
(1)温度计水银球的位置:若要控制反应温度,应插入反应液中,若要选择收集某温度下的馏分,则应
放在蒸馏烧瓶支管口附近。
(2)冷凝管的选择:球形冷凝管只能用于冷凝回流,直形冷凝管既能用于冷凝回流,又能用于冷凝收集
馏分。
(3)冷凝管的进出水方向:下进上出。
(4)加热方法的选择
①酒精灯加热。酒精灯的火焰温度一般在400~500 ℃,所以需要温度不太高的实验都可用酒精灯加
热。
②水浴加热。水浴加热的温度不超过100 ℃。
(5)防暴沸:加碎瓷片,防止溶液暴沸,若开始忘加沸石,需冷却后补加。
4.熟悉常考问题
(1)有机物易挥发,因此在反应中通常要采用冷凝回流装置,以减少有机物的挥发,提高原料的利用率
和产物的产率。
(2)有机反应通常都是可逆反应,且易发生副反应,因此常使某种价格较低的反应物过量,以提高另一
反应物的转化率和产物的产率,同时在实验中需要控制反应条件,以减少副反应的发生。
(3)根据产品与杂质的性质特点选择合适的分离提纯方法,如蒸馏、分液等。
(4)产率计算公式:产率=×100%
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)蒸馏时,温度计水银球放在蒸馏烧瓶支管口处( )
(2)制取无水乙醇可向乙醇中加入CaO之后过滤( )
(3)可用氯气与甲烷按照比例4∶1在光照条件下反应制备纯净的CCl( )
4
(4)苯与溴水混合后加入FeBr ,发生放热反应,制备密度大于水的溴苯( )
3
(5)将冰醋酸、乙醇和2mol/L的硫酸加热制取乙酸乙酯( )
(6)制取乙酸丁酯和乙酸乙酯时都加入了浓硫酸和过量的乙酸( )
(7)制取乙烯时采用酸性高锰酸钾溶液除去二氧化硫杂质( )(8)制取乙酸乙酯时,导管应插入碳酸钠溶液中( )
(9)利用乙烷和氯气在催化剂存在的条件下制备氯乙烷( )
(10)实验室制备硝基苯加入试剂的顺序为:先加入浓硫酸,再滴加浓硝酸,最后滴加苯( )
【典例】
例1 (2020•新课标Ⅱ卷)苯甲酸可用作食品防腐剂。实验室可通过甲苯氧化制苯甲酸,其反应原理简
示如下:
+KMnO → + MnO +HCl→ +KCl
4 2
相对分子 密度/
名称 熔点/℃ 沸点/℃ 溶解性
质量 (g·mL−1)
不溶于水,易溶
甲苯 92 −95 110.6 0.867
于乙醇
苯甲 122.4(100℃左右 微溶于冷水,易
122 248 ——
酸 开始升华) 溶于乙醇、热水
实验步骤:
(1)在装有温度计、冷凝管和搅拌器的三颈烧瓶中加入1.5 mL甲苯、100 mL水和4.8 g(约0.03 mol)高锰
酸钾,慢慢开启搅拌器,并加热回流至回流液不再出现油珠。
(2)停止加热,继续搅拌,冷却片刻后,从冷凝管上口慢慢加入适量饱和亚硫酸氢钠溶液,并将反应混
合物趁热过滤,用少量热水洗涤滤渣。合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化至苯甲酸
析出完全。将析出的苯甲酸过滤,用少量冷水洗涤,放在沸水浴上干燥。称量,粗产品为1.0 g。
(3)纯度测定:称取0. 122 g粗产品,配成乙醇溶液,于100 mL容量瓶中定容。每次移取25. 00 mL溶
液,用0.01000 mol·L−1的KOH标准溶液滴定,三次滴定平均消耗21. 50 mL的KOH标准溶液。
回答下列问题:
(1)根据上述实验药品的用量,三颈烧瓶的最适宜规格为______(填标号)。
A.100 mL B.250 mL C.500 mL D.1000 mL
(2)在反应装置中应选用______冷凝管(填“直形”或“球形”),当回流液不再出现油珠即可判断反应
已完成,其判断理由是______。
(3)加入适量饱和亚硫酸氢钠溶液的目的是___________;该步骤亦可用草酸在酸性条件下处理,请用
反应的离子方程式表达其原理__________。
(4)“用少量热水洗涤滤渣”一步中滤渣的主要成分是_______。
(5)干燥苯甲酸晶体时,若温度过高,可能出现的结果是_______。(6)本实验制备的苯甲酸的纯度为_______;据此估算本实验中苯甲酸的产率最接近于_______(填标号)。
A.70% B.60% C.50% D.40%
(7)若要得到纯度更高的苯甲酸,可通过在水中__________的方法提纯。
【答案】(1)B (2)球形 无油珠说明不溶于水的甲苯已经被完全氧化
(3)除去过量的高锰酸钾,避免在用盐酸酸化时,产生氯气
2 MnO-+5H C O+6H+=2Mn2++10CO ↑+8H O
4 2 2 4 2 2
(4)MnO (5)苯甲酸升华而损失 (6)86.0% C (7)重结晶
2
【解析】(1)加热液体,所盛液体的体积不超过三颈烧瓶的一半,三颈烧瓶中已经加入100m的水,
1.5mL甲苯,4.8g高锰酸钾,应选用250mL的三颈烧瓶,故选B;(2)为增加冷凝效果,在反应装置中宜选
用球形冷凝管,当回流液中不再出现油珠时,说明反应已经完成,因为:没有油珠说明不溶于水的甲苯已
经完全被氧化;(3)高锰酸钾具有强氧化性,能将Cl-氧化。加入适量的饱和亚硫酸氢钠溶液是为了除去过
量的高锰酸钾,避免在用盐酸酸化时,产生氯气;该步骤亦可用草酸处理,生成二氧化碳和锰盐,离子方
程式为:5HC O+2MnO -+6H+=2Mn2++10CO↑+8HO;(4)由信息甲苯用高锰酸钾氧化时生成苯甲酸
2 2 4 4 2 2
钾和二氧化锰,“用少量热水洗涤滤渣”一步中滤渣的主要成分是:MnO ;(5)苯甲酸100℃时易升华,干
2
燥苯甲酸时,若温度过高,苯甲酸升华而损失;(6)由关系式C HCOOH~KOH得,苯甲酸的纯度为:
6 5
×100%=86.0%;1.5mL甲苯理论上可得到苯甲酸的质
量: =1.72g,产品的产率为 ×100%=50%;(7)提纯苯甲酸可
用重结晶的方法。
例2 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:
可能用到的有关数据如下:
相对分子质量 密度/ g·cm-3 沸点/℃ 溶解性
环己醇 100 0.961 8 161 微溶于水环己烯 82 0.810 2 83 难溶于水
合成反应:
在a中加入20 g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1 mL浓硫酸。b中通入冷却水后,开始
缓慢加热a,控制馏出物的温度不超过90 ℃。
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置
一段时间后弃去氯化钙。最终通过蒸馏得到纯净环己烯10 g。
回答下列问题:
(1)装置b的名称是________。
(2)加入碎瓷片的作用是______________________________________________;
如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是________(填字母)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为_____________________________。
(4)分液漏斗在使用前须清洗干净并________;在本实验分离过程中,产物应该从分液漏斗的
________(填“上口倒出”或“下口放出”)。
(5)分离提纯过程中加入无水氯化钙的目的是______________________________。
(6)在环己烯粗产物蒸馏过程中,不可能用到的仪器有________(填字母,下同)。
A.圆底烧瓶 B.温度计 C.吸滤瓶 D.球形冷凝管 E.接收器
(7)本实验所得到的环己烯产率是________。
A.41% B.50% C.61% D.70%
【答案】(1)直形冷凝管 (2)防止暴沸 B
(3) (4)检漏 上口倒出
(5)干燥(或除水除醇) (6)CD (7)C
【解析】(1)装置b为直形冷凝管,可用于冷凝回流。(2)加入碎瓷片的作用是防止有机物在加热时发生
暴沸。如果在加热时发现忘记加碎瓷片,这时必须停止加热,待冷却后补加碎瓷片。(3)醇分子间最容易发
生脱水反应生成醚类化合物。(4)分液漏斗在使用前必须要检漏。实验生成的环己烯的密度比水的要小,所
以环己烯应从上口倒出。(5)加入无水氯化钙的目的:除去水(做干燥剂)和除去环己醇(因为乙醇可以和氯化
钙反应,类比推知,环己醇和氯化钙也可以反应)。(6)观察题中实验装置图知蒸馏过程中不可能用到吸滤
瓶及球形冷凝管。(7)20 g环己醇的物质的量为=0.2 mol,理论上生成环己烯的物质的量为0.2 mol,环己烯
的质量为0.2 mol×82 g·mol-1=16.4 g,实际得到环己烯的质量为10 g,则产率为×100%≈61%。
【对点提升】
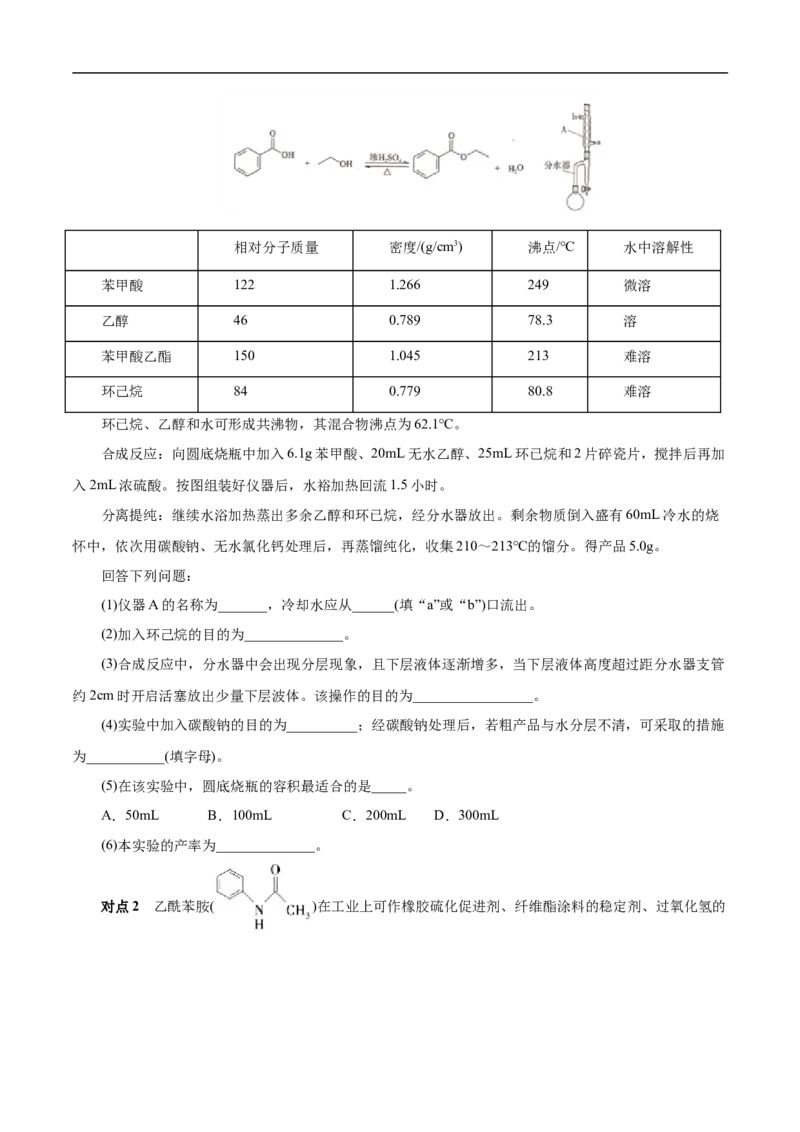
对点1 实验室制备苯甲酸乙酯的反应装置示意图和有关数据如下:相对分子质量 密度/(g/cm3) 沸点/℃ 水中溶解性
苯甲酸 122 1.266 249 微溶
乙醇 46 0.789 78.3 溶
苯甲酸乙酯 150 1.045 213 难溶
环己烷 84 0.779 80.8 难溶
环已烷、乙醇和水可形成共沸物,其混合物沸点为62.1℃。
合成反应:向圆底烧瓶中加入6.1g苯甲酸、20mL无水乙醇、25mL环已烷和2片碎瓷片,搅拌后再加
入2mL浓硫酸。按图组装好仪器后,水裕加热回流1.5小时。
分离提纯:继续水浴加热蒸出多余乙醇和环已烷,经分水器放出。剩余物质倒入盛有60mL冷水的烧
怀中,依次用碳酸钠、无水氯化钙处理后,再蒸馏纯化,收集210~213℃的馏分。得产品5.0g。
回答下列问题:
(1)仪器A的名称为_______,冷却水应从______(填“a”或“b”)口流出。
(2)加入环己烷的目的为______________。
(3)合成反应中,分水器中会出现分层现象,且下层液体逐渐增多,当下层液体高度超过距分水器支管
约2cm时开启活塞放出少量下层波体。该操作的目的为_________________。
(4)实验中加入碳酸钠的目的为__________;经碳酸钠处理后,若粗产品与水分层不清,可采取的措施
为___________(填字母)。
(5)在该实验中,圆底烧瓶的容积最适合的是_____。
A.50mL B.100mL C.200mL D.300mL
(6)本实验的产率为______________。
对点2 乙酰苯胺( )在工业上可作橡胶硫化促进剂、纤维酯涂料的稳定剂、过氧化氢的稳定剂等,可通过本胺( )和乙酸酐( )反应制得。
已知:纯乙酰苯胺是白色片状晶体,相对分子质量为135,熔点为114℃,易溶于有机溶剂。在水中的
溶解度如下。
温度 20 25 50 80 100
溶解度/(g/100g水) 0.46 0.56 0.84 3.45 5.5
实验室制备乙酰苯胺的步骤如下(部分装置省略):
Ⅰ.粗乙酰苯胺的制备。将7mL(0.075mol)乙酸酐放入三口烧瓶c中,在恒压滴液漏斗a中放入
5mL(0.055mol)新制得的苯胺。将苯胺在室温下逐滴滴加到三口烧瓶中。苯胺滴加完毕,在石棉网上用小火
加热回流30min,使之充分反应。待反应完成,在不断搅拌下,趁热把反应混合物缓慢地倒入盛有100mL
冷水的烧杯中,乙酰苯胺晶体析出。充分冷却至室温后,减压过滤,用_______洗涤晶体2~3次。用滤液冲
洗烧杯上残留的晶体,再次过滤,两次过滤得到的固体合并在一起。
Ⅱ.乙酰苯胺的提纯。将上述制得的粗乙酰苯胺固体移入250mL烧杯中,加入100mL热水,加热至沸腾,
待粗乙酰苯胺完全溶解后,再补加少量蒸馏水。稍冷后,加入少量活性炭吸附色素等杂质,在搅拌下微沸
5min,趁热过滤。待滤液冷却至室温,有晶体析出,_______,称量产品为3.28g。
回答下列问题:
(1)仪器b的名称是_______。
(2)写出反应的化学方程式_____________________________________。
(3)减压过滤的优点是_____________________________________;步骤Ⅰ用滤液而不用冷水冲洗烧杯的
原因是洗涤晶体宜选用_______(填字母)。
A.乙醇 B.CCl C.冷水 D.乙醚
4
(4)步骤Ⅱ中,粗乙酰苯胺溶解后,补加少量蒸馏水的目的是_______。
(5)步骤Ⅱ中,称量前的操作是_______。上述提纯乙酰苯胺的方法叫_______。
(6)乙酰苯胺的产率为_______。(计算结果保留3位有效数字)【巧学妙记】
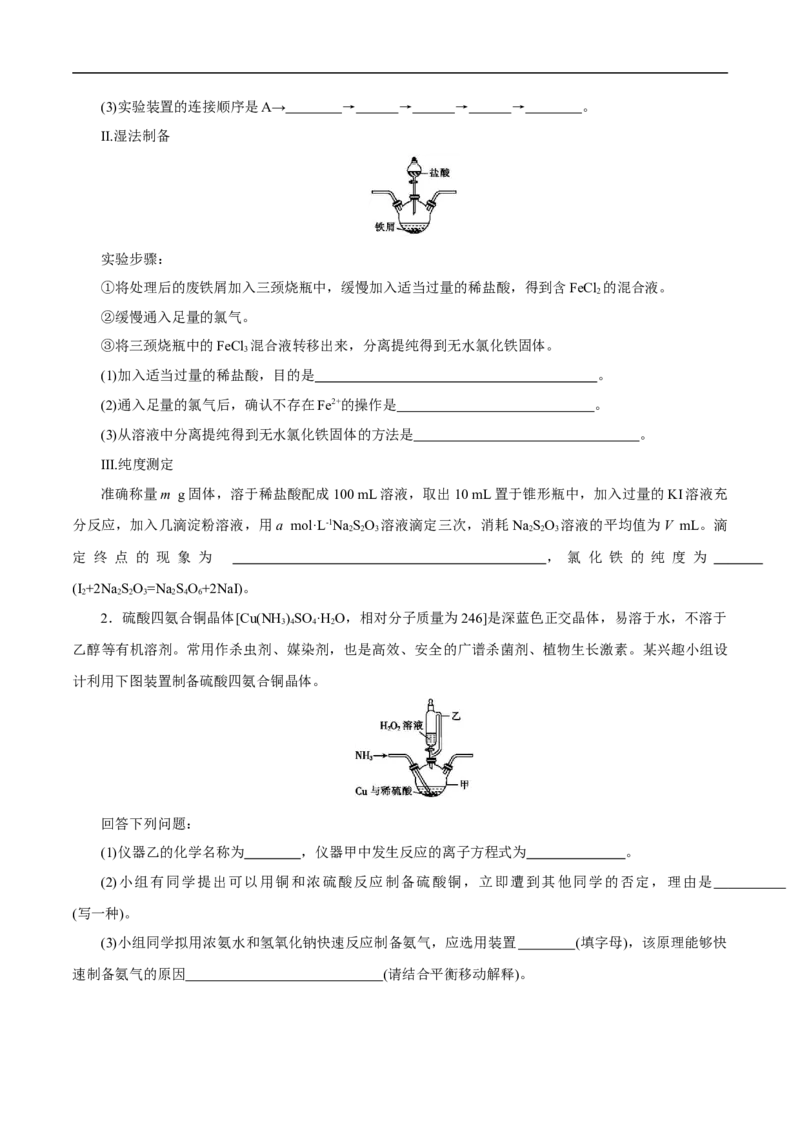
有机物制备的思维流程
1.氯化铁在工农业生产中有着广泛应用。某化学活动小组以废铁屑为原料,设计探究氯化铁制备的
实验方案。
查阅资料:①无水氯化铁在100 ℃左右时升华。②氯化铁遇水蒸气强烈水解。
Ⅰ.干法制取
(1)预处理的目的是除去铁屑表面附着的油脂,操作方法为 。
(2)仪器甲的名称为 ,装置A中反应的离子方程式为 。(3)实验装置的连接顺序是A→ → → → → 。
Ⅱ.湿法制备
实验步骤:
①将处理后的废铁屑加入三颈烧瓶中,缓慢加入适当过量的稀盐酸,得到含FeCl 的混合液。
2
②缓慢通入足量的氯气。
③将三颈烧瓶中的FeCl 混合液转移出来,分离提纯得到无水氯化铁固体。
3
(1)加入适当过量的稀盐酸,目的是 。
(2)通入足量的氯气后,确认不存在Fe2+的操作是 。
(3)从溶液中分离提纯得到无水氯化铁固体的方法是 。
Ⅲ.纯度测定
准确称量m g固体,溶于稀盐酸配成100 mL溶液,取出10 mL置于锥形瓶中,加入过量的KI溶液充
分反应,加入几滴淀粉溶液,用a mol·L-1NaSO 溶液滴定三次,消耗NaSO 溶液的平均值为V mL。滴
2 2 3 2 2 3
定 终 点 的 现 象 为 , 氯 化 铁 的 纯 度 为
(I+2Na SO=Na SO+2NaI)。
2 2 2 3 2 4 6
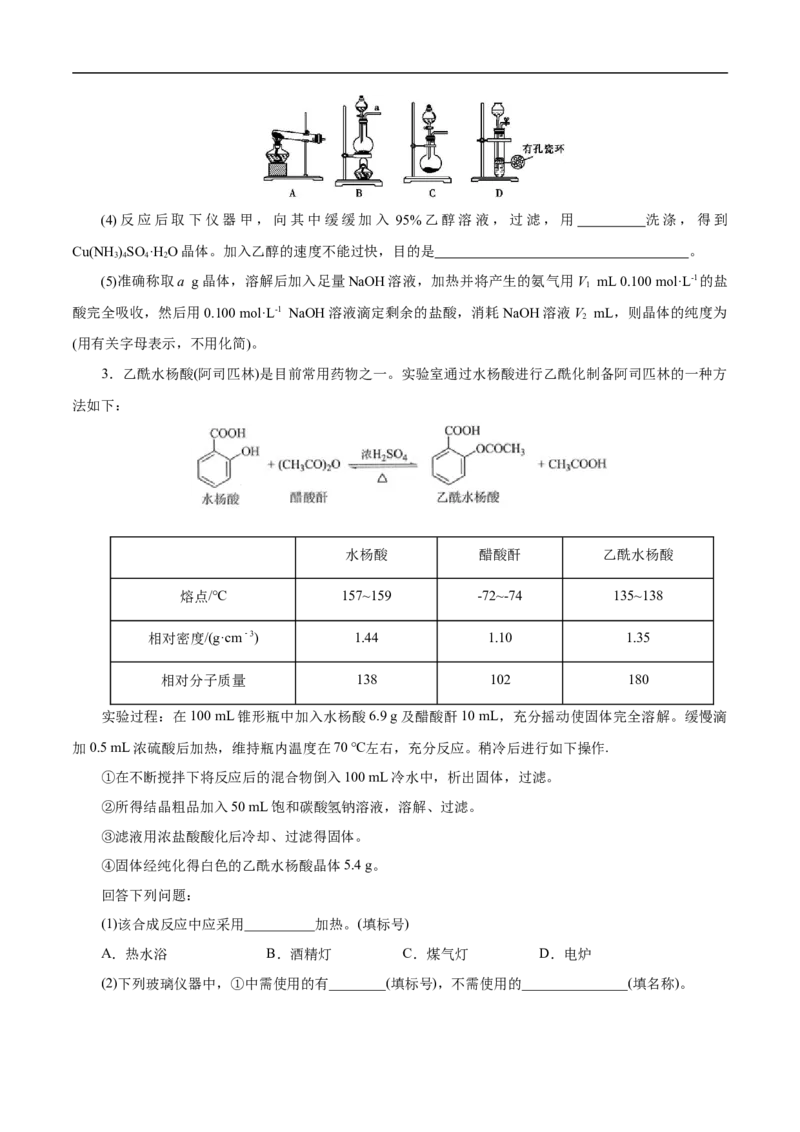
2.硫酸四氨合铜晶体[Cu(NH )SO ·H O,相对分子质量为246]是深蓝色正交晶体,易溶于水,不溶于
3 4 4 2
乙醇等有机溶剂。常用作杀虫剂、媒染剂,也是高效、安全的广谱杀菌剂、植物生长激素。某兴趣小组设
计利用下图装置制备硫酸四氨合铜晶体。
回答下列问题:
(1)仪器乙的化学名称为 ,仪器甲中发生反应的离子方程式为 。
(2)小组有同学提出可以用铜和浓硫酸反应制备硫酸铜,立即遭到其他同学的否定,理由是
(写一种)。
(3)小组同学拟用浓氨水和氢氧化钠快速反应制备氨气,应选用装置 (填字母),该原理能够快
速制备氨气的原因 (请结合平衡移动解释)。(4)反应后取下仪器甲,向其中缓缓加入 95%乙醇溶液,过滤,用 洗涤,得到
Cu(NH )SO ·H O晶体。加入乙醇的速度不能过快,目的是 。
3 4 4 2
(5)准确称取a g晶体,溶解后加入足量NaOH溶液,加热并将产生的氨气用V mL 0.100 mol·L-1的盐
1
酸完全吸收,然后用0.100 mol·L-1 NaOH溶液滴定剩余的盐酸,消耗NaOH溶液V mL,则晶体的纯度为
2
(用有关字母表示,不用化简)。
3.乙酰水杨酸(阿司匹林)是目前常用药物之一。实验室通过水杨酸进行乙酰化制备阿司匹林的一种方
法如下:
水杨酸 醋酸酐 乙酰水杨酸
熔点/℃ 157~159 -72~-74 135~138
相对密度/(g·cm﹣3) 1.44 1.10 1.35
相对分子质量 138 102 180
实验过程:在100 mL锥形瓶中加入水杨酸6.9 g及醋酸酐10 mL,充分摇动使固体完全溶解。缓慢滴
加0.5 mL浓硫酸后加热,维持瓶内温度在70 ℃左右,充分反应。稍冷后进行如下操作.
①在不断搅拌下将反应后的混合物倒入100 mL冷水中,析出固体,过滤。
②所得结晶粗品加入50 mL饱和碳酸氢钠溶液,溶解、过滤。
③滤液用浓盐酸酸化后冷却、过滤得固体。
④固体经纯化得白色的乙酰水杨酸晶体5.4 g。
回答下列问题:
(1)该合成反应中应采用__________加热。(填标号)
A.热水浴 B.酒精灯 C.煤气灯 D.电炉
(2)下列玻璃仪器中,①中需使用的有________(填标号),不需使用的_______________(填名称)。(3)①中需使用冷水,目的是______________________________________。
(4)②中饱和碳酸氢钠的作用是____________________,以便过滤除去难溶杂质。
(5)④采用的纯化方法为____________。
(6)本实验的产率是_________%。
4.苯甲酰氯( )是制备染料、香料、药品和树脂的重要中间体。以光气法制备苯甲酰氯的原理
如下(该反应为放热反应):
+COCl → +CO +HCl
2 2
已知物质性质如下表:
物质 熔点/℃ 沸点/℃ 溶解性
苯甲酸 122.1 249 微溶于水,易溶于乙醇、乙醚等有机溶剂
较易溶于苯、甲苯等。遇水迅速水解,生成氯
碳酰氯(COCl ) -188 8.2 化氢,与氨很快反应,主要生成尿素
2
[CO(NH)]和氯化铵等无毒物质
2 2
溶于乙醚、氯仿和苯。遇水或乙醇逐渐分解,
苯甲酰氯 -1 197
生成苯甲酸或苯甲酸乙酯和氯化氢
不溶于水,溶于醇、苯。极易挥发,稳定性
三氯甲烷CHCl ) -63.5 63.1
3 差,450℃以上发生热分解
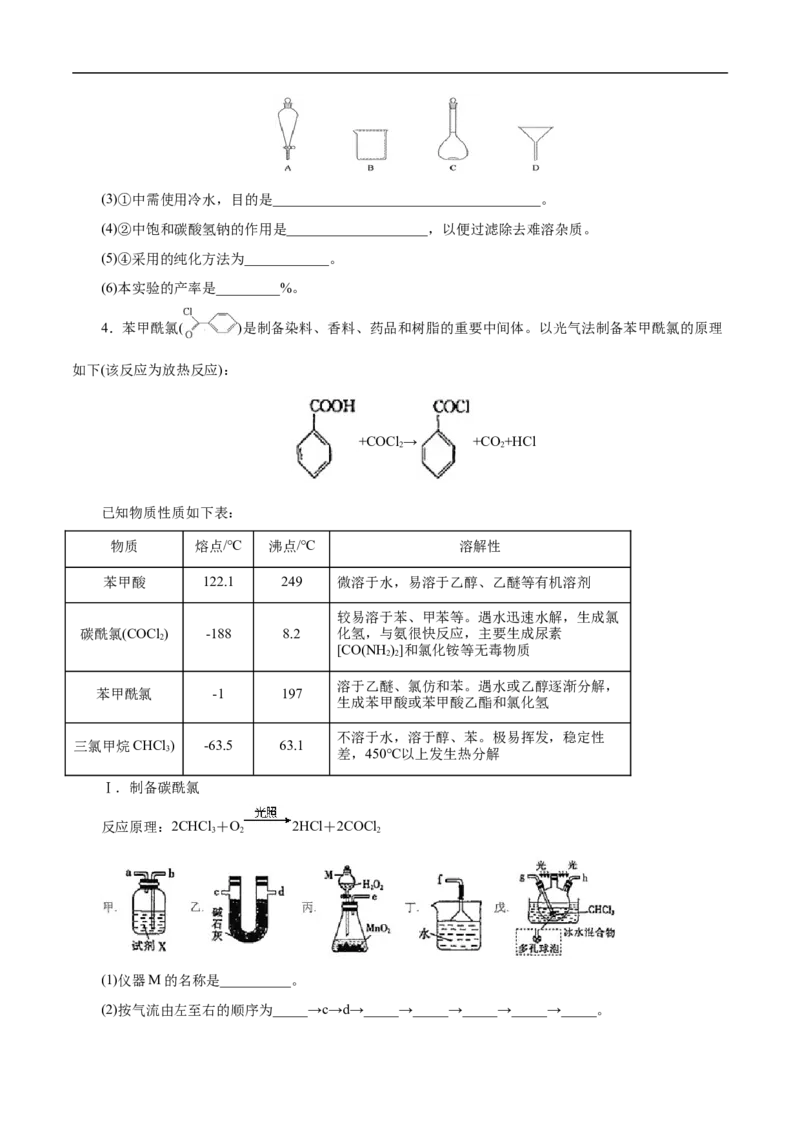
Ⅰ.制备碳酰氯
反应原理:2CHCl +O 2HCl+2COCl
3 2 2
(1)仪器M的名称是__________。
(2)按气流由左至右的顺序为_____→c→d→_____→_____→_____→_____→_____。(3)试剂X是______(填名称)。
(4)装置乙中碱石灰的作用是___________________。
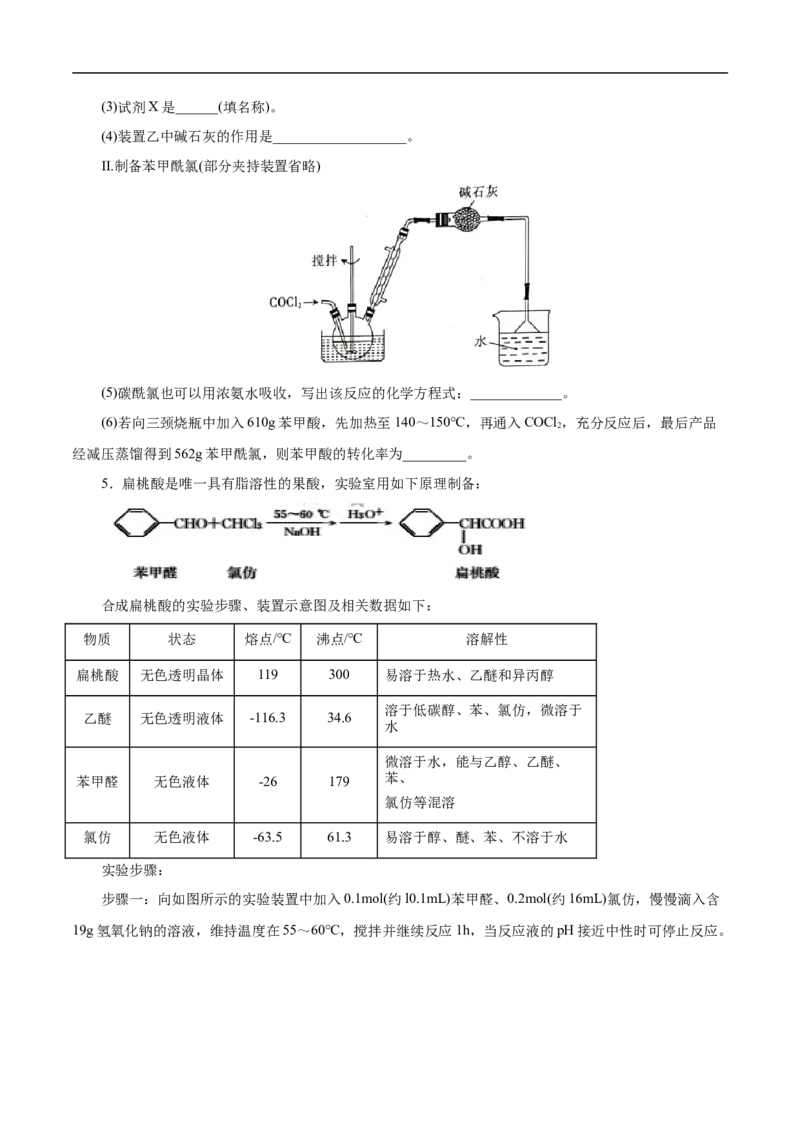
II.制备苯甲酰氯(部分夹持装置省略)
(5)碳酰氯也可以用浓氨水吸收,写出该反应的化学方程式:_____________。
(6)若向三颈烧瓶中加入610g苯甲酸,先加热至140~150℃,再通入COCl ,充分反应后,最后产品
2
经减压蒸馏得到562g苯甲酰氯,则苯甲酸的转化率为_________。
5.扁桃酸是唯一具有脂溶性的果酸,实验室用如下原理制备:
合成扁桃酸的实验步骤、装置示意图及相关数据如下:
物质 状态 熔点/℃ 沸点/℃ 溶解性
扁桃酸 无色透明晶体 119 300 易溶于热水、乙醚和异丙醇
溶于低碳醇、苯、氯仿,微溶于
乙醚 无色透明液体 -116.3 34.6
水
微溶于水,能与乙醇、乙醚、
苯甲醛 无色液体 -26 179 苯、
氯仿等混溶
氯仿 无色液体 -63.5 61.3 易溶于醇、醚、苯、不溶于水
实验步骤:
步骤一:向如图所示的实验装置中加入0.1mol(约l0.1mL)苯甲醛、0.2mol(约16mL)氯仿,慢慢滴入含
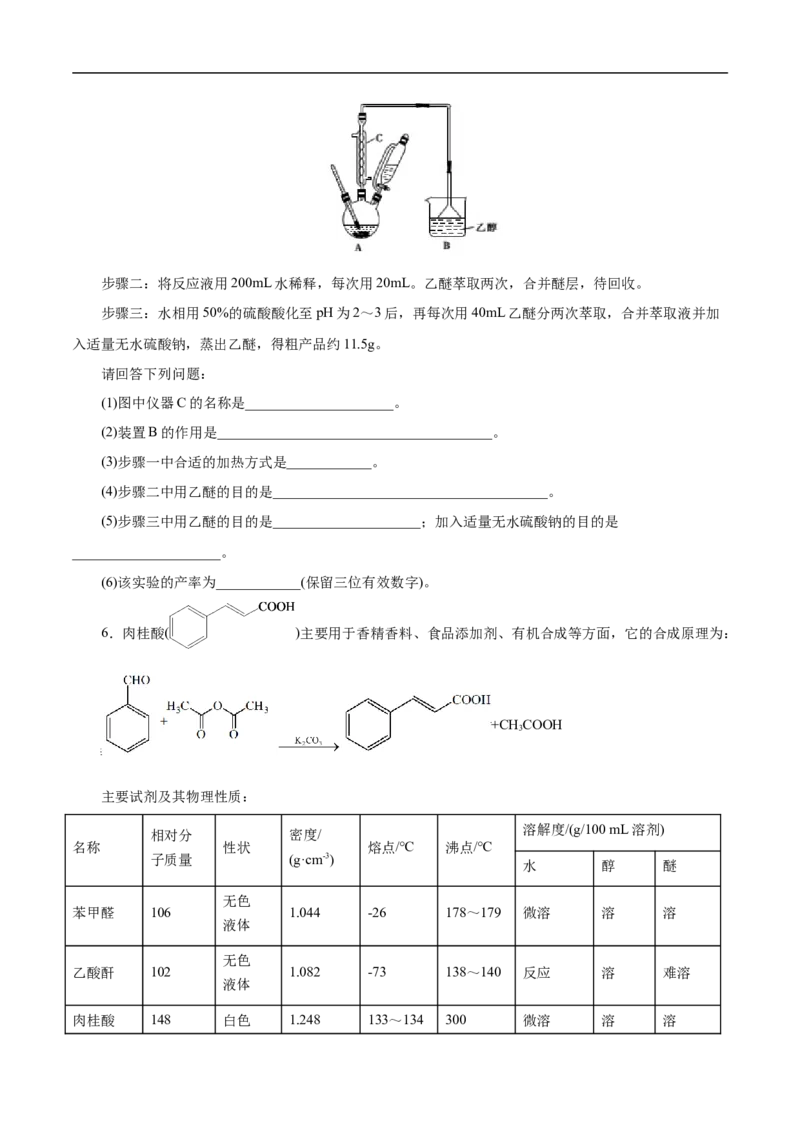
19g氢氧化钠的溶液,维持温度在55~60℃,搅拌并继续反应1h,当反应液的pH接近中性时可停止反应。步骤二:将反应液用200mL水稀释,每次用20mL。乙醚萃取两次,合并醚层,待回收。
步骤三:水相用50%的硫酸酸化至pH为2~3后,再每次用40mL乙醚分两次萃取,合并萃取液并加
入适量无水硫酸钠,蒸出乙醚,得粗产品约11.5g。
请回答下列问题:
(1)图中仪器C的名称是_____________________。
(2)装置B的作用是_______________________________________。
(3)步骤一中合适的加热方式是____________。
(4)步骤二中用乙醚的目的是_______________________________________。
(5)步骤三中用乙醚的目的是_____________________;加入适量无水硫酸钠的目的是
_____________________。
(6)该实验的产率为____________(保留三位有效数字)。
6.肉桂酸( )主要用于香精香料、食品添加剂、有机合成等方面,它的合成原理为:
+CH COOH
3
主要试剂及其物理性质:
溶解度/(g/100 mL溶剂)
相对分 密度/
名称 性状 熔点/℃ 沸点/℃
子质量 (g·cm-3)
水 醇 醚
无色
苯甲醛 106 1.044 -26 178~179 微溶 溶 溶
液体
无色
乙酸酐 102 1.082 -73 138~140 反应 溶 难溶
液体
肉桂酸 148 白色 1.248 133~134 300 微溶 溶 溶粉末
试剂用量:
试剂名称 苯甲醛 乙酸酐 无水碳酸钾 10%氢氧化钠 浓盐酸 活性炭
试剂用量 3.0 mL 5.5 mL 4~5 g 40 mL 25 mL 1.0 g
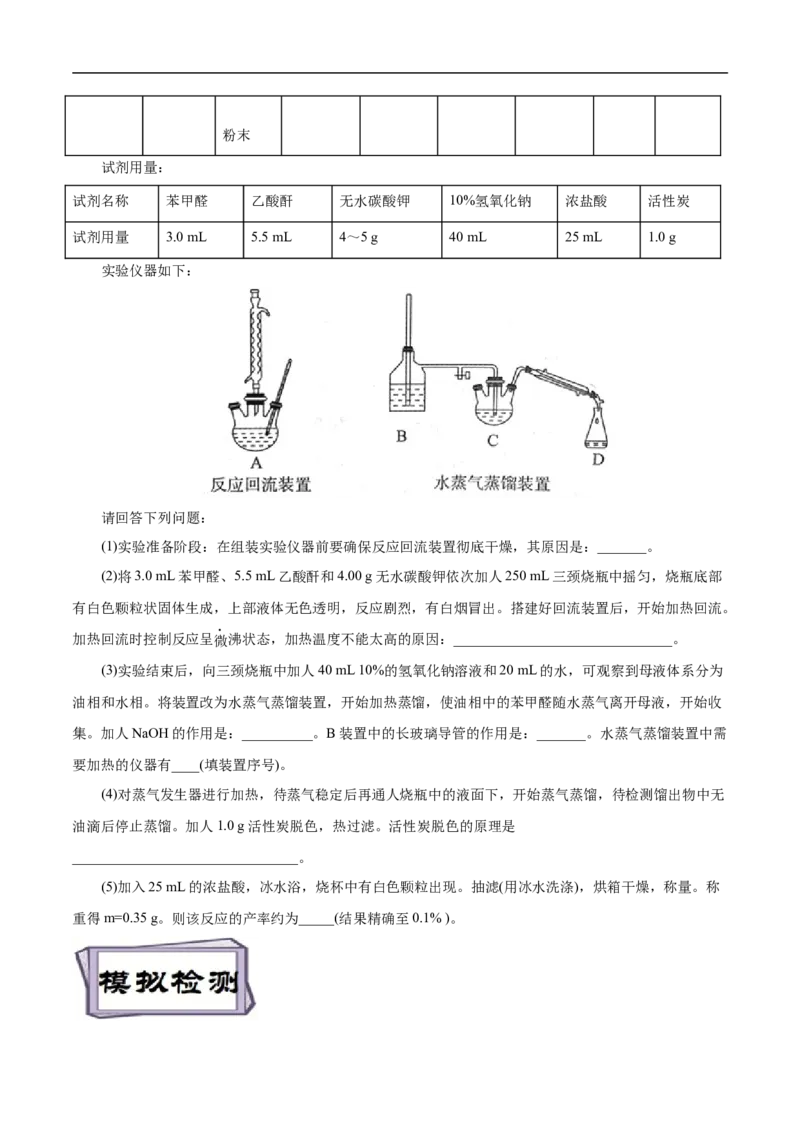
实验仪器如下:
请回答下列问题:
(1)实验准备阶段:在组装实验仪器前要确保反应回流装置彻底干燥,其原因是:_______。
(2)将3.0 mL苯甲醛、5.5 mL乙酸酐和4.00 g无水碳酸钾依次加人250 mL三颈烧瓶中摇匀,烧瓶底部
有白色颗粒状固体生成,上部液体无色透明,反应剧烈,有白烟冒出。搭建好回流装置后,开始加热回流。
加热回流时控制反应呈微沸状态,加热温度不能太高的原因:_______________________________。
(3)实验结束后,向三颈烧瓶中加人40 mL 10%的氢氧化钠溶液和20 mL的水,可观察到母液体系分为
油相和水相。将装置改为水蒸气蒸馏装置,开始加热蒸馏,使油相中的苯甲醛随水蒸气离开母液,开始收
集。加人NaOH的作用是:__________。B装置中的长玻璃导管的作用是:_______。水蒸气蒸馏装置中需
要加热的仪器有____(填装置序号)。
(4)对蒸气发生器进行加热,待蒸气稳定后再通人烧瓶中的液面下,开始蒸气蒸馏,待检测馏出物中无
油滴后停止蒸馏。加人1.0 g活性炭脱色,热过滤。活性炭脱色的原理是
________________________________。
(5)加入25 mL的浓盐酸,冰水浴,烧杯中有白色颗粒出现。抽滤(用冰水洗涤),烘箱干燥,称量。称
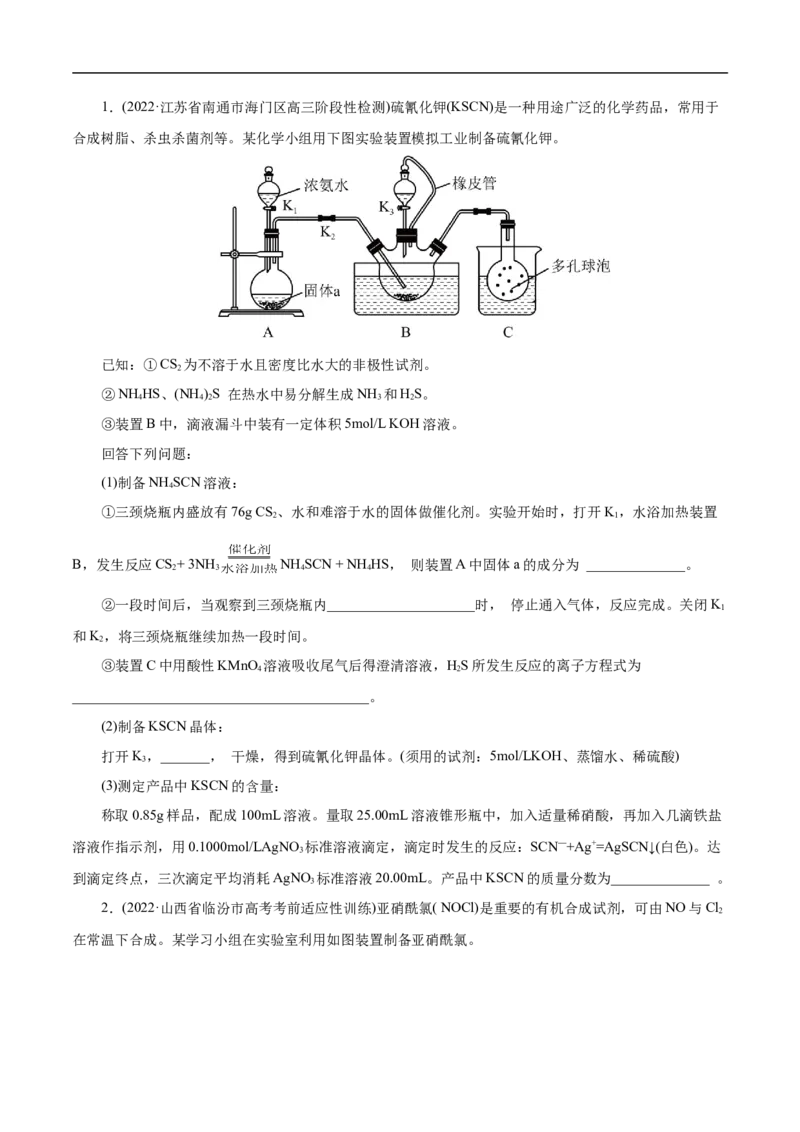
重得m=0.35 g。则该反应的产率约为_____(结果精确至0.1% )。1.(2022·江苏省南通市海门区高三阶段性检测)硫氰化钾(KSCN)是一种用途广泛的化学药品,常用于
合成树脂、杀虫杀菌剂等。某化学小组用下图实验装置模拟工业制备硫氰化钾。
已知:①CS 为不溶于水且密度比水大的非极性试剂。
2
②NH HS、(NH )S 在热水中易分解生成NH 和HS。
4 4 2 3 2
③装置B中,滴液漏斗中装有一定体积5mol/L KOH溶液。
回答下列问题:
(1)制备NH SCN溶液:
4
①三颈烧瓶内盛放有76g CS 、水和难溶于水的固体做催化剂。实验开始时,打开K,水浴加热装置
2 1
B,发生反应CS+ 3NH NH SCN + NH HS, 则装置A中固体a的成分为 ______________。
2 3 4 4
②一段时间后,当观察到三颈烧瓶内_____________________时, 停止通入气体,反应完成。关闭K
1
和K,将三颈烧瓶继续加热一段时间。
2
③装置C中用酸性KMnO 溶液吸收尾气后得澄清溶液,HS所发生反应的离子方程式为
4 2
__________________________________________。
(2)制备KSCN晶体:
打开K,_______, 干燥,得到硫氰化钾晶体。(须用的试剂:5mol/LKOH、蒸馏水、稀硫酸)
3
(3)测定产品中KSCN的含量:
称取0.85g样品,配成100mL溶液。量取25.00mL溶液锥形瓶中,加入适量稀硝酸,再加入几滴铁盐
溶液作指示剂,用0.1000mol/LAgNO 标准溶液滴定,滴定时发生的反应:SCN—+Ag+=AgSCN↓(白色)。达
3
到滴定终点,三次滴定平均消耗AgNO 标准溶液20.00mL。产品中KSCN的质量分数为______________ 。
3
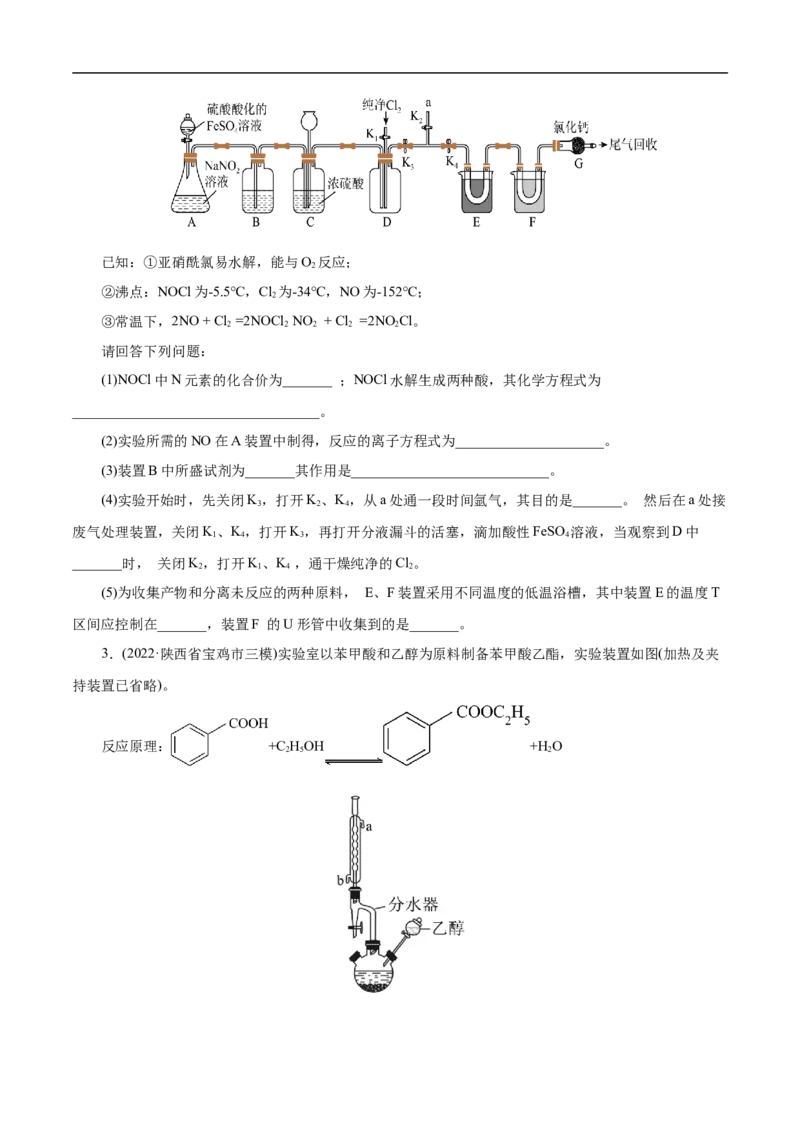
2.(2022·山西省临汾市高考考前适应性训练)亚硝酰氯( NOCl)是重要的有机合成试剂,可由NO与Cl
2
在常温下合成。某学习小组在实验室利用如图装置制备亚硝酰氯。已知:①亚硝酰氯易水解,能与O 反应;
2
②沸点:NOCl为-5.5℃,Cl 为-34℃,NO为-152℃;
2
③常温下,2NO + Cl =2NOCl NO + Cl =2NOCl。
2 2 2 2 2
请回答下列问题:
(1)NOCl中N元素的化合价为_______ ;NOCl水解生成两种酸,其化学方程式为
___________________________________。
(2)实验所需的NO在A装置中制得,反应的离子方程式为_____________________。
(3)装置B中所盛试剂为_______其作用是____________________________。
(4)实验开始时,先关闭K,打开K、K,从a处通一段时间氩气,其目的是_______。 然后在a处接
3 2 4
废气处理装置,关闭K、K,打开K,再打开分液漏斗的活塞,滴加酸性FeSO 溶液,当观察到D中
1 4 3 4
_______时, 关闭K,打开K、K ,通干燥纯净的Cl。
2 1 4 2
(5)为收集产物和分离未反应的两种原料, E、F装置采用不同温度的低温浴槽,其中装置E的温度T
区间应控制在_______,装置F 的U形管中收集到的是_______。
3.(2022·陕西省宝鸡市三模)实验室以苯甲酸和乙醇为原料制备苯甲酸乙酯,实验装置如图(加热及夹
持装置已省略)。
反应原理: +C HOH +H O
2 5 2物质 颜色、状态 沸点(℃) 密度(g·cm-3)
苯甲酸 无色晶体 249(100°C升华) 1.27
苯甲酸乙酯 无色液体 212.6 1.05
乙醇 无色液体。 78.3 0.79
环己烷 无色液体 80.8 0.73
实验步骤如下:
步骤1:在三颈烧瓶中加入12.20g苯甲酸、20mL环己烷、5mL浓硫酸、沸石,并通过分液漏斗加入
60mL(过量)乙醇,控制温度在65~70℃加热回流2h。反应时“环己烷-乙醇-水”会形成共沸物(沸点62.6℃)
蒸馏出来,再利用分水器不断分离除去水,回流环己烷和乙醇。
步骤2:反应一段时间,打开旋塞放出分水器中液体,关闭旋塞,继续加热维持反应。
步骤3:将三颈烧瓶内反应液倒入盛有适量水的烧杯中,分批加入NaCO 至溶液呈中性。
2 3
步骤4:用分液漏斗分离出有机层,水层用25mL乙醚萃取分液,然后合并至有机层。加入氯化钙,
对粗产物进行蒸馏,低温蒸出乙醚后,继续升温,接收210~213℃的馏分,得到产品10.00mL。
请回答下列问题:
(1)制备苯甲酸乙酯时,应采用_______方式加热;冷凝管中水流方向_______。
(2)根据上述实验药品的用量,三颈烧瓶最适宜规格为_______。
A.100mL B.150mL C.250mL D.500mL
(3)加入环己烷的目的是____________________________。
(4)装置中分水器的作用是_______;判断反应已经完成的标志是_______。
(5)步骤3若加入NaCO 不足,在之后蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是
2 3
____________________________。
(6)步骤4中对水层用乙醚再萃取后合并至有机层的目的是_________________。下图关于步骤4中对
水层的萃取分液的相关操作的正确顺序为_______(用编号排序);对粗产物进行蒸馏时应选用的_______冷
凝管(选填“直形”“球形”或“蛇形”)。(7)本实验中苯甲酸乙酯的产率为_______。
4.(2022·重庆市主城区高三第二次学业教学质量抽测)葡萄糖酸锌[Zn(C H O) 相对分子质量455],是
6 11 7 2
一种有机补锌剂,易溶于热水,不溶于乙醇,温度高于100°C即开始分解。实验室制备葡萄糖酸锌装置如
图1(夹持、控温装置略):
(1)图1中支管a的作用是_____________________,X处为冷凝回流装置,图2中仪器使用正确且效果
最好的是_______。(填字母)。
(2)该反应需控制温度在90°C左右,其原因为_____________________,可采用的加热方式是_______。
(3)三颈烧瓶中发生反应的化学方程式为_____________________。
(4)反应完毕后,再经过一系列实验操作得到葡萄糖酸锌粗品。粗品含少量难溶于水的杂质,纯化粗品
的合理操作顺序是_______(填字母序号)。
A.待晶体充分析出后,减压过滤
B.在50°C下用恒温干燥箱烘干
C.趁热减压过滤,除去不溶物
D.将滤液冷却至室温,加入10mL95%乙醇溶液并搅拌促进晶体析出
E.取烧杯加入10mL蒸馏水,加热至微沸,加入粗品,得到葡萄糖酸锌饱和溶液
(5)测定产品纯度:取mg提纯后的产品溶于水配制成100.00mL溶液,取25.00mL置于锥形瓶中,向其
中滴入少量EBT作为指示剂(遇Zn2+生成Zn-EBT),再加入过量的VmLcmol/LEDTA无色溶液(遇Zn2+生成
1 1
Zn-EDTA),同时发生反应:Zn-EBT(酒红色)+EDTA=Zn-EDTA(无色)+EBT(蓝色)。再用cmol/LZn2+标准溶
2
液滴定至终点。三次滴定平均消耗锌标准溶液VmL。
2①滴定终点的现象为_______。
②该产品的纯度为_______。(用含m,c、c,V、V 的代数式表示)
1 2 1 2
5.(2022·贵州省遵义市二模)丙烯腈(CH=CHCN)是合成纤维、合成橡胶和合成树脂的重要单体,可以
2
由乙炔与HCN反应制得。原理如下CH≡CH+HCN CH=CHCN
2
Ⅰ.制备催化剂CuCl
2
(1)通过查阅资料有两种方案可以制备
方案1:铜屑与HO 在浓盐酸中反应
2 2
方案2:铜丝在氯气中燃烧
方案1的实验原理如图所示
①器a的名称____________。
②请写出方案1的反应原理__________________(用离子方程式表达)。
(2)用恒压滴液漏斗分批多次滴加HO,且HO 过量,原因是______________。
2 2 2 2
(3)方案2燃烧后的固体溶于水,过滤后发现一些白色固体X,为检测X的成分,某同学将其溶于稀硫
酸,白色固体变为红色,且溶液呈蓝色,推测X为_____
Ⅱ.合成丙烯腈
已知:①电石的主要成分是CaC ,还含有少量硫化钙
2
②HCN易挥发,有毒,具有较强的还原性(4)HCN的电子式_____
(5)纯净的乙炔是无色、无臭的气体。但用电石制取的乙炔时常伴有有臭鸡蛋气味,这种物质是
___________________。
(6)从下列选择装置D中可盛放的溶液
A.高锰酸钾溶液B.NaOH溶液 C.饱和食盐水 D.盐酸溶液
(7)工业用200 kg 含CaC 质量分数80%的电石,生产得到丙烯腈79.5 kg,计算产率
2
___________________。
6.(2022·陕西省渭南市二模)2—硝基—1,3—苯二酚是重要的医药中间体。实验室常以间苯二酚为原
料,经磺化、硝化、去磺酸基三步合成:
部分物质相关性质如表:
名称 相对分子质量 性状 熔点/℃ 水溶性(常温)
间苯二酚 110 白色针状晶体 110.7 易溶
2—硝基—1,3—苯二 桔红色针状晶
155 87.8 难溶
酚 体
制备过程如下:
第一步:磺化。称取77.0g间苯二酚,碾成粉末放入烧瓶中,慢慢加入适量浓硫酸并不断搅拌,控制
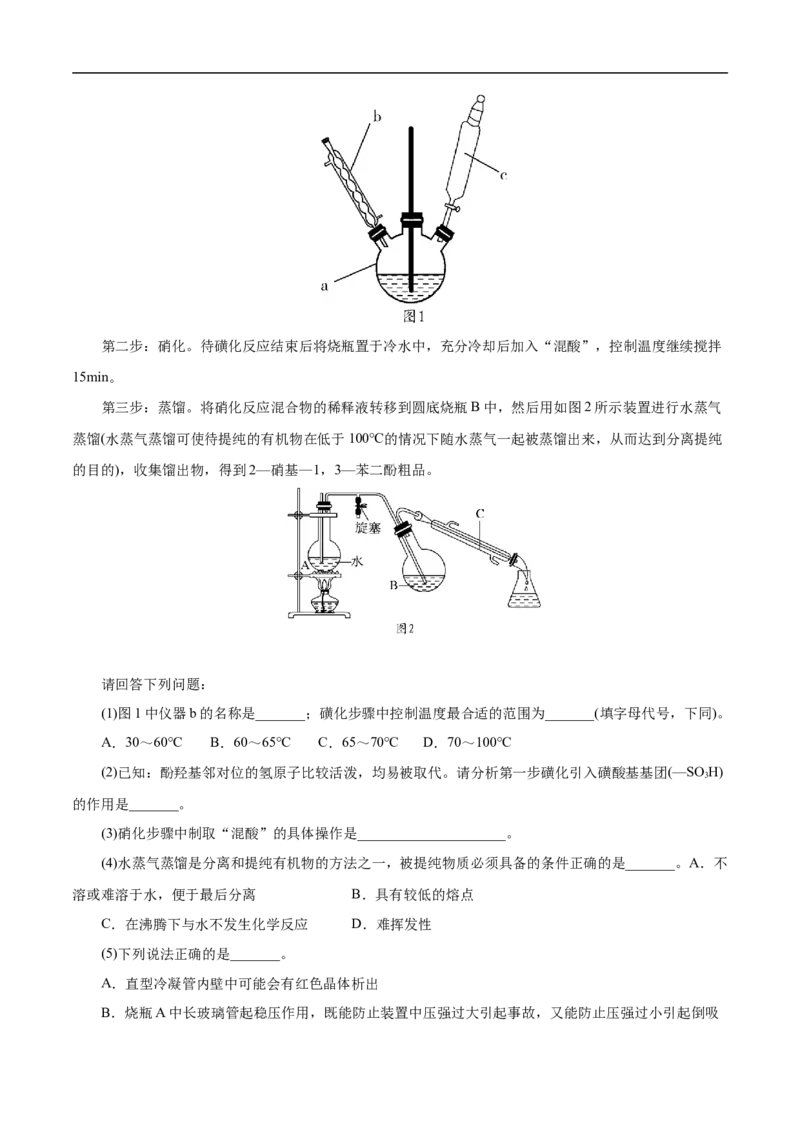
温度在一定范围内搅拌15min(如图1)。第二步:硝化。待磺化反应结束后将烧瓶置于冷水中,充分冷却后加入“混酸”,控制温度继续搅拌
15min。
第三步:蒸馏。将硝化反应混合物的稀释液转移到圆底烧瓶B中,然后用如图2所示装置进行水蒸气
蒸馏(水蒸气蒸馏可使待提纯的有机物在低于100℃的情况下随水蒸气一起被蒸馏出来,从而达到分离提纯
的目的),收集馏出物,得到2—硝基—1,3—苯二酚粗品。
请回答下列问题:
(1)图1中仪器b的名称是_______;磺化步骤中控制温度最合适的范围为_______(填字母代号,下同)。
A.30~60℃ B.60~65℃ C.65~70℃ D.70~100℃
(2)已知:酚羟基邻对位的氢原子比较活泼,均易被取代。请分析第一步磺化引入磺酸基基团(—SO H)
3
的作用是_______。
(3)硝化步骤中制取“混酸”的具体操作是_____________________。
(4)水蒸气蒸馏是分离和提纯有机物的方法之一,被提纯物质必须具备的条件正确的是_______。A.不
溶或难溶于水,便于最后分离 B.具有较低的熔点
C.在沸腾下与水不发生化学反应 D.难挥发性
(5)下列说法正确的是_______。
A.直型冷凝管内壁中可能会有红色晶体析出
B.烧瓶A中长玻璃管起稳压作用,既能防止装置中压强过大引起事故,又能防止压强过小引起倒吸C.反应一段时间后,停止蒸馏,先熄灭酒精灯,再打开旋塞,最后停止通冷凝水
(6)蒸馏所得2—硝基—1,3—苯二酚中仍含少量杂质,可用少量乙醇水混合剂洗涤。请设计简单实验
证明2—硝基—1,3—苯二酚已经洗涤干净______________。
(7)本实验最终获得15.5g桔红色晶体,则2—硝基—1,3—苯二酚的产率约为_______(保留3位有效数
字)。
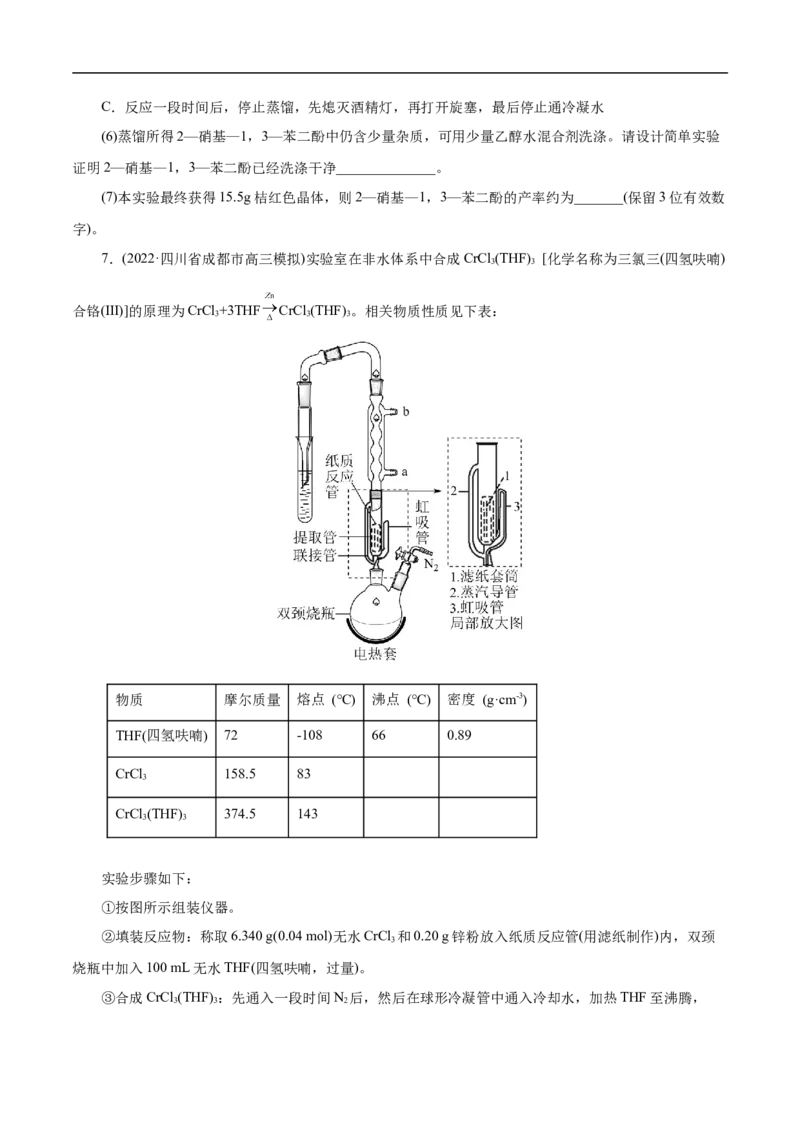
7.(2022·四川省成都市高三模拟)实验室在非水体系中合成CrCl (THF) [化学名称为三氯三(四氢呋喃)
3 3
合铬(Ⅲ)]的原理为CrCl +3THF CrCl (THF) 。相关物质性质见下表:
3 3 3
物质 摩尔质量 熔点 (℃) 沸点 (℃) 密度 (g·cm-3)
THF(四氢呋喃) 72 -108 66 0.89
CrCl 158.5 83
3
CrCl (THF) 374.5 143
3 3
实验步骤如下:
①按图所示组装仪器。
②填装反应物:称取6.340 g(0.04 mol)无水CrCl 和0.20 g锌粉放入纸质反应管(用滤纸制作)内,双颈
3
烧瓶中加入100 mL无水THF(四氢呋喃,过量)。
③合成CrCl (THF) :先通入一段时间N 后,然后在球形冷凝管中通入冷却水,加热THF至沸腾,
3 3 2THF蒸气通过联接管进入提取管中,在冷凝管中冷凝回流到纸质反应管中进行反应,当纸质反应管中的液
面高于虹吸管最高处时,发生虹吸现象,纸质管中的液体流入双颈烧瓶,从而实现了 THF与CrCl 的连续
3
反应及产物的连续萃取。
④分离CrCl (THF) :回流2.5 h,再通入N 冷却至室温。取下双颈烧瓶,在通风橱中蒸发THF至有较
3 3 2
多固体析出,冷却、抽滤、干燥称量,得产品6.290 g。
请回答:
(1)步骤①后需进行的实验操作是___________,步骤③中冷却水进水口是___________(填“a”或
“b”)。
(2)CrCl 和CrCl (THF) 在 THF的溶解性分别为___________、___________(填“溶”或“不溶”)。
3 3 3
(3)步骤③通入N 的目的可能是___________。
2
(4)该实验中THF的作用是___________。
(5)该实验过程用电热套加热,不可用明火直接加热的原因是___________。
(6)本实验制得产品CrCl (THF) 的产率为___________(保留3位有效数字)。
3 3
1.【2022•山东卷】实验室制备KMnO 过程为:①高温下在熔融强碱性介质中用KClO 氧化MnO 制
4 3 2
备KMnO ;②水溶后冷却,调溶液 至弱碱性,KMnO 歧化生成KMnO 和MnO ;③减压过滤,将滤
2 4 2 4 4 2
液蒸发浓缩、冷却结晶,再减压过滤得KMnO 。下列说法正确的是( )
4
A.①中用瓷坩埚作反应器
B.①中用NaOH作强碱性介质
C.②中KMnO 只体现氧化性
2 4
D.MnO 转化为KMnO 的理论转化率约为66.7%
2 4
2.【2022•广东选择性考试】实验室用MnO 和浓盐酸反应生成Cl 后,按照净化、收集、性质检验及
2 2
尾气处理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是( )
3.(2021•全国甲卷)实验室制备下列气体的方法可行的是( )气体 方法
A 氨气 加热氯化铵固体
B 二氧化氮 将铝片加到冷浓硝酸中
C 硫化氢 向硫化钠固体滴加浓硫酸
D 氧气 加热氯酸钾和二氧化锰的混合物
4.(2021•全国乙卷)在实验室采用如图装置制备气体,合理的是( )
化学试剂 制备的气体
A Ca(OH) +NHCl NH
2 4 3
B MnO+HCl(浓) Cl
2 2
C MnO+KClO O
2 3 2
D NaCl+H SO (浓) HCl
2 4
5.【2022•全国乙卷】二草酸合铜(Ⅱ)酸钾(K Cu [(C O)])可用于无机合成、功能材料制备。实验室制
2 2 4 2
备二草酸合铜(Ⅱ)酸钾可采用如下步骤:
Ⅰ.取已知浓度的CuSO 溶液,搅拌下滴加足量 溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,
4
过滤。
Ⅱ.向草酸(H C O)溶液中加入适量KCO 固体,制得KHC O 和KC O 混合溶液。
2 2 4 2 3 2 4 2 2 4
Ⅲ.将Ⅱ的混合溶液加热至80-85℃,加入Ⅰ中的黑色沉淀。全部溶解后,趁热过滤。
Ⅳ.将Ⅲ的滤液用蒸汽浴加热浓缩,经一系列操作后,干燥,得到二草酸合铜(Ⅱ)酸钾晶体,进行表征
和分析。
回答下列问题:
(1)由CuSO ·5H O配制Ⅰ中的CuSO 溶液,下列仪器中不需要的是________(填仪器名称)。
4 2 4(2)长期存放的CuSO ·5H O中,会出现少量白色固体,原因是________。
4 2
(3)Ⅰ中的黑色沉淀是________(写化学式)。
(4)Ⅱ中原料配比为n(H C O):n(K CO)=1.5:1,写出反应的化学方程式________。
2 2 4 2 3
(5)Ⅱ中,为防止反应过于剧烈而引起喷溅,加入KCO 应采取________的方法。
2 3
(6)Ⅲ中应采用________进行加热。
(7)Ⅳ中“一系列操作”包括________。
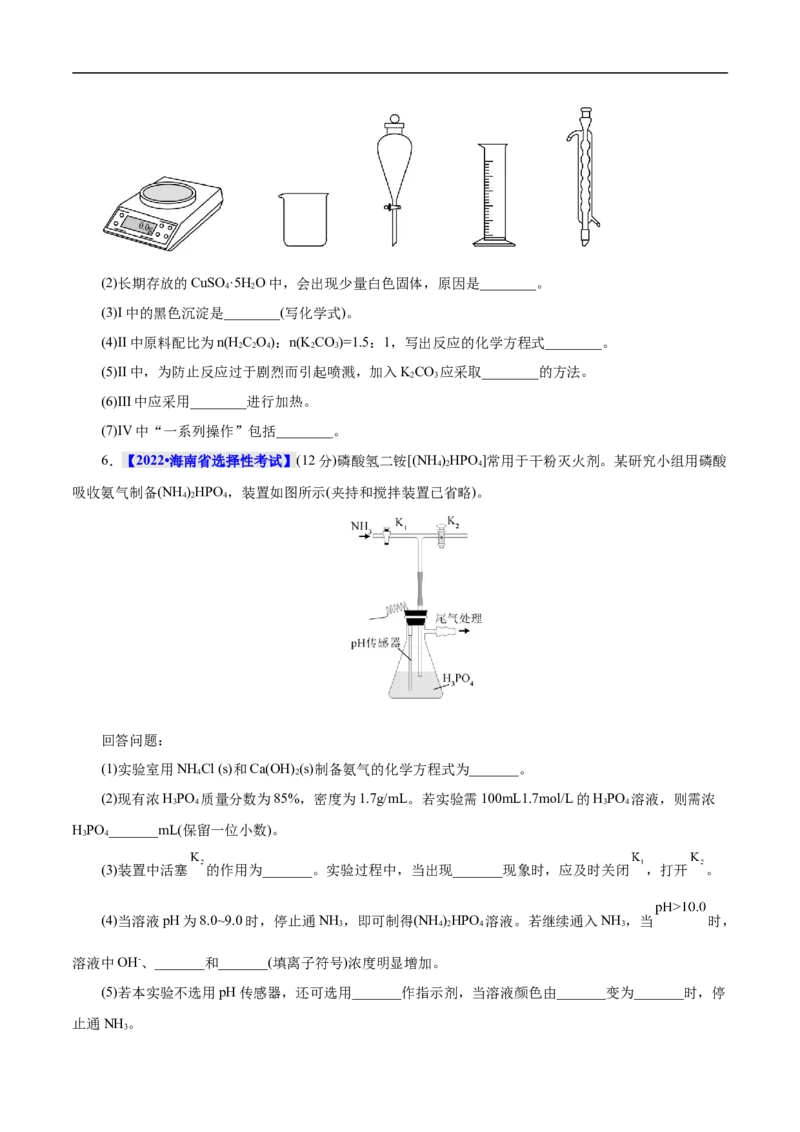
6.【2022•海南省选择性考试】(12分)磷酸氢二铵[(NH )HPO ]常用于干粉灭火剂。某研究小组用磷酸
4 2 4
吸收氨气制备(NH )HPO ,装置如图所示(夹持和搅拌装置已省略)。
4 2 4
回答问题:
(1)实验室用NH Cl (s)和Ca(OH) (s)制备氨气的化学方程式为_______。
4 2
(2)现有浓HPO 质量分数为85%,密度为1.7g/mL。若实验需100mL1.7mol/L的HPO 溶液,则需浓
3 4 3 4
HPO _______mL(保留一位小数)。
3 4
(3)装置中活塞 的作用为_______。实验过程中,当出现_______现象时,应及时关闭 ,打开 。
(4)当溶液pH为8.0~9.0时,停止通NH ,即可制得(NH )HPO 溶液。若继续通入NH ,当 时,
3 4 2 4 3
溶液中OH-、_______和_______(填离子符号)浓度明显增加。
(5)若本实验不选用pH传感器,还可选用_______作指示剂,当溶液颜色由_______变为_______时,停
止通NH 。
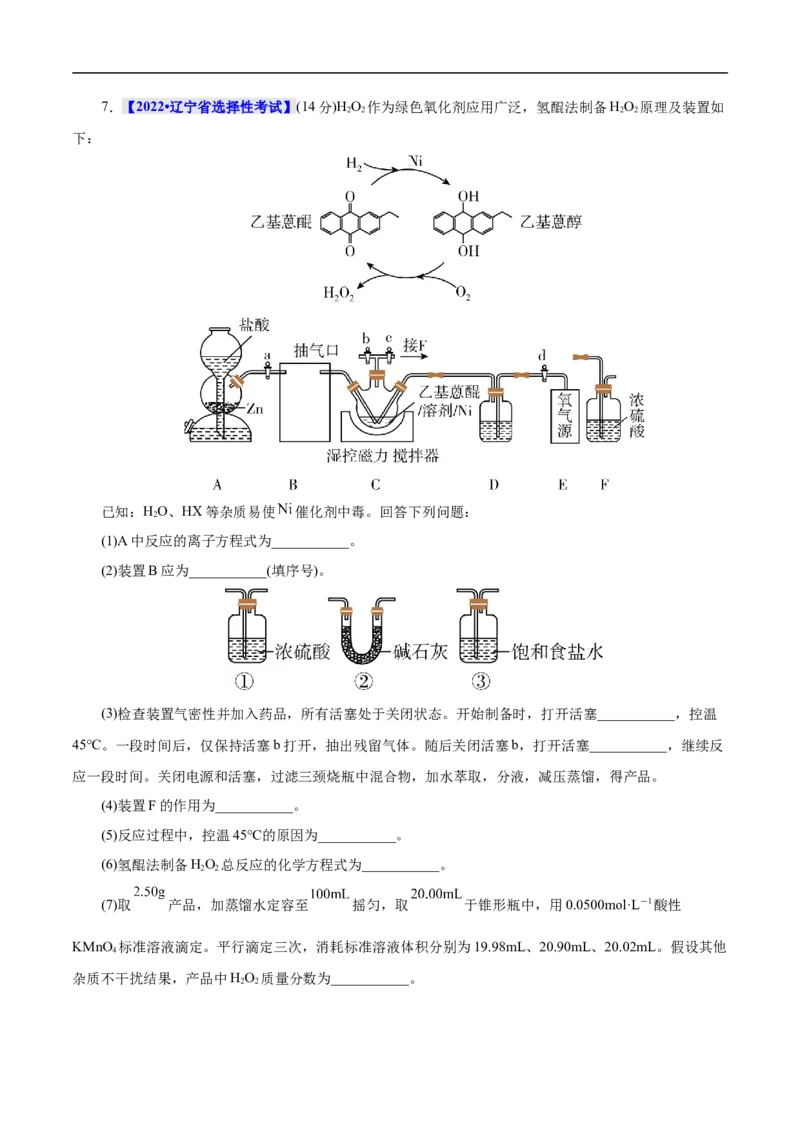
37.【2022•辽宁省选择性考试】(14分)H O 作为绿色氧化剂应用广泛,氢醌法制备HO 原理及装置如
2 2 2 2
下:
已知:HO、HX等杂质易使 催化剂中毒。回答下列问题:
2
(1)A中反应的离子方程式为___________。
(2)装置B应为___________(填序号)。
(3)检查装置气密性并加入药品,所有活塞处于关闭状态。开始制备时,打开活塞___________,控温
45℃。一段时间后,仅保持活塞b打开,抽出残留气体。随后关闭活塞b,打开活塞___________,继续反
应一段时间。关闭电源和活塞,过滤三颈烧瓶中混合物,加水萃取,分液,减压蒸馏,得产品。
(4)装置F的作用为___________。
(5)反应过程中,控温45℃的原因为___________。
(6)氢醌法制备HO 总反应的化学方程式为___________。
2 2
(7)取 产品,加蒸馏水定容至 摇匀,取 于锥形瓶中,用0.0500mol·L-1酸性
KMnO 标准溶液滴定。平行滴定三次,消耗标准溶液体积分别为19.98mL、20.90mL、20.02mL。假设其他
4
杂质不干扰结果,产品中HO 质量分数为___________。
2 2