文档内容
《化学》三色速记手册
HO ⇄ H+ + OH-
2
实验测得:25℃时,1L纯水中只有1×10-7mol的水分子发生电离,故25 ℃时的纯水中c
(H+)=c(OH-)=10-7mol/L
(三)水的离子积
一定温度下,c(H+)与c(OH-)的乘积是一个常数,称为水的离子积常数,
简称水的离子积,用符号K 表示,即Kw=c(H+)·c(OH-)。
w
1.在一定温度下,水的离子积都是一个常数,在25℃时 Kw=1×10-14
2.Kw随温度的变化而变化,温度升高,Kw增大
3.水的离子积常数揭示了在任何水溶液中均存在水的电离平衡,都有H+和OH-共存。在酸性
或碱性的稀溶液中,当温度为25 ℃时,Kw=c(H+)·c(OH-)=1×10-14始终为同一常数。
4.在酸性或碱性的稀溶液中,由水电离出的 c(H+)和c(OH-)总相等。
(四)溶液的酸碱性和PH值
1.PH
水溶液里H+浓度的负对数叫做pH,即pH=-lgc(H+)。
常温条件下:若 pH=7,则为中性溶液;
pH<7,则为酸性溶液;
pH>7,则为碱性溶液。
pH越小,c(H+)越大,溶液的酸性越强;pH越大,c(OH-)越大,溶液的碱性越强。
(五)同离子效应和盐效应
1.同离子效应
当弱电解质,例如HAc,达到解离平衡时:HAc ⇄ H++ Ac-
达到平衡后,向溶液中加入固体NaAc
强电解质完全解离:NaAc = Na++ Ac-
由于Ac-的引入,将破坏已建立的弱电解质的解离平衡:
HAc ⇄ H++ Ac-
Ac-增多,弱电解质解离平衡左移,HAc的α减小。
同离子效应:在弱电解质的溶液中,加入与其具有相同离子的强电解质,从而使解离平衡
左移,降低弱电解质的解离度。这种现象称为同离子效应。
2.盐效应
在HAc中,加入与其没有共同离子NaCl,对HAc的解离度是否会有影响呢?
加入NaCl以后:α=1.68%;与未加入NaCl时,α=1.33%相比,加入NaCl后解离度增大。
盐效应:在弱电解质中加入与其没有共同离子的强电解质,会使弱电解质的电离度有所增
加。这种作用称为盐效应。
(六)盐类水解
在溶液中由盐电离出来的离子跟水电离出来的H+或OH-结合生成弱电解质的反应,叫做盐类
的水解。
1.弱酸强碱盐
以NaAc溶于水生成的溶液为例,可以写出NaAc的水解平衡式:
NaAc = Na+ + Ac-
Ac- + HO ⇌ HAc + OH-
2
水解的结果使得溶液中 [OH-]>[ H+],NaAc 溶液显碱性。
2.强酸弱碱
以NHCl溶于水生成的溶液为例,可以写出NHCl的水解平衡式:
4 4
NHCl = NH+ + Cl-
4 4
第 22 页《化学》三色速记手册
NH+ + HO ⇌ NH•HO + H+
4 2 3 2
NH+和OH-结合成弱电解质,使HO的电离平衡发生移动,结果溶液中[H+]>[OH-] ,溶液显
4 2
酸性。
3.弱酸弱碱盐
以NHAc为例,其水解平衡式可写成:
4
由于生成了弱电解质NH·HO和HAc,同时消耗了H+和OH-,使水的电离平衡向右移动,而
3 2
且移动程度更大。弱酸弱碱盐的水溶液呈酸性还是呈碱性取决于组成盐的弱酸弱碱的相对强
弱。
如果K=K,溶液呈中性,如果K>K,溶液呈酸性;如果K<K,溶液呈碱性。
a b a b a b
4.强酸强碱盐
因为强酸强碱盐完全电离出来的阴阳离子不能与水电离出来的H+和OH-结合,生成弱酸与弱
碱分子,不影响水的电离平衡,溶液中的H+和OH-浓度相等,所以这种盐的溶液呈中性。
盐类水解规律
有弱才水解
无弱不水解
都弱都水解
谁强显谁性
同强显中性
5.盐类水解中的三大守恒
(1)电荷守恒
电解质溶液中不论存在多少种离子,溶液总是呈电中性的,即阳离子所带的正电荷总数一定
等于阴离子所带的负电荷总数。
例如NaHCO 溶液中:
3
c(Na+)+c(H+)=c(HCO-)+c(OH-)+2c(CO2-)
3 3
(2)物料守恒(元素质量守恒)
在电解质溶液中,由于某些离子发生水解或电离,离子的存在形式发生了变化。但就该离子
所含的某种元素来说,其质量在变化前后是守恒的,即元素质量守恒,也称物料守恒。
例如在NaS溶液中,S元素以S2-、HS-、HS三种形式存在,但不管如何,Na原子的物质的
2 2
量总是S原子物质的量的2倍。根据物料守恒,必然有:
c(Na+)=2[c(S2-)+c(HS-)+c(HS)]
2
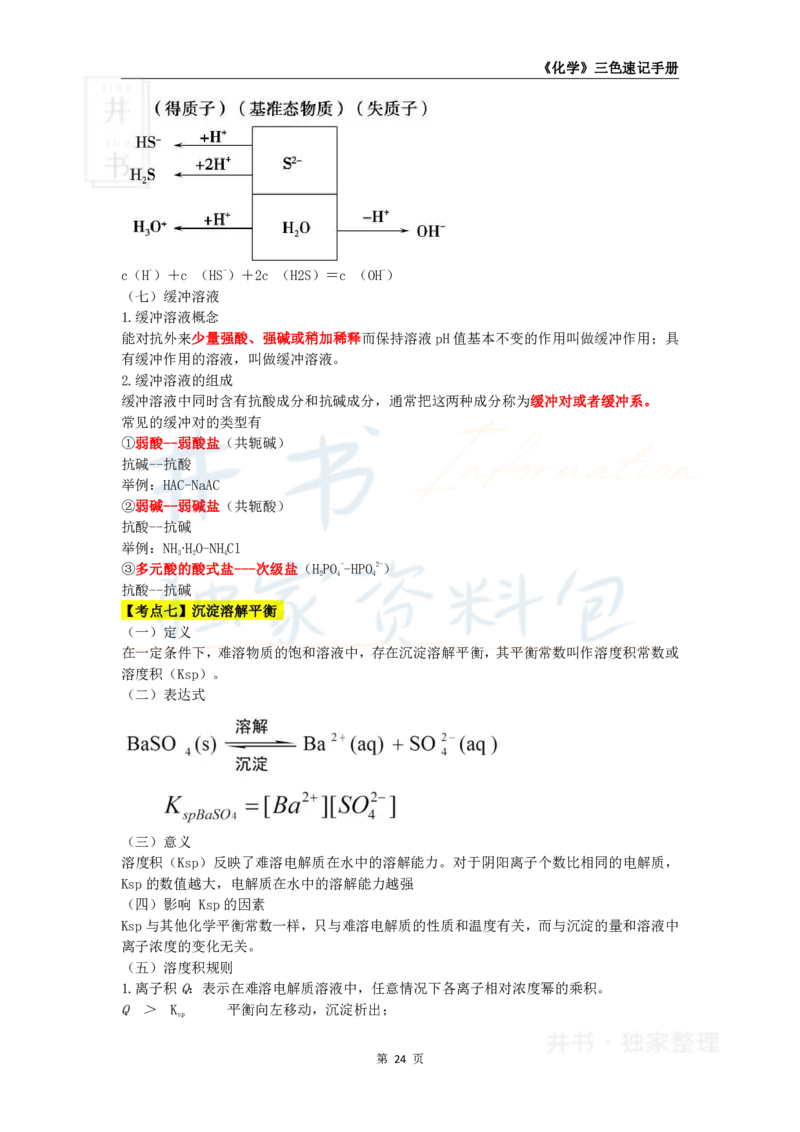
(3)质子守恒
NaS 溶液中的质子转移示意图
2
第 23 页《化学》三色速记手册
c(H+)+c (HS-)+2c (H2S)=c (OH-)
(七)缓冲溶液
1.缓冲溶液概念
能对抗外来少量强酸、强碱或稍加稀释而保持溶液pH值基本不变的作用叫做缓冲作用;具
有缓冲作用的溶液,叫做缓冲溶液。
2.缓冲溶液的组成
缓冲溶液中同时含有抗酸成分和抗碱成分,通常把这两种成分称为缓冲对或者缓冲系。
常见的缓冲对的类型有
①弱酸--弱酸盐(共轭碱)
抗碱--抗酸
举例:HAC-NaAC
②弱碱--弱碱盐(共轭酸)
抗酸--抗碱
举例:NH∙HO-NHCl
3 2 4
③多元酸的酸式盐---次级盐(HPO--HPO2-)
2 4 4
抗酸--抗碱
【考点七】沉淀溶解平衡
(一)定义
在一定条件下,难溶物质的饱和溶液中,存在沉淀溶解平衡,其平衡常数叫作溶度积常数或
溶度积(Ksp)。
(二)表达式
(三)意义
溶度积(Ksp)反映了难溶电解质在水中的溶解能力。对于阴阳离子个数比相同的电解质,
Ksp的数值越大,电解质在水中的溶解能力越强
(四)影响 Ksp的因素
Ksp与其他化学平衡常数一样,只与难溶电解质的性质和温度有关,而与沉淀的量和溶液中
离子浓度的变化无关。
(五)溶度积规则
1.离子积Q:表示在难溶电解质溶液中,任意情况下各离子相对浓度幂的乘积。
Q > K 平衡向左移动,沉淀析出;
sp
第 24 页《化学》三色速记手册
Q = K 处于平衡状态,饱和溶液;
sp
Q < K 平衡向右移动,无沉淀析出;
sp
2.沉淀的溶解
沉淀溶解的必要条件:Q < K
sp
减小离子浓度的办法有下面几种:
①生成弱电解质使沉淀溶解
②氧化还原反应使沉淀溶解
③生成配合物使沉淀溶解
3.分级沉淀
如果溶液中含有两种或两种以上的离子,都能与同一种试剂生成难溶电解质沉淀,当向溶液
中加入这种沉淀剂时就会先后生成几种沉淀,这种先后沉淀的现象称为分级沉淀。
率先满足Q> K 的难溶电解质沉淀先析出。
sp
4.沉淀的转化
【考点八】氧化还原平衡
(一)原电池
1.电极反应
原电池中,电子流出的一极为负极,负极上发生氧化反应;电子流入的一极为正极,正极
上发生还原反应。
Zn负极:Zn=Zn2++2e(氧化反应)
Cu正极:Cu2++2e=Cu(还原反应)
将两个电极反应相加得到中反应,称为电池反应。
电池反应:Zn+Cu2+=Zn2++Cu
(二)电解池(外加电源的是电解池)
电解池:把电能转化为化学能的装置
阳极:2Cl--2e-=Cl↑
2
阴极:Cu2++2e-=Cu
移动方向
电子
原电池 负→正; 电解池 阳→阴
离子
原电池:正正负负; 电解池:阴阳相吸
第 25 页《化学》三色速记手册
(三)电池
1.一次电池—碱性锌锰干电池
干电池的电压通常约为1.5V,不能充电。负极是Zn,正极是MnO
2
负极反应:Zn+2OH--2e=Zn(OH)(负极质量增大)
2
正极反应:2MnO+2HO+2e-= 2MnOOH+2OH-
2 2
总反应:Zn+2MnO+2HO=Zn(OH)+2MnOOH
2 2 2
2.二次电池(或可充电电池)
铅蓄电池是最常见的二次电池,可以放电和充电,负极材料是Pb,正极材料是PbO,电解
2
质溶液是HSO 溶液。
2 4
①放电时的反应
负极:Pb+SO2-- 2e=PbSO(负极质量增大)
4 4
正极:PbO+4H++SO2-+2e=PbSO+2HO
2 4 4 2
电池总反应:Pb+PbO+2HSO=2PbSO+2HO
2 2 4 4 2
②充电时的反应
阴极:PbSO+2e-=Pb+SO2-
4 4
阳极:PbSO+2HO-2e=PbO+4H++SO2-
4 2 2 4
电池总反应:2PbSO+2HO=Pb+PbO+2HSO
4 2 2 2 4
(3)燃料电池
原理:利用原电池的工作原理,连续地将燃料和氧化剂(如O2)的化学能直接转化为电能。
燃料电池是一种高效、环境友好的发电装置,它的电极材料一般具有很强的催化活性,如铂
电极、活性炭电极等。
燃料电池由3个主要部分组成:
负极(燃料电极);
正极(氧气或空气电极);
电解质溶液。
两电极材料均为惰性电极,电极本身不发生反应,而是由引入到两电极上的燃料和氧化剂发
生反应。
常见的燃料电池:
(1)氢氧燃料电池
氢氧燃料电池是目前最成熟的燃料电池,可分为酸性和碱性两种。
负极:H 被氧化失去电子变成H+,电子由负极流向电池的正极,同时,H+通过电解质溶液移
2
向正极。
正极:O 得电子发生还原反应。
2
第四章 金属及非金属化合物
【考点一】钠及其化合物
(一)钠的物理性质
导电、
颜色 状态 硬度 密度 熔点
导热性
银白色、有 小,可以用 р(水)>р(钠)
固体 97.8℃ 良好
金属光泽 小刀切割 >р(煤油)
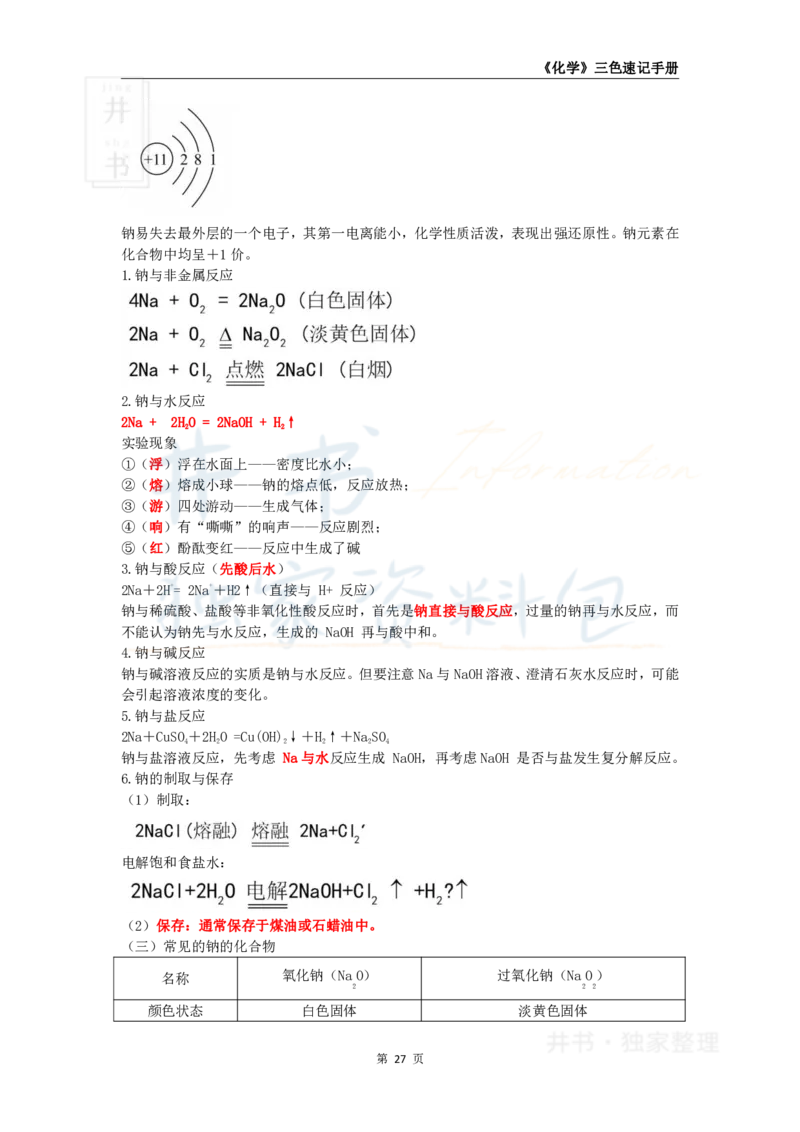
(二)钠的化学性质
钠的原子结构
第 26 页《化学》三色速记手册
钠易失去最外层的一个电子,其第一电离能小,化学性质活泼,表现出强还原性。钠元素在
化合物中均呈+1价。
1.钠与非金属反应
2.钠与水反应
2Na + 2HO = 2NaOH + H↑
2 2
实验现象
①(浮)浮在水面上——密度比水小;
②(熔)熔成小球——钠的熔点低,反应放热;
③(游)四处游动——生成气体;
④(响)有“嘶嘶”的响声——反应剧烈;
⑤(红)酚酞变红——反应中生成了碱
3.钠与酸反应(先酸后水)
2Na+2H+= 2Na++H2↑(直接与 H+ 反应)
钠与稀硫酸、盐酸等非氧化性酸反应时,首先是钠直接与酸反应,过量的钠再与水反应,而
不能认为钠先与水反应,生成的 NaOH 再与酸中和。
4.钠与碱反应
钠与碱溶液反应的实质是钠与水反应。但要注意Na与NaOH溶液、澄清石灰水反应时,可能
会引起溶液浓度的变化。
5.钠与盐反应
2Na+CuSO+2HO =Cu(OH)↓+H↑+NaSO
4 2 2 2 2 4
钠与盐溶液反应,先考虑 Na与水反应生成 NaOH,再考虑NaOH 是否与盐发生复分解反应。
6.钠的制取与保存
(1)制取:
电解饱和食盐水:
(2)保存:通常保存于煤油或石蜡油中。
(三)常见的钠的化合物
名称 氧化钠(NaO) 过氧化钠(NaO)
2 2 2
颜色状态 白色固体 淡黄色固体
第 27 页《化学》三色速记手册
阴阳离子个数比 1:2 1:2
类型 碱性氧化物 金属氧化物
氧元素化合价 -2 -1
与水反应 NaO+HO=2NaOH 2NaO+2HO=4NaOH+O↑
2 2 2 2 2 2
与CO 反应 NaO+CO=NaCO 2NaO+2CO=2NaCO+O
2 2 2 2 3 2 2 2 2 3 2
与盐酸反应 NaO+2HCl=2NaCl+HO 2NaO+4HCl=4NaCl+O↑+2HO
2 2 2 2 2 2
名称 碳酸钠(NaCO) 碳酸氢钠(NaHCO)
2 3 3
俗名 纯碱或苏打 小苏打
易溶于水(但比Na2CO 溶解度小),
水溶性 易溶于水,溶液呈碱性 3
溶液呈碱性
稳定,但碳酸钠晶体
稳定性
(NaCO·10HO)易风化
主 2 3 2
要
性 + 2- + - +
质 与H反应 CO +2H=CO↑+H2O HCO +H=HO+CO↑
3 2 3 2 2
2+ - -
Ca +OH+HCO =CaCO↓+HO(碱过量)
与碱Ca -
与OH不反应, 3 3 2
(OH)2 2+ - - 2-
Ca +2OH+2HCO =CaCO↓+2HO+CO
2+ 2-
反应 但Ca +CO =CaCO↓ 3 3 2 3
3 3
(碱不足)
制玻璃、造纸、制皂、
主要用途 发酵粉、制药
洗涤剂
(四)碱金属
碱金属元素包含锂(Li)、钠(Na)、钾(K)、铷(Rb)、铯(Cs)、钫(Fr)六种。
(1)相似性
1.原子结构:最外层上都只有1个电子,次外层均为8个(Li为2个)电子。
2.单质的物理性质:都具有银白色金属光泽(铯略带金色光泽),质软,密度小,熔点低,
导热、导电性好。
3.单质的化学性质:都能与氧气和水反应,生成物都是含R+(R为碱金属元素)的离子化
合物。
4.最高价氧化物对应的水化物(ROH)均是强碱,ROH 的碱性逐渐增强。
(2)特殊性
1.锂的密度比煤油小,不能保存在煤油中,通常密封在石蜡里。
2.碱金属 Li -Cs 的密度呈增大趋势,但 ρ(Na)>ρ(K)。
3.酸式盐的溶解度一般比相应的正盐大,但S(Na2CO3)>S(NaHCO3)。
4.锂易与氮气反应(生成Li3N)。
5.锂的熔点最高,金属性最弱,因而锂与水反应较慢且反应时锂并不熔化。
6.碱金属单质及其离子的焰色反应呈现不同的颜色。
第 28 页《化学》三色速记手册
7.试剂瓶中的药品取出后,一般不能放回原瓶,但金属Na、K等需立即放回原瓶。
(3)焰色反应
1.概念
某些金属或它们的化合物在无色火焰中灼烧时会使火焰呈现特殊颜色的反应。其原理是碱金
属元素灼烧时发生电子跃迁释放出不同能量的光子,使火焰呈现出不同的颜色。焰色反应为
物理变化,属于元素自身的性质。
2.常见元素的焰色
钠:黄色
钾:紫色(透过蓝色钴玻璃)。
【考点二】镁、铝及其化合物
(一)镁、铝单质
镁 铝
银白色固体,较软,密度 2.70
3
银白色固体,质软,密度 1.738 g/cm,熔点
物理性质 g/cm3,熔点 660.4℃,沸点
645 ℃,沸点1090 ℃。
2467 ℃。
以化合态形式存在,主要以铝
存在 以化合态形式存在,主要存在于地壳和海水中
土矿存在
可用来制造合金、导线、电缆、
用途 可用来制造合金
防锈油漆、食品包装
1.与非金属反应
2.与酸反应
Mg + 2H+ = Mg2+ + H↑
2
与稀HNO 反应生成 Mg(NO)、NOx、HO
3 3 2 2
2Al+6H+=2Al3++3H↑
2
在冷的浓HSO 或浓HNO 中钝化
2 4 3
3.与氧化物反应
(二)氧化镁和氧化铝
氧化物 MgO AlO
2 3
第 29 页《化学》三色速记手册
工业制备 铝土矿→AlO
2 3
白色固体,熔点高,
重要物理性质 白色固体,熔点高,密度较小
密度小
HO MgO+HO=Mg(OH) 很慢 不溶解,也不反应
2 2 2,
主要
2+ + 3+
化学 H+ MgO+2H+=Mg +HO AlO+6H=2Al +3HO
2 2 3 2
性质
- - -
OH 不反应 AlO+2OH =2AlO +HO
2 3 2 2
制造耐火、耐高温器材;
重要用途 制造耐火、耐高温器材
工业冶炼铝
(三)氢氧化镁和氢氧化铝
1.氢氧化镁
Mg(OH) 是一种难溶于水的中强碱,其饱和溶液能使酚酞试液变为浅红色。
2
(1)与酸反应:Mg(OH)+2H+= Mg2++2HO
2 2
(2)热稳定性差:
(3)溶解平衡:可溶于浓NHCl等盐溶液中
4
Mg(OH)+2NH+ =Mg2++2NH·HO
2 4 3 2
2.氢氧化铝
Al(OH) 是难溶的白色胶体物质,不能使酚酞试液变色。
3
它是典型的两性氢氧化物,既能跟强酸反应,又能跟强碱反应。
(1)两性:
Al(OH)+3H+ =Al3++3HO
3 2
Al(OH)+OH- =AlO-+2HO 或 Al(OH)+OH- =[Al(OH)]-
3 2 2 3 4
(2)两式电离平衡:
AlO-+H++HO ⇌ Al(OH) ⇌ Al3++3OH-
2 2 3
酸式电离 碱式电离
(3)热稳定性:
(四)铝及其化合物之间的相互转化
第 30 页