文档内容
《化学》三色速记手册
1.概念
从晶体中“截取”出来具有代表性的最小部分。是能够反映晶体结构特征的最小重复单元。
2.晶胞的结构
一般来说,晶胞都是从晶体中截取下来的大小、形状完全相同的平行六面体,晶胞只是晶体
微观空间里的一个基本单元,在它的上下左右前后无间隙并排着无数晶胞,而且所有晶胞的
形状及其内部的原子种类、个数及几何排列是完全相同的。
3.晶胞中原子数目的确定——均摊法
若晶胞中某个粒子为n个晶胞所共用,则该粒子有1/n属于这个晶胞
均摊是指每个图形平均拥有的粒子数目。
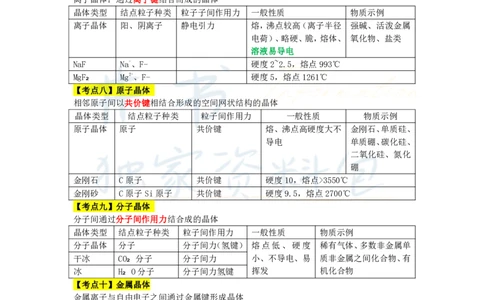
【考点七】离子晶体
离子晶体:通过离子键结合而成的晶体
晶体类型 结点粒子种类 粒子子间作用力 一般性质 物质示例
离子晶体 阳、阴离子 静电引力 熔,沸点较高(离子半径 强碱、活泼金属
电荷)、略硬、脆,熔体、 氧化物、盐类
溶液易导电
NaF Na+、F- 硬度2~2.5,熔点993℃
MgF₂ Mg2+、F- 硬度5,熔点1261℃
【考点八】原子晶体
相邻原子间以共价键相结合形成的空间网状结构的晶体
晶体类型 结点粒子种类 粒子间作用力 一般性质 物质示例
原子晶体 原子 共价键 熔、沸点高硬度大不 金刚石、单质硅、
导电 单质硼、碳化硅、
二氧化硅、氮化
硼
金刚石 C原子 共价键 硬度10,熔点>3550℃
金刚砂 C原子Si原子 共价键 硬度9.5,熔点2700℃
【考点九】分子晶体
分子间通过分子间作用力结合成的晶体
晶体类型 结点粒子种类 粒子间作用力 一般性质 物质示例
分子晶体 分子 分子间力(氢键) 熔点低、硬度 稀有气体、多数非金属单
干冰 CO₂ 分子 分子间力 小、不导电、易 质非金属之间化合物、有
冰 H₂ O分子 分子间力氢键 挥发 机化合物
【考点十】金属晶体
金属离子与自由电子之间通过金属键形成晶体
第 15 页《化学》三色速记手册
第三章 化学反应基本原理
【考点一】反应热
化学反应在生成新物质的同时,常伴随能量的变化,而能量的变化通常表现为热量的变化,
即表现为放出热量或吸收热量。在化学反应过程中放出或吸收的热量通常叫做反应热。
(二)化学键与化学反应中能量变化的关系
当物质发生化学变化时,反应物中的旧化学键断裂要吸收能量,而生成物中新化学键的形
成要放出能量。即化学反应不仅有新物质生成,还伴随着能量变化。因此,化学键的断裂和
形成是化学反应中能量变化的主要原因。
(二)焓变
当系统在等压条件下,从状态1变到状态2时,反应中吸收或放出的热量称为化学反应的焓
变。符号△H,表示:△H=H-H=(U+pV)-(U +pV)=Q
2 1 2 2 1 1 p
焓是与内能有关的物理量,在化学反应中,所释放或吸收的能量都可用热量来表示反应热,
又称“焓变”。
(三)吸热反应和放热反应
单位反应放出或者吸收热量的多少叫反应热。
△H= E -E
生 反
单位一般采用kJ/mol。
在恒压下,放热反应,△H<0;吸热反应,△H>0。
(四)燃烧热和中和热
1.燃烧热
在101kPa时,1mol可燃物完全燃烧时所放出的热量,叫做该物质的燃烧热。燃烧热的单位
一般用kJ/mol表示。
2.中和热
强酸、强碱的稀溶液完全中和生成1mol液态水所放出的热量,表示为:H+ +OH- =HO ;
(aq) (aq) 2 (l)
ΔH=-57.3kJ/mol。
(五)热化学反应方程式
1.定义
表示参加反应物质的量和反应热的关系的化学方程式叫做热化学方程式。
2.书写要求
第 16 页《化学》三色速记手册
(1)应注明反应热的符号(+或-)、数值和单位(kJ/mol)。
(2)注意反应热△H与测定条件(温度,压强)有关。因此书写热化学方程式时应注明△H
测定条件。绝大多数△H是在25 ℃、101kPa下测定的,这时可不注明温度和压强。
(3)注意反应物和生成物的聚集状态不同,反应热数值不同。因此,必须注明物质的聚集
状态(s、l、g)才能完整的体现出热化学方程式的意义。对于化学式形式相同的同素异形
体,还必须注明名称,如C(金刚石,s)。
(4)注意热化学方程式中各物质化学式前面的化学计量数仅表示该物质的物质的量,因此
化学计量数可以是整数,也可以是分数。
(5)由于△H与反应的物质的量有关,所以方程式中化学式前面的化学计量数必须与△H
相对应,如果化学计量数必须加倍,则△H也要加倍。当反应逆向进行时,其反应热与正反
应的反应数值相等,符号相反。
(六)盖斯定律
(七)能源
(八)化学反应进行的方向
1.自发过程
(1)定义
自发过程:指定条件下不需要消耗外力(功或热)而能够自动进行的过程。
(2)自发反应的方向
①过程向体系能量降低的方向进行。
②过程向体系混乱度增大的方向进行。
2.熵
混乱度是指系统内部质点运动的无序程度,质点的运动越无序,其混乱度就越大。室温下自
发进行的吸热反应发生后,系统的混乱度就增大。系统混乱度增大,是吸热反应自发进行的
推动力。
熵:是体系内部质点运动的混乱度的量度,符号为S,单位J/K。
3.吉布斯自由能
综合考虑能量降低和熵增加两个自发过程的推动力,定义了”吉布斯自由能”,简称“自由
能”,用符号G表示。
数学定义为:G=H-TS
单位:J,常用单位为kJ
自由能的改变量:△G =△H-T△S
4.化学反应方向判断的依据
在等温、等压条件下,化学反应的吉布斯自由能变化是焓变和熵变的综合效应。即△G=ΔH-T
△S
对于封闭体系在恒温、恒压、不做非体积功的条件下,利用吉布斯自由能变可以判断过程的
自发方向。
△G < 0 过程正向自发
△G > 0 非自发
△G = 0 过程处于平衡状态
封闭体系在恒温恒压和不做其他功的条件下,其自发过程总是向自由能降低的方向进行,当
自由能降低到最低值时就达到平衡。
【考点二】化学反应速率
(一)定义
是指在一定条件下,反应物转化为生成物的速率;
第 17 页《化学》三色速记手册
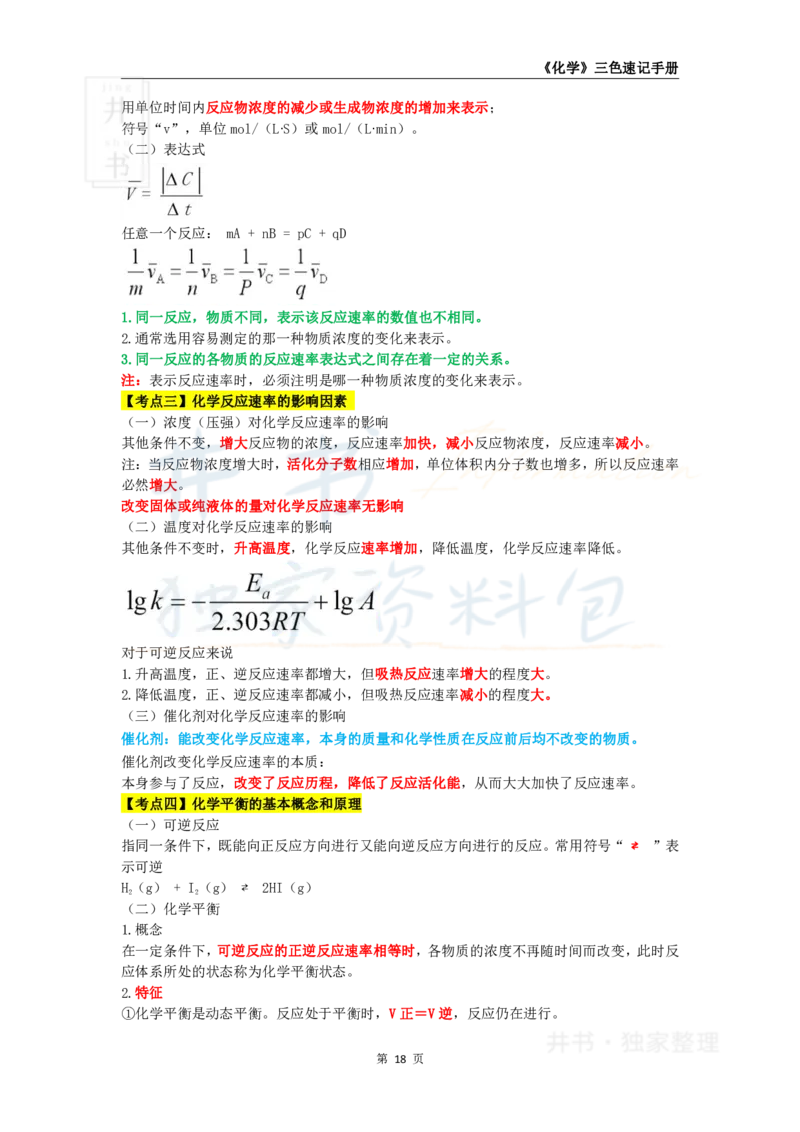
用单位时间内反应物浓度的减少或生成物浓度的增加来表示;
符号“v”,单位mol/(L∙S)或mol/(L∙min)。
(二)表达式
任意一个反应: mA + nB = pC + qD
1.同一反应,物质不同,表示该反应速率的数值也不相同。
2.通常选用容易测定的那一种物质浓度的变化来表示。
3.同一反应的各物质的反应速率表达式之间存在着一定的关系。
注:表示反应速率时,必须注明是哪一种物质浓度的变化来表示。
【考点三】化学反应速率的影响因素
(一)浓度(压强)对化学反应速率的影响
其他条件不变,增大反应物的浓度,反应速率加快,减小反应物浓度,反应速率减小。
注:当反应物浓度增大时,活化分子数相应增加,单位体积内分子数也增多,所以反应速率
必然增大。
改变固体或纯液体的量对化学反应速率无影响
(二)温度对化学反应速率的影响
其他条件不变时,升高温度,化学反应速率增加,降低温度,化学反应速率降低。
对于可逆反应来说
1.升高温度,正、逆反应速率都增大,但吸热反应速率增大的程度大。
2.降低温度,正、逆反应速率都减小,但吸热反应速率减小的程度大。
(三)催化剂对化学反应速率的影响
催化剂:能改变化学反应速率,本身的质量和化学性质在反应前后均不改变的物质。
催化剂改变化学反应速率的本质:
本身参与了反应,改变了反应历程,降低了反应活化能,从而大大加快了反应速率。
【考点四】化学平衡的基本概念和原理
(一)可逆反应
指同一条件下,既能向正反应方向进行又能向逆反应方向进行的反应。常用符号“ ⇄ ”表
示可逆
H(g) + I(g) ⇄ 2HI(g)
2 2
(二)化学平衡
1.概念
在一定条件下,可逆反应的正逆反应速率相等时,各物质的浓度不再随时间而改变,此时反
应体系所处的状态称为化学平衡状态。
2.特征
①化学平衡是动态平衡。反应处于平衡时,V正=V逆,反应仍在进行。
第 18 页《化学》三色速记手册
②化学平衡时,可逆反应处于相对静止状态。外界条件不发生改变,体系中各物质的浓度保
持不变。
③化学平衡是可逆反应达到的最大程度。反应条件不变,到达平衡的途径无论如何变化,最
终所处的平衡状态都是相同的。
④化学平衡是在一定条件下建立的。外界条件一旦发生改变,V正和V逆将不再相等,原来
的平衡即被破坏,直到建立新的动态平衡。
3.平衡常数
(1)经验平衡常数
通过实验测量平衡状态时各组分的浓度或分压而求得的平衡常数
任一反应:aA(g)+ bB(g)⇄ dD(g)+ eE(g)
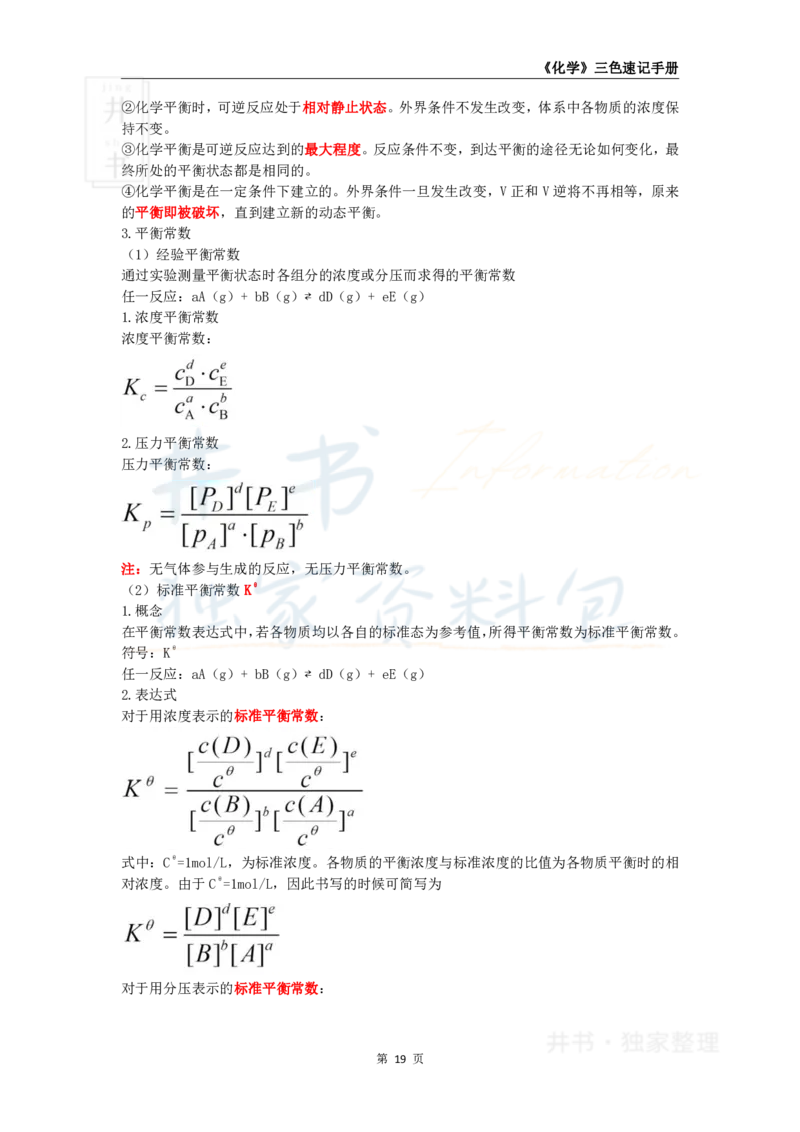
1.浓度平衡常数
浓度平衡常数:
2.压力平衡常数
压力平衡常数:
注:无气体参与生成的反应,无压力平衡常数。
(2)标准平衡常数Kθ
1.概念
在平衡常数表达式中,若各物质均以各自的标准态为参考值,所得平衡常数为标准平衡常数。
符号:Kθ
任一反应:aA(g)+ bB(g)⇄ dD(g)+ eE(g)
2.表达式
对于用浓度表示的标准平衡常数:
式中:Cθ=1mol/L,为标准浓度。各物质的平衡浓度与标准浓度的比值为各物质平衡时的相
对浓度。由于Cθ=1mol/L,因此书写的时候可简写为
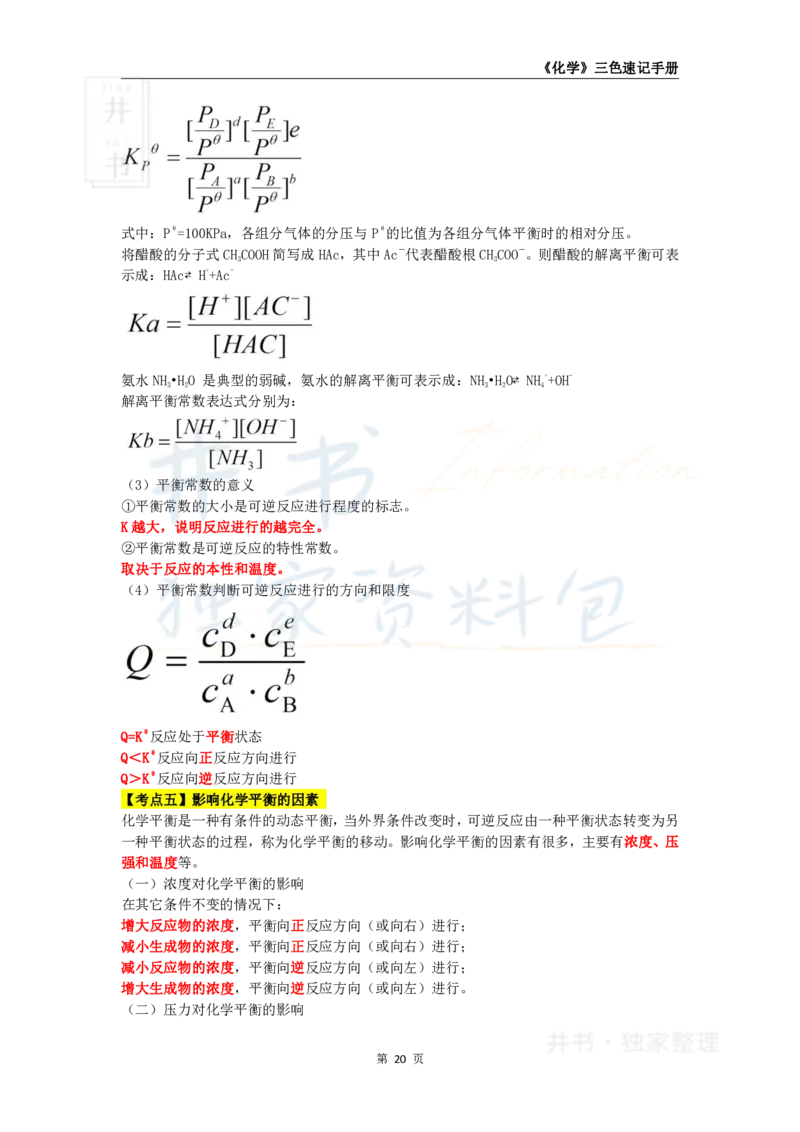
对于用分压表示的标准平衡常数:
第 19 页《化学》三色速记手册
式中:Pθ=100KPa,各组分气体的分压与Pθ的比值为各组分气体平衡时的相对分压。
将醋酸的分子式CHCOOH简写成HAc,其中Ac-代表醋酸根CHCOO-。则醋酸的解离平衡可表
3 3
示成:HAc⇄ H++Ac-
氨水NH•HO 是典型的弱碱,氨水的解离平衡可表示成:NH•HO⇄ NH++OH-
3 2 3 2 4
解离平衡常数表达式分别为:
(3)平衡常数的意义
①平衡常数的大小是可逆反应进行程度的标志。
K越大,说明反应进行的越完全。
②平衡常数是可逆反应的特性常数。
取决于反应的本性和温度。
(4)平衡常数判断可逆反应进行的方向和限度
Q=Kθ反应处于平衡状态
Q<Kθ反应向正反应方向进行
Q>Kθ反应向逆反应方向进行
【考点五】影响化学平衡的因素
化学平衡是一种有条件的动态平衡,当外界条件改变时,可逆反应由一种平衡状态转变为另
一种平衡状态的过程,称为化学平衡的移动。影响化学平衡的因素有很多,主要有浓度、压
强和温度等。
(一)浓度对化学平衡的影响
在其它条件不变的情况下:
增大反应物的浓度,平衡向正反应方向(或向右)进行;
减小生成物的浓度,平衡向正反应方向(或向右)进行;
减小反应物的浓度,平衡向逆反应方向(或向左)进行;
增大生成物的浓度,平衡向逆反应方向(或向左)进行。
(二)压力对化学平衡的影响
第 20 页《化学》三色速记手册
1.反应前后气体分子总数不相等
如:2NO(g) ⇄ NO(g)
2 2 4
(红棕色) (无色)
增大压强,平衡体系向着生成NO 的方向,即向着气体分子总数减小的方向移动,体系中气
2 4
体的颜色由深变浅。
减小压强,平衡体系向着生成NO 的方向,即向着气体分子总数增大的方向移动,体系中气
2
体的颜色由浅变深。
2.反应前后气体分子数相等
如:CO(g)+HO(g)⇄ CO(g)+H(g)
2 2 2
反应物和生成物的浓度发生同等程度的变化,故增大压强,不改变化学反应的平衡状态,化
学平衡不发生移动。
3.惰性气体的影响
(1)在惰性气体存在下达到平衡后,再恒温压缩,ΣVi≠0,平衡向气体分子数减小的方向
移动,ΣVi=0,平衡不移动。
(2)对恒温恒容下已达到平衡的反应,引入惰性气体,反应物和生成物P不变,Q=Kθ ,平
衡不移动。
(3)对恒温恒压下已达到平衡的反应,引入惰性气体,总压不变,体积增大,反应物和生
成物分压减小,如果ΣVi≠0,平衡向气体分子数增大的方向移动。
3.温度对化学平衡的影响
(1)温度对化学平衡的影响
实验:2NO ⇄ NO -56.9KJ/mol
2 2 4
(红棕色) (无色)
1中的气体颜色变深,说明NO 浓度增加,
2
平衡向逆向(即吸热方向)移动。
2中的气体颜色变浅,说明NO 浓度增加,
2 4
平衡向正向(即放热方向)移动
两点说明:
①温度对化学平衡的影响与前两种情况有着本质的区别 :
温度的变化不仅引起化学平衡的移动,而且也会导致k值的变化。
②可逆反应,在一定条件下,
升高温度,化学平衡向着吸热反应的方向移动;
降低温度,化学平衡向着放热反应的方向移动。
3.催化剂对化学平衡的影响
催化剂不能改变标准平衡常数和反应商,因此不能使化学平衡发生移动。但催化剂能同等程
度地加快正、逆反应速率,缩短到达平衡状态的时间。
4.勒夏特列原理
改变平衡系统的条件之一,如温度、压力或浓度,平衡就会向减弱这个改变的方向移动。只
适用于已经达到平衡的体系,对于未达到平衡的体系是不能应用的。
【考点六】酸碱平衡
(一)电离
概念:电解质在水溶液里或熔融状态下产生能够自由移动的离子的过程。
电离的条件:熔融状态(离子化合物)或水溶液里(离子化合物和共价化合物)。
电解质溶液导电的原因:电解质在溶液中发生电离,产生了能够自由移动的离子。
(二)水的电离
第 21 页