文档内容
机密★启用前
试卷类型:A
2025 年广东省普通高中学业水平选择性考试
化学
本试卷共 8页,20小题,满分 100分。考试用时 75分钟。
注意事项:1.答题前,考生务必用黑色字迹的钢笔或签字笔将自己的姓名、考生号、考场号和
座位号填写在答题卡上。用 2B 铅笔将试卷类型(A)填涂在答题卡相应位置上。将条形码横贴
在答题卡右上角“条形码粘贴处”。
2.作答选择题时,选出每小题答案后,用 2B铅笔把答题卡上对应题目选项的答案信息点涂黑:
如需改动,用橡皮擦干净后,再选涂其他答案,答案不能答在试卷上。
3.非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内相应
位置上:如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液。不按
以上要求作答的答案无效。
4.考生必须保持答题卡的整洁。考试结束后,将试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 S 32 Cl 35.5 Ti 48 Fe 56
一、选择题:本大题共 16小题,共 44分。第 1~10小题,每小题 2分;第 11~16小题,每小题
4分。在每小题列出的四个选项中,只有一项符合题目要求。
1.中华传统技艺,凸显人民智慧。下列选项所涉及材料的主要成分属于合金的是( )
A.纸哪吒 B.石印章 C.木活字 D.不锈钢针
2.在法拉第发现苯200周年之际,我国科学家首次制备了以金属M为中心的多烯环配合物。该配合物具有芳
香性,其多烯环结构(如图)形似梅花。该多烯环上( )
A.
1 / 10
C − H 键是共价键 B.有8个碳碳双键
C.共有16个氢原子 D.不能发生取代反应
3.现代科技,增强国力,增进民生福祉。下列说法正确的是( )
A.我国科学家首次测得了月球背面月幔水含量1molH O质量为10g
2
B.利用MoS 成功为金属材料“重塑金身”。MoS 中Mo的化合价为+6
2 2
C.穿上电动机械腿,助力行走不是梦。行走时电池将电能转化为化学能D.沙海养鱼蹚出治沙新路,让沙海沙山变成金山银山。鱼肉富含蛋白质
4.劳动创造美好生活。下列对劳动项目涉及的相关化学知识表述错误的是( )
选项 劳动项目 化学知识
A 向燃煤中加入生石灰以脱硫减排
CaSO +CO2− ƒ CaCO +SO2−
4 3 3 4
B
用
2 / 10
B a C l
2
和盐酸检验粗盐中是否含 S O 24 − B a 2 + + S O 24 − = B a S O
4
C
使用 M g C l
2
溶液点卤制豆腐 MgCl 使蛋白质盐析
2
D 用铁粉、活性炭、食盐等制暖贴 使用时铁粉被氧化,反应放热
A.A B.B C.C D.D
5.声波封印,材料是音乐存储技术的基础。下列说法错误的是( )
A.制作黑胶唱片使用的聚氯乙烯,其单体是CH CH Cl
3 2
B.磁带可由四氧化三铁涂覆在胶带上制成,Fe O 具有磁性
3 4
C.光碟擦写过程中材料在晶态和非晶态间的可逆转换,涉及物理变化
D.固态硬盘芯片常使用单晶硅作为基础材料,单晶硅是一种共价晶体
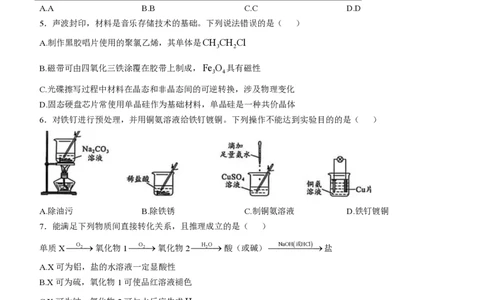
6.对铁钉进行预处理,并用铜氨溶液给铁钉镀铜。下列操作不能达到实验目的的是( )
A.除油污 B.除铁锈 C.制铜氨溶液 D.铁钉镀铜
7.能满足下列物质间直接转化关系,且推理成立的是( )
单质X ⎯ O⎯ 2 → 氧化物1 ⎯ O⎯ 2 → 氧化物2 ⎯ H⎯ O2 ⎯→ 酸(或碱) ⎯ N⎯ a O H⎯ (或 ⎯ H C )l⎯ → 盐
A.X可为铝,盐的水溶液一定显酸性
B.X可为硫,氧化物1可使品红溶液褪色
C.X可为钠,氧化物2可与水反应生成H
2
D.X可为碳,盐的热稳定性:NaHCO Na CO
3 2 3
8.下列陈述Ⅰ与陈述Ⅱ均正确,且两者间具有因果关系的是( )
选项 陈述Ⅰ 陈述Ⅱ
A 浓硝酸保存在棕色试剂瓶中 浓硝酸具有强氧化性
B 向蔗糖中加适量浓硫酸,蔗糖变黑 浓硫酸具有脱水性
C Fe2+与K
3
Fe(CN)
6
可生成蓝色物质 KSCN溶液可用于检验Fe3+D
MnO 与浓盐酸共热,生成黄绿色气体
2
3 / 10
C l
2
+ S O
2
+ 2 H
2
O = H
2
S O
4
+ 2 H C l
A.A B.B C.C D.D
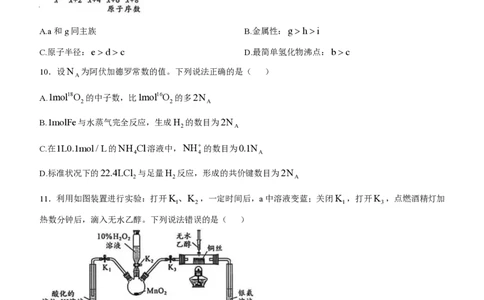
9.元素a~i为短周期元素,其第一电离能与原子序数的关系如图。下列说法正确的是( )
A.a和g同主族 B.金属性:ghi
C.原子半径: e d c D.最简单氢化物沸点: b c
10.设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A. 1 m o l 1 8 O
2
的中子数,比 1 m o l 1 6 O
2
的多 2 N
A
B. 1 m o l F e 与水蒸气完全反应,生成 H
2
的数目为 2 N
A
C.在 1 L 0 . 1 m o l / L 的 N H
4
C l 溶液中, N H +4 的数目为 0 .1 N
A
D.标准状况下的22.4LCl 与足量H 反应,形成的共价键数目为2N
2 2 A
11.利用如图装置进行实验:打开 K 、1 K
2
,一定时间后,a中溶液变蓝;关闭 K
1
,打开 K
3
,点燃酒精灯加
热数分钟后,滴入无水乙醇。下列说法错误的是( )
A.a中现象体现了 I − 的还原性
B.b中H O 既作氧化剂也作还原剂
2 2
C.乙醇滴加过程中,c中的铜丝由黑变红,说明乙醇被氧化
D.d中有银镜反应发生,说明c中产物有乙酸
12.CuCl微溶于水,但在Cl−浓度较高的溶液中因形成 CuCl − 和 CuCl 2− 而溶解.将适量CuCl完全溶于
2 3盐酸,得到含
4 / 10
C u C l
2
− 和 C u C l
3
2 − 的溶液,下列叙述正确的是( )
A.加水稀释, C u C l
3
2 − 浓度一定下降
B.向溶液中加入少量NaCl固体,
CuCl −
浓度一定上升
2
C. H C u C l
2
的电离方程式为: H C u C l
2
= H + + C u + + 2 C l −
D.体系中,c ( Cu+) +c ( H+) =c ( Cl−) +c ( CuCl −) +c ( CuCl 2−) +c ( OH−)
2 3
13.由结构不能推测出对应性质的是( )
选项 结构 性质
A
SO 的VSEPR模型为平面三角形 SO 具有氧化性
3 3
B 钾和钠的原子结构不同,电子跃迁时能量变化不同 钾和钠的焰色不同
C 乙烯和乙炔分子均含有 π 键 两者均可发生加聚反应
D 石墨层中未参与杂化的p轨道中的电子,可在整个碳原子平面中运动 石墨具有类似金属的导电性
A.A B.B C.C D.D
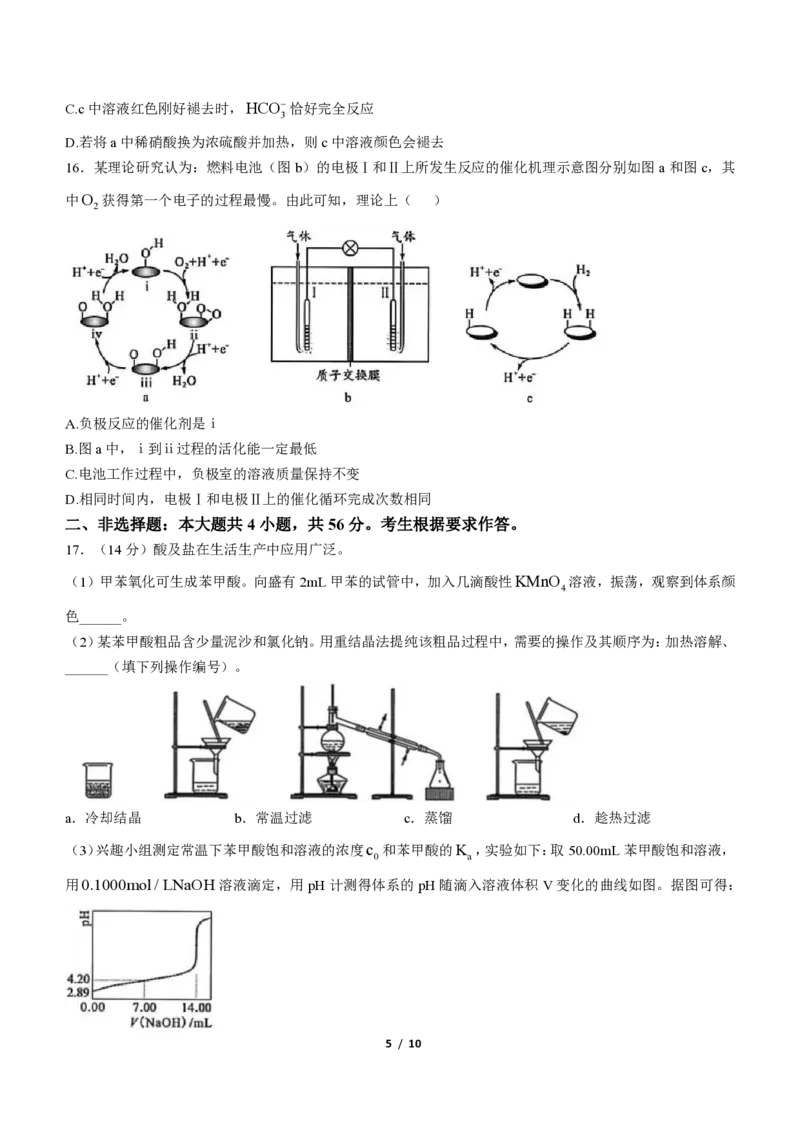
14.一种高容量水系电池示意图如图。已知:放电时,电极Ⅱ上 M n O
2
减少;电极材料每转移1mol电子,对
应的理论容量为 2 6 . 8 A h 。下列说法错误的是( )
A.充电时Ⅱ为阳极
B.放电时Ⅱ极室中溶液的pH降低
C.放电时负极反应为: M n S − 2 e − = S + M n 2 +
D.充电时16gS能提供的理论容量为 2 6 . 8 A h
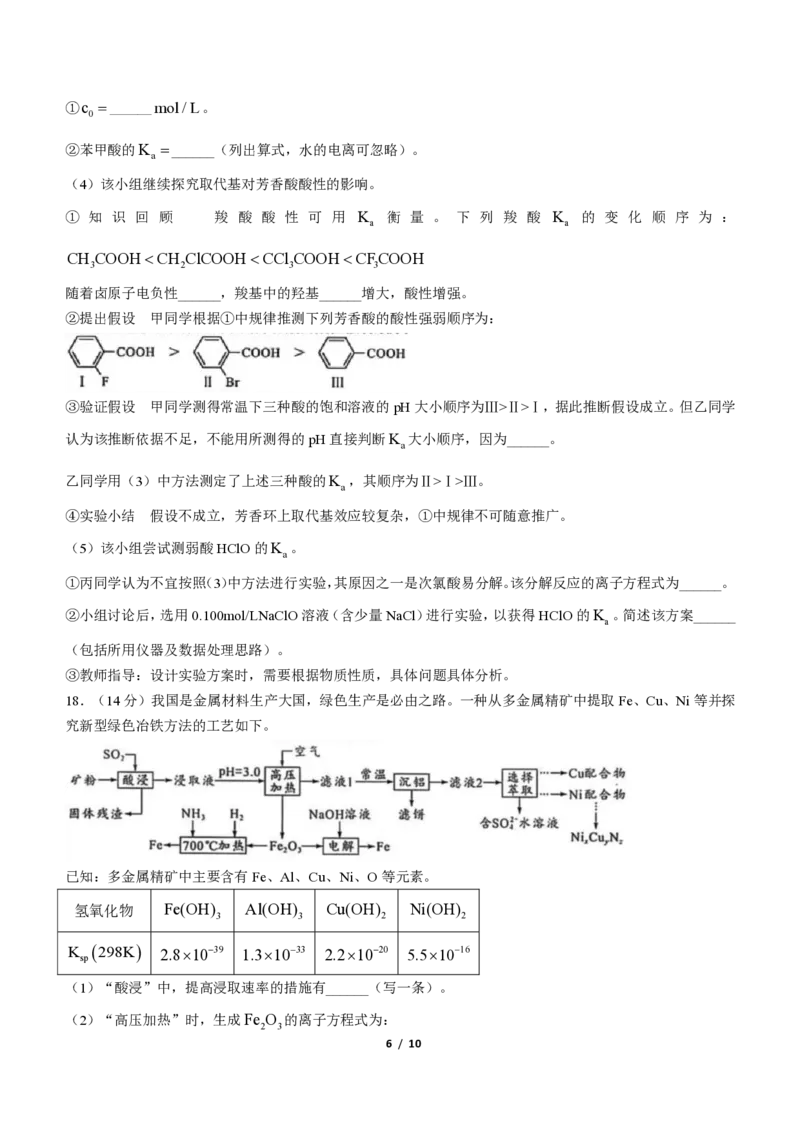
15.按如图组装装置并进行实验:将铜丝插入溶液中,当c中红色褪去时,将铜丝拔离液面。下列叙述错误的
是( )
A.a中有化合反应发生,并有颜色变化
B.b中气体变红棕色时,所含氮氧化物至少有两种C.c中溶液红色刚好褪去时,
5 / 10
H C O −3 恰好完全反应
D.若将a中稀硝酸换为浓硫酸并加热,则c中溶液颜色会褪去
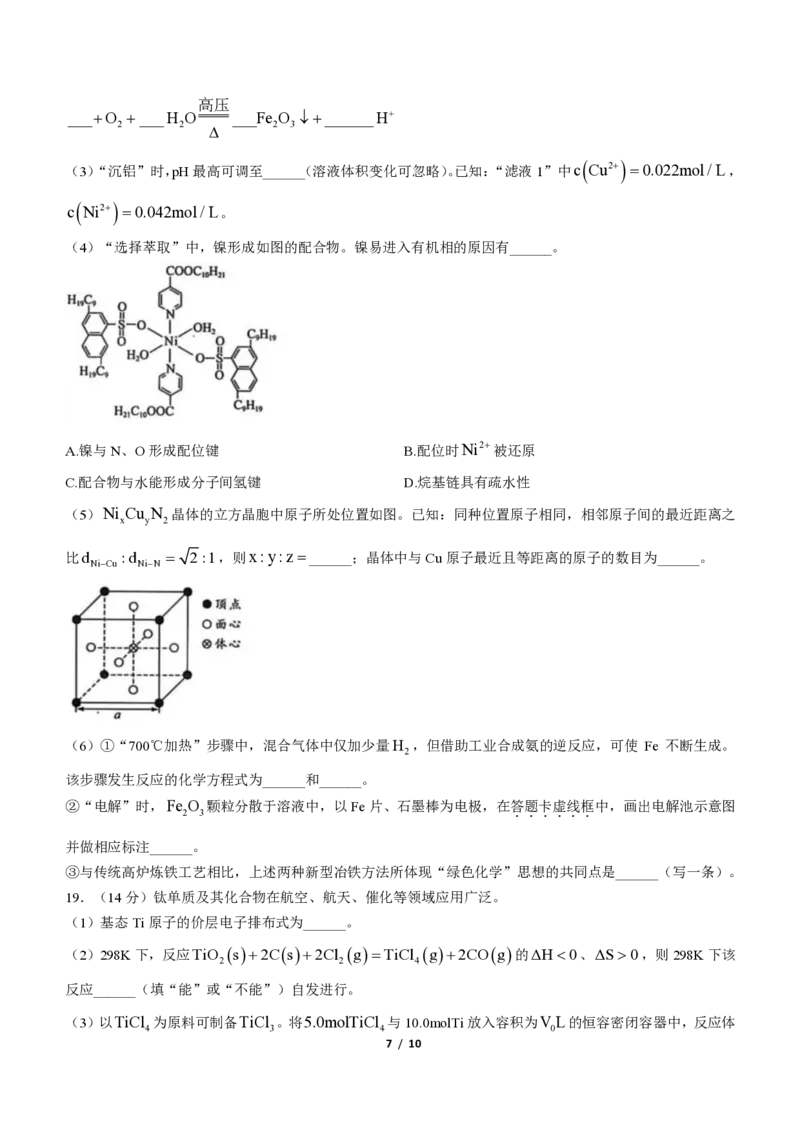
16.某理论研究认为:燃料电池(图 b)的电极Ⅰ和Ⅱ上所发生反应的催化机理示意图分别如图 a和图c,其
中 O
2
获得第一个电子的过程最慢。由此可知,理论上( )
A.负极反应的催化剂是ⅰ
B.图a中,ⅰ到ⅱ过程的活化能一定最低
C.电池工作过程中,负极室的溶液质量保持不变
D.相同时间内,电极Ⅰ和电极Ⅱ上的催化循环完成次数相同
二、非选择题:本大题共 4小题,共 56分。考生根据要求作答。
17.(14分)酸及盐在生活生产中应用广泛。
(1)甲苯氧化可生成苯甲酸。向盛有2mL甲苯的试管中,加入几滴酸性 K M n O
4
溶液,振荡,观察到体系颜
色______。
(2)某苯甲酸粗品含少量泥沙和氯化钠。用重结晶法提纯该粗品过程中,需要的操作及其顺序为:加热溶解、
______(填下列操作编号)。
a.冷却结晶 b.常温过滤 c.蒸馏 d.趁热过滤
(3)兴趣小组测定常温下苯甲酸饱和溶液的浓度 c
0
和苯甲酸的 K
a
,实验如下:取50.00mL苯甲酸饱和溶液,
用 0 . 1 0 0 0 m o l / L N a O H 溶液滴定,用pH计测得体系的pH随滴入溶液体积V变化的曲线如图。据图可得:①
6 / 10
c
0
= ______ m o l / L 。
②苯甲酸的K =______(列出算式,水的电离可忽略)。
a
(4)该小组继续探究取代基对芳香酸酸性的影响。
① 知 识 回 顾 羧 酸 酸 性 可 用 K 衡 量 。 下 列 羧 酸
a
K
a
的 变 化 顺 序 为 :
C H
3
C O O H C H
2
C l C O O H C C l
3
C O O H C F
3
C O O H
随着卤原子电负性______,羧基中的羟基______增大,酸性增强。
②提出假设 甲同学根据①中规律推测下列芳香酸的酸性强弱顺序为:
③验证假设 甲同学测得常温下三种酸的饱和溶液的pH大小顺序为Ⅲ>Ⅱ>Ⅰ,据此推断假设成立。但乙同学
认为该推断依据不足,不能用所测得的pH直接判断 K
a
大小顺序,因为______。
乙同学用(3)中方法测定了上述三种酸的 K
a
,其顺序为Ⅱ>Ⅰ>Ⅲ。
④实验小结 假设不成立,芳香环上取代基效应较复杂,①中规律不可随意推广。
(5)该小组尝试测弱酸HClO的 K
a
。
①丙同学认为不宜按照(3)中方法进行实验,其原因之一是次氯酸易分解。该分解反应的离子方程式为______。
②小组讨论后,选用0.100mol/LNaClO溶液(含少量NaCl)进行实验,以获得HClO的 K
a
。简述该方案______
(包括所用仪器及数据处理思路)。
③教师指导:设计实验方案时,需要根据物质性质,具体问题具体分析。
18.(14分)我国是金属材料生产大国,绿色生产是必由之路。一种从多金属精矿中提取Fe、Cu、Ni等并探
究新型绿色冶铁方法的工艺如下。
已知:多金属精矿中主要含有Fe、Al、Cu、Ni、O等元素。
氢氧化物 Fe(OH) Al(OH)
3 3
C u ( O H )
2
Ni(OH)
2
K (298K)
sp
2 .8 1 0 − 3 9 1.310−33 2 .2 1 0 − 2 0 5 .5 1 0 − 1 6
(1)“酸浸”中,提高浸取速率的措施有______(写一条)。
(2)“高压加热”时,生成Fe O 的离子方程式为:
2 37 / 10
_ _ _ + O
2
+ _ _ _ H
2
O
高
压
_ _ _ F e
2
O
3
+ _ _ _ _ _ _ H +
(3)“沉铝”时,pH最高可调至______(溶液体积变化可忽略)。已知:“滤液1”中 c ( C u 2 + ) = 0 . 0 2 2 m o l / L ,
c
( Ni2+)
=0.042mol/L。
(4)“选择萃取”中,镍形成如图的配合物。镍易进入有机相的原因有______。
A.镍与N、O形成配位键 B.配位时Ni2+被还原
C.配合物与水能形成分子间氢键 D.烷基链具有疏水性
(5) N i
x
C u
y
N
2
晶体的立方晶胞中原子所处位置如图。已知:同种位置原子相同,相邻原子间的最近距离之
比 d
N i− C u
: d
N i− N
= 2 : 1 ,则x:y:z =______;晶体中与Cu原子最近且等距离的原子的数目为______。
(6)①“700℃加热”步骤中,混合气体中仅加少量 H
2
,但借助工业合成氨的逆反应,可使 Fe 不断生成。
该步骤发生反应的化学方程式为______和______。
②“电解”时, F e
2
O
3
颗粒分散于溶液中,以Fe片、石墨棒为电极,在答题卡虚线框中,画出电解池示意图
......
并做相应标注______。
③与传统高炉炼铁工艺相比,上述两种新型冶铁方法所体现“绿色化学”思想的共同点是______(写一条)。
19.(14分)钛单质及其化合物在航空、航天、催化等领域应用广泛。
(1)基态Ti原子的价层电子排布式为______。
(2)298K下,反应TiO (s)+2C(s)+2Cl (g)=TiCl (g)+2CO(g)的ΔH0、ΔS0,则298K下该
2 2 4
反应______(填“能”或“不能”)自发进行。
(3)以TiCl 为原料可制备TiCl 。将5.0molTiCl 与10.0molTi放入容积为VL的恒容密闭容器中,反应体
4 3 4 0系存在下列过程。
编号 过程
8 / 10
Δ H
(a) T i ( s ) + T i C l
4
( g ) ƒ 2 T i C l
2
( s ) ΔH
1
(b) T i C l
2
( s ) + T i C l
4
( g ) ƒ 2 T i C l
3
( g ) +200.1kJ/mol
(c) T i ( s ) + 3 T i C l
4
( g ) ƒ 4 T i C l
3
( g ) + 1 3 2 . 4 k J / m o l
(d) TiCl (g)ƒ TiCl (s) ΔH
3 3 2
①ΔH =______kJ/mol。
1
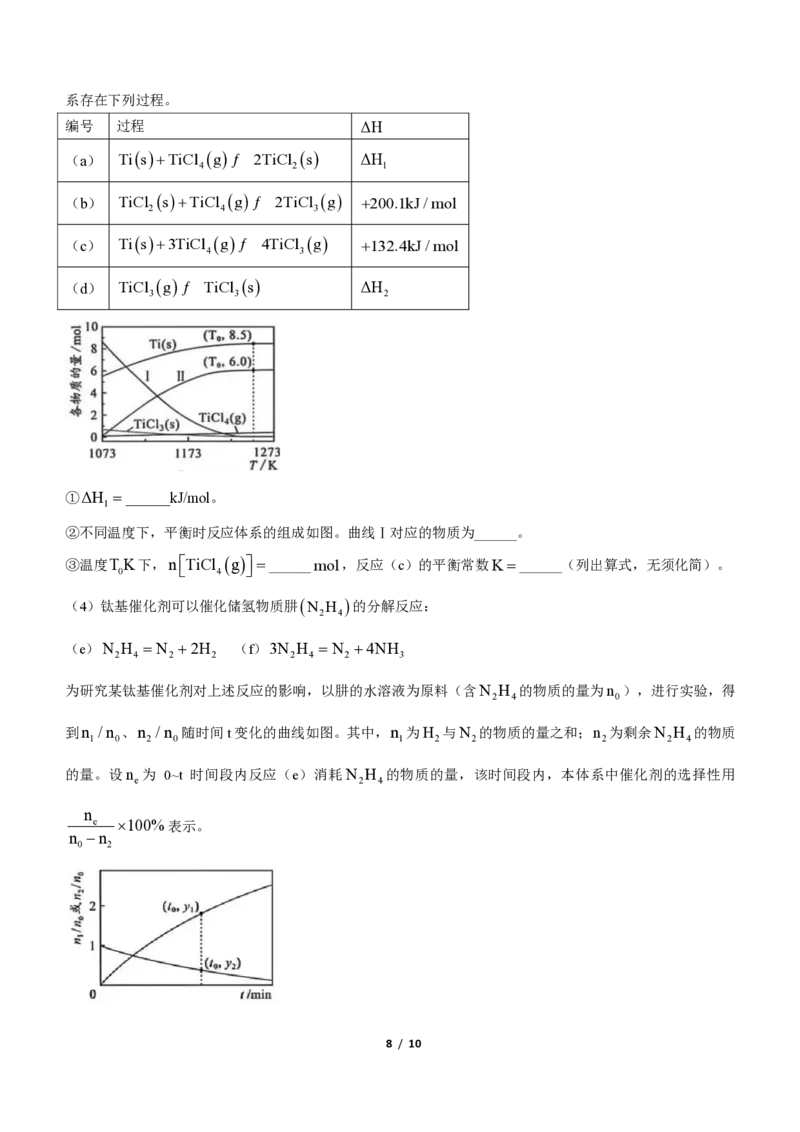
②不同温度下,平衡时反应体系的组成如图。曲线Ⅰ对应的物质为______。
③温度T
0
K下,n
TiCl
4
(g)
=______ m o l ,反应(c)的平衡常数 K = ______(列出算式,无须化简)。
(4)钛基催化剂可以催化储氢物质肼 ( N
2
H
4
) 的分解反应:
(e) N
2
H
4
= N
2
+ 2 H
2
(f) 3 N
2
H
4
= N
2
+ 4 N H
3
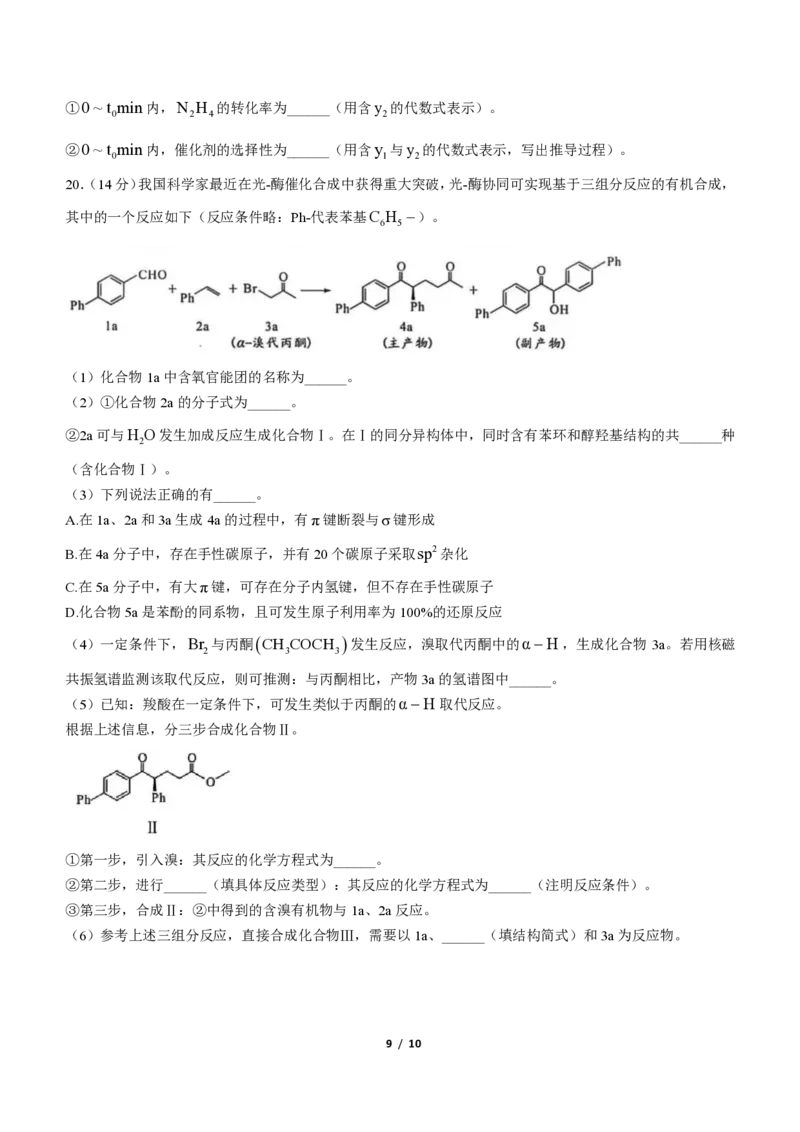
为研究某钛基催化剂对上述反应的影响,以肼的水溶液为原料(含 N
2
H
4
的物质的量为 n
0
),进行实验,得
到 n
1
/ n
0
、 n
2
/ n
0
随时间t变化的曲线如图。其中, n
1
为 H
2
与 N
2
的物质的量之和; n
2
为剩余 N
2
H
4
的物质
的量。设 n
e
为 0~t 时间段内反应(e)消耗N H 的物质的量,该时间段内,本体系中催化剂的选择性用
2 4
n
0
n
−
e
n
2
1 0 0 % 表示。①
9 / 10
0 ~ t
0
m i n 内, N
2
H
4
的转化率为______(用含 y
2
的代数式表示)。
② 0 ~ t
0
m i n 内,催化剂的选择性为______(用含 y
1
与 y
2
的代数式表示,写出推导过程)。
20.(14分)我国科学家最近在光-酶催化合成中获得重大突破,光-酶协同可实现基于三组分反应的有机合成,
其中的一个反应如下(反应条件略:Ph-代表苯基 C
6
H
5
− )。
(1)化合物1a中含氧官能团的名称为______。
(2)①化合物2a的分子式为______。
②2a可与H O发生加成反应生成化合物Ⅰ。在Ⅰ的同分异构体中,同时含有苯环和醇羟基结构的共______种
2
(含化合物Ⅰ)。
(3)下列说法正确的有______。
A.在1a、2a和3a生成4a的过程中,有 π 键断裂与σ键形成
B.在4a分子中,存在手性碳原子,并有20个碳原子采取sp2杂化
C.在5a分子中,有大 π 键,可存在分子内氢键,但不存在手性碳原子
D.化合物5a是苯酚的同系物,且可发生原子利用率为100%的还原反应
(4)一定条件下, B r
2
与丙酮 ( C H
3
C O C H
3
) 发生反应,溴取代丙酮中的 α − H ,生成化合物 3a。若用核磁
共振氢谱监测该取代反应,则可推测:与丙酮相比,产物3a的氢谱图中______。
(5)已知:羧酸在一定条件下,可发生类似于丙酮的α−H取代反应。
根据上述信息,分三步合成化合物Ⅱ。
①第一步,引入溴:其反应的化学方程式为______。
②第二步,进行______(填具体反应类型):其反应的化学方程式为______(注明反应条件)。
③第三步,合成Ⅱ:②中得到的含溴有机物与1a、2a反应。
(6)参考上述三组分反应,直接合成化合物Ⅲ,需要以1a、______(填结构简式)和3a为反应物。10 / 10