文档内容
湖北省襄阳随州部分高中2024—2025学年下学期期末联考
高二化学试题
本试卷共8页,19题,全卷满分100分,考试用时75分钟。
★祝考试顺利★
注意事项:
1、答题前,请将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并
将准考证号条形码粘贴在答题卡上的制定位置。
2、选择题的作答:每小题选出答案后,用 2B铅笔把答题卡上对应题目的答案标号涂
黑,写在试卷、草稿纸和答题卡上的非答题区域均无效。
3、非选择题作答:用黑色签字笔直接答在答题卡对应的答题区域内,写在试卷、草稿
纸和答题卡上的非答题区域均无效。
4、考试结束后,请将答题卡上交。
一、选择题:本题共15小题,每题3分,共45分,每小题仅有一项是符合题意。
1.下列事实不能用勒夏特列原理解释的是( )
A.溴水中有下列平衡:Br +HOHBr+HBrO,当加入少量AgNO 溶液后,溶液
2 2 3
的颜色变浅
B.对于反应:2HI(g)H(g)+I(g),缩小容器的容积可使平衡体系的颜色变深
2 2
C.反应:CO(g)+NO (g)CO(g)+NO(g) ΔH<0,升高温度可使平衡向逆反应方向
2 2
移动
D.对于合成NH 的反应,为提高NH 的产率,理论上应采取低温措施
3 3
2.将SO 和O 通入恒容密闭容器中,一定条件下发生反应
2 2
2SO (g)+O(g)2SO (g) ΔH=-197 kJ/mol,其中SO 的平衡转化率随温度、压强的变
2 2 3 2
化关系如图所示,下列说法正确的是( )
A.p<p
1 2
B.达平衡时缩小容器体积,正反应速率增大,逆反应速率减小
C.SO 的键角小于SO
2 3D.X点和Y点对应的化学平衡常数K(X)<K(Y)
3.已知次磷酸(H PO )为一元酸,欲证明它是弱电解质,下列操作方法不正确的是(
3 2
)
A.用物质的量浓度相同的NaCl溶液和NaH PO 溶液进行导电性实验,比较灯泡的亮
2 2
度
B.用一定浓度的NaOH溶液分别滴定等体积、等pH的盐酸和次磷酸溶液,比较消耗
碱液的体积
C.加热滴有酚酞试液的NaH PO 溶液,溶液颜色变深
2 2
D.常温下,稀释0.1 mol·L-1次磷酸溶液至原溶液体积的100倍,测得pH在4~5之
间
4.常温下,已知K (ZnS)=1.6×10-24,K (CuS)=6.3×10-36。如图表示CuS和ZnS饱
sp sp
和溶液中阳离子(R2+)浓度与阴离子(S2-)浓度的负对数关系。下列说法不正确的是( )
A.线A表示的是CuS,线B表示的是ZnS
B.向CuS饱和溶液中加入CuCl 固体,CuS的溶解平衡逆向移动,K (CuS)减小
2 sp
C.p点表示CuS或ZnS的不饱和溶液
D.向线A表示的溶液中加入NaS溶液,不可能实现n点到m点的转化
2
5.下列说法正确的是( )
A.NaCO 溶液可用带玻璃塞的试剂瓶保存
2 3
B.将饱和的AlCl 溶液蒸干并灼烧,可得到AlCl 固体
3 3
C.配制FeCl 溶液时,可将FeCl 固体溶解在硫酸中,然后加水稀释
3 3
D.配制SbCl 溶液时,应将SbCl 固体溶于较浓的盐酸中,再加水稀释到所需浓度
3 3
6.某温度下,HNO 和CHCOOH的电离常数分别为5.0×10-4和1.7×10-5。将pH和
2 3
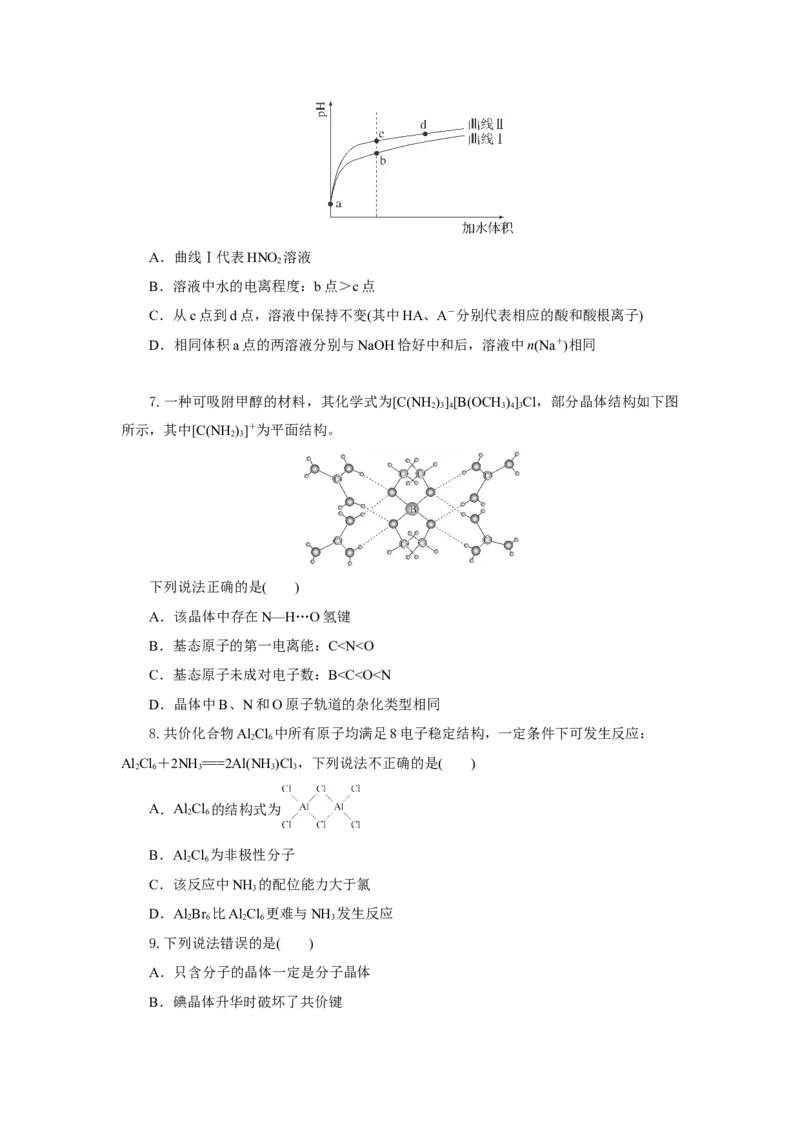
体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的
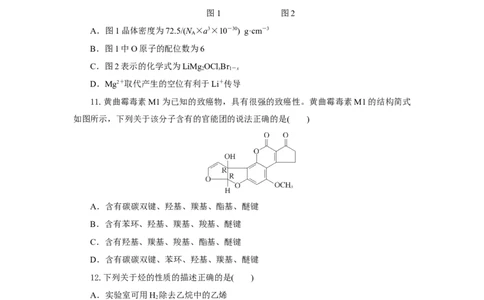
是( )A.曲线Ⅰ代表HNO 溶液
2
B.溶液中水的电离程度:b点>c点
C.从c点到d点,溶液中保持不变(其中HA、A-分别代表相应的酸和酸根离子)
D.相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同
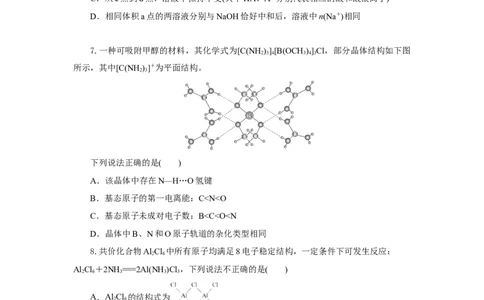
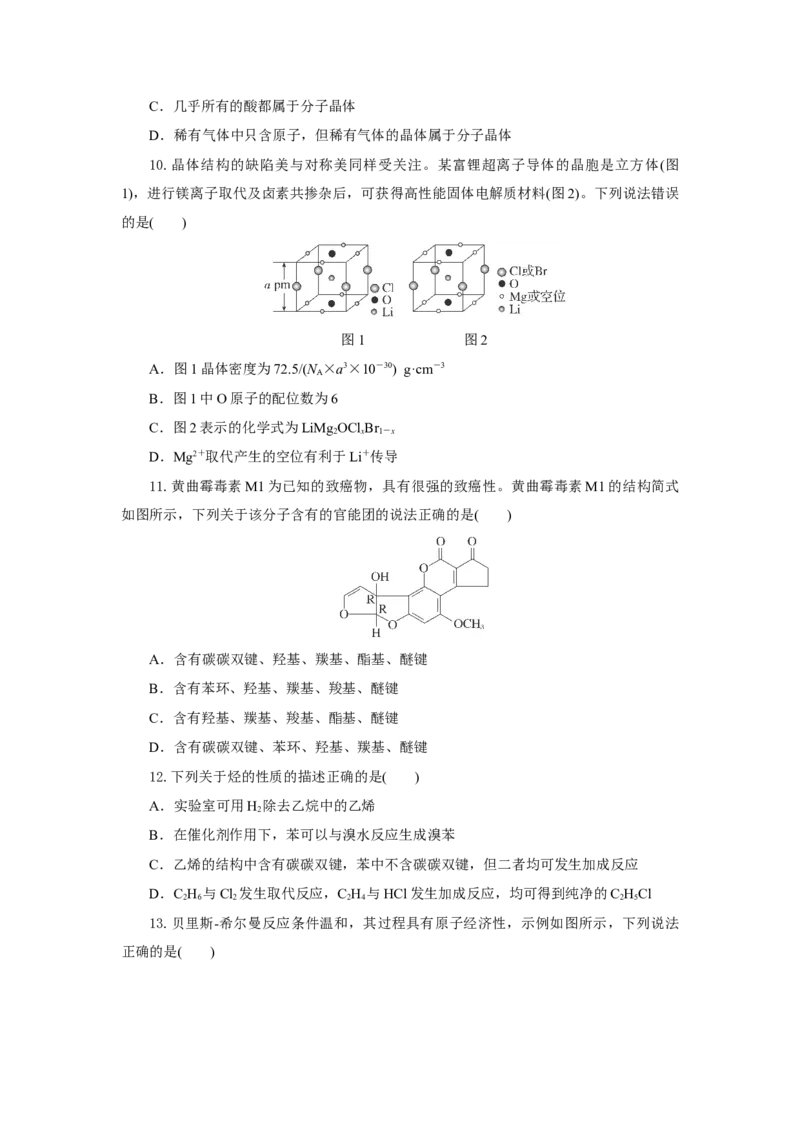
7.一种可吸附甲醇的材料,其化学式为[C(NH )][B(OCH )]Cl,部分晶体结构如下图
2 3 4 3 4 3
所示,其中[C(NH )]+为平面结构。
2 3
下列说法正确的是( )
A.该晶体中存在N—H…O氢键
B.基态原子的第一电离能:C”“<”或“=”)c(HCO);、
反应NH+HCO+HO===NH·H O+HCO 的平衡常数 K=____________。(已知常温下
2 3 2 2 3
NH ·H O的电离常数K =2×10-5,HCO 的电离常数K =4×10-7,K =4×10-11)(4
3 2 b 2 3 a1 a2
分)
(2)已知K [Mg(OH) ]=2×10-11,常温下在某MgSO 溶液里c(Mg2+)=0.002 mol·L-1,
sp 2 4
如果生成Mg(OH) 沉淀,应调整溶液pH,使之大于________;
2
在0.20 L的0.002 mol·L-1 MgSO 溶液中加入等体积的0.10 mol·L-1的氨水溶液,电离
4
常数K (NH ·H O)=2×10-5,试通过计算判断__________(填“有”或“无”)Mg(OH) 沉淀
b 3 2 2
生成。(4分)
(3)CuCl悬浊液中加入NaS,发生的反应为
2
2CuCl(s)+S2-(aq)Cu S(s)+2Cl-(aq),该反应的平衡常数 K=____________[已知
2
K (CuCl)=1.2×10-6,K (Cu S)=2.5×10-43]。(3分)
sp sp 2
(4)已知常温下HSO 的电离常数:K =1.0×10-1.9,K =1.0×10-7.2,
2 3 a1 a2
计算0.1 mol·L-1NaHSO 溶液的pH为________(忽略SO的二级水解)。(3分)
3
18.(14分)现有几组物质的熔点(℃)数据如表所示:
A组 B组 C组 D组
金刚石:3550 Li:181 HF:-83 NaCl:801硅晶体:1410 Na:98 HCl:-115 KCl:776
硼晶体:2300 K:64 HBr:-89 RbCl:718
二氧化硅:
Rb:39 HI:-51 CsCl:645
1723
据此回答下列问题:
(1)A组属于________晶体,其熔化时克服的微粒间的作用力是______________。 (4
分)
(2)B组晶体共同的物理性质是________(填序号)。 (3分)
①有金属光泽 ②导电性 ③导热性
④延展性
(3)C组中HF熔点反常是因为_______________________________。(4分)
(4)D组晶体可能具有的性质是________(填序号)。 (3分)
①硬度小 ②水溶液能导电 ③固体能导电
④熔融状态能导电
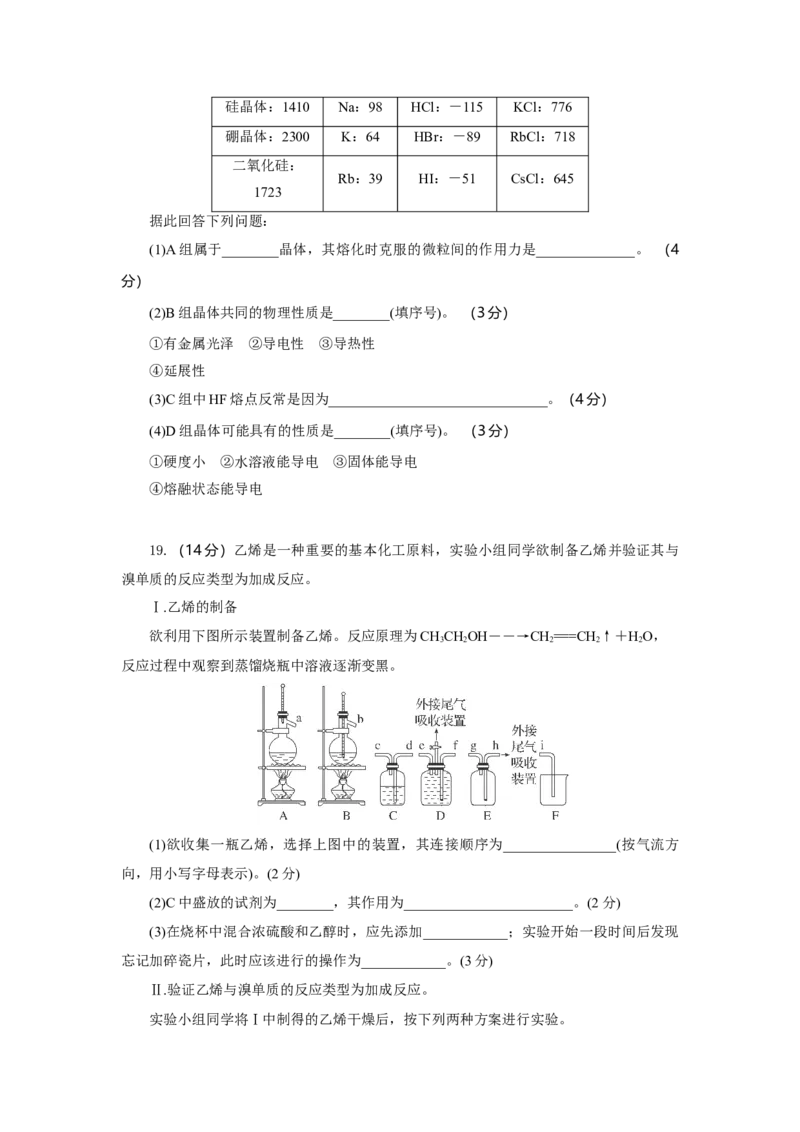
19.(14分)乙烯是一种重要的基本化工原料,实验小组同学欲制备乙烯并验证其与
溴单质的反应类型为加成反应。
Ⅰ.乙烯的制备
欲利用下图所示装置制备乙烯。反应原理为CHCHOH――→CH===CH ↑+HO,
3 2 2 2 2
反应过程中观察到蒸馏烧瓶中溶液逐渐变黑。
(1)欲收集一瓶乙烯,选择上图中的装置,其连接顺序为________________(按气流方
向,用小写字母表示)。(2分)
(2)C中盛放的试剂为________,其作用为________________________。(2分)
(3)在烧杯中混合浓硫酸和乙醇时,应先添加____________;实验开始一段时间后发现
忘记加碎瓷片,此时应该进行的操作为____________。(3分)
Ⅱ.验证乙烯与溴单质的反应类型为加成反应。
实验小组同学将Ⅰ中制得的乙烯干燥后,按下列两种方案进行实验。方案 操作 现象
一 将纯净的乙烯通入溴水中 溴水褪色
①溴的CCl 溶液褪色
4
②___________________________________
向充满纯净乙烯的塑料瓶中注入适量
二 __________________________
溴的CCl 溶液,振荡
4
_____________________________________
________________________
(4)乙烯与溴单质发生加成反应的化学方程式为
_____________________________________________________________
_______________________________________________________。(2分)
(5)方案一不能证明乙烯与溴单质发生了加成反应,原因为__________。(2分)
(6)方案二中现象②应为_______________________,要想用此方案证明乙烯与溴单质
发生的反应是加成反应,还需补充的实验为继续向方案二塑料瓶中加入少量
__________________,振荡后,若________________________,证明发生了加成反应。(3
分)