文档内容
湖北省孝感市部分高中2024—2025学年下学期期末联考
高二化学试题
本试卷共8页,19题,全卷满分100分,考试用时75分钟。
★祝考试顺利★
注意事项:
1、答题前,请将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并
将准考证号条形码粘贴在答题卡上的制定位置。
2、选择题的作答:每小题选出答案后,用 2B铅笔把答题卡上对应题目的答案标号涂
黑,写在试卷、草稿纸和答题卡上的非答题区域均无效。
3、非选择题作答:用黑色签字笔直接答在答题卡对应的答题区域内,写在试卷、草稿
纸和答题卡上的非答题区域均无效。
4、考试结束后,请将答题卡上交。
一、选择题:本题共15小题,每题3分,共45分,每小题仅有一项是符合题意。
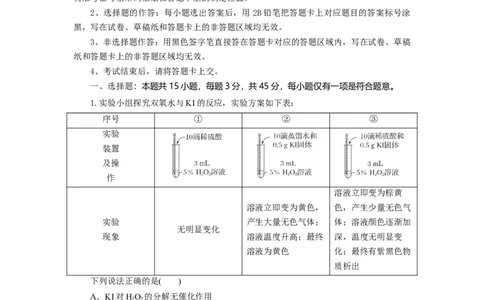
1.实验小组探究双氧水与KI的反应,实验方案如下表:
序号 ① ② ③
实验
装置
及操
作
溶液立即变为棕黄
溶液立即变为黄色, 色,产生少量无色气
实验 产生大量无色气体; 体;溶液颜色逐渐加
无明显变化
现象 溶液温度升高;最终 深,温度无明显变
溶液为黄色 化;最终有紫黑色物
质析出
下列说法正确的是( )
A.KI对HO 的分解无催化作用
2 2
B.对比实验②和③,酸性条件下HO 氧化KI的速率更大
2 2
C.实验②③中的温度差异说明HO 氧化KI的反应放出大量热
2 2
D.对比实验②和③,③中的现象可能是因为HO 分解的速率大于HO 氧化KI的速
2 2 2 2
率
2.甲酸常被用于橡胶、医药等工业。在一定条件下可分解生成CO和HO。在有、无
2
催化剂条件下的能量与反应历程的关系如图所示。下列说法错误的是( )A.途径一未使用催化剂,途径二比途径一甲酸平衡转化率高
B.ΔH=ΔH<0,E >E
1 2 a1 a2
C.途径二H+参与反应,通过改变反应途径加快反应速率
D.途径二反应的快慢由生成 的速率决定
3.向碘水中加入KI溶液,发生反应:I-(aq)+I(aq)I(aq),充分反应达平衡后,测
2
得微粒浓度如表:
微粒 I- I I
2
浓度(mol·L-1) 2.5×10-3 2.5×10-3 4.0×10-3
下列说法不正确的是( )
A.向所得溶液中加入CCl ,振荡静置,水层c(I)降低
4 2
B.向所得溶液中加入等体积水,c(I)<1.25×10-3mol·L-1
2
C.该温度下,反应I-+II的K=640
2
D.配制碘水时,加入少量KI,可促进I 的溶解
2
4.硅是大数据时代的关键材料。工业上常在1800~2000 ℃时,用碳单质还原的方法
制取单质硅。涉及反应的相关数据如表所示。下列说法正确的是( )
ΔH/ ΔS/(J·
反应
(kJ·mol-1) K-1·mol-1)
反应(1):SiO(s)+2C(s)===Si(s)+
2
+687.27 359.04
2CO(g)
反应(2):SiO(s)+C(s)===Si(s)+
2
+514.85 183.35
CO(g)
2
A.反应(1)可证明Si的还原性大于C
B.生活中利用单晶硅良好的导光性能作光导纤维C.工业生产条件下反应(2)无法自发进行
D.C(s)+CO(g)===2CO(g) ΔH=-172.42 kJ·mol-1
2
5.由于血液中存在如下平衡过程:
CO(g)CO(aq)、CO(aq)+HO(l)HCO(aq)、HCO(aq)H+(aq)+HCO(aq),使血
2 2 2 2 2 3 2 3
液的pH维持在7.35~7.45。如超出这个范围会造成酸中毒(pH过低)或碱中毒(pH过高),急
性中毒时需静脉注射NH Cl或NaHCO 进行治疗。下列叙述正确的是( )
4 3
A.血液中CO 浓度过高会导致酸中毒,使血液中的值增大
2
B.治疗碱中毒时,患者需降低呼吸频率,以增加血液中CO 浓度
2
C.急性酸中毒时,救治方式是静脉注射NH Cl溶液
4
D.酸或碱中毒时,会导致血液中的酶发生水解
6.室温下,向20.00 mL 0.1000 mol·L-1盐酸中滴加0.1000 mol·L-1 NaOH溶液,溶液
的pH随NaOH溶液体积的变化如图。已知lg 5≈0.7。下列说法不正确的是( )
A.NaOH与盐酸恰好完全反应时,pH=7
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
D.V(NaOH)=30.00 mL时,pH≈12.3
7.20 ℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1氨水的图像如图所示,下列说
法正确的是( )
A.a点时c(Cl-)=2c(NH ·H O)+2c(NH)
3 2
B.b点表示酸碱恰好完全反应
C.c点时c(NH)>c(Cl-)>c(H+)>c(OH-)
D.a、b、c、d点均有c(NH)+c(H+)=c(Cl-)+c(OH-)
8.一定温度下,将足量的BaSO 固体溶于50 mL水中,充分搅拌,慢慢加入NaCO 固
4 2 3
体,随着c(CO)增大,溶液中c(Ba2+)的变化曲线如图所示。下列说法正确的是( )A.BaCO 的K =2.5×10-9
3 sp
B.加入NaCO 固体,立即有BaCO 固体生成
2 3 3
C.该温度下,K (BaSO)>K (BaCO)
sp 4 sp 3
D.曲线BC段内,=
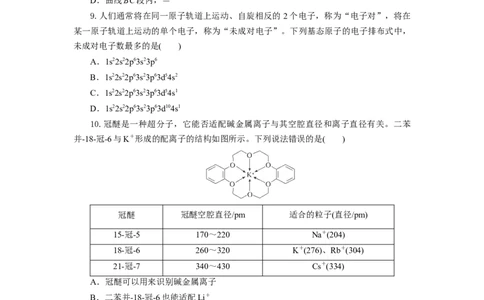
9.人们通常将在同一原子轨道上运动、自旋相反的 2个电子,称为“电子对”,将在
某一原子轨道上运动的单个电子,称为“未成对电子”。下列基态原子的电子排布式中,
未成对电子数最多的是( )
A.1s22s22p63s23p6
B.1s22s22p63s23p63d54s2
C.1s22s22p63s23p63d54s1
D.1s22s22p63s23p63d104s1
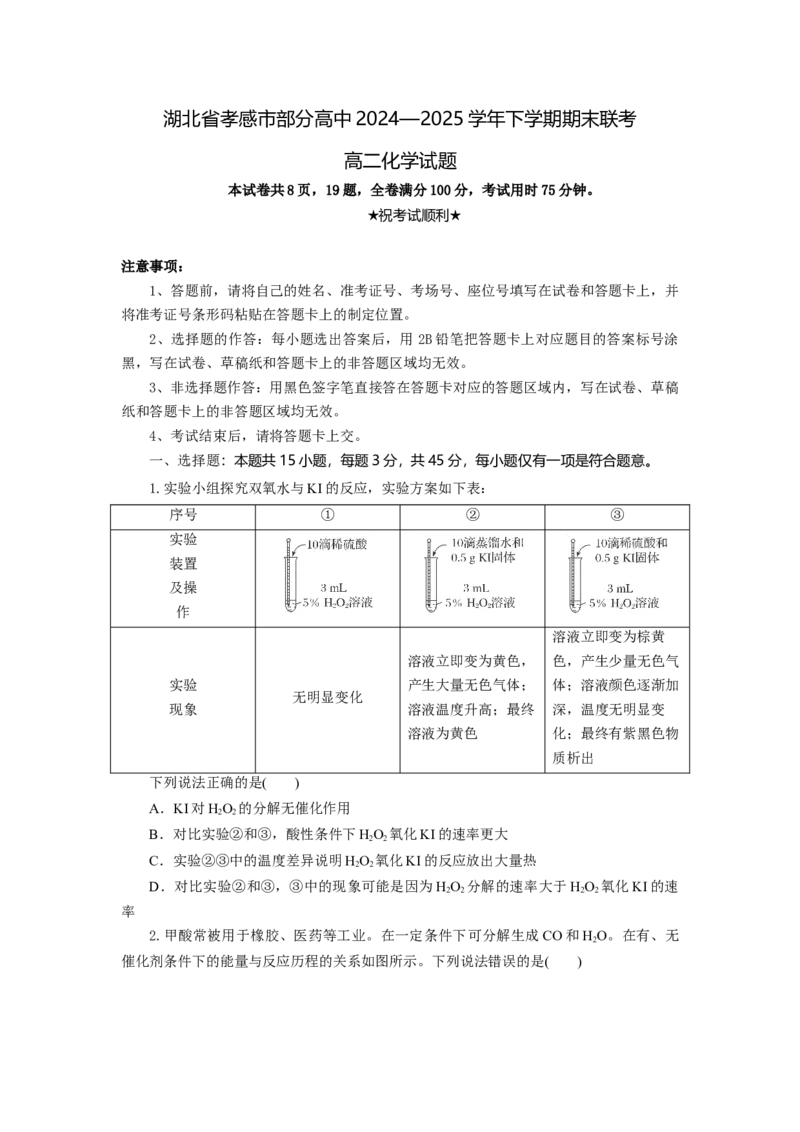
10.冠醚是一种超分子,它能否适配碱金属离子与其空腔直径和离子直径有关。二苯
并-18-冠-6与K+形成的配离子的结构如图所示。下列说法错误的是( )
冠醚 冠醚空腔直径/pm 适合的粒子(直径/pm)
15-冠-5 170~220 Na+(204)
18-冠-6 260~320 K+(276)、Rb+(304)
21-冠-7 340~430 Cs+(334)
A.冠醚可以用来识别碱金属离子
B.二苯并-18-冠-6也能适配Li+
C.该冠醚分子中碳原子杂化方式有2种
D.一个配离子中配位键的数目为6
11.关于下列晶体的熔、沸点高低排列判断不正确的是( )
A.CF<CCl <CBr <CI
4 4 4 4
B.金刚石>碳化硅>晶体硅
C.HO>HS>HSe>HTe
2 2 2 2
D.NaF>NaCl>NaBr>NaI
12.下列物质在给定条件下的同分异构体数目正确的是( )A.含有碳碳三键的C H 的同分异构体有3种
4 6
B.分子式是C H O 且属于羧酸的同分异构体有5种
6 12 2
C.含苯环的C H 的同分异构体有3种
8 10
D. 的一溴代物有5种
13.薰衣草醇的分子结构如图所示,下列有关薰衣草醇的说法不正确的是( )
A.分子式为C H O
10 16
B.含有两种官能团
C.能使酸性高锰酸钾溶液褪色
D.能发生取代反应、加成反应
14.N-乙基吲哚具有良好的储氢性能,其储氢析氢过程如下图所示。有关N-乙基吲哚
的说法正确的是( )
A.分子式为C H N
14 11
B.属于芳香烃
C.存在一个手性碳原子
D.1 mol N-乙基吲哚最多能储6 mol H
2
15.高分子M广泛用于牙膏、牙科黏合剂等口腔护理产品,合成路线如图:
下列说法错误的是( )
A.试剂a是甲醇,B分子中可能共平面的原子最多有8个
B.化合物B不存在顺反异构体
C.化合物C的核磁共振氢谱有一组峰
D.合成M的聚合反应是缩聚反应
二、非选择题:本题共4小题,共55分。
16、(13分)合成氨是人类科学技术发展史上的一项重大突破,目前工业上用氢气和
氮气直接合成氨。
(1)固氮一直是科学家致力研究的重要课题,有关热力学数据如下:大气固氮N(g)
2
反应 工业固氮N(g)+3H(g)2NH (g)
2 2 3
+O(g)2NO(g)
2
温度/℃ 25 2000 25 350 400 450
平衡常 3.84× 5×
0.1 1.847 0.504 0.152
数K 10-31 108
常温下,大气固氮的倾向________工业固氮(填“大于”或“小于”)。
(2)N (g)与H(g)反应的能量变化如图所示,则N(g)与H(g)反应制备NH (l)的热化学方
2 2 2 2 3
程式为:___________________________________。
(3)T ℃时,在2 L恒容密闭容器中加入1.2 mol N 和2 mol H 模拟一定条件下工业固氮
2 2
[N (g)+3H(g)2NH (g)],体系中n(NH )随时间的变化如图所示:
2 2 3 3
①前2分钟内的平均反应速率v(NH )=____________mol·L-1·min-1;
3
②有关工业固氮的说法正确的是________(填字母)。
A.使用催化剂可提高反应物的转化率
B.循环使用N、H 可提高NH 的产率
2 2 3
C.温度控制在500 ℃左右有利于反应向正方向进行
D.增大压强有利于加快反应速率,所以压强越大越好
③T ℃时,该反应的平衡常数为________;
(4)研究表明某些过渡金属催化剂可以加速氨气的分解,某温度下,用等质量的不同金
属分别催化等浓度的氨气,测得氨气分解的初始速率(单位:mmol/min)与催化剂的对应关
系如表所示。
催化剂 Fe Pd Ru Rh Pt Ni
初始速率 0.5 1.8 7.9 4.0 2.2 3.0
在不同催化剂的催化作用下,氨气分解反应中的活化能最大的催化剂是________(填化
学式)。17.(14分)金属氢氧化物在酸中的溶解度不同,因此可以利用这一性质,控制溶液
的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度[S/(mol·L-1)]
如图所示。
难溶金属氢氧化物的S-pH图
(1)pH=3时溶液中铜元素的主要存在形式是________(填化学式)。
(2)若要除去CuCl 溶液中的少量Fe3+,应该控制溶液的pH为________(填字母)。
2
A.<1 B.4左右
C.>6
(3)在Ni(NO ) 溶液中含有少量的Co2+杂质,________(填“能”或“不能”)通过调节
3 2
溶液pH的方法来除去,理由是_______________________。
18. ( 14 分 ) (1)X 、 Y 两 者 物 理 性 质 有 差 异 的 主 要 原 因 是
_________________________。
水中溶解度 熔点/ 沸点/
物质 结构简式
/g(25 ℃) ℃ ℃
X 0.2 45 100
Y 1.7 114 295
(2)CO(NH ) 分子中C原子的杂化方式为________________,1 mol该分子中σ键的
2 2
数目为__________,该物质易溶于水的主要原因是________________。
(3)F 与其他卤素单质反应可以形成卤素互化物,例如ClF 、BrF 等。已知反应Cl(g)
2 3 3 2
+3F(g) ===2ClF (g) ΔH=-313 kJ·mol-1,F—F键的键能为159 kJ·mol-1,Cl—Cl键的
2 3
键能为242 kJ·mol-1,则ClF 中Cl—F键的平均键能为____________kJ·mol-1。ClF 的熔、
3 3
沸点比BrF 的________(填“高”或“低”)。
3
(4)维生素 B 的结构简式如图,该晶体溶于水的过程中要克服的微粒间作用力有
1
__________________________________________。19.(14分)从石油裂解中得到的1,3-丁二烯可进行以下多步反应,得到重要的高分
子化合物D和富马酸。
(1)反应①的反应类型是_______________________________。
(2)第②步反应的试剂是_______________________________。
(3)写出B的结构简式:_______________________________。
(4)写出D的顺式结构:______________________________。
(5)写出第⑦步反应的化学方程式:_________________________。
(6)以上反应中属于消去反应的是________(填序号)。