文档内容
湖北省2024—2025学年下学期八校期末联考
高二化学试题
本试卷共8页,19题,全卷满分100分,考试用时75分钟。
★祝考试顺利★
注意事项:
1、答题前,请将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并
将准考证号条形码粘贴在答题卡上的制定位置。
2、选择题的作答:每小题选出答案后,用 2B铅笔把答题卡上对应题目的答案标号涂
黑,写在试卷、草稿纸和答题卡上的非答题区域均无效。
3、非选择题作答:用黑色签字笔直接答在答题卡对应的答题区域内,写在试卷、草稿
纸和答题卡上的非答题区域均无效。
4、考试结束后,请将答题卡上交。
一、选择题:本题共15小题,每题3分,共45分,每小题仅有一项是符合题意。
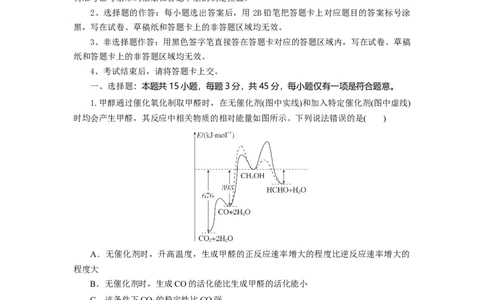
1.甲醇通过催化氧化制取甲醛时,在无催化剂(图中实线)和加入特定催化剂(图中虚线)
时均会产生甲醛,其反应中相关物质的相对能量如图所示。下列说法错误的是( )
A.无催化剂时,升高温度,生成甲醛的正反应速率增大的程度比逆反应速率增大的
程度大
B.无催化剂时,生成CO的活化能比生成甲醛的活化能小
C.该条件下CO 的稳定性比CO强
2
D.加入该催化剂不能改变反应的焓变
解析:A A.由题图可知,甲醇催化氧化制取甲醛的反应是放热反应,升高温度,平
衡逆向移动,即生成甲醛的正反应速率增大的程度比逆反应速率增大的程度小,故A错
误;B.由题图可知,甲醇生成甲醛的峰值较大,生成CO的峰值较小,即无催化剂时,生
成CO的活化能比生成甲醛的活化能小,故B正确;C.由题图可知,CO 具有的能量比
2
CO具有的能量低,该条件下CO 的稳定性比CO强,故C正确;D.催化剂能改变反应途
2
径,但不改变生成物和反应物的能量,所以加入该催化剂不能改变反应的焓变,故D正确。
答案:A
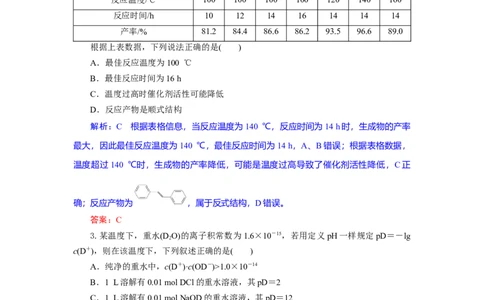
2.苯乙烯与溴苯在一定条件下发生Heck反应:
溴苯用量/mmol 100 100 100 100 100 100 100
催化剂用量/ mmol 2 2 2 2 2 2 2
反应温度/℃ 100 100 100 100 120 140 160
反应时间/h 10 12 14 16 14 14 14
产率/% 81.2 84.4 86.6 86.2 93.5 96.6 89.0
根据上表数据,下列说法正确的是( )
A.最佳反应温度为100 ℃
B.最佳反应时间为16 h
C.温度过高时催化剂活性可能降低
D.反应产物是顺式结构
解析:C 根据表格信息,当反应温度为140 ℃,反应时间为14 h时,生成物的产率
最大,因此最佳反应温度为140 ℃,最佳反应时间为14 h,A、B错误;根据表格数据,
温度超过140 ℃时,生成物的产率降低,可能是温度过高导致了催化剂活性降低,C正
确;反应产物为 ,属于反式结构,D错误。
答案:C
3.某温度下,重水(D O)的离子积常数为1.6×10-15,若用定义pH一样规定pD=-lg
2
c(D+),则在该温度下,下列叙述正确的是( )
A.纯净的重水中,c(D+)·c(OD-)>1.0×10-14
B.1 L溶解有0.01 mol DCl的重水溶液,其pD=2
C.1 L溶解有0.01 mol NaOD的重水溶液,其pD=12
D.纯净的重水中,pD=7
解析:B 该温度下重水(D O)的离子积常数为1.6×10-15<1.0×10-14,故A错误;c(DCl)
2
==0.01 mol/L,则 c(D+)=0.01 mol/L,所以 pD=2,故 B 正确;c(NaOD)==0.01
mol/L,则c(D+)= mol/L=1.6×10-13 mol/L,则pD>12,故C错误;c(D+)= mol/L=4×10
-8 mol/L,所以pD>7,故D错误。
答案:B
4.中对白矾之用有如下叙述:“吐利风热之痰涎,取其酸苦涌泄也;治诸血痛,脱肛……取其酸涩而收也……”下列说法正确的是( )
A.治血痛的原因是利用了胶体的吸附作用
B.白矾溶于水后微粒浓度排序:c(H O)>c(SO)>c(Al3+)>c(K+)>c(H+)>c(OH-)
2
C.白矾和氯化铁均可用作水处理剂,均可以杀菌消毒
D.白矾常在油条中作膨化剂的原理是Al3++3HCO===Al(OH) ↓+3CO↑
3 2
解析:D Al3+水解生成氢氧化铝胶体,治血痛的原因是利用了胶体的聚沉,故A错
误;白矾是硫酸铝钾晶体[KAl(SO)·12HO],其水溶液因铝离子水解而显酸性,铝离子减
4 2 2
少,微粒浓度排序:c(H O)>c(SO)>c(K+)>c(Al3+)>c(H+)>c(OH-),故B错误;白矾和
2
氯化铁在水溶液中水解生成胶体具有较大表面积,具有吸附作用,吸附悬浮在水中的杂
质,可以净水,但不能杀菌消毒,故C错误;白矾常用于油条中作膨化剂是利用铝离子和
小苏打中碳酸氢根离子发生相互促进水解反应生成二氧化碳气体,Al3++
3HCO===Al(OH) ↓+3CO↑,故D正确。
3 2
答案:D
5.某温度时,CuS、MnS在水中的沉淀溶解平衡曲线如图所示(M表示Cu或Mn),下
列说法错误的是( )
A.a点对应的K 大于b点对应的K
sp sp
B.该温度下向CuSO 溶液中加入MnS后,K (MnS)不变
4 sp
C.在含有CuS和MnS固体的溶液中,c(Cu2+)∶c(Mn2+)=(2×10-23)∶1
D.该温度下,K (CuS)小于K (MnS)
sp sp
解析:A 溶度积仅与温度有关,温度不变,溶度积不变,a、b两点对应的K (CuS)
sp
相等,A错误、B 正确;由图可知,K (CuS)=0.01×6×10-34=6×10-36,K (MnS)=
sp sp
0.01×3×10-11=3×10-13,D正确;在含有CuS和MnS固体的溶液中,====2×10-
23,C正确。
答案:A
6.C的衰变反应为:C→X+e,下列有关说法正确的是( )
A.C与X互为同位素
B.X、C的第一电离能X>C
C.C和C的价层轨道电子数相差2
D.上述反应中X元素的中子数为8
解析:B X为N,与C的质子数不同,不是同位素,A错误;X为N,同周期元素从左到右第一电离能呈增大趋势,且N的2p轨道为半充满较稳定结构,失去一个电子较难,
则第一电离能N>C,B正确;C和C的价层轨道电子数相同,相差2的是质量数或中子
数,C错误;上述反应中X元素是N,中子数为14-7=7,D错误。
答案:B
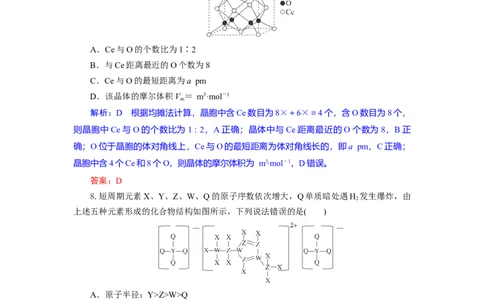
7.氢能具有高热值、零污染和资源丰富等优点。一种光解水产生氢气的催化剂晶胞结
构如图所示,已知晶胞参数为a pm。设N 为阿伏加德罗常数的值,下列说法错误的是(
A
)
A.Ce与O的个数比为1∶2
B.与Ce距离最近的O个数为8
C.Ce与O的最短距离为a pm
D.该晶体的摩尔体积V = m3·mol-1
m
解析:D 根据均摊法计算,晶胞中含Ce数目为8×+6×=4个,含O数目为8个,
则晶胞中Ce与O的个数比为1∶2,A正确;晶体中与Ce距离最近的O个数为8,B正
确;O位于晶胞的体对角线上,Ce与O的最短距离为体对角线长的,即a pm,C正确;
晶胞中含4个Ce和8个O,则晶体的摩尔体积为 m3·mol-1,D错误。
答案:D
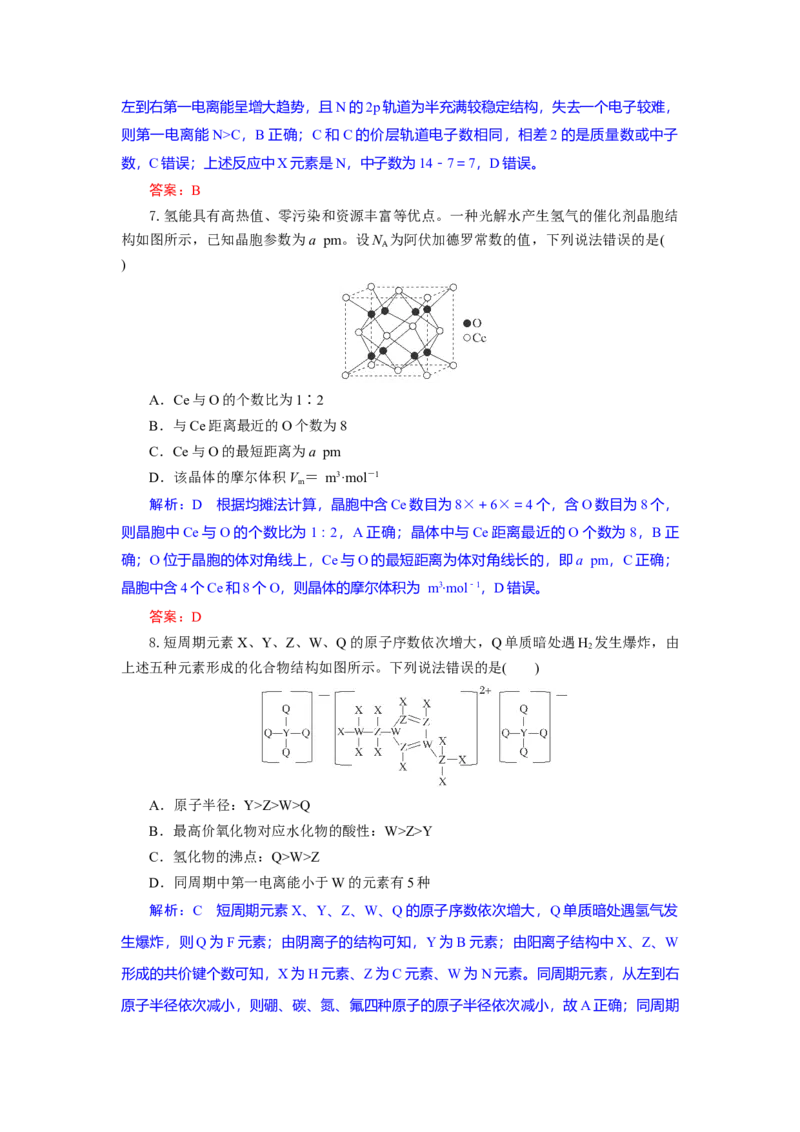
8.短周期元素X、Y、Z、W、Q的原子序数依次增大,Q单质暗处遇H 发生爆炸,由
2
上述五种元素形成的化合物结构如图所示。下列说法错误的是( )
A.原子半径:Y>Z>W>Q
B.最高价氧化物对应水化物的酸性:W>Z>Y
C.氢化物的沸点:Q>W>Z
D.同周期中第一电离能小于W的元素有5种
解析:C 短周期元素X、Y、Z、W、Q的原子序数依次增大,Q单质暗处遇氢气发
生爆炸,则Q为F元素;由阴离子的结构可知,Y为B元素;由阳离子结构中X、Z、W
形成的共价键个数可知,X为H元素、Z为C元素、W为N元素。同周期元素,从左到右
原子半径依次减小,则硼、碳、氮、氟四种原子的原子半径依次减小,故A正确;同周期元素,从左到右元素的非金属性依次增强,最高价氧化物对应水化物的酸性依次增强,则
硼酸、碳酸、硝酸的酸性依次增强,故B正确;碳元素的氢化物为烃,固态烃和液态烃的
沸点高于氨气和氟化氢,故C错误;同周期元素,从左到右第一电离能呈增大趋势,氮原
子的2p轨道为稳定的半充满结构,元素的第一电离能大于相邻元素,则第二周期中第一电
离能小于氮元素的元素有锂、铍、硼、碳、氧,共5种,故D正确。
答案:C
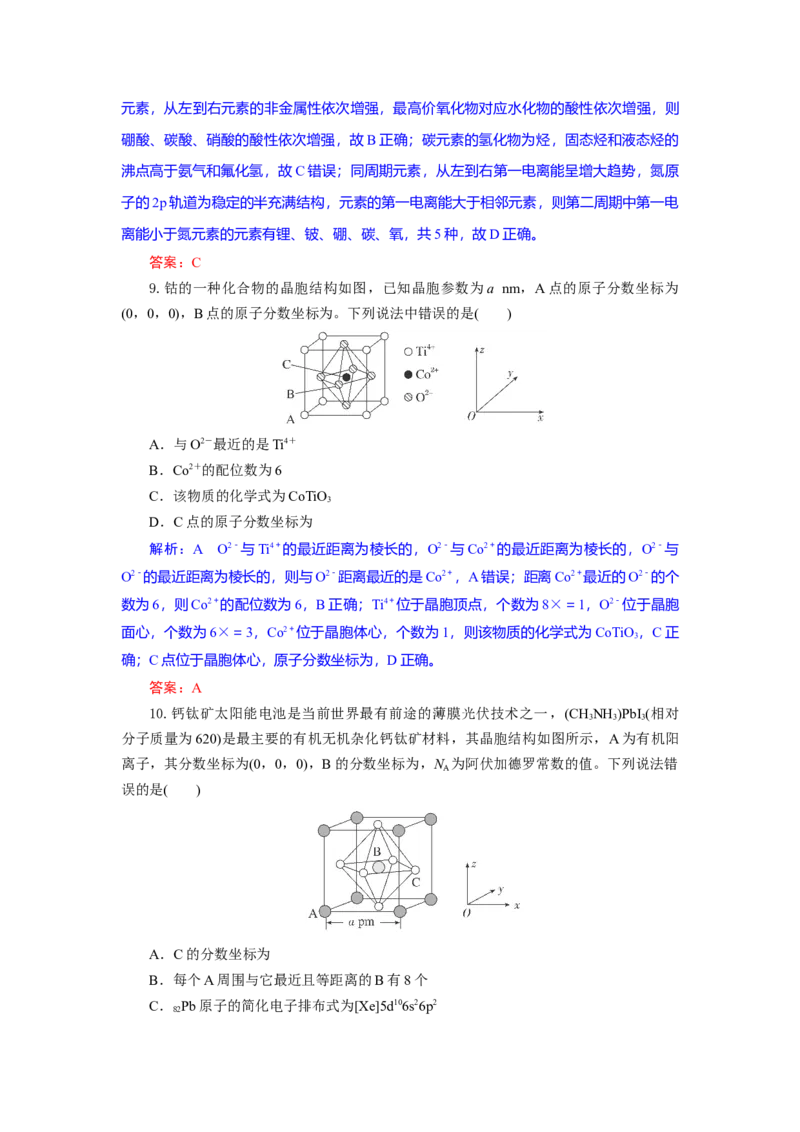
9.钴的一种化合物的晶胞结构如图,已知晶胞参数为a nm,A点的原子分数坐标为
(0,0,0),B点的原子分数坐标为。下列说法中错误的是( )
A.与O2-最近的是Ti4+
B.Co2+的配位数为6
C.该物质的化学式为CoTiO
3
D.C点的原子分数坐标为
解析:A O2-与Ti4+的最近距离为棱长的,O2-与Co2+的最近距离为棱长的,O2-与
O2-的最近距离为棱长的,则与O2-距离最近的是Co2+,A错误;距离Co2+最近的O2-的个
数为6,则Co2+的配位数为6,B正确;Ti4+位于晶胞顶点,个数为8×=1,O2-位于晶胞
面心,个数为6×=3,Co2+位于晶胞体心,个数为1,则该物质的化学式为CoTiO ,C正
3
确;C点位于晶胞体心,原子分数坐标为,D正确。
答案:A
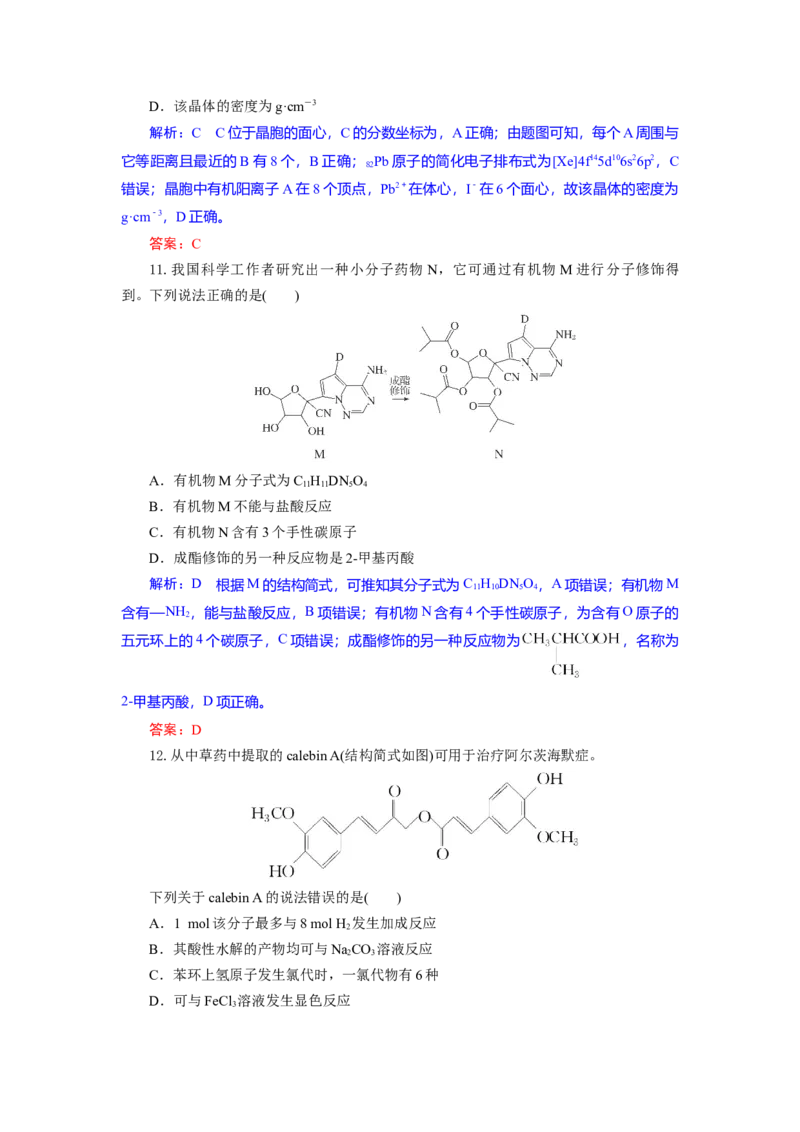
10.钙钛矿太阳能电池是当前世界最有前途的薄膜光伏技术之一,(CHNH )PbI (相对
3 3 3
分子质量为620)是最主要的有机无机杂化钙钛矿材料,其晶胞结构如图所示,A为有机阳
离子,其分数坐标为(0,0,0),B的分数坐标为,N 为阿伏加德罗常数的值。下列说法错
A
误的是( )
A.C的分数坐标为
B.每个A周围与它最近且等距离的B有8个
C. Pb原子的简化电子排布式为[Xe]5d106s26p2
82D.该晶体的密度为g·cm-3
解析:C C位于晶胞的面心,C的分数坐标为,A正确;由题图可知,每个A周围与
它等距离且最近的B有8个,B正确; Pb原子的简化电子排布式为[Xe]4f145d106s26p2,C
82
错误;晶胞中有机阳离子A在8个顶点,Pb2+在体心,I-在6个面心,故该晶体的密度为
g·cm-3,D正确。
答案:C
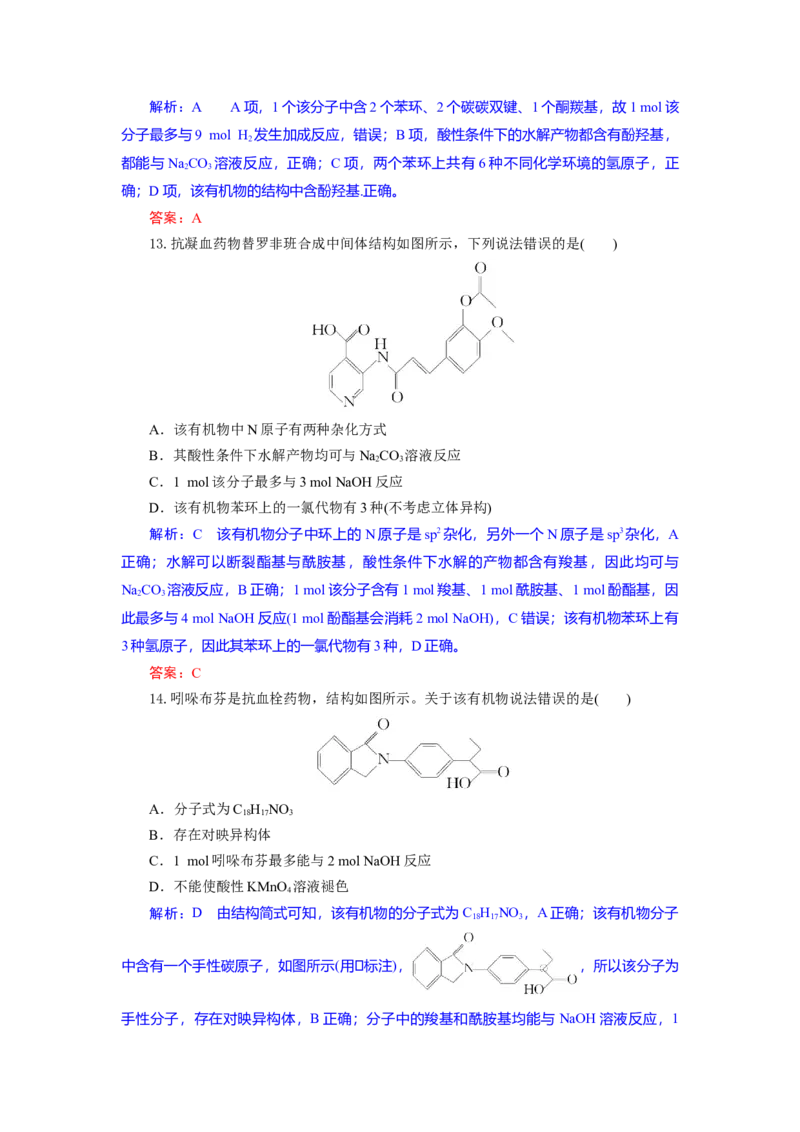
11.我国科学工作者研究出一种小分子药物N,它可通过有机物M进行分子修饰得
到。下列说法正确的是( )
A.有机物M分子式为C H DN O
11 11 5 4
B.有机物M不能与盐酸反应
C.有机物N含有3个手性碳原子
D.成酯修饰的另一种反应物是2-甲基丙酸
解析:D 根据M的结构简式,可推知其分子式为C
11
H
10
DN
5
O 4,A项错误;有机物M
含有—NH 2,能与盐酸反应,B项错误;有机物N含有4个手性碳原子,为含有O原子的
五元环上的4个碳原子,C项错误;成酯修饰的另一种反应物为 ,名称为
2-甲基丙酸,D项正确。
答案:D
12.从中草药中提取的calebin A(结构简式如图)可用于治疗阿尔茨海默症。
下列关于calebin A的说法错误的是( )
A.1 mol该分子最多与8 mol H 发生加成反应
2
B.其酸性水解的产物均可与NaCO 溶液反应
2 3
C.苯环上氢原子发生氯代时,一氯代物有6种
D.可与FeCl 溶液发生显色反应
3解析:A A项,1个该分子中含2个苯环、2个碳碳双键、1个酮羰基,故1 mol该
分子最多与9 mol H 发生加成反应,错误;B项,酸性条件下的水解产物都含有酚羟基,
2
都能与NaCO 溶液反应,正确;C项,两个苯环上共有6种不同化学环境的氢原子,正
2 3
确;D项,该有机物的结构中含酚羟基.正确。
答案:A
13.抗凝血药物替罗非班合成中间体结构如图所示,下列说法错误的是( )
A.该有机物中N原子有两种杂化方式
B.其酸性条件下水解产物均可与NaCO 溶液反应
2 3
C.1 mol该分子最多与3 mol NaOH反应
D.该有机物苯环上的一氯代物有3种(不考虑立体异构)
解析:C 该有机物分子中环上的N原子是sp2杂化,另外一个N原子是sp3杂化,A
正确;水解可以断裂酯基与酰胺基,酸性条件下水解的产物都含有羧基,因此均可与
NaCO 溶液反应,B正确;1 mol该分子含有1 mol羧基、1 mol酰胺基、1 mol酚酯基,因
2 3
此最多与4 mol NaOH反应(1 mol酚酯基会消耗2 mol NaOH),C错误;该有机物苯环上有
3种氢原子,因此其苯环上的一氯代物有3种,D正确。
答案:C
14.吲哚布芬是抗血栓药物,结构如图所示。关于该有机物说法错误的是( )
A.分子式为C H NO
18 17 3
B.存在对映异构体
C.1 mol吲哚布芬最多能与2 mol NaOH反应
D.不能使酸性KMnO 溶液褪色
4
解析:D 由结构简式可知,该有机物的分子式为C H NO ,A正确;该有机物分子
18 17 3
中含有一个手性碳原子,如图所示(用标注), ,所以该分子为
手性分子,存在对映异构体,B正确;分子中的羧基和酰胺基均能与 NaOH溶液反应,1mol该物质最多可消耗2 mol NaOH,C正确;该物质与苯环直接相连的碳原子上有氢原
子,则能被酸性高锰酸钾氧化,D错误。
答案:D
15.分枝酸可用于生化研究,其结构简式如图。下列关于分枝酸的叙述正确的是( )
A.分子中含有3种官能团
B.可发生加聚和氧化反应
C.1 mol分枝酸最多可与3 mol NaHCO 发生反应
3
D.所有原子可能都处于同一平面
解析:B 该分子中含有碳碳双键、羟基、羧基、醚键共4种官能团,A错误;分子含
有碳碳双键,可发生加聚和氧化反应,B正确;1分子分枝酸中只有2个羧基能与碳酸氢钠
反应生成二氧化碳,1 mol分枝酸最多可与2 mol NaHCO 发生反应,C错误;分枝酸中存
3
在连接4个原子的饱和碳原子,具有四面体结构,分子中所有原子一定不共平面,D错
误。
答案:B
二、非选择题:本题共4小题,共55分。
16、(12分)(1)常温下,用氨水吸收CO 可得到NH HCO 溶液,在NH HCO 溶液
2 4 3 4 3
中,c(NH)________(填“>”“<”或“=”)c(HCO);反应 NH+HCO+HO===NH·H O+
2 3 2
HCO 的平衡常数K=____________。(已知常温下NH ·H O的电离常数K =2×10-5,
2 3 3 2 b
HCO 的电离常数K =4×10-7,K =4×10-11) (3分)
2 3 a1 a2
(2)已知K [Mg(OH) ]=2×10-11,常温下在某MgSO 溶液里c(Mg2+)=0.002 mol·L-1,
sp 2 4
如果生成Mg(OH) 沉淀,应调整溶液pH,使之大于________;在0.20 L的0.002 mol·L-1
2
MgSO 溶液中加入等体积的0.10 mol·L-1的氨水溶液,电离常数K (NH ·H O)=2×10-5,
4 b 3 2
试通过计算判断__________(填“有”或“无”)Mg(OH) 沉淀生成。(3分)
2
(3)CuCl悬浊液中加入NaS,发生的反应为2CuCl(s)+S2-(aq)Cu S(s)+2Cl-(aq),
2 2
该反应的平衡常数K=____________[已知K (CuCl)=1.2×10-6,K (Cu S)=2.5×10-43]。
sp sp 2
(3分)
(4)已知常温下HSO 的电离常数:K =1.0×10-1.9,K =1.0×10-7.2,计算0.1 mol·L-
2 3 a1 a2
1NaHSO 溶液的pH为________(忽略SO的二级水解)。(3分)
3
解析:(1)由于NH ·HO的电离常数大于HCO 的第一步电离常数,再根据盐类水解规
3 2 2 3律可得HCO的水解程度更大,因此c(NH)>c(HCO);反应NH+HCO+HO===NH·HO+
2 3 2
HCO 的平衡常数K====1.25×10-3。
2 3
(2)MgSO 溶液中c(Mg2+)=0.002 mol·L-1,开始沉淀时 c(OH-)= mol·L-1=10-4
4
mol·L-1,则c(H+)=10-10 mol·L-1,因此生成Mg(OH) 沉淀,应调整溶液pH,使之大于
2
10;在0.20 L的0.002 mol·L-1 MgSO 溶液中加入等体积的0.10 mol·L-1的氨水溶液,镁离
4
子浓度变为0.001 mol·L-1;c(OH-)= mol·L-1=0.001 mol·L-1,c(Mg2+)·c2(OH-)=10-
9>K =2×10-11,有沉淀产生。
sp
(3)平衡常数K==
===5.76×1030。
(4)HSOSO+H+的平衡常数K ==1.0×10-7.2,c(SO)≈c(H+),c(HSO)≈0.1 mol·L
a2
-1,则c2(H+)=1.0×10-7.2×c(HSO)=1.0×10-7.2×0.1=10-8.2,c(H+)=10-4.1 mol·L-1,故
pH=-lg c(H+)=4.1。
答案:(1)> 1.25×10-3
(2)10 有
(3)5.76×1030
(4)4.1
17.(12分)(1)金属锰有多种晶型,其中δ-Mn的结构为体心立方堆积,晶胞参数为a
pm。δ-Mn中锰的原子半径为________pm。已知阿伏加德罗常数的值为N ,δ-Mn的密度ρ
A
=__________ g·cm-3(列出计算式)。(3分)
(2)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍
射实验测得MgO的晶胞参数为a=0.420 nm,则r(O2-)为____________nm。MnO也属于
NaCl型结构,晶胞参数为a′=0.448 nm,则r(Mn2+)为____________ nm。(3分)
(3)Li O具有反萤石结构,晶胞如图所示。已知晶胞参数为0.4665 nm,阿伏加德罗常
2
数的值为N ,则LiO的密度为__________ g·cm-3(列出计算式)。(3分)
A 2
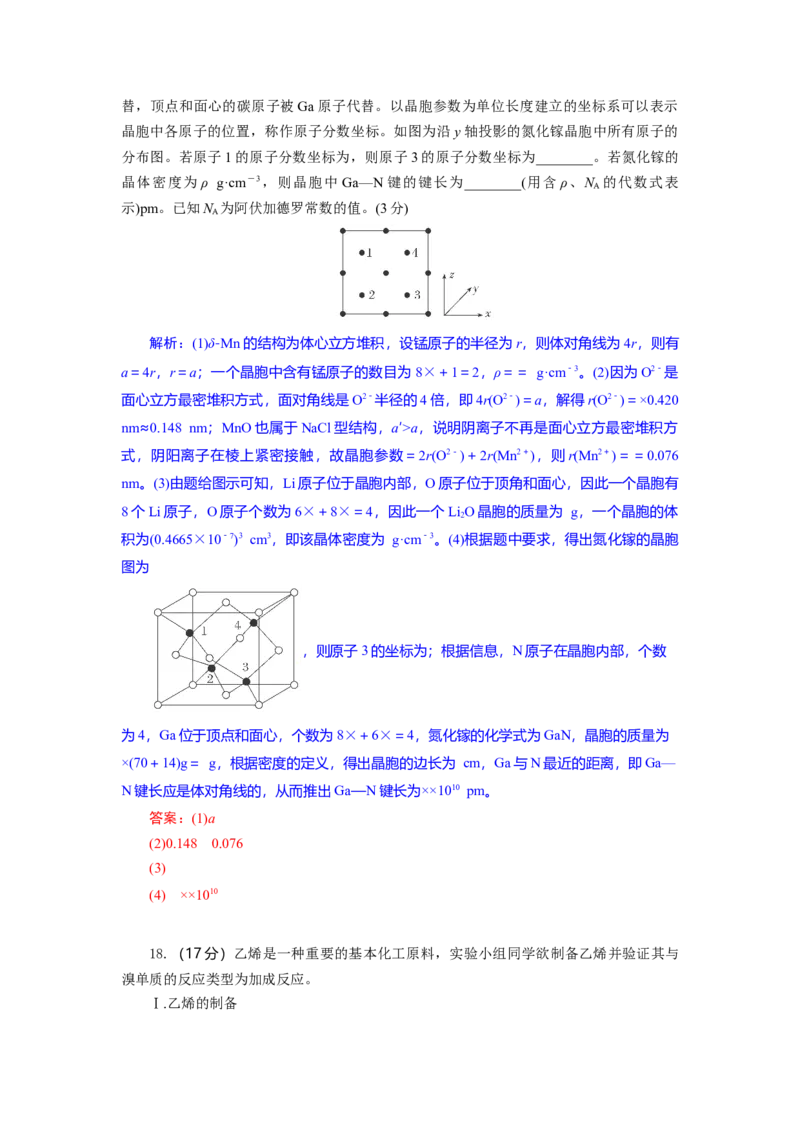
(4)氮化镓是新型半导体材料,其晶胞结构可看作金刚石晶胞内部的碳原子被N原子代替,顶点和面心的碳原子被Ga原子代替。以晶胞参数为单位长度建立的坐标系可以表示
晶胞中各原子的位置,称作原子分数坐标。如图为沿y轴投影的氮化镓晶胞中所有原子的
分布图。若原子1的原子分数坐标为,则原子3的原子分数坐标为________。若氮化镓的
晶体密度为 ρ g·cm-3,则晶胞中 Ga—N 键的键长为________(用含 ρ、N 的代数式表
A
示)pm。已知N 为阿伏加德罗常数的值。(3分)
A
解析:(1)δ-Mn的结构为体心立方堆积,设锰原子的半径为r,则体对角线为4r,则有
a=4r,r=a;一个晶胞中含有锰原子的数目为8×+1=2,ρ== g·cm-3。(2)因为O2-是
面心立方最密堆积方式,面对角线是O2-半径的4倍,即4r(O2-)=a,解得r(O2-)=×0.420
nm≈0.148 nm;MnO也属于NaCl型结构,a′>a,说明阴离子不再是面心立方最密堆积方
式,阴阳离子在棱上紧密接触,故晶胞参数=2r(O2-)+2r(Mn2+),则r(Mn2+)==0.076
nm。(3)由题给图示可知,Li原子位于晶胞内部,O原子位于顶角和面心,因此一个晶胞有
8个Li原子,O原子个数为6×+8×=4,因此一个LiO晶胞的质量为 g,一个晶胞的体
2
积为(0.4665×10-7)3 cm3,即该晶体密度为 g·cm-3。(4)根据题中要求,得出氮化镓的晶胞
图为
,则原子3的坐标为;根据信息,N原子在晶胞内部,个数
为4,Ga位于顶点和面心,个数为8×+6×=4,氮化镓的化学式为GaN,晶胞的质量为
×(70+14)g= g,根据密度的定义,得出晶胞的边长为 cm,Ga与N最近的距离,即Ga—
N键长应是体对角线的,从而推出Ga—N键长为××1010 pm。
答案:(1)a
(2)0.148 0.076
(3)
(4) ××1010
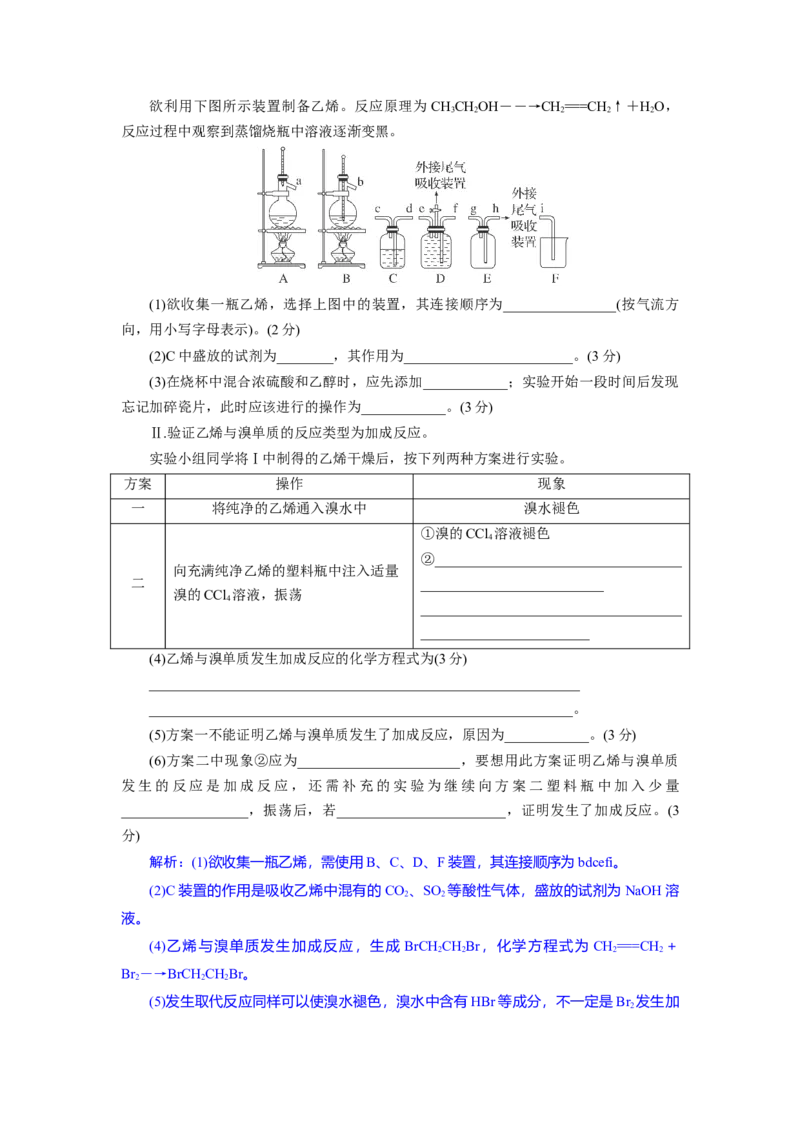
18.(17分)乙烯是一种重要的基本化工原料,实验小组同学欲制备乙烯并验证其与
溴单质的反应类型为加成反应。
Ⅰ.乙烯的制备欲利用下图所示装置制备乙烯。反应原理为 CHCHOH――→CH===CH ↑+HO,
3 2 2 2 2
反应过程中观察到蒸馏烧瓶中溶液逐渐变黑。
(1)欲收集一瓶乙烯,选择上图中的装置,其连接顺序为________________(按气流方
向,用小写字母表示)。(2分)
(2)C中盛放的试剂为________,其作用为________________________。(3分)
(3)在烧杯中混合浓硫酸和乙醇时,应先添加____________;实验开始一段时间后发现
忘记加碎瓷片,此时应该进行的操作为____________。(3分)
Ⅱ.验证乙烯与溴单质的反应类型为加成反应。
实验小组同学将Ⅰ中制得的乙烯干燥后,按下列两种方案进行实验。
方案 操作 现象
一 将纯净的乙烯通入溴水中 溴水褪色
①溴的CCl 溶液褪色
4
②___________________________________
向充满纯净乙烯的塑料瓶中注入适量
二 __________________________
溴的CCl 溶液,振荡
4
_____________________________________
________________________
(4)乙烯与溴单质发生加成反应的化学方程式为(3分)
_____________________________________________________________
____________________________________________________________。
(5)方案一不能证明乙烯与溴单质发生了加成反应,原因为____________。(3分)
(6)方案二中现象②应为_______________________,要想用此方案证明乙烯与溴单质
发生的反应是加成反应,还需补充的实验为继续向方案二塑料瓶中加入少量
__________________,振荡后,若________________________,证明发生了加成反应。(3
分)
解析:(1)欲收集一瓶乙烯,需使用B、C、D、F装置,其连接顺序为bdcefi。
(2)C装置的作用是吸收乙烯中混有的CO 、SO 等酸性气体,盛放的试剂为NaOH溶
2 2
液。
(4)乙烯与溴单质发生加成反应,生成 BrCHCHBr,化学方程式为 CH===CH +
2 2 2 2
Br ―→BrCHCHBr。
2 2 2
(5)发生取代反应同样可以使溴水褪色,溴水中含有HBr等成分,不一定是Br 发生加
2成反应。
(6)由于塑料瓶内气体体积减小,压强减小,所以现象②应为塑料瓶变瘪,要想用此方
案证明乙烯与溴单质发生的反应是加成反应,还需补充证明产物中不含HBr的实验,继续
向方案二塑料瓶中加入少量紫色石蕊溶液,振荡后,若溶液不变红(或加入少量硝酸酸化的
硝酸银溶液,无淡黄色沉淀生成),证明发生了加成反应。
答案:(1)bdcefi
(2)NaOH溶液 除去乙烯中混有的SO 、CO 等酸性气体
2 2
(3)乙醇 冷却后再加
(4)CH ===CH +Br ―→
2 2 2
(5)发生取代反应同样可以使溴水褪色,溴水中含有HBr等成分,不一定是Br 发生加
2
成反应
(6)塑料瓶变瘪 紫色石蕊溶液(或硝酸酸化的硝酸银溶液) 溶液不变红(或无淡黄色沉
淀生成)
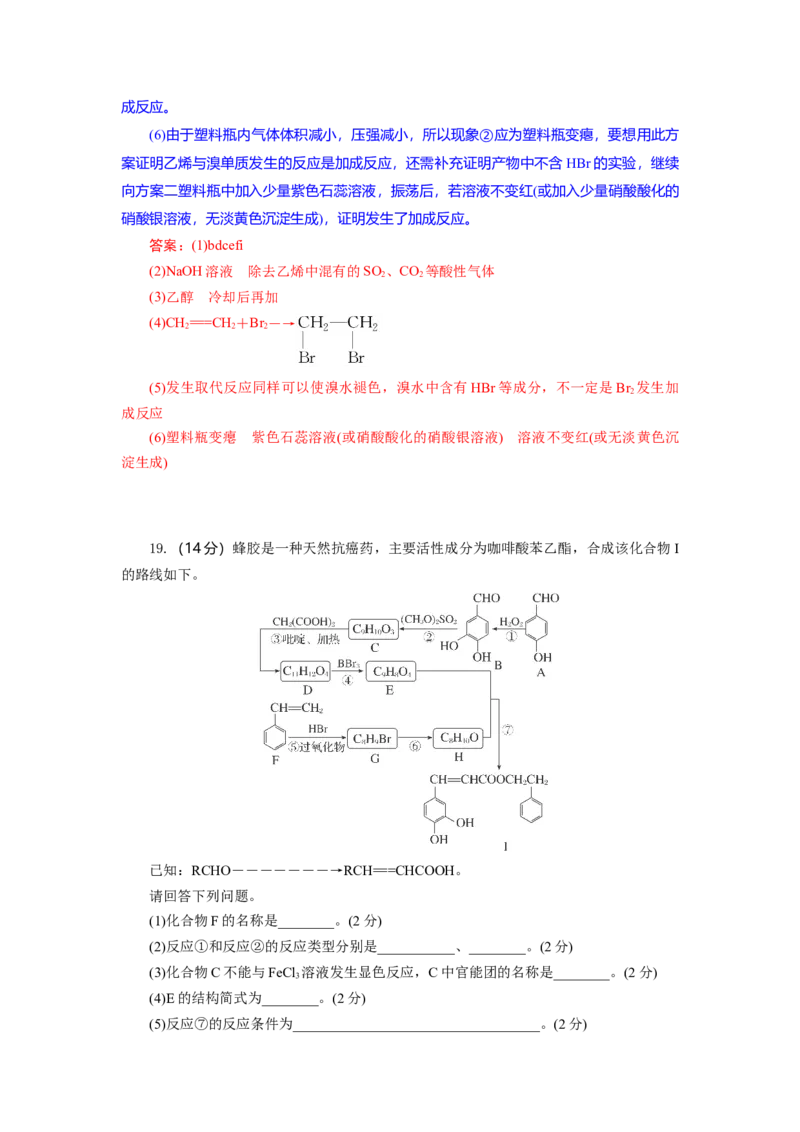
19.(14分)蜂胶是一种天然抗癌药,主要活性成分为咖啡酸苯乙酯,合成该化合物I
的路线如下。
已知:RCHO―――――――→RCH===CHCOOH。
请回答下列问题。
(1)化合物F的名称是________。(2分)
(2)反应①和反应②的反应类型分别是___________、________。(2分)
(3)化合物C不能与FeCl 溶液发生显色反应,C中官能团的名称是________。(2分)
3
(4)E的结构简式为________。(2分)
(5)反应⑦的反应条件为___________________________________。(2分)(6)反应⑥的化学方程式为_________________________________。(2分)
(7)化合物W与E互为同分异构体,二者所含官能团种类和数目完全相同,且苯环上有
3 个取代基,其核磁共振氢谱显示有 6 种不同化学环境的氢原子,峰面积之比为
2∶2∶1∶1∶1∶1,符合要求的W的结构简式共有________种,写出其中一种的结构简
式:__________________________________。(2分)
解析:双氧水具有强氧化性,A与过氧化氢发生氧化反应生成B,化合物C不能与
FeCl 溶液发生显色反应,结合 C 的分子式可判断 B 发生取代反应生成 C 为
3
,C发生已知信息中的反应生成D为 。对
比D、E的分子式,结合I的结构简式可知E为 ,故H
为 、G为 ,据此解答。
(1)根据F的结构简式可判断化合物F的名称是苯乙烯;(2)根据以上分析可知反应①和
反应②的反应类型分别是氧化反应和取代反应;(3)C为 ,C中官能团的
名称是醛基、醚键;(4)根据以上分析可知E的结构简式为 ;
(5)反应⑦是酯化反应,反应条件为浓硫酸、加热;(6)反应⑥是卤代烃的水解反应,反应方
程式为 +NaOH――→ +NaBr;(7)化合物W与E互
为同分异构体,两者所含官能团种类和数目完全相同,且苯环上有3个取代基,三个取代
基为—OH、—OH、—CH===CHCOOH,或者为—OH、—OH、—C(COOH)===CH ,其
2
中核磁共振氢谱显示有6种不同化学环境的氢,峰面积比为2∶2∶1∶1∶1∶1的有两种,
结构简式分别为 。
答案:(1)苯乙烯 (2)氧化反应 取代反应