文档内容
湖北省孝感市部分高中2024—2025学年下学期期末联考
高二化学试题
本试卷共8页,19题,全卷满分100分,考试用时75分钟。
★祝考试顺利★
注意事项:
1、答题前,请将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并
将准考证号条形码粘贴在答题卡上的制定位置。
2、选择题的作答:每小题选出答案后,用 2B铅笔把答题卡上对应题目的答案标号涂
黑,写在试卷、草稿纸和答题卡上的非答题区域均无效。
3、非选择题作答:用黑色签字笔直接答在答题卡对应的答题区域内,写在试卷、草稿
纸和答题卡上的非答题区域均无效。
4、考试结束后,请将答题卡上交。
一、选择题:本题共15小题,每题3分,共45分,每小题仅有一项是符合题意。
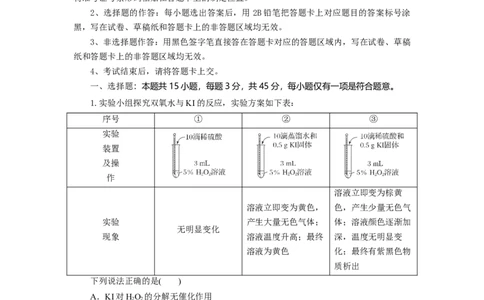
1.实验小组探究双氧水与KI的反应,实验方案如下表:
序号 ① ② ③
实验
装置
及操
作
溶液立即变为棕黄
溶液立即变为黄色, 色,产生少量无色气
实验 产生大量无色气体; 体;溶液颜色逐渐加
无明显变化
现象 溶液温度升高;最终 深,温度无明显变
溶液为黄色 化;最终有紫黑色物
质析出
下列说法正确的是( )
A.KI对HO 的分解无催化作用
2 2
B.对比实验②和③,酸性条件下HO 氧化KI的速率更大
2 2
C.实验②③中的温度差异说明HO 氧化KI的反应放出大量热
2 2
D.对比实验②和③,③中的现象可能是因为HO 分解的速率大于HO 氧化KI的速
2 2 2 2
率
解析:B 对比实验①②的实验现象,实验①无明显现象,实验②溶液立即变为黄
色,产生大量无色气体,说明碘化钾是过氧化氢分解的催化剂,A错误;由实验②和③的
实验现象可知,实验②溶液立即变为黄色,实验③溶液立即变为棕黄色,说明酸性条件下生成的I 的量更多,过氧化氢溶液氧化碘化钾的反应速率更大,B正确;由实验②③的实
2
验现象可知,过氧化氢分解的反应为放热反应,在实验中放出大量热,C错误;实验②溶
液立即变为黄色,产生大量无色气体,说明实验②主要发生KI催化HO 分解的反应,实
2 2
验③溶液立即变为棕黄色,产生少量无色气体,说明实验③主要发生HO 氧化KI的反
2 2
应,则酸性条件下过氧化氢氧化碘化钾的反应速率明显大于过氧化氢催化分解的速率,D
错误。
答案:B
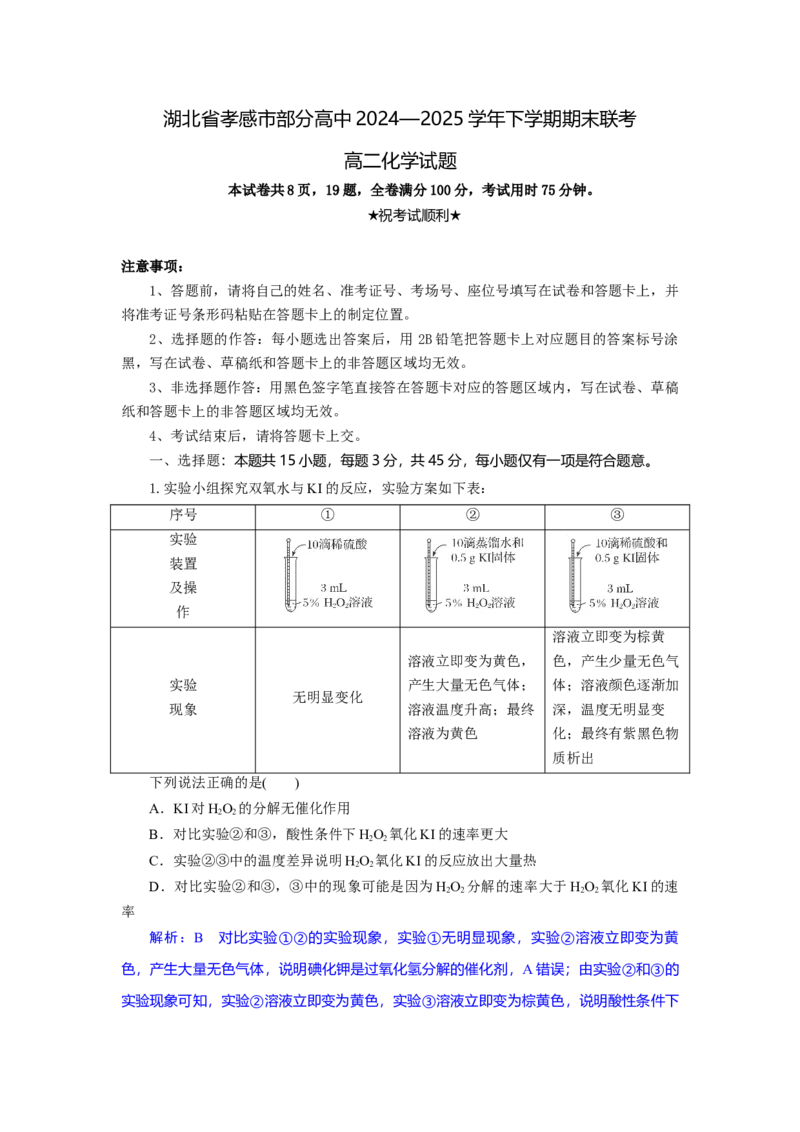
2.甲酸常被用于橡胶、医药等工业。在一定条件下可分解生成CO和HO。在有、无
2
催化剂条件下的能量与反应历程的关系如图所示。下列说法错误的是( )
A.途径一未使用催化剂,途径二比途径一甲酸平衡转化率高
B.ΔH=ΔH<0,E >E
1 2 a1 a2
C.途径二H+参与反应,通过改变反应途径加快反应速率
D.途径二反应的快慢由生成 的速率决定
解析:A A.催化剂可以降低活化能,因此途径一未使用催化剂,但催化剂不能改变
平衡状态,所以途径二和途径一的甲酸平衡转化率相同,A错误;B.催化剂可以降低活化
能,但不能改变焓变,由于反应物的总能量高于生成物的总能量,因此ΔH=ΔH<0,
1 2
E >E ,B正确;C.途径二H+参与反应,但反应前后质量和化学性质未发生改变,作为
a1 a2
催化剂通过改变反应途径加快反应速率,C正确;D.生成 的活化能高,则途径二反应的快慢由生成 的速率决定,D正确。
答案:A
3.向碘水中加入KI溶液,发生反应:I-(aq)+I(aq)I(aq),充分反应达平衡后,测
2
得微粒浓度如表:
微粒 I- I I
2
浓度(mol·L-1) 2.5×10-3 2.5×10-3 4.0×10-3
下列说法不正确的是( )
A.向所得溶液中加入CCl ,振荡静置,水层c(I)降低
4 2
B.向所得溶液中加入等体积水,c(I)<1.25×10-3mol·L-1
2
C.该温度下,反应I-+II的K=640
2
D.配制碘水时,加入少量KI,可促进I 的溶解
2
解析:B 碘单质在水中的溶解度小于在有机溶剂四氯化碳中的溶解度,向所得溶液
中加入CCl ,振荡静置,水层c(I)降低,A正确;
4 2
K===640,向所得溶液中加入等体积水,体积扩大一倍,各离子浓度瞬间减少一半,
Q===1280>K=640,故平衡逆向移动,c(I)>1.25×10-3mol·L-1,B错误、C正确;碘单
2
质在水中的溶解度小,配制碘水时,加入少量KI,平衡向右移动,促进I 的溶解,D正
2
确。
答案:B
4.硅是大数据时代的关键材料。工业上常在1800~2000 ℃时,用碳单质还原的方法
制取单质硅。涉及反应的相关数据如表所示。下列说法正确的是( )
ΔH/ ΔS/(J·
反应
(kJ·mol-1) K-1·mol-1)
反应(1):SiO(s)+2C(s)===Si(s)+
2
+687.27 359.04
2CO(g)
反应(2):SiO(s)+C(s)===Si(s)+
2
+514.85 183.35
CO(g)
2
A.反应(1)可证明Si的还原性大于C
B.生活中利用单晶硅良好的导光性能作光导纤维
C.工业生产条件下反应(2)无法自发进行
D.C(s)+CO(g)===2CO(g) ΔH=-172.42 kJ·mol-1
2
答案:C
5.由于血液中存在如下平衡过程:
CO(g)CO(aq)、CO(aq)+HO(l)HCO(aq)、HCO(aq)H+(aq)+HCO(aq),使血
2 2 2 2 2 3 2 3
液的pH维持在7.35~7.45。如超出这个范围会造成酸中毒(pH过低)或碱中毒(pH过高),急性中毒时需静脉注射NH Cl或NaHCO 进行治疗。下列叙述正确的是( )
4 3
A.血液中CO 浓度过高会导致酸中毒,使血液中的值增大
2
B.治疗碱中毒时,患者需降低呼吸频率,以增加血液中CO 浓度
2
C.急性酸中毒时,救治方式是静脉注射NH Cl溶液
4
D.酸或碱中毒时,会导致血液中的酶发生水解
解析:B 血液中CO 浓度过高,氢离子浓度增大,会导致酸中毒,
2
其中==的值减小,A错误;急性酸中毒时,救治方式是静脉注射 NaHCO 溶液,C错
3
误;酸或碱中毒时,会导致血液中的酶发生变性而不是水解,D错误。
答案:B
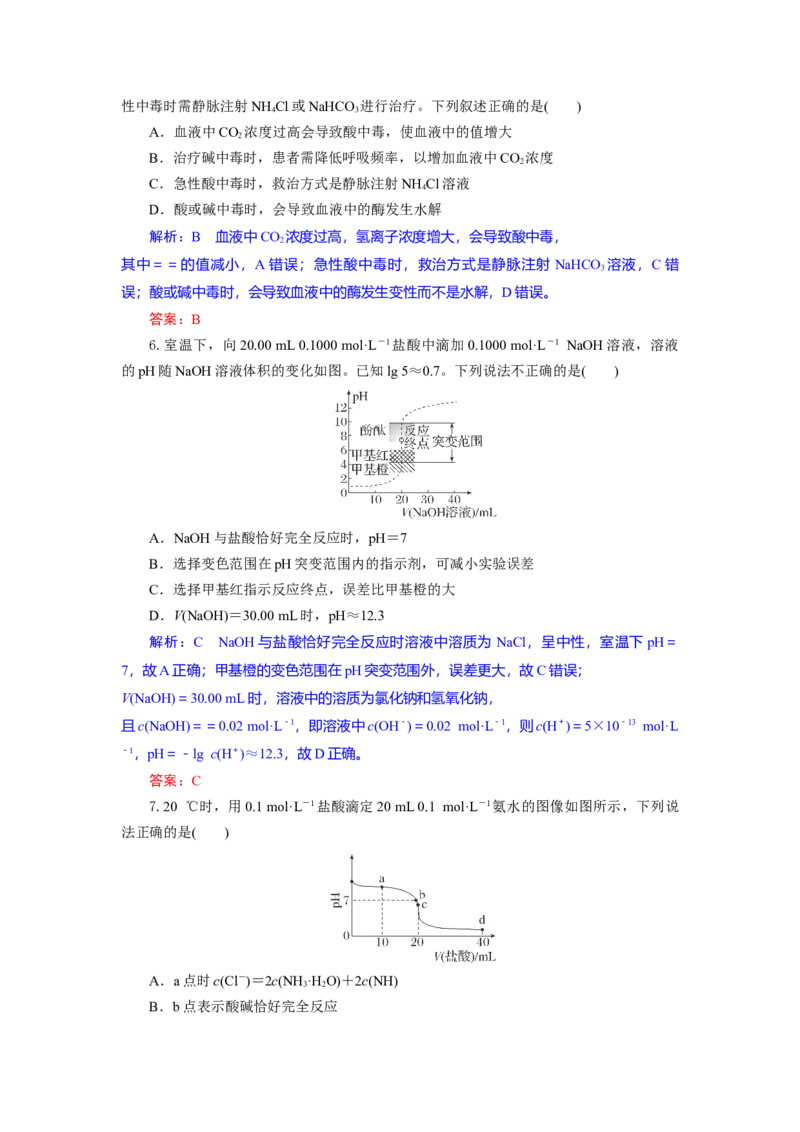
6.室温下,向20.00 mL 0.1000 mol·L-1盐酸中滴加0.1000 mol·L-1 NaOH溶液,溶液
的pH随NaOH溶液体积的变化如图。已知lg 5≈0.7。下列说法不正确的是( )
A.NaOH与盐酸恰好完全反应时,pH=7
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
D.V(NaOH)=30.00 mL时,pH≈12.3
解析:C NaOH与盐酸恰好完全反应时溶液中溶质为 NaCl,呈中性,室温下pH=
7,故A正确;甲基橙的变色范围在pH突变范围外,误差更大,故C错误;
V(NaOH)=30.00 mL时,溶液中的溶质为氯化钠和氢氧化钠,
且c(NaOH)==0.02 mol·L-1,即溶液中c(OH-)=0.02 mol·L-1,则c(H+)=5×10-13 mol·L
-1,pH=-lg c(H+)≈12.3,故D正确。
答案:C
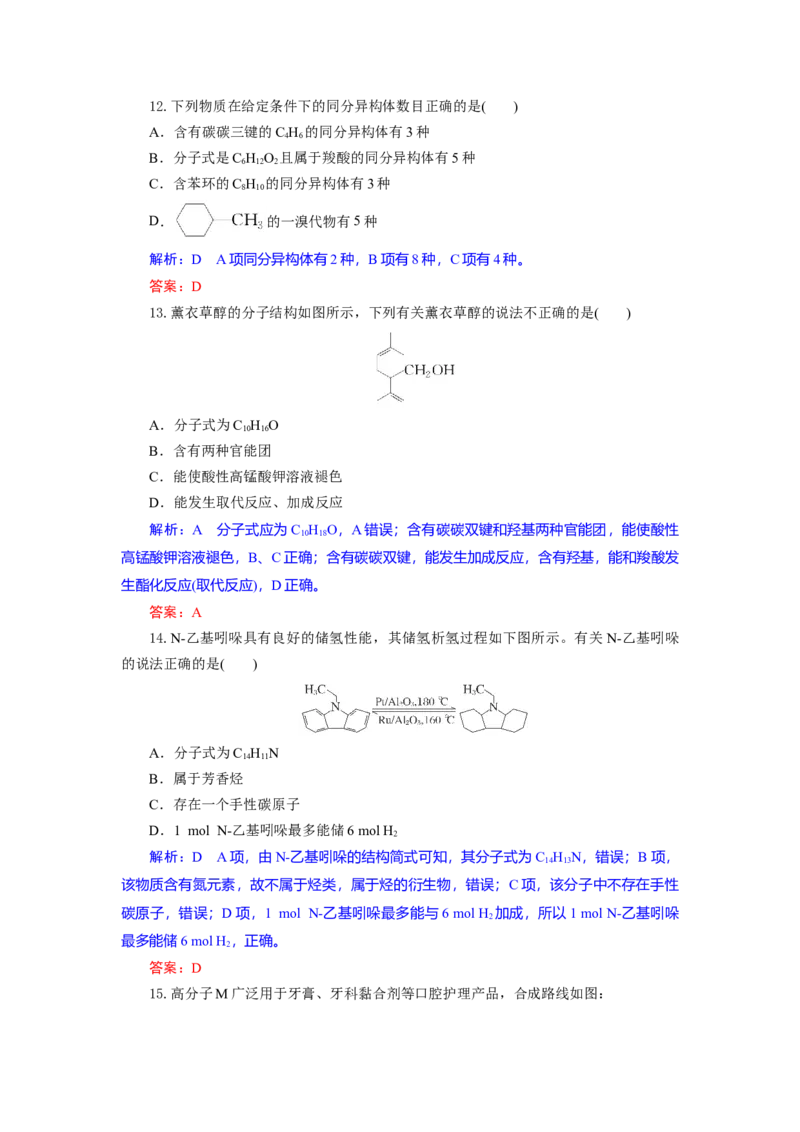
7.20 ℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1氨水的图像如图所示,下列说
法正确的是( )
A.a点时c(Cl-)=2c(NH ·H O)+2c(NH)
3 2
B.b点表示酸碱恰好完全反应C.c点时c(NH)>c(Cl-)>c(H+)>c(OH-)
D.a、b、c、d点均有c(NH)+c(H+)=c(Cl-)+c(OH-)
解析:D a点时加入的盐酸为10 mL,所得溶液的溶质为等物质的量浓度的氯化铵和
一水合氨,根据元素质量守恒:2c(Cl-)=c(NH ·HO)+c(NH),故A错误;c点时加入的盐
3 2
酸为20 mL,表示酸碱恰好完全反应,b点表示碱过量,盐酸完全反应,故B错误;c点
时,酸碱恰好完全反应生成氯化铵,溶液显酸性,c(H+)>c(OH-),根据电荷守恒:
c(NH)+c(H+)=c(Cl-)+c(OH-)可知,c(NH)K (BaCO)
sp 4 sp 3
D.曲线BC段内,=
解析:A 当c(CO)=0时,c(SO)=c(Ba2+)=1.0×10-5 mol·L-1,故BaSO 的溶度积
4
K =1.0×10-5×1.0×10-5=1.0×10-10。由题图可知当c(CO)>2.5×10-4 mol·L-1时,开始
sp
有BaCO 生成,BaCO 的溶度积K =2.5×10-4×1.0×10-5=2.5×10-9,C、B项错误,A
3 3 sp
项正确;曲线BC段内,BaSO(s)和BaCO (s)在溶液中都达到了沉淀溶解平衡状态,故==
4 3
==25,D项错误。
答案:A
9.人们通常将在同一原子轨道上运动、自旋相反的 2个电子,称为“电子对”,将在
某一原子轨道上运动的单个电子,称为“未成对电子”。下列基态原子的电子排布式中,
未成对电子数最多的是( )
A.1s22s22p63s23p6
B.1s22s22p63s23p63d54s2
C.1s22s22p63s23p63d54s1
D.1s22s22p63s23p63d104s1
解析:C 1s22s22p63s23p6中未成对电子数为0;1s22s22p63s23p63d54s2中未成对电子数为5;1s22s22p63s23p63d54s1中未成对电子数为6;1s22s22p63s23p63d104s1中未成对电子数为1。
答案:C
10.冠醚是一种超分子,它能否适配碱金属离子与其空腔直径和离子直径有关。二苯
并-18-冠-6与K+形成的配离子的结构如图所示。下列说法错误的是( )
冠醚 冠醚空腔直径/pm 适合的粒子(直径/pm)
15-冠-5 170~220 Na+(204)
18-冠-6 260~320 K+(276)、Rb+(304)
21-冠-7 340~430 Cs+(334)
A.冠醚可以用来识别碱金属离子
B.二苯并-18-冠-6也能适配Li+
C.该冠醚分子中碳原子杂化方式有2种
D.一个配离子中配位键的数目为6
解析:B 由表知,碱金属离子的直径在冠醚空腔直径范围内,二者可以适配,冠醚
可以用来识别碱金属离子,A正确;Li+半径小于K+,则二苯并-18-冠-6不能适配Li+,B
错误;该冠醚分子中苯环碳原子为sp2杂化、其他碳链上的碳原子为sp3杂化,C正确;由
结构简式可知,一个配离子中配位键的数目为6,D正确。
答案:B
11.关于下列晶体的熔、沸点高低排列判断不正确的是( )
A.CF<CCl <CBr <CI
4 4 4 4
B.金刚石>碳化硅>晶体硅
C.HO>HS>HSe>HTe
2 2 2 2
D.NaF>NaCl>NaBr>NaI
解析:C 组成和结构相似的分子晶体,分子晶体的相对分子质量越大,熔、沸点越
高,则晶体熔、沸点由低到高顺序为CF <CCl <CBr <CI ,故A正确;共价晶体的键长
4 4 4 4
越短,共价键越强,熔、沸点越高,键长C—C<C—Si<Si—Si,则熔、沸点由高到低为
金刚石>碳化硅>晶体硅,故B正确;水分子间能够形成氢键,其余不能,分子晶体的相
对分子质量越大,熔、沸点越高,则晶体熔、沸点由高到低顺序为HO>HTe>HSe>
2 2 2
HS,故C不正确;离子半径越小,离子键越强,则晶格能越大,熔、沸点越高,F、Cl、
2
Br、I的离子半径依次增大,则熔、沸点由高到低:NaF>NaCl>NaBr>NaI,故D正确。
答案:C12.下列物质在给定条件下的同分异构体数目正确的是( )
A.含有碳碳三键的C H 的同分异构体有3种
4 6
B.分子式是C H O 且属于羧酸的同分异构体有5种
6 12 2
C.含苯环的C H 的同分异构体有3种
8 10
D. 的一溴代物有5种
解析:D A项同分异构体有2种,B项有8种,C项有4种。
答案:D
13.薰衣草醇的分子结构如图所示,下列有关薰衣草醇的说法不正确的是( )
A.分子式为C H O
10 16
B.含有两种官能团
C.能使酸性高锰酸钾溶液褪色
D.能发生取代反应、加成反应
解析:A 分子式应为C H O,A错误;含有碳碳双键和羟基两种官能团,能使酸性
10 18
高锰酸钾溶液褪色,B、C正确;含有碳碳双键,能发生加成反应,含有羟基,能和羧酸发
生酯化反应(取代反应),D正确。
答案:A
14.N-乙基吲哚具有良好的储氢性能,其储氢析氢过程如下图所示。有关N-乙基吲哚
的说法正确的是( )
A.分子式为C H N
14 11
B.属于芳香烃
C.存在一个手性碳原子
D.1 mol N-乙基吲哚最多能储6 mol H
2
解析:D A项,由N-乙基吲哚的结构简式可知,其分子式为C H N,错误;B项,
14 13
该物质含有氮元素,故不属于烃类,属于烃的衍生物,错误;C项,该分子中不存在手性
碳原子,错误;D项,1 mol N-乙基吲哚最多能与6 mol H 加成,所以1 mol N-乙基吲哚
2
最多能储6 mol H ,正确。
2
答案:D
15.高分子M广泛用于牙膏、牙科黏合剂等口腔护理产品,合成路线如图:下列说法错误的是( )
A.试剂a是甲醇,B分子中可能共平面的原子最多有8个
B.化合物B不存在顺反异构体
C.化合物C的核磁共振氢谱有一组峰
D.合成M的聚合反应是缩聚反应
解 析 : D 合 成 M 的 聚 合 反 应 是 加 聚 反 应 , 是 CH===CHOCH 与
2 3
的加聚。
答案:D
二、非选择题:本题共4小题,共55分。
16、(13分)合成氨是人类科学技术发展史上的一项重大突破,目前工业上用氢气和
氮气直接合成氨。
(1)固氮一直是科学家致力研究的重要课题,有关热力学数据如下:
大气固氮N(g)
2
反应 工业固氮N(g)+3H(g)2NH (g)
2 2 3
+O(g)2NO(g)
2
温度/℃ 25 2000 25 350 400 450
平衡常 3.84× 5×
0.1 1.847 0.504 0.152
数K 10-31 108
常温下,大气固氮的倾向________工业固氮(填“大于”或“小于”)。
(2)N (g)与H(g)反应的能量变化如图所示,则N(g)与H(g)反应制备NH (l)的热化学方
2 2 2 2 3
程式为:___________________________________。
(3)T ℃时,在2 L恒容密闭容器中加入1.2 mol N 和2 mol H 模拟一定条件下工业固氮
2 2
[N (g)+3H(g)2NH (g)],体系中n(NH )随时间的变化如图所示:
2 2 3 3①前2分钟内的平均反应速率v(NH )=____________mol·L-1·min-1;
3
②有关工业固氮的说法正确的是________(填字母)。
A.使用催化剂可提高反应物的转化率
B.循环使用N、H 可提高NH 的产率
2 2 3
C.温度控制在500 ℃左右有利于反应向正方向进行
D.增大压强有利于加快反应速率,所以压强越大越好
③T ℃时,该反应的平衡常数为________;
(4)研究表明某些过渡金属催化剂可以加速氨气的分解,某温度下,用等质量的不同金
属分别催化等浓度的氨气,测得氨气分解的初始速率(单位:mmol/min)与催化剂的对应关
系如表所示。
催化剂 Fe Pd Ru Rh Pt Ni
初始速率 0.5 1.8 7.9 4.0 2.2 3.0
在不同催化剂的催化作用下,氨气分解反应中的活化能最大的催化剂是________(填化
学式)。
解析:(1)根据表格数据可知:在相同温度下,大气固氮平衡常数远小于工业固氮,化
学平衡常数越大,说明反应正向进行的程度越大,因此常温下,大气固氮的倾向小于工业
固氮;
(2)根据图示可知反应物总能量比生成物总能量高,因此该反应为放热反应,
0.5 mol N 完全反应变为NH (l)时放出热量为Q=300 kJ+20 kJ-254 kJ=66 kJ,故该反应
2 3
的热化学方程式可表示为:N(g)+3H(g)2NH (l) ΔH=-132 kJ/mol;
2 2 3
(3)①在前2 min内NH 的物质的量增加了0.45 mol,反应容器为2 L,
3
则根据v=Δc/t可得,
用NH 表示的反应速率v(NH )==0.1125 mol·L-1·min-1;
3 3
②A.使用催化剂对正、逆反应速率的影响相同,平衡不发生移动,因此不能提高反应
物的转化率,A错误;B.循环使用N 、H 可使更多的反应物变为生成物,因此能够提高
2 2
NH 的产率,B正确;C.该反应的正反应是放热反应,温度降低平衡正向移动,有利于反
3
应向正方向进行,温度控制在500 ℃左右,是因为在该温度下催化剂的活性最大,反应速
率较快,C错误;D.该反应的正反应是气体体积减小的反应,从理论上讲增大压强有利于
加快反应速率,提高物质平衡转化率,但压强越大,对设备的材料承受的压力要求也越
高,所以不是压强越大就越好,D错误;③由图可知,达平衡时n(NH )=0.8 mol,根据题
3意列出三段式:
N + 3H2NH
2 2 3
起始/(mol·L-1) 0.6 1 0
转化/(mol·L-1) 0.2 0.6 0.4
平衡/(mol·L-1) 0.4 0.4 0.4
则平衡常数K===6.25;(4)物质发生反应时的活化能越大,反应进行的化学速率就
越小。根据表格数据可知:以Fe作催化剂时反应速率最小,则氨分解反应的活化能最大,
故在不同催化剂的催化作用下,氨气分解反应中的活化能最大的催化剂是Fe。
答案:(1)小于
(2)N (g)+3H(g)2NH (l) ΔH=-132 kJ/mol
2 2 3
(3)①0.1125 ②B ③6.25 (4)Fe
17.(14分)金属氢氧化物在酸中的溶解度不同,因此可以利用这一性质,控制溶液
的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度[S/(mol·L-1)]
如图所示。
难溶金属氢氧化物的S-pH图
(1)pH=3时溶液中铜元素的主要存在形式是________(填化学式)。
(2)若要除去CuCl 溶液中的少量Fe3+,应该控制溶液的pH为________(填字母)。
2
A.<1 B.4左右
C.>6
(3)在Ni(NO ) 溶液中含有少量的Co2+杂质,________(填“能”或“不能”)通过调节
3 2
溶液pH的方法来除去,理由是_______________________。
解析:(1)据图知pH为4~5时,Cu2+开始沉淀为Cu(OH) ,因此pH=3时,
2
主要以Cu2+形式存在。
(2)若要除去CuCl 溶液中的Fe3+,应保证Fe3+完全沉淀,而Cu2+还未沉淀,据图知应
2
控制溶液pH为4左右。
(3)据图知,Co2+和Ni2+沉淀的pH范围相差太小,无法通过调节溶液pH的方法除去
Ni(NO ) 溶液中的Co2+。
3 2
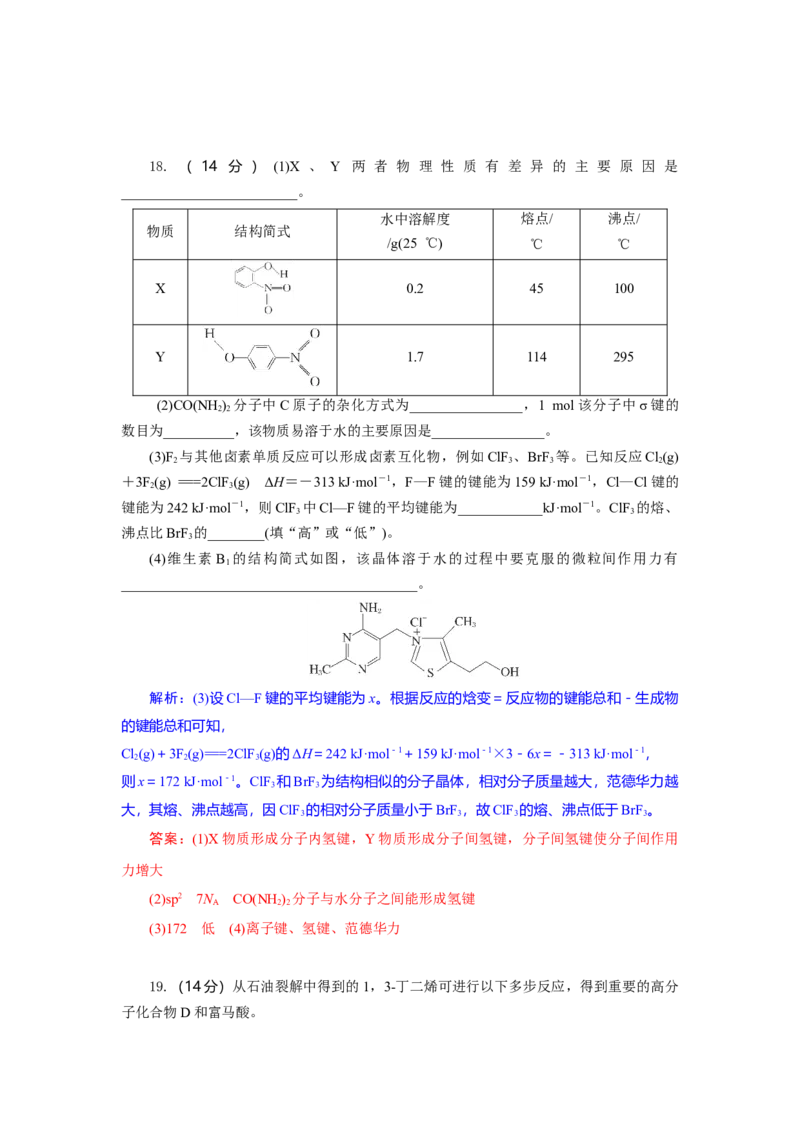
答案:(1)Cu2+ (2)B (3)不能 Co2+和Ni2+沉淀的pH范围相差太小18. ( 14 分 ) (1)X 、 Y 两 者 物 理 性 质 有 差 异 的 主 要 原 因 是
_________________________。
水中溶解度 熔点/ 沸点/
物质 结构简式
/g(25 ℃) ℃ ℃
X 0.2 45 100
Y 1.7 114 295
(2)CO(NH ) 分子中C原子的杂化方式为________________,1 mol该分子中σ键的
2 2
数目为__________,该物质易溶于水的主要原因是________________。
(3)F 与其他卤素单质反应可以形成卤素互化物,例如ClF 、BrF 等。已知反应Cl(g)
2 3 3 2
+3F(g) ===2ClF (g) ΔH=-313 kJ·mol-1,F—F键的键能为159 kJ·mol-1,Cl—Cl键的
2 3
键能为242 kJ·mol-1,则ClF 中Cl—F键的平均键能为____________kJ·mol-1。ClF 的熔、
3 3
沸点比BrF 的________(填“高”或“低”)。
3
(4)维生素 B 的结构简式如图,该晶体溶于水的过程中要克服的微粒间作用力有
1
__________________________________________。
解析:(3)设Cl—F键的平均键能为x。根据反应的焓变=反应物的键能总和-生成物
的键能总和可知,
Cl(g)+3F(g)===2ClF (g)的ΔH=242 kJ·mol-1+159 kJ·mol-1×3-6x=-313 kJ·mol-1,
2 2 3
则x=172 kJ·mol-1。ClF 和BrF 为结构相似的分子晶体,相对分子质量越大,范德华力越
3 3
大,其熔、沸点越高,因ClF 的相对分子质量小于BrF,故ClF 的熔、沸点低于BrF。
3 3 3 3
答案:(1)X物质形成分子内氢键,Y物质形成分子间氢键,分子间氢键使分子间作用
力增大
(2)sp2 7N CO(NH) 分子与水分子之间能形成氢键
A 2 2
(3)172 低 (4)离子键、氢键、范德华力
19.(14分)从石油裂解中得到的1,3-丁二烯可进行以下多步反应,得到重要的高分
子化合物D和富马酸。(1)反应①的反应类型是_______________________________。
(2)第②步反应的试剂是_______________________________。
(3)写出B的结构简式:_______________________________。
(4)写出D的顺式结构:______________________________。
(5)写出第⑦步反应的化学方程式:_________________________。
(6)以上反应中属于消去反应的是________(填序号)。
解析:B为HOCH
2
CHClCH
2
CH
2
OH,A为HOCH
2
CH===CHCH
2
OH,2-氯-1,3-丁二烯
发生加聚反应生成的高分子化合物D为 ;2-氯-1,4-丁二酸
发生消去反应生成C,则C为NaOOCCH===CHCOONa,然后酸化得富马酸,富马酸的结
构简式为HOOCCH===CHCOOH。(5)2-氯-1,4-丁二酸发生消去反应生成C,第⑦步反应
的化学方程式为
HOOCCHClCH
2
COOH+3NaOH――→NaOOCCH===CHCOONa+NaCl+3H
2
O。
(6)①为加成反应、②为水解反应或取代反应、③为加成反应、④为消去反应、⑤为加聚反
应、⑥为氧化反应、⑦为消去反应,以上反应中属于消去反应的是④⑦。
答案:(1)加成反应 (2)NaOH的水溶液
(3)HOCHCHClCH CHOH
2 2 2
(5)HOOCCHClCH COOH+3NaOH――→NaOOCCH===CHCOONa+NaCl+3HO
2 2
(6)④⑦