文档内容
2025 年 1 月浙江卷化学试题
一、单选题
1.下列属于极性分子的是
A.HCl B.N C.He D.CH
2 4
【答案】A
【解析】A.HCl是由极性键形成的双原子分子,正负电荷中心不重合,属于极性分子,A正确;
B.N 是非极性键形成的单质分子,正负电荷中心重合,属于非极性分子,B错误;
2
C.He是单原子分子,正负电荷中心重合,属于非极性分子,C错误;
D.CH 是由极性键形成的正四面体结构,正负电荷中心重合,属于非极性分子,D错误;
4
故选A。
2.下列化学用语表示不正确的是
...
A.基态S原子的电子排布式:2s22p4 B.质量数为14的碳原子: 14C
6
C.乙烯的结构简式:CH =CH D.H O的电子式:
2 2 2
【答案】A
【解析】A.硫原子质子数为16,位于第三周期ⅥA族,基态S原子的电子排布式:1s22s22p63s23p4,A错误;
B.碳原子质子数为6,质量数为14的碳原子表示为: 14C,B正确;
6
C.乙烯的官能团是碳碳双键,结构简式为:CH =CH ,C正确;
2 2
D.水是共价化合物,水分子中O原子是中心原子,电子式为 ,D正确;
故选A。
3.化学与生产生活密切相关,下列说法不正确的是
...
A.ClO 具有强氧化性,可用于杀菌消毒
2
B.聚丙烯是高分子材料,可用作吸水剂
C.Na CO 溶液呈碱性,可用于除油污
2 3
D.硬铝密度小、强度高,抗腐蚀能力强,可用作飞机材料
【答案】B
【解析】A.ClO 具有强氧化性,能使蛋白质变性,可用于杀菌消毒,A正确;
2
B.聚丙烯属于有机合成高分子材料,不含有亲水基团,不能用作吸水剂,B错误;
C.油污可以在碱性环境下水解,Na CO 溶液由于碳酸根离子的水解,使溶液呈碱性,因此可用于除油污,C正确;
2 3
D.硬铝合金具有密度小、强度高的优良特性,其表面会形成致密的氧化膜,抗腐蚀性强,因此可用作航空材料,
D正确;
故选B。
4.根据元素周期律,下列说法不正确的是
...
A.第一电离能:N>O>S B.化合物中键的极性:SiCl >PCl
4 3
C.碱性:LiOH>KOH D.化合物中离子键百分数:MgO>Al O
2 3
【答案】C
【解析】A.根据同一周期从左往右元素的第一电离能呈增大趋势,ⅡA与ⅢA,ⅤA与ⅥA反常,故第一电离能:
N>O>S,A正确;
B.已知同一周期从左往右元素的电负性依次增大,电负性Si<P<Cl,电负性差值越大,键的极性越大,故化合物
中键的极性:SiCl >PCl ,B正确;
4 3
C.同一主族从上往下元素的金属性依次增大,金属性Li<K,故碱性:LiOH<KOH,C错误;
D.已知同一周期从左往右元素的电负性依次增大,即电负性Mg<Al,故Mg与O的电负性差值>Al与O的电负
性差值,电负性差值越大离子键百分数越大,故化合物中离子键百分数:MgO>Al O ,D正确;
2 3
故选:C。
5.关于实验室安全,下列说法不正确的是
...
A.若不慎盐酸沾到皮肤上,应立即用大量水冲洗,然后用3%~5%NaHCO 溶液冲洗
3B.实验室制备Cl 时,可用NaOH溶液吸收尾气
2
C.水银易挥发,若不慎有水银洒落,无需处理
D.PbS难溶于水,可用Na S处理废水中的Pb2+,再将沉淀物集中送至环保单位进一步处理
2
【答案】C
【解析】A.不慎将强酸沾到皮肤上,应立即用大量水冲洗,将其稀释,然后用弱碱性物质如3%~5%的NaHCO
3
溶液进行中和,A正确;
B.Cl 是有毒气体,可根据其能够与碱反应的性质,利用NaOH溶液进行尾气处理,B正确;
2
C.水银是重金属,有毒,硫能与汞反应生成硫化汞,若不慎有水银洒落,可撒上硫粉进行处理,C错误;
D.PbS难溶于水,Na S可与Pb2+反应生成硫化物沉淀,因此处理废水中Pb2+等重金属离子常用沉淀法,D正确;
2
故选C。
6.关于溴的性质,下列说法不正确的是
...
A.Br-可被Cl 氧化为Br
2 2
B.Br 与SO 水溶液反应的还原产物为Br-
2 2
C.Br +2Fe2+=2Fe3++2Br-,说明氧化性:Br >Fe3+
2 2
D.1molBr 与足量NaOH溶液反应生成NaBr和NaBrO ,转移5mol电子
2 3
【答案】D
【解析】A.氯气具有强氧化性,可将Br-氧化为Br ,A正确;
2
B.Br 与SO 水溶液反应,生成HBr和H SO ,还原产物为Br-,B正确;
2 2 2 4
C.根据反应Br +2Fe2+=2Fe3++2Br-可知,氧化剂为Br ,氧化产物为Fe3+,氧化剂的氧化性大于氧化产物的氧化
2 2
性,故氧化性:Br >Fe3+,C正确;
2
D.Br 与足量NaOH溶液反应生成NaBr和NaBrO ,反应方程式为:3Br +6NaOH=5NaBr+NaBrO +3H O,3molBr
2 3 2 3 2 2
参与反应,电子转移5mol,D错误;
故选D。
7.下列物质的结构或性质不能说明其用途的是
..
A.葡萄糖分子结构中有多个羟基,故葡萄糖可与银氨溶液反应制作银镜
B.具有网状结构的交联橡胶弹性好、强度高,故可用作汽车轮胎材料
C.SiC的碳、硅原子间通过共价键形成空间网状结构,硬度大,故SiC可用作砂轮磨料
D.NaHCO 能中和酸并受热分解产生气体,故可用作加工馒头的膨松剂
3
【答案】A
【解析】A.葡萄糖分子中含有醛基,具有还原性,能发生银镜反应,可与银氨溶液反应制作银镜,A正确;
B.橡胶的分子链可以交联,交联后的橡胶受外力作用发生变形时,具有迅速复原的能力,因此其弹性好,强度高,且具
有良好的物理力学性能和化学稳定性,故可用作汽车轮胎材料,B错误;
C.SiC中原子以共价键形成空间网状结构,熔点高、硬度大,可用作砂轮、砂纸的磨料,C错误;
D.NaHCO 可中和酸生成二氧化碳气体,并受热分解产生大量二氧化碳气体,可用作食品膨松剂,D错误;
3
故选A。
8.下列方程式不正确的是
...
A.MnO 与浓盐酸反应:MnO +4H++2Cl− ≜Mn2++Cl ↑+2H O
2 2 2 2
B.NO 与H O反应:3NO +H O=2H++2NO−+NO
2 2 2 2 3
Δ
C.将少量灼热的CuO加入CH CH OH中:CH CH OH+CuO→CH CHO+Cu+H O
3 2 3 2 3 2
D.将SO 通入酸性KMnO 溶液:5SO +2MnO−+4H+ =5SO2−+2Mn2++2H O
2 4 2 4 4 2
【答案】D
【解析】A.MnO 与浓盐酸在加热条件下反应生成氯化锰、氯气、水,所给离子方程式正确,A正确;
2
B.二氧化氮与水反应生成硝酸和一氧化氮,所给离子方程式正确,B正确;
C.乙醇的催化氧化生成乙醛,该反应氧化铜被还原生成铜,所给方程式正确,C正确;
D.二氧化硫与酸性高锰酸钾溶液反应生成硫酸钾、硫酸锰和硫酸,反应的离子方程式为:5SO +2MnO−+2H O=
2 4 2
5SO2−+2Mn2++4H+,D错误;
4
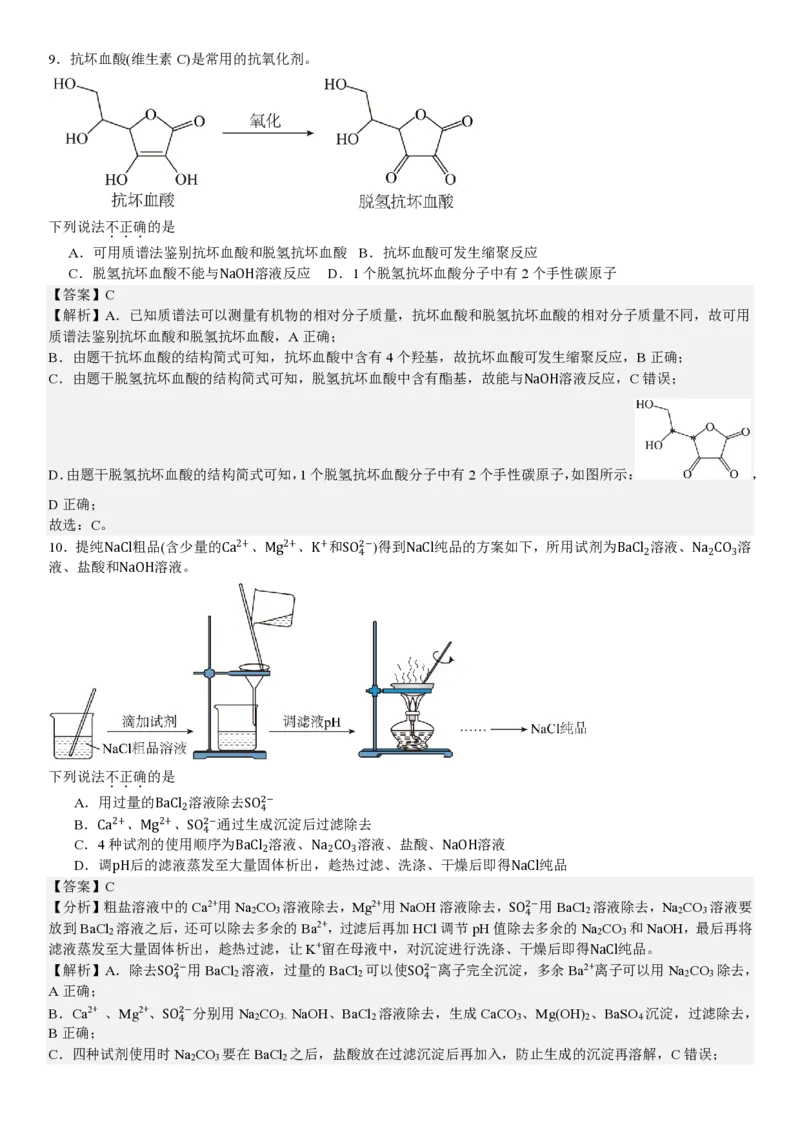
故选D。9.抗坏血酸(维生素C)是常用的抗氧化剂。
下列说法不正确的是
...
A.可用质谱法鉴别抗坏血酸和脱氢抗坏血酸 B.抗坏血酸可发生缩聚反应
C.脱氢抗坏血酸不能与NaOH溶液反应 D.1个脱氢抗坏血酸分子中有2个手性碳原子
【答案】C
【解析】A.已知质谱法可以测量有机物的相对分子质量,抗坏血酸和脱氢抗坏血酸的相对分子质量不同,故可用
质谱法鉴别抗坏血酸和脱氢抗坏血酸,A正确;
B.由题干抗坏血酸的结构简式可知,抗坏血酸中含有4个羟基,故抗坏血酸可发生缩聚反应,B正确;
C.由题干脱氢抗坏血酸的结构简式可知,脱氢抗坏血酸中含有酯基,故能与NaOH溶液反应,C错误;
D.由题干脱氢抗坏血酸的结构简式可知,1个脱氢抗坏血酸分子中有2个手性碳原子,如图所示: ,
D正确;
故选:C。
10.提纯NaCl粗品(含少量的Ca2+、Mg2+、K+和SO2−)得到NaCl纯品的方案如下,所用试剂为BaCl 溶液、Na CO 溶
4 2 2 3
液、盐酸和NaOH溶液。
下列说法不正确的是
...
A.用过量的BaCl 溶液除去SO2−
2 4
B.Ca2+、Mg2+、SO2−通过生成沉淀后过滤除去
4
C.4种试剂的使用顺序为BaCl 溶液、Na CO 溶液、盐酸、NaOH溶液
2 2 3
D.调pH后的滤液蒸发至大量固体析出,趁热过滤、洗涤、干燥后即得NaCl纯品
【答案】C
【分析】粗盐溶液中的Ca2+用Na CO 溶液除去,Mg2+用NaOH溶液除去,SO2−用BaCl 溶液除去,Na CO 溶液要
2 3 4 2 2 3
放到BaCl 溶液之后,还可以除去多余的Ba2+,过滤后再加HCl调节pH值除去多余的Na CO 和NaOH,最后再将
2 2 3
滤液蒸发至大量固体析出,趁热过滤,让K+留在母液中,对沉淀进行洗涤、干燥后即得NaCl纯品。
【解析】A.除去SO2−用BaCl 溶液,过量的BaCl 可以使SO2−离子完全沉淀,多余Ba2+离子可以用Na CO 除去,
4 2 2 4 2 3
A正确;
B.Ca2+ 、Mg2+、SO2−分别用Na CO NaOH、BaCl 溶液除去,生成CaCO 、Mg(OH) 、BaSO 沉淀,过滤除去,
4 2 3、 2 3 2 4
B正确;
C.四种试剂使用时Na CO 要在BaCl 之后,盐酸放在过滤沉淀后再加入,防止生成的沉淀再溶解,C错误;
2 3 2D.过滤后再加入HCl调节滤液的pH值,最后蒸发至大量固体析出,趁热过滤、洗涤、干燥后即得NaCl纯品,K+
留在母液中,D正确;
故选C。
11.下列说法正确的是
A.常温常压下H (g)和O (g)混合无明显现象,则反应2H (g)+O (g)=2H O(l)在该条件下不自发
2 2 2 2 2
B.3H (g)+N (g)⇌2NH (g) ΔH<0,升高温度,平衡逆移,则反应的平衡常数减小
2 2 3
C.CO(g)+H (g)⇌C(s)+H O(g) ΔH<0,则正反应的活化能大于逆反应的活化能
2 2
D.Na(s)+ 1 Cl (g)=NaCl(s) ΔH<0, Na+(g)+Cl−(g)=NaCl(s) ΔH<0,则Na(s)+ 1 Cl (g)=Na+(g)+
2 2
2 2
Cl−(g) ΔH<0
【答案】B
【解析】A.根据复合判据ΔG=ΔH-TΔS,该反应ΔH<0、ΔS<0,温度较低时ΔG<0,故低温能自发进行,A错误;
B.该反应为放热反应,升高温度,平衡逆移,平衡常数减小,B正确;
C.该反应为放热反应,则E −E <0,则正反应的活化能小于逆反应的活化能,C错误;
正 逆
D.①:Na(s)+ 1 Cl (g)=NaCl(s) ΔH <0, ②:Na+(g)+Cl−(g)=NaCl(s) ΔH <0,根据盖斯定律,反应①
2 1 2
2
-反应②得到目标反应Na(s)+ 1 Cl (g)=Na+(g)+Cl−(g),则ΔH=𝛥H -𝛥H ,由于不能明确𝛥H 、𝛥H 相对大小,则ΔH
2 1 2 1 2
2
不能确定,D错误;
故选B。
12.一种可充放电Li−O 电池的结构示意图如图所示。该电池放电时,产物为Li O和Li O ,随温度升高Q(消耗
2 2 2 2
1molO 转移的电子数)增大。下列说法不正确的是
2 ...
A.熔融盐中LiNO 的物质的量分数影响充放电速率
3
B.充放电时,Li+优先于K+通过固态电解质膜
C.放电时,随温度升高Q增大,是因为正极区O2−转化为O2−
2
D.充电时,锂电极接电源负极
【答案】C
【分析】Li−O 电池放电时,锂电极为负极,发生反应:Li−e- =Li+,多孔功能电极为正极,低温时发生反应:
2
O +2e-=O2−,随温度升高Q增大,正极区O2−转化为O2−;充电时,锂电极为阴极,得到电子,多孔功能电极为阳
2 2 2
极,O2−或O2−失去电子。
2
放电 放电
【解析】A.根据分析可知,电池总反应方程式为:O +2Li ⇌ Li O 或O +4Li ⇌ 2Li O,充放电时有Li+参与或
2 2 2 2 2
充电 充电
生成,因此熔融盐中LiNO 的物质的量分数影响充放电速率,A正确;
3
B.Li+比K+的半径小,因此Li+优先于K+通过固态电解质膜,B正确;
C.放电时,正极得到电子,O2−中氧原子为-1价,O2−中氧原子为-2价,因此随温度升高Q增大,正极区O2−转化
2 2
为O2−,C错误;
D.充电时,锂电极为阴极,连接电源负极,D正确;
故选C。
13.某化合物Fe(NH ) Cl 的晶胞如图所示,下列说法不正确的是
3 2 2 ...A.晶体类型为混合晶体 B.NH 与二价铁形成配位键
3
C.该化合物与水反应有难溶物生成 D.该化合物热稳定性比FeCl 高
2
【答案】D
【解析】A.由图可知该化合物中存在离子键、配位键和分子间作用力,故晶体类型为混合晶体,A正确;
B.NH 与二价铁通过配位键形成[Fe(NH ) ]2+,B正确;
3 3 2
C.Fe(NH ) Cl 与水反应可以生成Fe(OH) 沉淀,方程式为Fe(NH ) Cl +2H O=Fe(OH) ↓+2NH Cl,C正确;
3 2 2 2 3 2 2 2 2 4
D.Fe(NH ) Cl 中[Fe(NH ) ]2+离子半径大于Fe2+,[Fe(NH ) ]2+与Cl-之间的键能小于Fe2+与Cl-之间的键能,
3 2 2 3 2 3 2
Fe(NH ) Cl 热稳定性小于FeCl ,D错误;
3 2 2 2
故选D。
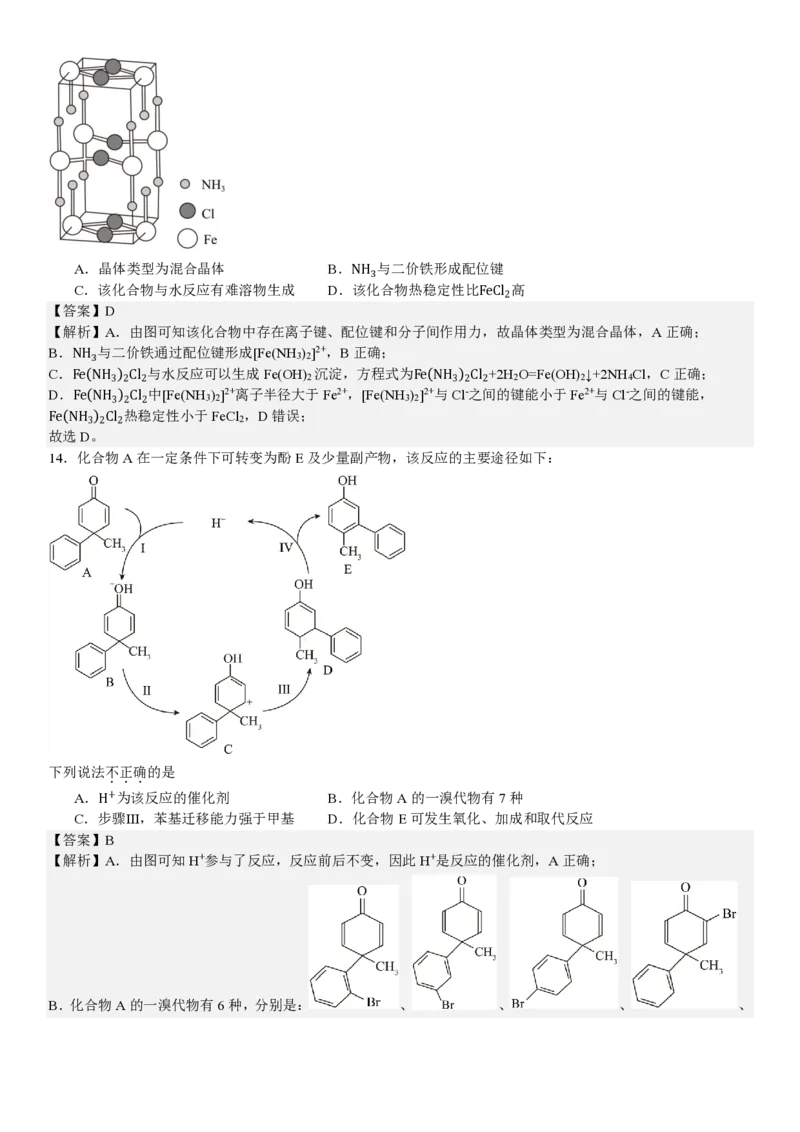
14.化合物A在一定条件下可转变为酚E及少量副产物,该反应的主要途径如下:
下列说法不正确的是
...
A.H+为该反应的催化剂 B.化合物A的一溴代物有7种
C.步骤Ⅲ,苯基迁移能力强于甲基 D.化合物E可发生氧化、加成和取代反应
【答案】B
【解析】A.由图可知H+参与了反应,反应前后不变,因此H+是反应的催化剂,A正确;
B.化合物A的一溴代物有6种,分别是: 、 、 、 、、 ,B错误;
C.步骤III可知C转化到D,苯基发生了迁移,甲基没有迁移,说明苯基的迁移能力强于甲基,C正确;
D.化合物E中有酚羟基可以发生氧化反应,苯环可以发生加成反应和取代反应,D正确;
故选B。
15.25℃时,H CO 的电离常数K =4.5×10−7,K =4.7×10−11;K (CaCO )=3.4×10−9。下列描述不正确的
2 3 a1 a2 sp 3 ...
是
A.HCO−+H O⇌OH−+H CO ,K=2.2×10−8
3 2 2 3
B.2HCO− ⇌H CO +CO2−,K=1.0×10−4
3 2 3 3
C.HCO−+Ca2+ ⇌CaCO (s)+H+,K=1.4×10−2
3 3
D.NaHCO 溶液中,c(H+)+c(H CO )=c(OH−)+c(CO2−),则c(H+)= Ka1 [Ka2c(HCO3 −)+Kw ]
3 2 3 3 Kal+c(HCO
3
−)
【答案】D
【解析】A.HCO−+H O⇌OH−+H CO ,K= c(OH−)×c(H2CO3 ) = Kw = 10−14 =2.2×10−8,A正确;
3 2 2 3 c(HCO
3
−) Ka1 4.5×10−7
B.2HCO− ⇌H CO +CO2−,K= c(CO3 2−)×c(H2CO3 ) = Ka2 = 4.7×10−11 =1.0×10−4,B正确;
3 2 3 3 c2(HCO
3
−) Ka1 4.5×10−7
C.HCO−+Ca2+ ⇌CaCO (s)+H+,K= c(H+) = Ka2 = 4.7×10−11 =1.4×10−2,C正确;
3 3 c(HCO
3
−)×c(Ca2+) Ksp (CaCO3 ) 3.4×10−9
D.Ka1 [Ka2c(HCO3 −)+Kw ] = c(H c + ( ) H × 2 c C (H O3 C ) O3 −) [ c(CO c( 3 2 H − C ) O ×c 3 − ( ) H+) ×c(HCO3 −)+c(H+)×c(OH−)] =c2(H+)×[ c(CO3 2−)+c(OH−) ],由于c(H+)+
Kal+c(HCO 3 −) c(H+)×c(HCO3 −) +c(HCO−) c(H2CO3 )+c(H+)
c(H2CO3) 3
c(H CO )=c(OH−)+c(CO2−),Ka1 [Ka2c(HCO3 −)+Kw ] = c2(H+),D错误;
2 3 3 Kal+c(HCO
3
−)
故选D。
16.蛋白质中N元素含量可按下列步骤测定:
下列说法不正确的是
...
A.步骤Ⅰ,须加入过量浓H SO ,以确保N元素完全转化为NH+
2 4 4
B.步骤Ⅱ,浓NaOH溶液过量,有利于氨的蒸出
C.步骤Ⅲ,用定量、过量盐酸标准溶液吸收NH ,以甲基红(变色的pH范围:4.4~6.2)为指示剂,用NaOH标准
3
溶液滴定,经计算可得N元素的含量
D.尿素[CO(NH ) ]样品、NaNO 样品的N元素含量均可按上述步骤测定
2 2 3
【答案】D
【分析】蛋白质中的N元素以氨基或酰胺基形式存在,在浓硫酸、K SO 和催化剂CuSO 作用下发生反应生成NH+,
2 4 4 4
再加入浓NaOH溶液让NH+转化为NH 蒸出,NH 用一定量的盐酸吸收,多余的盐酸用标准NaOH溶液通过滴定测
4 3 3
定出来,从而计算出N的含量。
【解析】A.步骤Ⅰ,加入过量浓H SO ,使蛋白质中的氨基和酰胺基全部转化为NH+,确保N元素完全转化为NH+,
2 4 4 4
A正确;B.根据NH++OH-⇋NH ·H O⇋NH +H O,NaOH过量,增大OH-浓度有利于氨的蒸出,B正确;
4 3 2 3 2
C.步骤Ⅲ,用定量、过量盐酸标准溶液吸收NH 后,过量的HCl用标准NaOH溶液滴定,反应后溶液中有NaCl
3
和NH Cl,终点显酸性,用在酸性范围内变色的甲基红为指示剂,C正确;
4
D.NaNO 中的N元素在浓硫酸、K SO 和催化剂CuSO 作用下不会转化为NH+,不能按上述步骤测定,D错误;
3 2 4 4 4
故选D。
二、解答题
17.磷是生命活动中不可或缺的元素。请回答:
(1)关于ⅤA族元素原子结构的描述,下列说法正确的是_______。
A.基态P原子3p轨道上的电子自旋方向相同 B.As3+的最外层电子数为18
C.P3+的半径小于P5+的半径 D.电子排布为[Ne]3s13p4的P原子处于激发态
(2)某化合物的晶胞如图。
①化学式是 ;
②将0.01mol该化合物加入到含少量石蕊的10mLH O中,实验现象是 (从酸碱性和溶解性角度推测)。
2
(3)两分子H PO (K =4.8×10−13)脱水聚合得到一分子H P O (K =2.0×10−7),从PO3−、HP O3−的结构角度分
3 4 a3 4 2 7 a3 4 2 7
析K 差异的原因 。
a3
(4)兴趣小组对某磷灰石[主要成分为Ca (PO ) OH、Ca (PO ) F、Ca (PO ) Cl和少量SiO ]进行探究,设计了两种制
5 4 3 5 4 3 5 4 3 2
备H PO 的方法:
3 4
Ⅰ.用稍过量的浓H SO 与磷灰石反应,得到H PO 溶液、少量SiF 气体、渣(主要成分为CaSO )。
2 4 3 4 4 4
Ⅱ.将磷灰石脱水、还原,得到的白磷(P )燃烧后与水反应制得H PO 溶液。
4 3 4
①方法I,所得H PO 溶液中含有的杂质酸是 。
3 4
②以方法Ⅰ中所得渣为硫源,设计实验制备无水Na SO ,流程如下:
2 4
溶液A是 ,系列操作B是 ,操作C是 。
③方法Ⅱ中,脱水得到的Ca (PO ) O(足量)与炭(C)、SiO 高温下反应,生成白磷(P )和另一种可燃性气体,该反应
10 4 6 2 4
的化学方程式是 。
【答案】(1)AD
(2) Ca PCl 溶液变蓝,有气体放出
3 3
(3)PO3−的负电荷密度大,更易结合氢离子
4
(4) 盐酸、氢氟酸 碳酸钠溶液 过滤、加硫酸、蒸发浓缩、冷却结晶、过滤、洗涤 加热脱水
高温
2Ca (PO ) O+30C+20SiO = 20CaSiO +3P +30CO↑
10 4 6 2 3 4
【解析】(1)A.基态P原子价电子排布式为3s23p3,根据洪特规则,3p轨道上的3个电子自旋方向相同,A正确;
B.基态As原子价电子排布式为4s24p3,As3+的价电子排布式为4s2,最外层电子数为2,B错误;
C.P3+比P5+多一个电子层,所以P3+的半径大于P5+的半径,C错误;
D.基态P原子的电子排布式为[Ne]3s23p3的,电子排布为[Ne]3s13p4的P原子处于激发态,D正确;
故选AD。(2)①根据均摊原则,晶胞中Cl原子数6× 1 =3、P原子数8× 1 =1、Ca原子数12× 1 =3,所以化学式是Ca PCl ;
3 3
2 8 4
②Ca PCl 中P显-3价,将0.01mol该化合物加入到含少量石蕊的10mLH O中,反应生成氯化钙、氢氧化钙、PH
3 3 2 3
气体,溶液呈碱性,实验现象是溶液变蓝,有气体放出。
(3)当两分子H PO 脱水聚合时,结构发生变化,聚合结构的体积更大,负电荷分布更分散,更容易电离出氢离
3 4
子,而PO3−的负电荷密度大,更易结合氢离子,所以聚合后的K 值增大;
4 a3
(4)①方法I中,Ca (PO ) OH、Ca (PO ) F、Ca (PO ) Cl和浓硫酸反应生成硫酸钙、磷酸、氢氟酸、盐酸,氢
5 4 3 5 4 3 5 4 3
氟酸和SiO 反应生成SiF 气体和水,所得H PO 溶液中含有的杂质酸是盐酸、氢氟酸。
2 4 3 4
②碳酸钠和硫酸钙反应,硫酸钙转化为碳酸钙沉淀和硫酸钠,溶液A是碳酸钠溶液;过滤出碳酸钙,得硫酸钠、
碳酸钠混合液,加硫酸除碳酸钠,蒸发浓缩、冷却结晶、过滤、洗涤得Na SO ⋅xH O,系列操作B是过滤、加硫
2 4 2
酸、蒸发浓缩、冷却结晶、过滤、洗涤,Na SO ⋅xH O加热脱水得无水硫酸钠,操作C是加热脱水。
2 4 2
③方法Ⅱ中,脱水得到的Ca (PO ) O(足量)与炭(C)、SiO 高温下反应,生成白磷(P )和另一种可燃性气体,根据元
10 4 6 2 4
高温
素守恒,可燃性气体为CO,该反应的化学方程式是2Ca (PO ) O+30C+20SiO = 20CaSiO +3P +30CO↑。
10 4 6 2 3 4
18.二甲胺[(CH ) NH]、N,N-二甲基甲酰胺[HCON(CH ) ]均是用途广泛的化工原料。请回答:
3 2 3 2
(1)用氨和甲醇在闭容器中合成二甲胺,反应方程式如下:
Ⅰ.NH (g)+CH OH(g)⇌CH NH (g)+H O(g)
3 3 3 2 2
Ⅱ.CH NH (g)+CH OH(g)⇌(CH ) NH(g)+H O(g)
3 2 3 3 2 2
Ⅲ.(CH ) NH(g)+CH OH(g)⇌(CH ) N(g)+H O(g)
3 2 3 3 3 2
可改变甲醇平衡转化率的因素是_______。
A.温度 B.投料比[n(NH ):n(CH OH)] C.压强 D.催化剂
3 3
(2)25℃下,(CH ) NH·H O的电离常数为Kb,-lgK =3.2,则1mol/L[(CH ) NH ] +Cl-水溶液的pH= 。
3 2 2 b 3 2 2
(3)在[(CH ) NH ] +Cl-的有机溶液中电化学还原CO 制备HCON(CH ) 阴极上生成HCON(CH ) 的电极反应方程式
3 2 2 2 3 2 3 2
是 。
(4)上述电化学方法产率不高,工业中常用如下反应生产HCON(CH ) :(CH ) NH(g)+CO(g)=HCON(CH ) (l)。
3 2 3 2 3 2
某条件下反应自发且熵减,则反应在该条件下ΔH 0(填“>”、“<”或“=”)。
(5)有研究采用CO 、H 和(CH ) NH催化反应制备HCON(CH ) 。在恒温密闭容器中,投料比
2 2 3 2 3 2
n(CO ):n(H ):n[(CH ) NH]=20:15:1,催化剂M足量。反应方程式如下:
2 2 3 2
催化剂
Ⅳ.CO (g)+H (g) HCOOH(g)
2 2
碱性物质
V.HCOOH(g)+(CH ) NH(g)=HCON(CH ) (g)+H O(g)
3 2 3 2 2
HCOOH、(CH ) NH、HCON(CH ) 三种物质的物质的量百分比随反应时间变化如图所示。
3 2 3 2
(例:HCOOH的物质的量百分比= n(HCOOH) ×100%)
n(HCOOH)+n[(CH3 ) 2NH]+n[HCON(CH3 )
2
]
①请解释HCOOH的物质的量百分比随反应时间变化的原因(不考虑催化剂M活性降低或失活) 。
②若用SiH 代替H 作为氢源与CO 反应生成HCOOH,可以降低反应所需温度。请从化学键角度解释原因 。
4 2 2
【答案】(1)AB
(2)5.4
(3)CO +2e-+2[(CH ) NH ] += HCON(CH ) +(CH ) NH+H O
2 3 2 2 3 2 3 2 2
(4)<
(5) t时刻之前反应Ⅳ的速率比反应Ⅴ的快,t时刻之后由于浓度的影响导致反应Ⅳ的速率比反应Ⅴ的慢 用H 作氢源需要断裂H-H键,用SiH 作氢源需要断裂Si-H键,由于Si原子半径大于H,Si-H的键能比H-H小,所
2 4
以用SiH 代替H 作为氢源与CO 反应生成HCOOH,可以降低反应所需温度
4 2 2
【解析】(1)A.已知化学反应必然有热效应,故改变温度化学平衡一定能够发生改变,即改变温度一定能够改变
甲醇的平衡转化率,A正确;
B.增大投料比[n(NH ):n(CH OH)] 将增大CH OH的转化率,相反减小投料比[n(NH ):n(CH OH)],将减小CH OH
3 3 3 3 3 3
的平衡转化率,B正确;
C.由题干方程式可知,反应前后气体的体积不变,故改变压强不能使上述化学平衡发生移动,即不能改变CH OH
3
的平衡转化率,C错误;
D.催化剂只能同等幅度的改变正逆化学反应速率,故不能使平衡发生移动,即不能改变CH OH的平衡转化率,D
3
错误;
故答案为:AB;
(2)25℃下,(CH ) NH·H O的电离常数为K ,-lgK =3.2,即K = c[(CH3)2NH 2 +]c(OH-) =10-3.2,则[(CH ) NH ]
3 2 2 b b b 3 2 2
c[(CH3)2NH•H2O]
++H O⇌(CH ) NH·H O+H+的水解平衡常数为:K = Kw= 10−14 =10-10.8,1mol/L[(CH ) NH ] +Cl-水溶液中
2 3 2 2 h Kb 10−3.2 3 2 2
K =
c[(CH3)2NH•H2O]c(H+)
=
c2(H+)
=10-10.8,故c(H+)=√10−10.8=10-5.4,故其pH=-lgc(H+)=-lg10-5.4=5.4,故答案为:5.4;
h c[(CH3)2NH
2
+] c[(CH3)2NH
2
+]
(3)已知电解池中阴极发生还原反应,故在[(CH ) NH ] +Cl-的有机溶液中电化学还原CO 制备HCON(CH ) 阴极
3 2 2 2 3 2
上生成HCON(CH ) 的电极反应方程式是:CO +2e-+2[(CH ) NH ] += HCON(CH ) +(CH ) NH+H O,故答案为:
3 2 2 3 2 2 3 2 3 2 2
CO +2e-+2[(CH ) NH ] += HCON(CH ) +(CH ) NH+H O;
2 3 2 2 3 2 3 2 2
(4)反应生产HCON(CH ) 的反应方程式(CH ) NH(g)+CO(g)=HCON(CH ) (l)是一个某条件下反应自发且熵减,
3 2 3 2 3 2
根据自由能变ΔG=ΔH-TΔS<0时反应自发可知,则反应在该条件下ΔH<0,故答案为:<;
(5)①由题干图示信息可知,t时刻之前HCOOH的物质的量百分比增大速率比HCON(CH ) 的增大速率,而t时
3 2
刻之后HCOOH逐渐减小至不变,HCON(CH ) 继续增大,故t时刻之前反应Ⅳ的速率比反应Ⅴ的快,t时刻之后由
3 2
于浓度的影响导致反应Ⅳ的速率比反应Ⅴ的慢,故答案为:t时刻之前反应Ⅳ的速率比反应Ⅴ的快,t时刻之后由于
浓度的影响导致反应Ⅳ的速率比反应Ⅴ的慢;
②用H 作氢源需要断裂H-H键,用SiH 作氢源需要断裂Si-H键,由于Si原子半径大于H,Si-H的键能比H-H
2 4
小,所以用SiH 代替H 作为氢源与CO 反应生成HCOOH,可以降低反应所需温度,故答案为:用H 作氢原需要
4 2 2 2
断裂H-H键,用SiH 作氢源需要断裂Si-H键,由于Si原子半径大于H,Si-H的键能比H-H小,所以用SiH 代替
4 4
H 作为氢源与CO 反应生成HCOOH,可以降低反应所需温度。
2 2
19.某研究小组探究AlCl 催化氯苯与氯化亚砜(SOCl )转化为化合物Z( )的反应。实验
3 2
流程为:
已知:
①实验在通风橱内进行。
②SOCl 遇水即放出SO 和HCl;AlCl 易升华。
2 2 3
③氯苯溶于乙醚,难溶于水;Z易溶于乙醚,难溶于水;乙醚不易溶于水。
请回答:
(1)在无水气氛中提纯少量AlCl 的简易升华装置如图所示,此处漏斗的作用是 。
3(2)写出下图中干燥管内可用的酸性固体干燥剂 (填1种)。
(3)步骤Ⅰ,下列说法正确的是_______。
A.氯苯试剂可能含有水,在使用前应作除水处理
B.三颈烧瓶置于冰水浴中,是为了控制反应温度
C.因实验在通风橱内进行,X处无需连接尾气吸收装置
D.反应体系中不再产生气泡时,可判定反应基本结束
(4)步骤Ⅱ,加入冰水的作用是 。
(5)步骤Ⅲ,从混合物M 中得到Z粗产物的所有操作如下,请排序 (填序号)。
2
①减压蒸馏 ②用乙醚萃取、分液 ③过滤 ④再次萃取、分液,合并有机相 ⑤加入无水Na SO 干燥剂吸水
2 4
(6) AlCl 可促进氯苯与SOCl 反应中S-Cl键的断裂,原因是 。
3 2
【答案】(1)AlCl 蒸汽遇冷的漏斗内壁凝华为AlCl 固体,收集AlCl
3 3 3
(2)P O 、硅胶
2 5
(3)ABD
(4)除去混合物中的SOCl 、AlCl ,实现有机相与无机相的分离,同时降低反应的速率
2 3
(5)②④⑤③①
(6)AlCl 易与Cl-形成络合物[AlCl ]-,促使SOCl 反应中S-Cl键的断裂
3 4 2
【解析】(1)已知AlCl 易升华,即受热之后变为蒸汽,遇冷之后又凝华为固体,故在无水气氛中提纯少量AlCl
3 3
的简易升华装置中漏斗的作用是:AlCl 蒸汽遇冷的漏斗内壁凝华为AlCl 固体,收集AlCl ,故答案为:AlCl 蒸汽
3 3 3 3
遇冷的漏斗内壁凝华为AlCl 固体,收集AlCl ;
3 3
(2)酸性干燥剂一般用于干燥酸性或中性气体,常见的酸性固体干燥剂有五氧化二磷或硅胶等,它可以吸收水分,
此处干燥剂是为了防止空气中水蒸气进入,可使用P O 、硅胶,故答案为:P O 、硅胶;
2 5 2 5
(3)A.由题干信息可知,SOCl 遇水即放出SO 和HCl,氯苯试剂可能含有水,故在使用前应作除水处理,A正
2 2
确;
B.由题干信息可知,AlCl 易升华,故三颈烧瓶置于冰水浴中,是为了控制反应温度,B正确;
3
C.由(2)题干信息可知,X处装入干燥剂起到干燥作用,而未能吸收尾气,故因实验在通风橱内进行,X处仍需连
接尾气吸收装置以增加实验的安全性和环保性,C错误;
D.已知氯苯和SOCl 在AlCl 催化作用下生成Z和HCl,即反应过程中能够产生难溶于有机物的HCl气泡,则可
2 3
知反应体系中不再产生气泡时,可判定反应基本结束,D正确;
故选:ABD;
(4)步骤Ⅰ所得M1中含有Z、氯苯和SOCl 、AlCl 等,结合题干信息可知,SOCl 遇水即放出SO 和HCl,且AlCl
2 3 2 2 3
易溶于水而难溶于有机物,故步骤Ⅱ中加入冰水的作用是除去混合物中的SOCl 、AlCl ,同时冰水可以降低反应速
2 3
率;故答案为:除去混合物中的SOCl 、AlCl ,实现有机相与无机相的分离,同时降低反应的速率;
2 3
(5)步骤Ⅱ得到的混合物M2中含有Z、氯苯,结合题干信息:氯苯溶于乙醚,难溶于水;Z易溶于乙醚,难溶于
水;乙醚不易溶于水,步骤Ⅲ从混合物M 中得到Z粗产物的所有操作为:用乙醚萃取、分液,再次萃取、分液,
2合并有机相,加入无水Na SO 干燥剂吸水,过滤出Na SO 晶体,即得到氯苯和Z的混合,在进行减压蒸馏,故答
2 4 2 4
案为:②④⑤③①;
(6)已知AlCl 易与Cl-形成络合物[AlCl ]-,故AlCl 可促进氯苯与SOCl 反应中S-Cl健的断裂,故答案为:AlCl
3 4 3 2 3
易与Cl-形成络合物[AlCl ]-,促使SOCl 反应中S-Cl键的断裂。
4 2
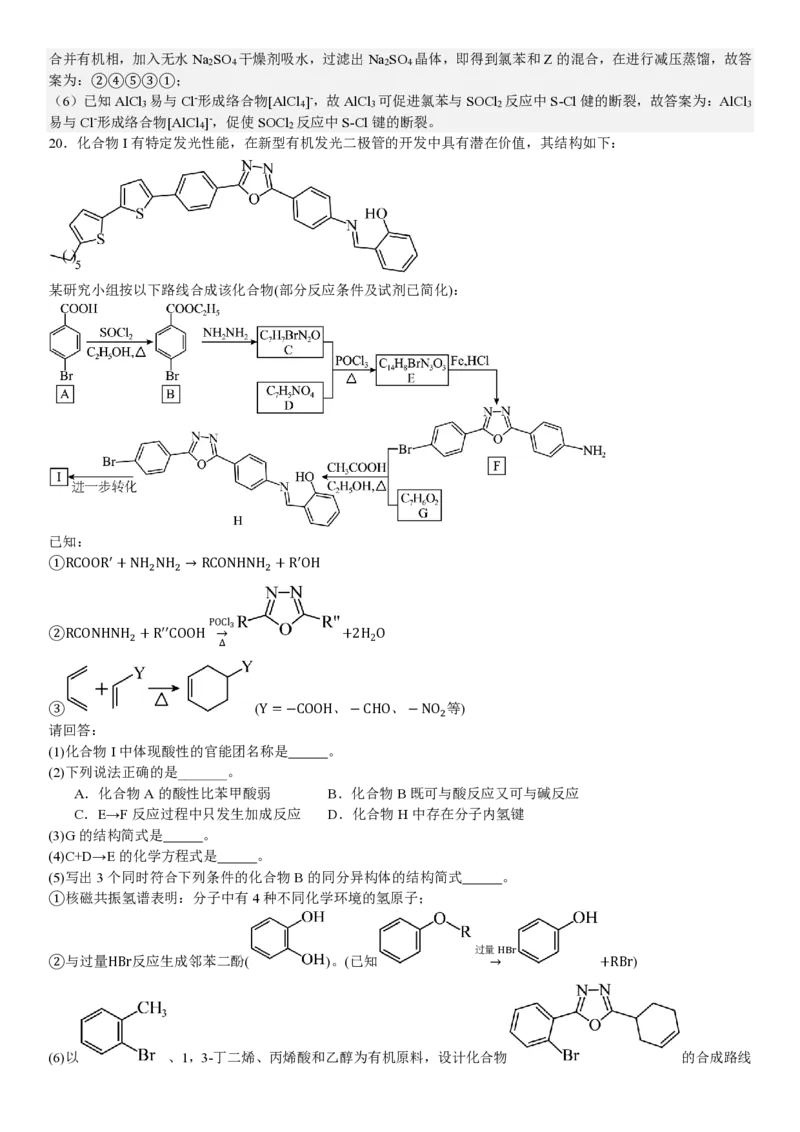
20.化合物I有特定发光性能,在新型有机发光二极管的开发中具有潜在价值,其结构如下:
某研究小组按以下路线合成该化合物(部分反应条件及试剂已简化):
已知:
①RCOOR′+NH NH →RCONHNH +R′OH
2 2 2
②RCONHNH +R′′COOH
PO
→
Cl3
+2H O
2 2
Δ
③ (Y=−COOH、−CHO、−NO 等)
2
请回答:
(1)化合物I中体现酸性的官能团名称是 。
(2)下列说法正确的是_______。
A.化合物A的酸性比苯甲酸弱 B.化合物B既可与酸反应又可与碱反应
C.E→F反应过程中只发生加成反应 D.化合物H中存在分子内氢键
(3)G的结构简式是 。
(4)C+D→E的化学方程式是 。
(5)写出3个同时符合下列条件的化合物B的同分异构体的结构简式 。
①核磁共振氢谱表明:分子中有4种不同化学环境的氢原子;
过量HBr
②与过量HBr反应生成邻苯二酚( )。(已知 → +RBr)
(6)以 、1,3-丁二烯、丙烯酸和乙醇为有机原料,设计化合物 的合成路线(用流程图表示,无机试剂任选) 。
【答案】(1)羟基
(2)BD
(3)
POCl3
(4) + → +2H O
2
Δ
(5) 、 、
(6) ;
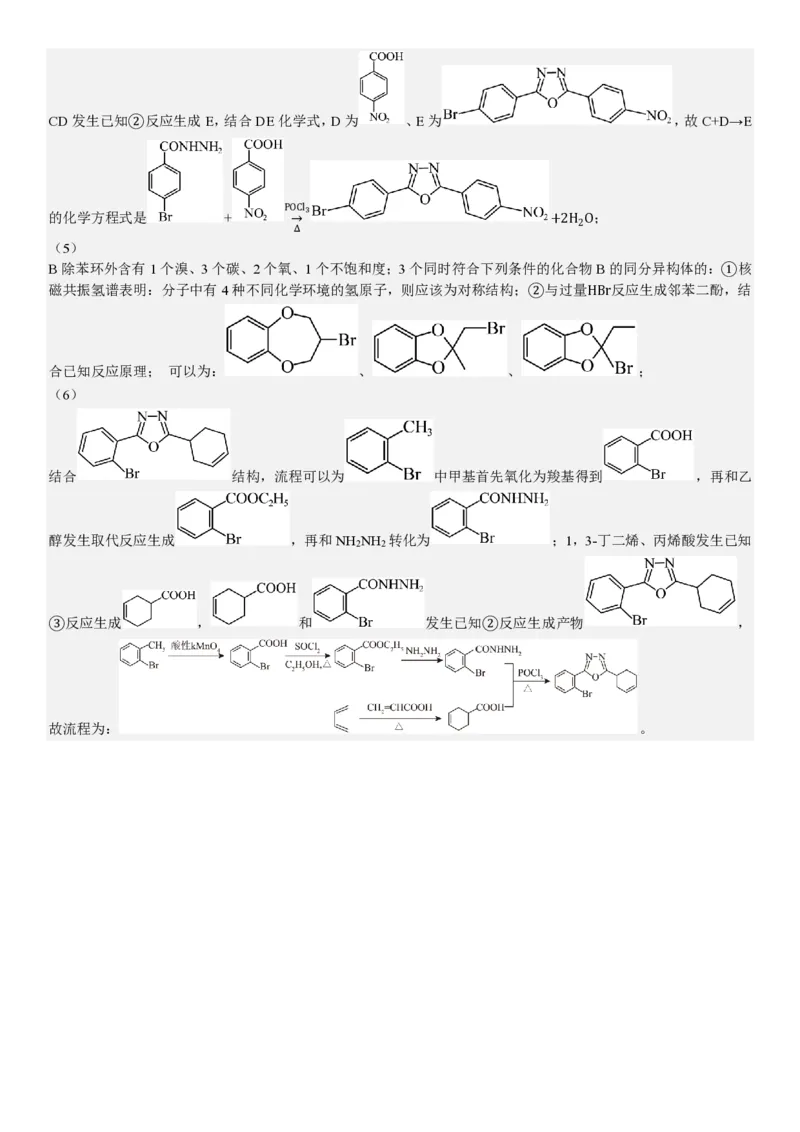
【分析】
由流程可知,A发生取代反应生成B,B发生已知反应原理生成C,结合C化学式,C为 ,CD发生已知
反应生成E,结合DE化学式,D为 、E为 ,E中硝基还原为氨基得到F,FG生
成H,结合G化学式,G为 ,H进一步转化为I;
【解析】(1)由I结构可知,I中体现酸性的官能团名称是酚羟基;
(2)A.溴原子在苯环上具有吸电子效应使得A中羧基更容易电离出氢离子,使其酸性增强,故化合物A中的酸
性比苯甲酸强,错误;
B.化合物B中含有酯基,可以发生酸性水解也可以发生碱性水解,故既可与酸反应又可与碱反应,正确;
C.E中硝基还原为氨基得到F,E→F反应过程中发生加成反应,同时铁和稀盐酸也会发生置换反应,错误;
D.当氢原子连接在电负性大且原子半径小的原子(例如氟、氧、氮)上时,可以形成氢键;化合物H中酚羟基和
临近氮能形成分子内氢键,正确;
故选BD;
(3)
由分析,G为: ;
(4)CD发生已知②反应生成E,结合DE化学式,D为 、E为 ,故C+D→E
POCl3
的化学方程式是 + → +2H O;
2
Δ
(5)
B除苯环外含有1个溴、3个碳、2个氧、1个不饱和度;3个同时符合下列条件的化合物B的同分异构体的:①核
磁共振氢谱表明:分子中有4种不同化学环境的氢原子,则应该为对称结构;②与过量HBr反应生成邻苯二酚,结
合已知反应原理; 可以为: 、 、 ;
(6)
结合 结构,流程可以为 中甲基首先氧化为羧基得到 ,再和乙
醇发生取代反应生成 ,再和NH NH 转化为 ;1,3-丁二烯、丙烯酸发生已知
2 2
③反应生成 , 和 发生已知②反应生成产物 ,
故流程为: 。