文档内容
湖南省株洲市 2021 年中考化学试题
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 S-32 Cl-35.5
Ca-40 Fe-56 Cu-64 Zn-65
一、选择题(本题共20小题,每小题2分,共40分。每小题只有一个选项符合题意)
1. 下列物质中属于化合物的是
A. 硫酸溶液 B. 冰 C. 水银 D. 氧气
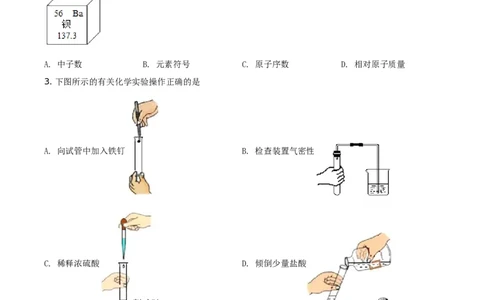
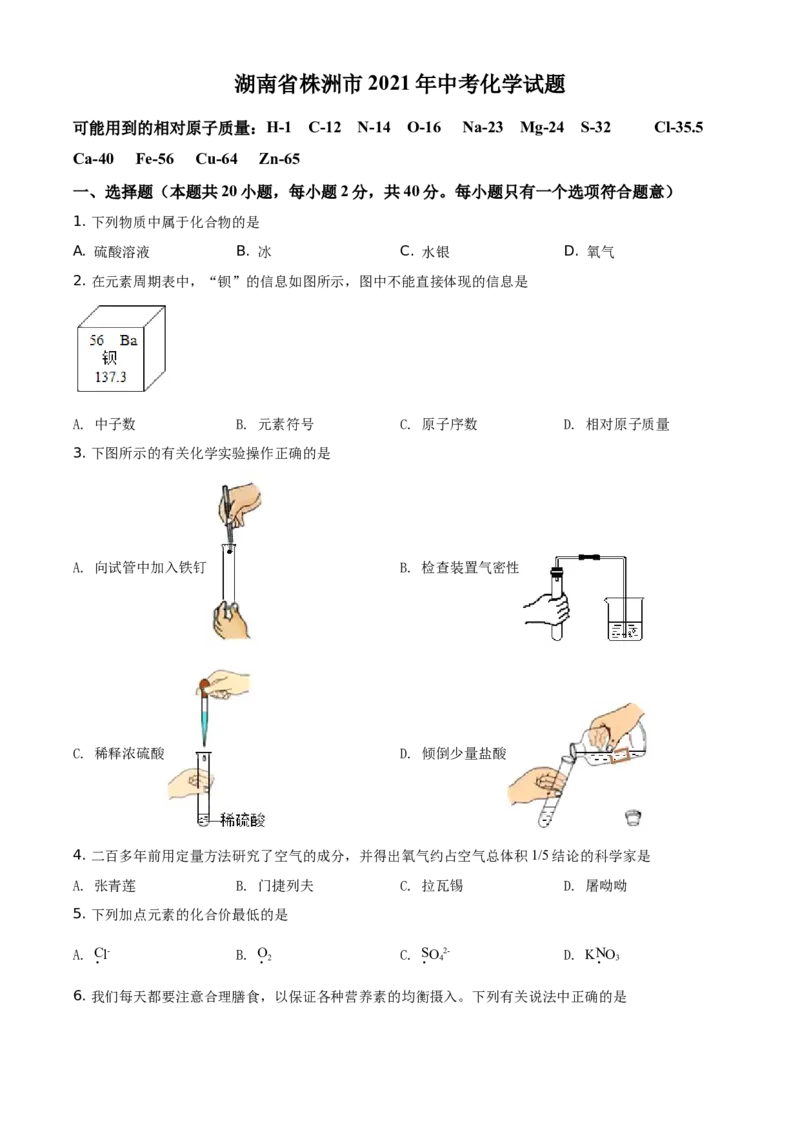
2. 在元素周期表中,“钡”的信息如图所示,图中不能直接体现的信息是
A. 中子数 B. 元素符号 C. 原子序数 D. 相对原子质量
3. 下图所示的有关化学实验操作正确的是
A. 向试管中加入铁钉 B. 检查装置气密性
C. 稀释浓硫酸 D. 倾倒少量盐酸
4. 二百多年前用定量方法研究了空气的成分,并得出氧气约占空气总体积1/5结论的科学家是
A. 张青莲 B. 门捷列夫 C. 拉瓦锡 D. 屠呦呦
5. 下列加点元素的化合价最低的是
A. Cl- B. O C. SO2- D. KNO
2 4 3
6. 我们每天都要注意合理膳食,以保证各种营养素的均衡摄入。下列有关说法中正确的是A. 缺乏维生素A会引起坏血病
B. 糖类是人类食物的重要成分,我们应多吃糖果来补充糖类
C. 纤维素不能被人体吸收,因此不必食用蔬菜、水果等富含纤维素的食物
D. 油脂是重要的营养物质,而人体摄入过多的油脂后,容易引发肥胖和心脑血管疾病
7. 下列仪器可以直接加热的是( )
A. 量筒 B. 试管 C. 烧杯 D. 集气瓶
8. 下列反应中属于化合反应的是
A.
B.
C.
D.
9. 水是一切生命体生存所必需的物质。下列处理水的方式中,涉及化学变化的是
A. 实验室用蒸馏法获得蒸馏水
B. 利用活性炭吸附水中的杂质
C. 浑浊的河水过滤后可得到清澈的水
D. 自来水厂净水过程中,用药剂消毒后才能供给用户
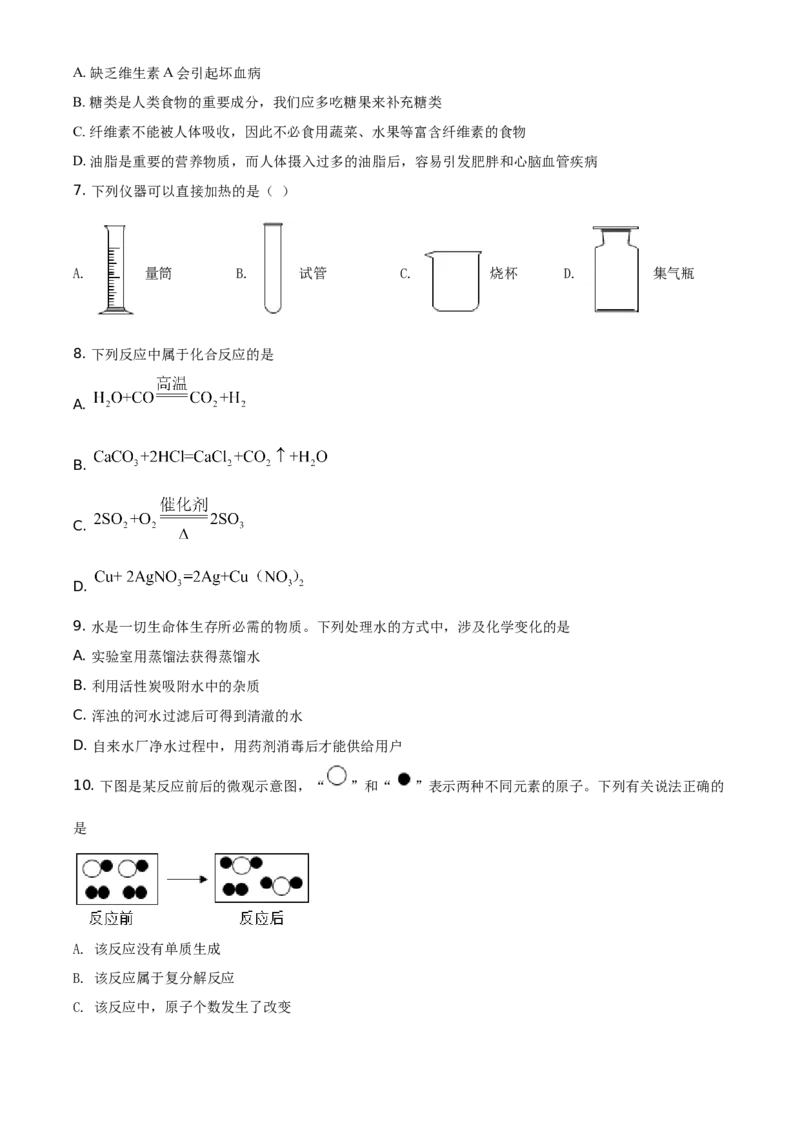
10. 下图是某反应前后的微观示意图,“ ”和“ ”表示两种不同元素的原子。下列有关说法正确的
是
A. 该反应没有单质生成
B. 该反应属于复分解反应
C. 该反应中,原子个数发生了改变D. 参加反应的两种分子( 和 )的个数比为1:1
11. 下列说法中不正确的是
A. 有机化合物中都含有碳元素
B. 生活中通过煮沸可以降低水的硬度
C. 玻璃钢是复合材料,可以用于建筑材料、车船体材料等
D. 超市不免费提供一次性塑料袋,主要是为了降低经营成本
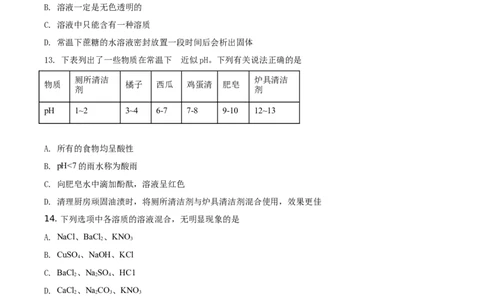
12. 下列关于溶液的说法中正确的是
A. 溶液一定是混合物
B. 溶液一定是无色透明的
C. 溶液中只能含有一种溶质
D. 常温下蔗糖的水溶液密封放置一段时间后会析出固体
13. 下表列出了一些物质在常温下 的近似pH。下列有关说法正确的是
厕所清洁 炉具清洁
物质 橘子 西瓜 鸡蛋清 肥皂
剂 剂
pH 1~2 3~4 6-7 7-8 9-10 12~13
A. 所有的食物均呈酸性
B. pH<7的雨水称为酸雨
C. 向肥皂水中滴加酚酞,溶液呈红色
D. 清理厨房顽固油渍时,将厕所清洁剂与炉具清洁剂混合使用,效果更佳
14. 下列选项中各溶质的溶液混合,无明显现象的是
A. NaCl、BaCl 、KNO
2 3
B. CuSO 、NaOH、KCl
4
C. BaCl 、NaSO 、HC1
2 2 4
D. CaCl 、NaCO、KNO
2 2 3 3
15. 经过实验探究,人们总结出了金属活动性顺序规律,下列有关说法正确的是
A. 金属铝比铁更耐腐蚀,是因为铁更活泼
B. 工业上可以利用单质铁回收硫酸锌溶液中的金属锌
C. 铜、银单质分别与稀盐酸混合,铜置换出氢气更快
D. 金属活动性顺序可作为金属能否在溶液中发生置换反应的一种判断依据
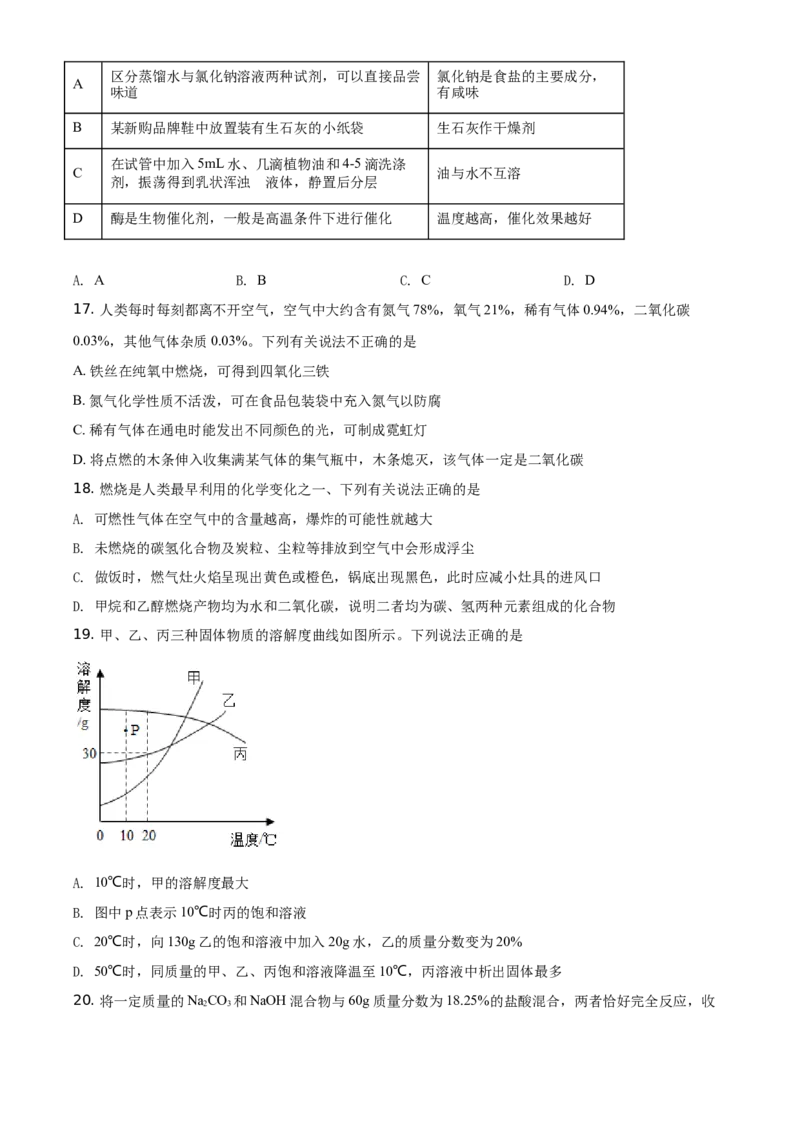
16. 下列实验操作或用途与分析均正确的是
操作或用途 分析区分蒸馏水与氯化钠溶液两种试剂,可以直接品尝 氯化钠是食盐的主要成分,
A
味道 有咸味
B 某新购品牌鞋中放置装有生石灰的小纸袋 生石灰作干燥剂
在试管中加入5mL水、几滴植物油和4-5滴洗涤
C 油与水不互溶
剂,振荡得到乳状浑浊 的液体,静置后分层
D 酶是生物催化剂,一般是高温条件下进行催化 温度越高,催化效果越好
A. A B. B C. C D. D
17. 人类每时每刻都离不开空气,空气中大约含有氮气78%,氧气21%,稀有气体0.94%,二氧化碳
0.03%,其他气体杂质0.03%。下列有关说法不正确的是
A. 铁丝在纯氧中燃烧,可得到四氧化三铁
B. 氮气化学性质不活泼,可在食品包装袋中充入氮气以防腐
C. 稀有气体在通电时能发出不同颜色的光,可制成霓虹灯
D. 将点燃的木条伸入收集满某气体的集气瓶中,木条熄灭,该气体一定是二氧化碳
18. 燃烧是人类最早利用的化学变化之一、下列有关说法正确的是
A. 可燃性气体在空气中的含量越高,爆炸的可能性就越大
B. 未燃烧的碳氢化合物及炭粒、尘粒等排放到空气中会形成浮尘
C. 做饭时,燃气灶火焰呈现出黄色或橙色,锅底出现黑色,此时应减小灶具的进风口
D. 甲烷和乙醇燃烧产物均为水和二氧化碳,说明二者均为碳、氢两种元素组成的化合物
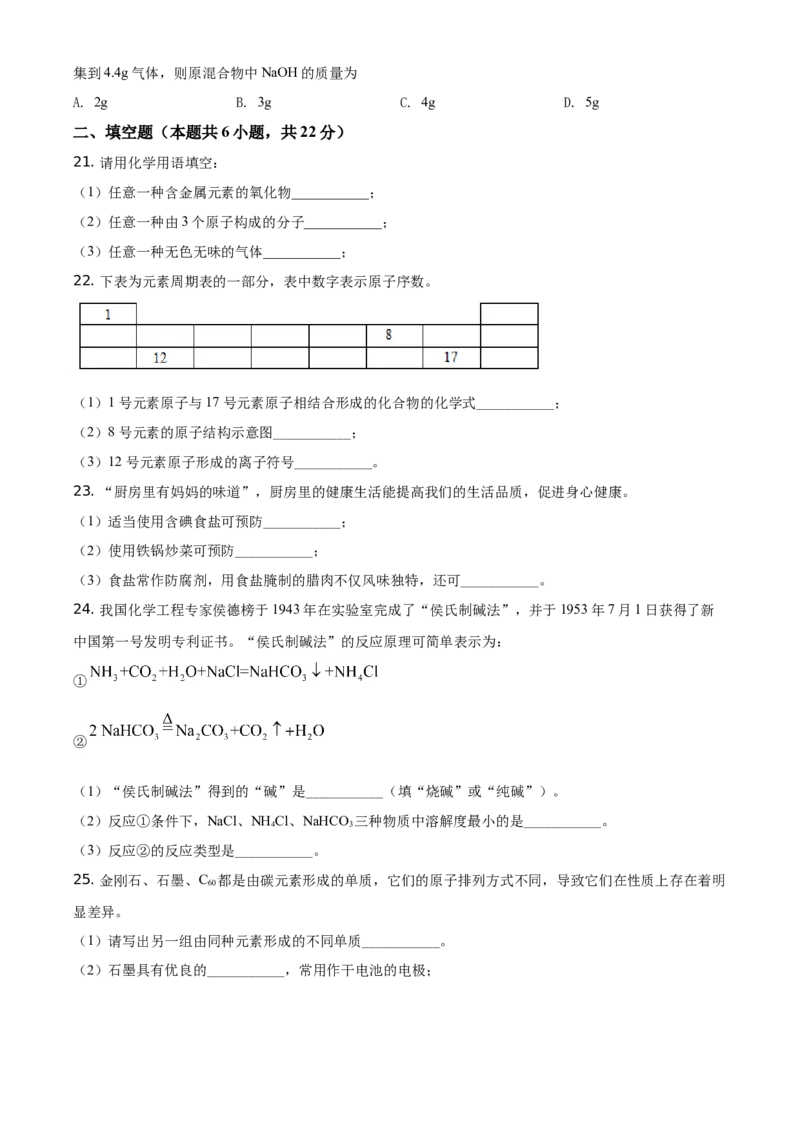
19. 甲、乙、丙三种固体物质的溶解度曲线如图所示。下列说法正确的是
A. 10℃时,甲的溶解度最大
B. 图中p点表示10℃时丙的饱和溶液
C. 20℃时,向130g乙的饱和溶液中加入20g水,乙的质量分数变为20%
D. 50℃时,同质量的甲、乙、丙饱和溶液降温至10℃,丙溶液中析出固体最多
20. 将一定质量的NaCO 和NaOH混合物与60g质量分数为18.25%的盐酸混合,两者恰好完全反应,收
2 3集到4.4g气体,则原混合物中NaOH的质量为
A. 2g B. 3g C. 4g D. 5g
二、填空题(本题共6小题,共22分)
21. 请用化学用语填空:
(1)任意一种含金属元素的氧化物___________;
(2)任意一种由3个原子构成的分子___________;
(3)任意一种无色无味的气体___________;
22. 下表为元素周期表的一部分,表中数字表示原子序数。
(1)1号元素原子与17号元素原子相结合形成的化合物的化学式___________;
(2)8号元素的原子结构示意图___________;
(3)12号元素原子形成的离子符号___________。
23. “厨房里有妈妈的味道”,厨房里的健康生活能提高我们的生活品质,促进身心健康。
(1)适当使用含碘食盐可预防___________;
(2)使用铁锅炒菜可预防___________;
(3)食盐常作防腐剂,用食盐腌制的腊肉不仅风味独特,还可___________。
24. 我国化学工程专家侯德榜于1943年在实验室完成了“侯氏制碱法”,并于1953年7月1日获得了新
中国第一号发明专利证书。“侯氏制碱法”的反应原理可简单表示为:
①
②
(1)“侯氏制碱法”得到的“碱”是___________(填“烧碱”或“纯碱”)。
(2)反应①条件下,NaCl、NH Cl、NaHCO 三种物质中溶解度最小的是___________。
4 3
(3)反应②的反应类型是___________。
25. 金刚石、石墨、C 都是由碳元素形成的单质,它们的原子排列方式不同,导致它们在性质上存在着明
60
显差异。
(1)请写出另一组由同种元素形成的不同单质___________。
(2)石墨具有优良的___________,常用作干电池的电极;(3)硅是一种良好的半导体材料。工业上制粗硅的反应为: ,该反应中SiO
2
发生___________(填“氧化”或“还原”)反应。
(4)已知反应:2Mg+CO 2___________+C,则Mg着火时___________(填“能”或“不能”)使
2
用干粉灭火器灭火。
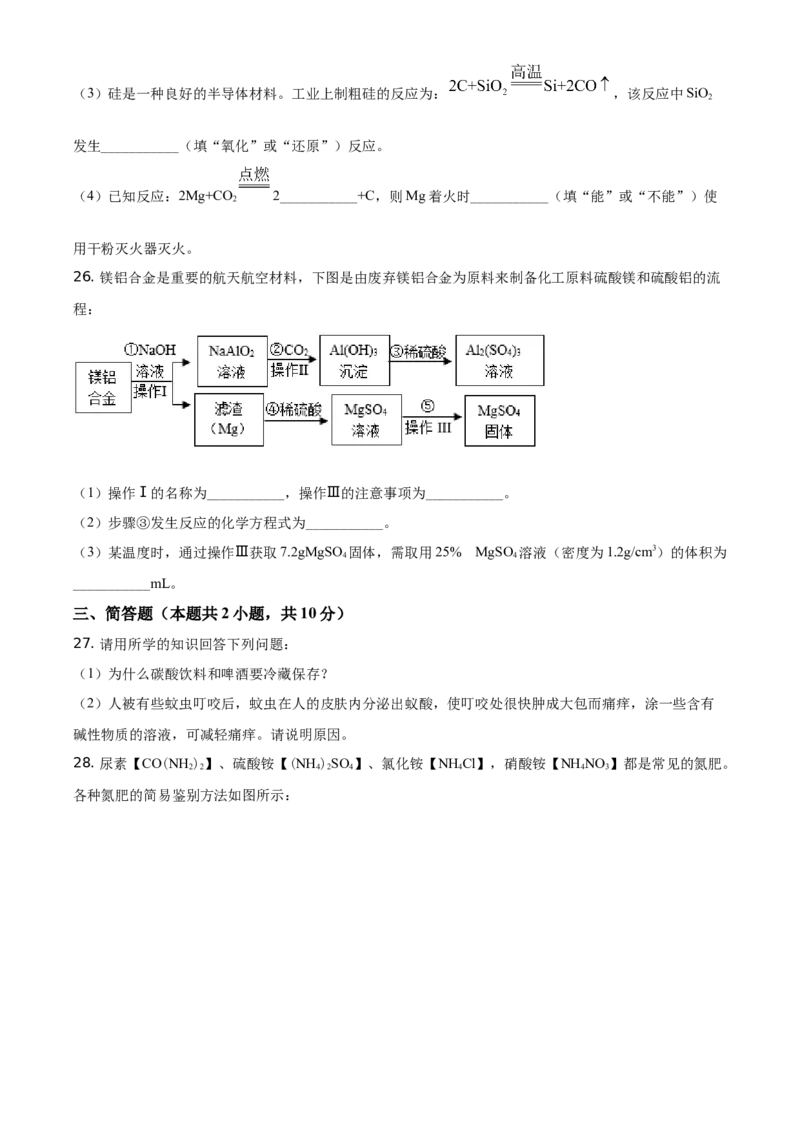
26. 镁铝合金是重要的航天航空材料,下图是由废弃镁铝合金为原料来制备化工原料硫酸镁和硫酸铝的流
程:
(1)操作Ⅰ的名称为___________,操作Ⅲ的注意事项为___________。
(2)步骤③发生反应的化学方程式为___________。
(3)某温度时,通过操作Ⅲ获取7.2gMgSO 固体,需取用25% 的MgSO 溶液(密度为1.2g/cm3)的体积为
4 4
___________mL。
三、简答题(本题共2小题,共10分)
27. 请用所学的知识回答下列问题:
(1)为什么碳酸饮料和啤酒要冷藏保存?
(2)人被有些蚊虫叮咬后,蚊虫在人的皮肤内分泌出蚁酸,使叮咬处很快肿成大包而痛痒,涂一些含有
碱性物质的溶液,可减轻痛痒。请说明原因。
28. 尿素【CO(NH )】、硫酸铵【(NH )SO 】、氯化铵【NH Cl】,硝酸铵【NH NO 】都是常见的氮肥。
2 2 4 2 4 4 4 3
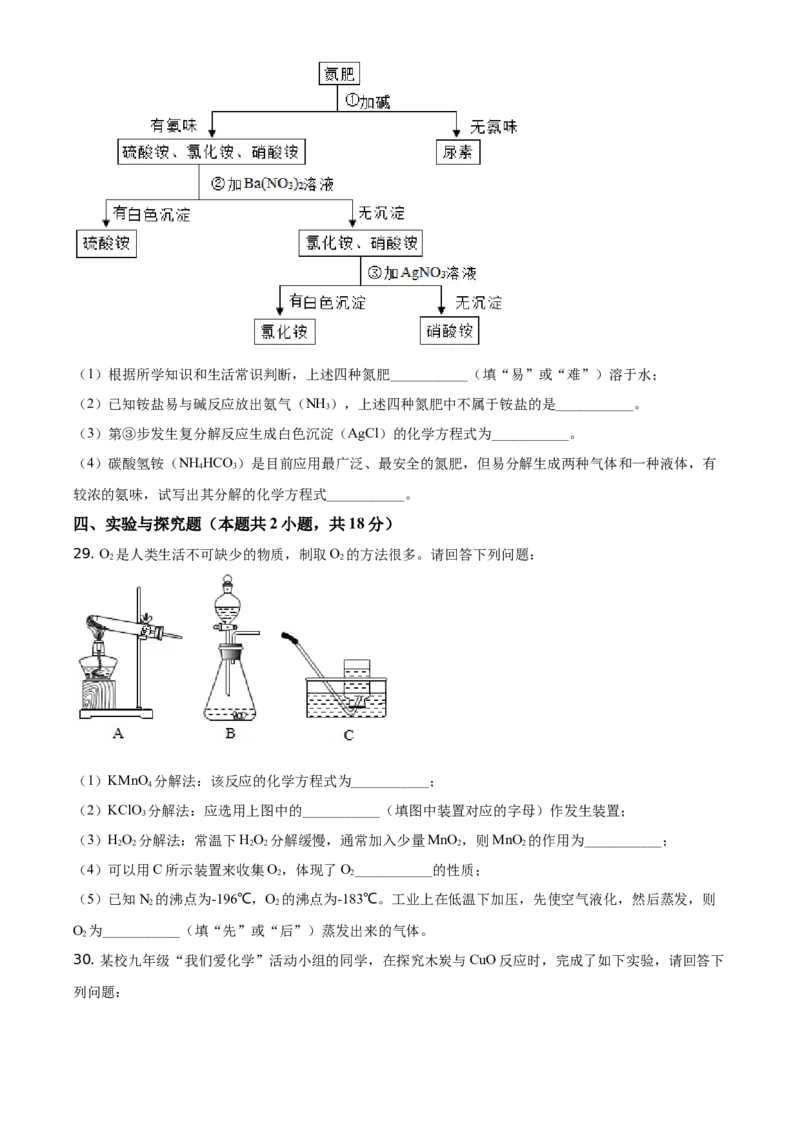
各种氮肥的简易鉴别方法如图所示:(1)根据所学知识和生活常识判断,上述四种氮肥___________(填“易”或“难”)溶于水;
(2)已知铵盐易与碱反应放出氨气(NH ),上述四种氮肥中不属于铵盐的是___________。
3
(3)第③步发生复分解反应生成白色沉淀(AgCl)的化学方程式为___________。
(4)碳酸氢铵(NH HCO )是目前应用最广泛、最安全的氮肥,但易分解生成两种气体和一种液体,有
4 3
较浓的氨味,试写出其分解的化学方程式___________。
四、实验与探究题(本题共2小题,共18分)
29. O 是人类生活不可缺少的物质,制取O 的方法很多。请回答下列问题:
2 2
(1)KMnO 分解法:该反应的化学方程式为___________;
4
(2)KClO 分解法:应选用上图中的___________(填图中装置对应的字母)作发生装置;
3
(3)HO 分解法:常温下HO 分解缓慢,通常加入少量MnO ,则MnO 的作用为___________;
2 2 2 2 2 2
(4)可以用C所示装置来收集O,体现了O___________的性质;
2 2
(5)已知N 的沸点为-196℃,O 的沸点为-183℃。工业上在低温下加压,先使空气液化,然后蒸发,则
2 2
O 为___________(填“先”或“后”)蒸发出来的气体。
2
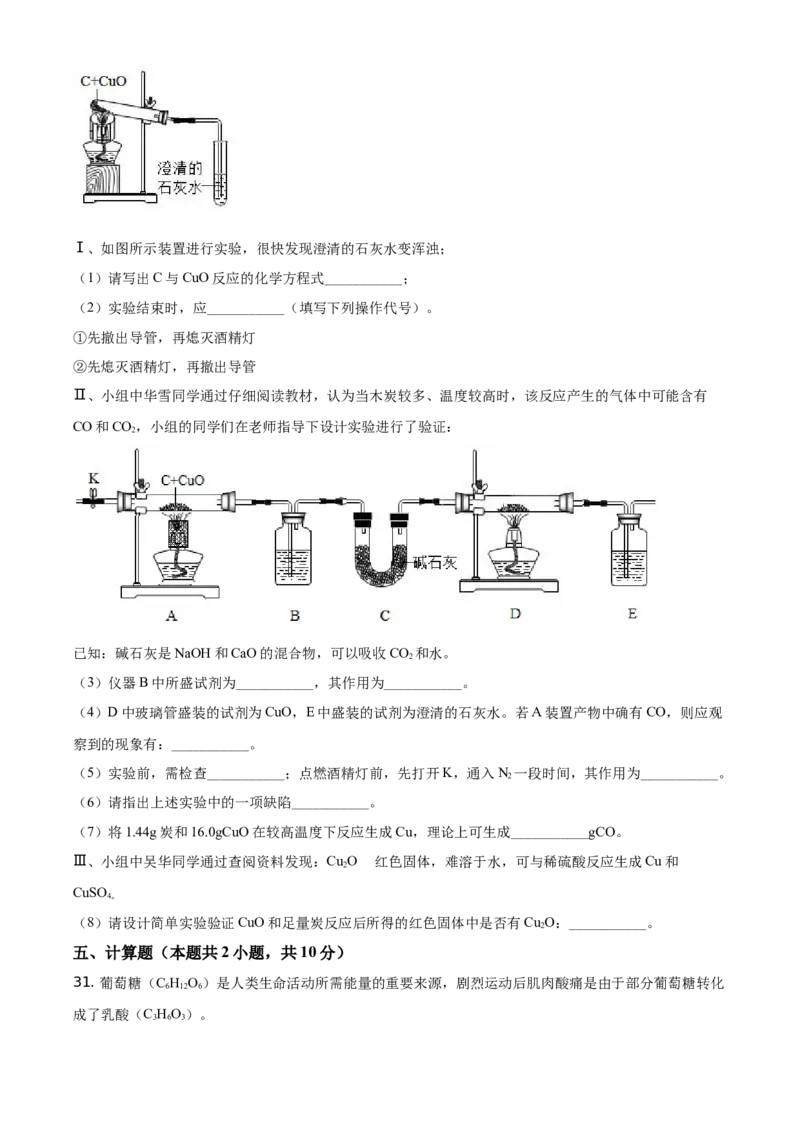
30. 某校九年级“我们爱化学”活动小组的同学,在探究木炭与CuO反应时,完成了如下实验,请回答下
列问题:Ⅰ、如图所示装置进行实验,很快发现澄清的石灰水变浑浊;
(1)请写出C与CuO反应的化学方程式___________;
(2)实验结束时,应___________(填写下列操作代号)。
①先撤出导管,再熄灭酒精灯
②先熄灭酒精灯,再撤出导管
Ⅱ、小组中华雪同学通过仔细阅读教材,认为当木炭较多、温度较高时,该反应产生的气体中可能含有
CO和CO,小组的同学们在老师指导下设计实验进行了验证:
2
已知:碱石灰是NaOH和CaO的混合物,可以吸收CO 和水。
2
(3)仪器B中所盛试剂为___________,其作用为___________。
(4)D中玻璃管盛装的试剂为CuO,E中盛装的试剂为澄清的石灰水。若A装置产物中确有CO,则应观
察到的现象有:___________。
(5)实验前,需检查___________;点燃酒精灯前,先打开K,通入N 一段时间,其作用为___________。
2
(6)请指出上述实验中的一项缺陷___________。
(7)将1.44g炭和16.0gCuO在较高温度下反应生成Cu,理论上可生成___________gCO。
Ⅲ、小组中吴华同学通过查阅资料发现:Cu O 为红色固体,难溶于水,可与稀硫酸反应生成Cu和
2
CuSO
4。
(8)请设计简单实验验证CuO和足量炭反应后所得的红色固体中是否有Cu O:___________。
2
五、计算题(本题共2小题,共10分)
31. 葡萄糖(C H O)是人类生命活动所需能量的重要来源,剧烈运动后肌肉酸痛是由于部分葡萄糖转化
6 12 6
成了乳酸(C HO)。
3 6 3(1)C H O 的相对分子质量为___________。
6 12 6
(2)葡萄糖中碳元素的质量分数___________乳酸中碳元素的质量分数(填“>”、“<”或“=”)。
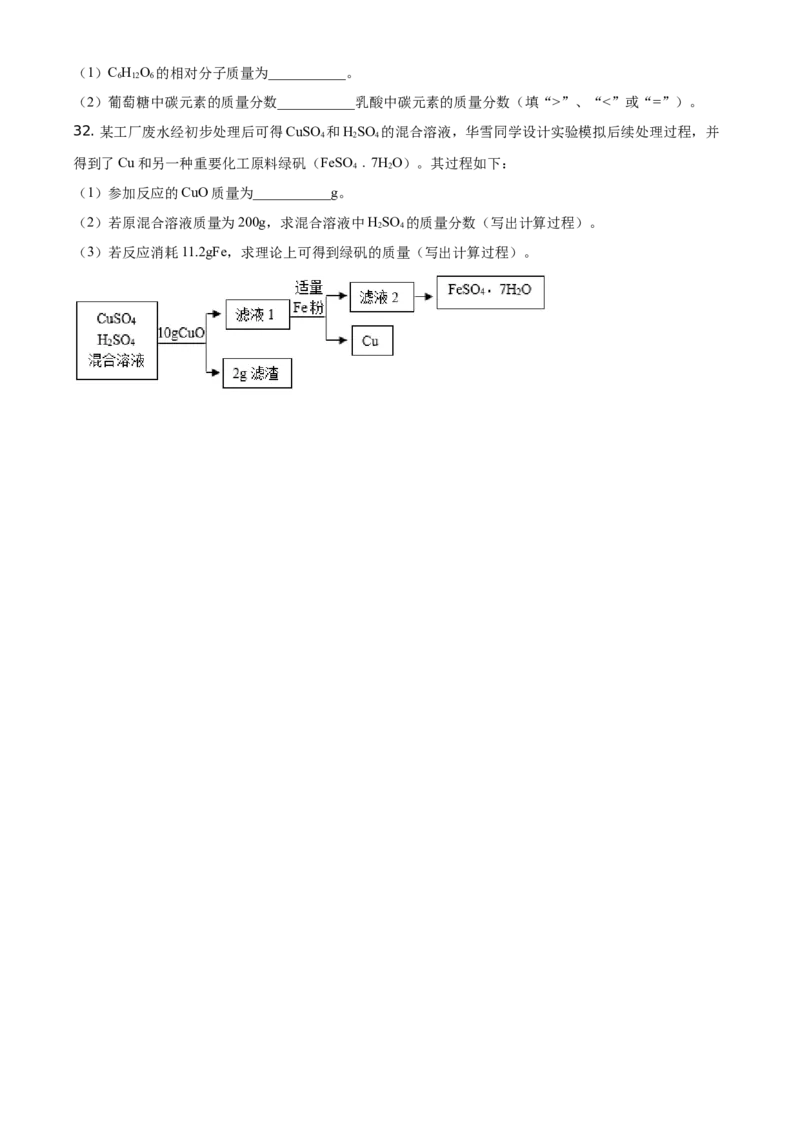
32. 某工厂废水经初步处理后可得CuSO 和HSO 的混合溶液,华雪同学设计实验模拟后续处理过程,并
4 2 4
得到了Cu和另一种重要化工原料绿矾(FeSO ﹒7HO)。其过程如下:
4 2
(1)参加反应的CuO质量为___________g。
(2)若原混合溶液质量为200g,求混合溶液中HSO 的质量分数(写出计算过程)。
2 4
(3)若反应消耗11.2gFe,求理论上可得到绿矾的质量(写出计算过程)。