文档内容
26 届高三模拟预测一
化学试卷
本试卷满分100分,考试用时75分钟
可能用到的相对原子质量:
一、单选题(本题共15题,每题3分,共45分。在每题列出的四个选项中,选出最符合题
目要求的一项。)
1.化学使环境更美好。下列说法错误的是( )
A.推广使用电动车,可减少光化学烟雾 B.燃煤时加生石灰,可减少温室气体产生
C.将CO 合成甲醇,有助于实现碳中和 D.使用可降解塑料,有利于减少白色污染
2
2.下列化学用语表述正确的是( )
A.中子数为12的氖核素: B.氯化镁的电子式:
C.甲醛分子的球棍模型: D. 的价层电子对互斥模型:
3.我国科研团队在人工合成淀粉方面取得突破性进展,通过CO、H 制得CHOH,进而合成了淀粉
2 2 3
[(C H O)]。用N 代表阿伏加德罗常数的值,下列说法正确的是( )
6 10 5 n A
A.0.2 mol CO 和H 混合气体的分子数为0.4N
2 2 A
B.通过CO 与H 制得32 g CHOH,转移电子数为4N
2 2 3 A
C.标准状况下,22.4 L CH OH中含有3N 的C—H 键
3 A
D.16.2 g淀粉[(C H O)]中含C原子数为0.6N
6 10 5 n A
4.氨氮废水是造成水体富营养化的原因之一,下图为处理氨氮废水的流程。
下列离子方程式书写错误的是( )
A.过程①:NH++OH-=NH·H O
4 3 2
B.过程②总反应式:3Cl +2NH·H O=6Cl-+N +2H O+6H+
2 3 2 2 2
C.过程③:Cl +SO2-+H O=2Cl-+SO2-+2H+
2 3 2 4
D.Cl 溶于水:Cl +H O Cl-+ClO-+2H+
2 2 2
5.分支酸可用于生化研究,其结构简式如图,关于分支酸的叙述不正确的是( )
A.1 mol分支酸至少可与3 mol NaOH反应
第 1 页 共 10 页
学科网(北京)股份有限公司第 1 页 共 10 页
B.该有机物可发生氧化反应和加聚反应
C.分子式为C H O
10 10 6
D.可使溴的CCl 溶液、酸性KMnO 溶液褪色
4 4
6.连二亚硫酸钠(Na SO)俗称保险粉,有强还原性,在空气中极易被氧化。用NaHSO 还原法制备保险粉
2 2 4 3
的流程如下: 下列说法错误的是( )
A.反应1说明酸性:H SO >H CO
2 3 2 3
B.反应1结束后,可用硝酸酸化的BaCl 溶液检验
2
NaHSO 是否被氧化
3
C.反应2中消耗的氧化剂和还原剂的物质的量之比为2∶1
D.反应2最好在无氧条件下进行
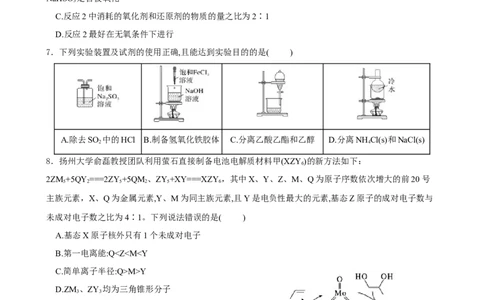
7.下列实验装置及试剂的使用正确,且能达到实验目的的是( )
A.除去SO 中的HCl B.制备氢氧化铁胶体 C.分离乙酸乙酯和乙醇 D.分离NH Cl(s)和NaCl(s)
2 4
8.扬州大学俞磊教授团队利用萤石直接制备电池电解质材料甲(XZY )的新方法如下:
6
2ZM +5QY===2ZY +5QM、ZY+XY===XZY ,其中X、Y、Z、M、Q为原子序数依次增大的前20号
5 2 5 2 5 6
主族元素,X、Q为金属元素,Y、M为同主族元素,且Y是电负性最大的元素,基态Z原子的成对电子数与
未成对电子数之比为4∶1。下列说法错误的是( )
A.基态X原子核外只有1个未成对电子
B.第一电离能:QM>Y
D.ZM 、ZY 均为三角锥形分子
3 3
9.1,2-丙二醇可用作制备不饱和聚酯树脂的原料,在化妆
品、牙膏和香皂中可与甘油配合用202作润湿剂。已知
1,2-丙二醇脱氧脱水反应的催化循环机理如图所示。下列
说法不正确的是( )
A.X的化学式为HO
2
B.催化过程中金属元素Mo成键数发生改变
C.MoO 是该反应的催化剂,可通过降低反应的活化能来提高化学反应速率
3
第 2 页 共 10 页
学科网(北京)股份有限公司第 2 页 共 10 页
D.整个反应的化学方程式为 + +CH CHO
3
10.利用废铝箔(主要成分为Al,含少量Mg、Fe等)制明矾[KAl(SO)·12H O]的一种工艺流程如图:
4 2 2
下列说法错误的是( )
A.该工艺步骤①与步骤②顺序互换会更节约生产成本
B.②中发生的反应有:Al(OH) +NaOH=Na[Al(OH) ]
3 4
C.③中稀HSO 酸化的目的是将Al(OH) 转化成Al3+
2 4 3
D.由④可知,室温下明矾的溶解度小于Al (SO ) 和KSO 的溶解度
2 4 3 2 4
11.三甲胺N(CH ) 是重要的化工原料。我国科学家利用(CH)NCHO(简称DMF)在铜催化作用下转化得
3 3 3 2
到N(CH ),下图是计算机模拟单个DMF分子在铜催化剂表面的反应历程如图所示(*表示物质吸附在铜
3 3
催化剂上),下列说法错误的是( )
A.该反应为放热反应,降温可提高DMF的平衡转化率
B.该历程包含6个基元反应,最大能垒(活化能)为1.19 eV
C.设法提高N(CH )+OH*+H*===N(CH )(g)+HO(g)的速率可以提高总反应速率
3 3 3 3 2
D.若1 mol DMF完全转化为三甲胺,则会吸收1.02 eV·N 的能量
A
12.下列探究方案能达到探究目的的是( )
选项 探究方案 探究目的
取少量Fe O 与足量盐酸反应后的溶液于试管中,滴加几 检验Fe O 与盐酸反应后的溶液中
A 3 4 3 4
滴K[Fe(CN) ]溶液,观察现象 含有Fe2+
3 6
第 3 页 共 10 页
学科网(北京)股份有限公司第 3 页 共 10 页
向0.1 mol·L-1 HO 溶液中滴加0.1 mol·L-1 KMnO 溶液,
B 2 2 4 探究HO 具有氧化性
观察溶液颜色变化 2 2
向蔗糖溶液中滴加稀硫酸,水浴加热,再加入新制
C 验证蔗糖发生水解
Cu(OH) 悬浊液
2
用pH试纸测定浓度均为0.1 mol·L-1的CHCOONa溶液
D 3 比较酸性:CH COOH>HClO
和NaClO溶液的pH,比较溶液pH大小 3
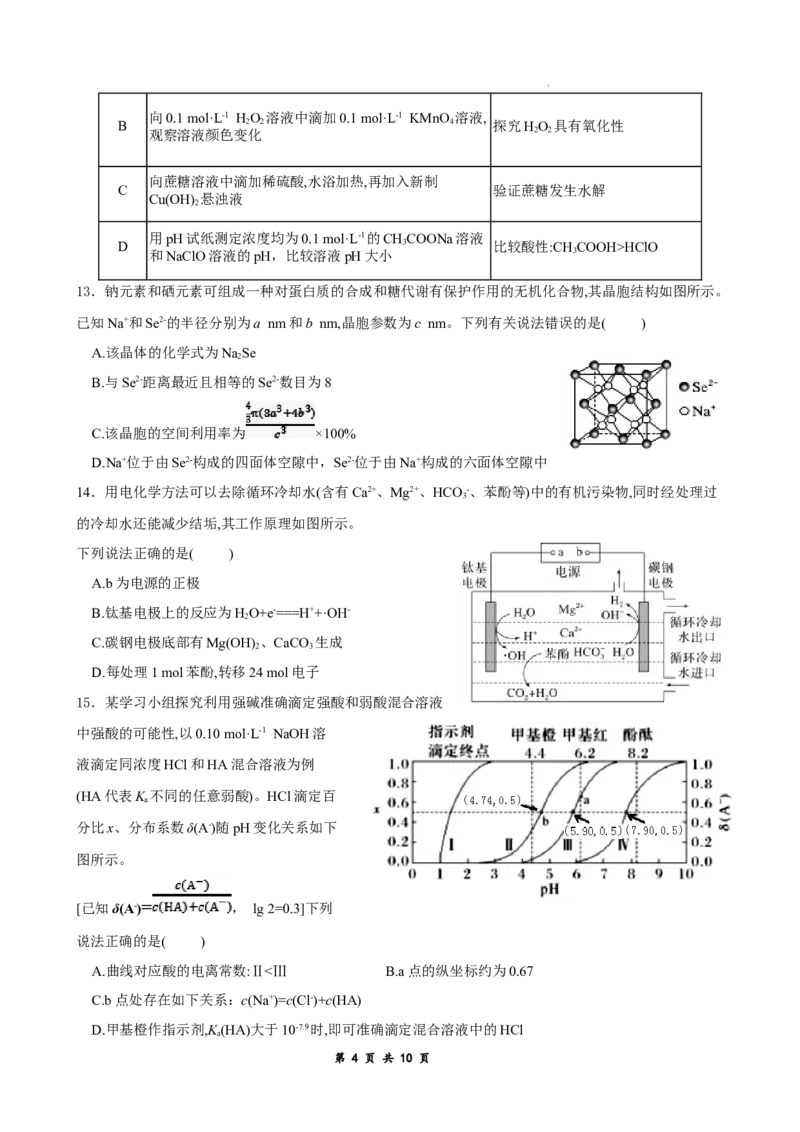
13.钠元素和硒元素可组成一种对蛋白质的合成和糖代谢有保护作用的无机化合物,其晶胞结构如图所示。
已知Na+和Se2-的半径分别为a nm和b nm,晶胞参数为c nm。下列有关说法错误的是( )
A.该晶体的化学式为NaSe
2
B.与Se2-距离最近且相等的Se2-数目为8
C.该晶胞的空间利用率为 ×100%
D.Na+位于由Se2-构成的四面体空隙中,Se2-位于由Na+构成的六面体空隙中
14.用电化学方法可以去除循环冷却水(含有Ca2+、Mg2+、HCO-、苯酚等)中的有机污染物,同时经处理过
3
的冷却水还能减少结垢,其工作原理如图所示。
下列说法正确的是( )
A.b为电源的正极
B.钛基电极上的反应为HO+e-===H++·OH-
2
C.碳钢电极底部有Mg(OH) 、CaCO 生成
2 3
D.每处理1 mol苯酚,转移24 mol电子
15.某学习小组探究利用强碱准确滴定强酸和弱酸混合溶液
中强酸的可能性,以0.10 mol·L-1 NaOH溶
液滴定同浓度HCl和HA混合溶液为例
(HA代表K 不同的任意弱酸)。HCl滴定百
a
分比x、分布系数δ(A-)随pH变化关系如下
图所示。
[已知δ(A-)= , lg 2=0.3]下列
说法正确的是( )
A.曲线对应酸的电离常数:Ⅱ<Ⅲ B.a点的纵坐标约为0.67
C.b点处存在如下关系:c(Na+)=c(Cl-)+c(HA)
D.甲基橙作指示剂,K(HA)大于10-7.9时,即可准确滴定混合溶液中的HCl
a
第 4 页 共 10 页
学科网(北京)股份有限公司第 4 页 共 10 页
二、非选择题:共55分
16.(14分)我国是金属材料生产大国,绿色生产是必由之路。一种从多金属精矿中提取Fe、
Cu、Ni等并探究新型绿色冶铁方法的工艺如下。
已知:多金属精矿中主要含有Fe、Al、Cu、Ni、O等元素。
氢氧化物
(1)“酸浸”中,提高浸取速率的措施有 (写一条)。
(2)“高压加热”时,生成 的离子方程式为:
(3)“沉铝”时,pH最高可调至 (溶液体积变化可
忽略)。已知:“滤液1”中 ,
。
(4)“选择萃取”中,镍形成如图的配合物。镍易进入有
机相的原因有_______。
A.镍与N、O形成配位键 B.配位时 被还原
C.配合物与水能形成分子间氢键 D.烷基链具有疏水性
(5) 晶体的立方晶胞中原子所处位置如图。已知:同种位置
原子相同,相邻原子间的最近距离之比 ,则 ;
晶体中与Cu原子最近且等距离的原子的数目为 。
第 5 页 共 10 页
学科网(北京)股份有限公司第 5 页 共 10 页
(6)“700℃加热”步骤中,混合气体中仅加少量 ,但借助工业合成氨的逆反应,可使Fe
不断生成。该步骤发生反应的化学方程式为
和 。
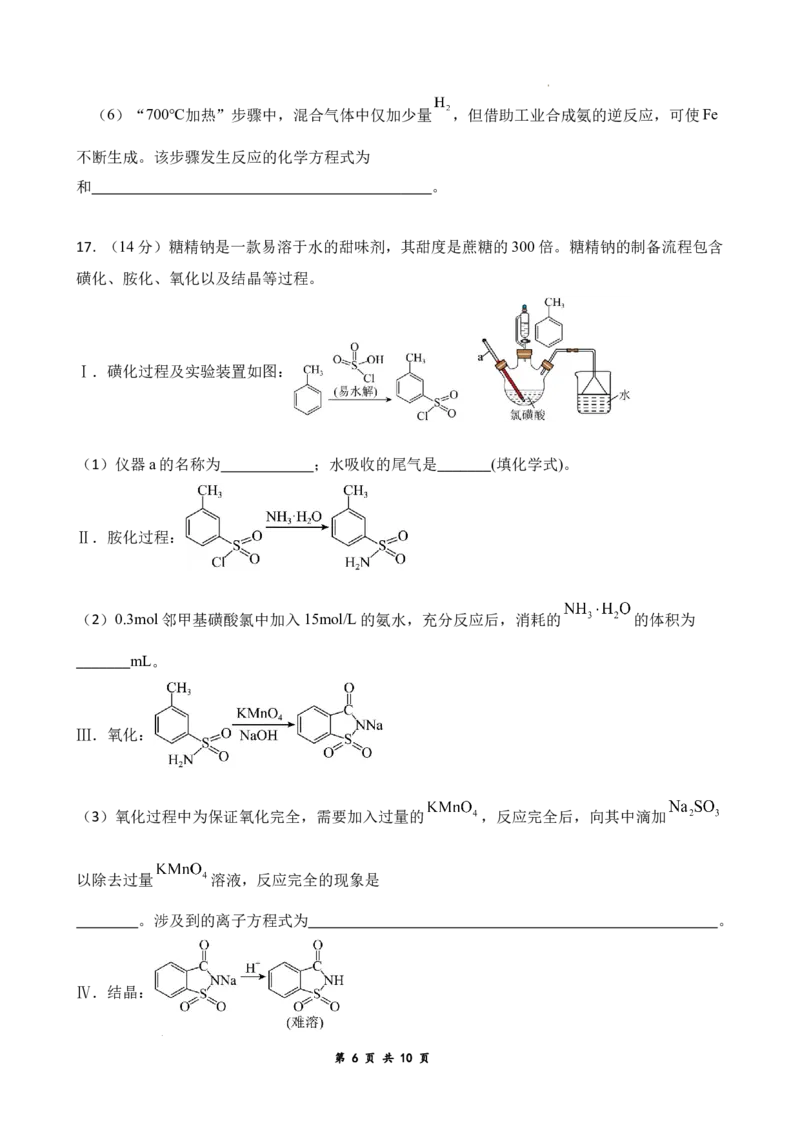
17. (14分)糖精钠是一款易溶于水的甜味剂,其甜度是蔗糖的300倍。糖精钠的制备流程包含
磺化、胺化、氧化以及结晶等过程。
Ⅰ.磺化过程及实验装置如图:
(1)仪器a的名称为 ;水吸收的尾气是_______(填化学式)。
Ⅱ.胺化过程:
(2)0.3mol邻甲基磺酸氯中加入15mol/L的氨水,充分反应后,消耗的 的体积为
_______mL。
Ⅲ.氧化:
(3)氧化过程中为保证氧化完全,需要加入过量的 ,反应完全后,向其中滴加
以除去过量 溶液,反应完全的现象是
。涉及到的离子方程式为 。
Ⅳ.结晶:
第 6 页 共 10 页
学科网(北京)股份有限公司第 6 页 共 10 页
(4)过滤不需要用到下列哪些仪器_______。
(5) 与 反应,产生大量的气体,该气体是_______。当 完全反应,
趁热过滤,冷却结晶的后续操作是 。
18.(13分)乙二醇(EG)是一种重要的基础化工原料,可通过石油化工和煤化工等工业路线合
成。
(1)石油化工路线中,环氧乙烷(EO)水合工艺是一种成熟的乙二醇生产方法,环氧乙烷和水反
应生成乙二醇,伴随生成二乙二醇(DEG)的副反应。
主反应: 副反应:
体系中环氧乙烷初始浓度为 ,恒温下反应30min,环氧乙烷完全转化,产物中
。
①0~30min内, 。
②下列说法正确的是 (填序号)。
a.主反应中,生成物总能量高于反应物总能量 b.0~30min内,
c.0~30min内, d.选择适当催化剂可提高乙二醇的最终产
率
(2)煤化工路线中,利用合成气直接合成乙二醇,原子利用率可达100%,具有广阔的发展前景。
如下: 。按化学
计量
第 7 页 共 10 页
学科网(北京)股份有限公司第 7 页 共 10 页
比进料,固定平衡转化率 ,探究温度与压强的关系。 分别为
0.4、0.5和0.6时,温度与压强的关系如图:
①代表 的曲线为 (填“ ”“ ”或“ ”);
原因是 。
② 0(填“>”“<”或“=”)。
③已知:反应 , ,x为组分的物质的量分数。
M、N两点对应的体系, (填“>”“<”或“=”),D点对应体系的 的值为
。
④已知:反应 , ,p为组分的分压。调整进料
比为 ,系统压强维持 ,使 ,此时
(用含有m和 的代数式表示)。
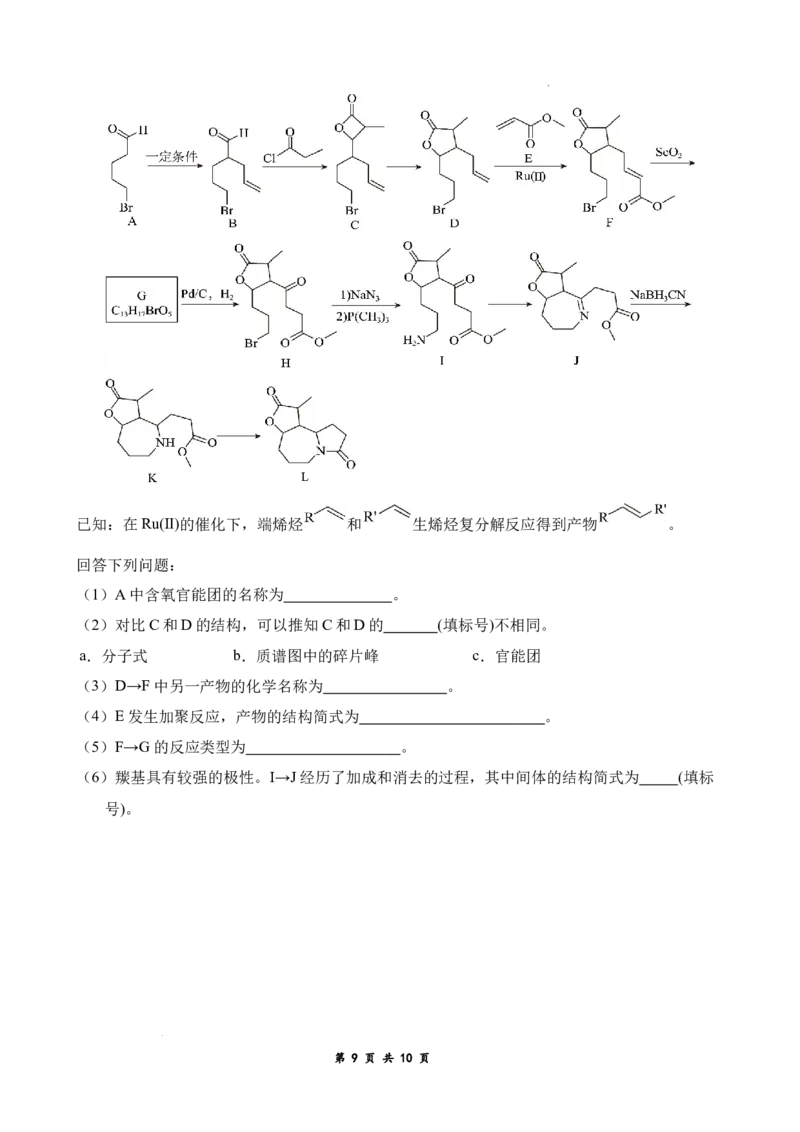
19.(14分)化合物L是某中药的活性成分。一种合成路线如下(略去部分试剂与反应条件,忽
略立体化学)。
第 8 页 共 10 页
学科网(北京)股份有限公司第 8 页 共 10 页
已知:在Ru(Ⅱ)的催化下,端烯烃 和 生烯烃复分解反应得到产物 。
回答下列问题:
(1)A中含氧官能团的名称为 。
(2)对比C和D的结构,可以推知C和D的 (填标号)不相同。
a.分子式 b.质谱图中的碎片峰 c.官能团
(3)D→F中另一产物的化学名称为 。
(4)E发生加聚反应,产物的结构简式为 。
(5)F→G的反应类型为 。
(6)羰基具有较强的极性。I→J经历了加成和消去的过程,其中间体的结构简式为 (填标
号)。
第 9 页 共 10 页
学科网(北京)股份有限公司第 9 页 共 10 页
a. b. c. d.
(7) 的化学方程式为 。
(8)写出一种满足下列条件的L的同分异构体的结构简式 (不考虑立体异构)。
①能与 发生显色反应;1mol该物质与足量NaOH溶液反应,消耗3molNaOH。
②核磁共振氢谱显示6组峰,且峰面积比为 。
③含有酯基和氨基(或取代的氨基, , 和 可以是H或烃基)。
第 10 页 共 10 页
学科网(北京)股份有限公司