文档内容
重庆市2019年初中学业水平暨高中招生考试化学试卷(A卷)
(全卷共四大题,满分70分,与物理共用120分钟)
注意事项:
1. 试题的答案书写在答题卡上,不得在试卷上直接作答。
2. 作答前认真阅读答题卡上的注意事项。
3. 考试结束,由监考人员将试卷和答题卡一并收回
可能用到的相对原子质量:H1 C12 O16 Na23 S32 C135.5 Fe56 Cu64
一、选择题(本大题共16小题,每小题2分,共32分,每小题只有一个选项符合题意)
(2019重庆中考A)1.我国主办2019年“世界环境日”活动,其主题聚焦“空气污染”。下
列不属于空气污染物的是( ) A.SO B.NO C.O D.PM
2 2 2 2.5
【答案】C
【解析】SO、NO 和PM 是空气污染物,O 不是空气污染物。故选C。
2 2 2.5 2
(2019重庆中考A)2.我国古代下列古代发明或技术中,主要原理涉及化学变化的是( )
A.矿石炼铁 B.水车灌溉 C.活字印刷 D.雕刻石像
【答案】A
【解析】矿石炼铁过程中由FeO 变成Fe,属于化学变化;水车灌溉、活字印刷和雕刻石像发生
2 3
变化过程中只是物质的形状、状态发生改变,没有生成新的物质,属于物理变化。故选A。
(2019重庆中考A)3.我国科学家屠呦呦因硏究青嵩素(C H O)取得巨大成就而获得诺贝尔
15 22 5
奖。青蒿素属于( )
A.单质 B.无机物 C.有机物 D.混合物
【答案】C
【解析】青嵩素含有碳、氢元素属于有机物。故选C。
(2019重庆中考A)4.下列变化不属于氧化反应的是( )
A.动物的呼吸 B.盐酸除铁锈 C.铁制品生锈 D.天然气燃烧
【答案】B
【解析】根据把得氧的反应叫作氧化反应判断动物的呼吸、铁制品生锈和天然气燃烧都属于
1氧化反应;盐酸除铁锈:6HCl+FeO=2FeCl+3HO不属于氧化反应。故选B。
2 3 3 2
(2019重庆中考A)5.某些袋装食品需要充气防腐,下列最宜作充入气体的是( )
A.氮气 B.氧气 C.甲烷 D.一氧化碳
【答案】A
【解析】氮气化学性质较稳定,无毒且来源广,可以作袋装食品保护气。故选A。
(2019重庆中考A)6.下列物质用途不正确的是( )
A.金属铜作导线 B.金刚石裁玻璃 C.小苏打制发酵粉 D.补铁剂预防甲状腺肿大
【答案】D
【解析】金属铜具有良好的导电性,可用作导线;金刚石硬度大可以裁玻璃;小苏打受热易分
解可以用作制发酵粉;补铁剂预防缺铁性贫血,补碘剂可以预防甲状腺肿大。故选D。
(2019重庆中考A)7.在元素周期表中汞元素的某些信息如右图所示,下列说法不正确的是(
)
A.汞原子中质子数为80 B.汞的原子序数为80
C.汞的相对原子质量为200.6 D.汞属于非金属元素
【答案】D
【解析】根据元素的原子序数=核电荷数=质子数=核外电子数判断:汞原子中质子数为80;汞
的原子序数为80;根据元素单元格信息判断汞的相对原子质量为200.6;汞属于金属元素。
故选D。
8. (2019重庆中考A)从安全角度考虑,下列说法正确的是( )
A.甲醛浸泡海鲜 B.霉变大米经煮熟后食用C.点燃H 前验纯D.煤炉上放一壶水防止CO中毒
2
【答案】C
【解析】甲醛有毒,不能浸泡海鲜;霉变大米含有黄曲霉素有毒,不能食用;氢气易爆炸,点燃
H 前要验纯;一氧化碳难溶于水,煤炉上放一壶水不能防止CO中毒。故选C。
2
(2019重庆中考A)9.一定条件下,某反应的微观示意图如下,有关说法正确的是( )
2A. 该反应属于置换反应
B. 反应前后元素的化合价未发生改变
C. 用生成物制得的氨水、氯化铵可用作化肥
D. 该反应的化学方程式为: 2N+3H 一定条件 2NH
2 2 3
【答案】C
【解析】根据微观示意图判断该反应方程式:N+3H 一定条件 2NH,该反应为化合反应;反应
2 2 3
前后元素的化合价发生改变;用生成物制得的氨水、氯化铵可用作化肥;该反应的化学方程
式为: 2N+3H 一定条件 2NH,该方程式氮原子个数未配平,应该改为N+3H 一定条件 2NH
2 2 3 2 2 3
。故选C。
(2019重庆中考A)10.2019年3月,四川省凉山州境内发生森林火灾。灭火过程中,突发林火
“爆燃”,导致多名扑火英雄献出了宝贵的生命。下列说法不正确的是( )
A.设置隔离带是为了清除可燃物
B.山风带入冷空气,能使林火熄灭
C.人工降雨能将温度降低至可燃物的着火点以下
D.林火“爆燃”可能是地表腐质层释放出大量可燃性气体所致
【答案】B
【解析】设置隔离带是为了清除可燃物,可以达到灭火的目的;山风带入冷空气,可以能使林
火燃烧更旺;人工降雨能将温度降低至可燃物的着火点以下,可以达到灭火的目的;林火
“爆燃”可能是地表腐质层释放出大量可燃性气体所致。故选B。
(2019重庆中考A)11.欲配制质量分数为6%的NaCl溶液,下列有关操作正确的是( )
A.取固体 B.称固体 C.量取水 D.溶解
3【答案】D
【解析】取氯化钠固体时,瓶塞到放在桌面上,防止药品腐蚀桌面;称氯化钠固体
时,砝码放在托盘天平的右盘,氯化钠放在左盘;量取水读数时,视线应该与凹液面最低处相
持平;溶解氯化钠时使用玻璃棒加快氯化钠溶解。故选D。
12. (2019重庆中考A)实验室用右图装置模拟炼铁。下列说法正确的是( )
A.磁铁矿的主要成分是FeO B.应先加热FeO 再通入CO
2 3 2 3
C.红棕色的逐渐变黑 D.气体通过澄清石灰水后可直接排放
【答案】C
【解析】赤铁矿的主要成分是FeO,磁铁矿的主要成分是FeO;炼铁过程中,由于一氧化碳易
2 3 3 4
爆炸,加热前先CO把装置内空气赶走,防止加热时产生爆炸,再加热FeO;反应过程中出现
2 3
红棕色的逐渐变黑;反应后尾气含有一氧化碳气体有毒,需要处理,不能直接排放,否则会污
染空气。故选C。
13.(2019重庆中考A)下列试剂分别滴入Ca(OH)、HSO、NaSO 三种溶液中,会出现三种不
2 2 4 2 4
同现象的是( )
A.NaCO 溶液 B.MgCl 溶液 C .Ba(OH) 溶液 D.酚酞溶液
2 3 2 2
【答案】A
【解析】向NaCO 溶液中分别滴入Ca(OH)、HSO、NaSO 三种溶液,分别出现白色沉淀、产生
2 3 2 2 4 2 4
气泡和不明显现象;向MgCl 溶液中分别滴入Ca(OH)、HSO、NaSO 三种溶液只出现白色沉
2 2 2 4 2 4
淀;向Ba(OH) 溶液分别滴入Ca(OH)、HSO、NaSO 三种溶液,出现白色沉淀;向酚酞溶液中
2 2 2 4 2 4
分别滴入Ca(OH)、HSO、NaSO 三种溶液,出现红色现象。故选A。
2 2 4 2 4
14.(2019重庆中考A)甲、乙的溶解度曲线如右图所示(不考虑水的变化)。下列说法正确的
是( )
4A.根据溶解度曲线可判断,甲的溶解度比乙的大
B.t℃时,甲的饱和溶液中溶质质量分数为40%
2
C.t℃时,将甲、乙饱和溶液分别降温至t℃,析出晶体甲的质量大
2 1
D.t℃时,将甲、乙饱和溶液分别升温至t℃,两溶液中溶质质量分数相等
1 2
【答案】D
【解析】根据溶解度曲线判断温度高于t℃时甲的溶解度比乙的大;t℃时,甲的饱和溶液中
2 2
40g
溶质质量分数: <40%;t℃时,将相同质量的甲、乙饱和溶液分
100%28.6% 2
40g100g
别降温至t℃,析出晶体甲的质量大;t℃时,将甲、乙饱和溶液分别升温至t℃,甲、乙均为
1 1 2
不饱和溶液,两溶液中溶质质量分数相等。故选D。
15.(2019重庆中考A)烹制鱼时,同时加料酒和食醋能使鱼肉味香可口,这是因为两者发生
了反应(未标明条件):CHOH+CHCOOH=HO+CHCOOCH(乙酸乙酯)。下列四种说法正确的有(
2 5 3 2 3 2 5
)
①乙醇具有良好的导电性
②加水稀释食醋,溶液pH值变大
③能闻到香味,是分子受热体积膨胀的缘故
④乙酸乙酯由4个碳原子、8个氢原子和2个氧原子构成
A.1种 B.2种 C.3种 D.4种
【答案】A
【解析】①乙醇不易导电性,错误;②加水稀释食醋,溶液pH值变大,正确;③能闻到香味,是
分子不断运动的缘故,错误;④一个乙酸乙酯分子由4个碳原子、8个氢原子和2个氧原子构
成,错误。故选A。
16.(2019重庆中考A)向盛有HCl和CuCl 混合溶液中逐滴加入NaOH溶液至过量,下列4个
2
图像能正确反应烧杯内的某些物理量变化趋势的是( )
5A. ①③ B.①②④ C.②④ D.①②③
【答案】D
【解析】向盛有HCl和CuCl 混合溶液中逐滴加入NaOH溶液至过量,先发生HCl和NaOH溶液
2
的中和反应,后CuCl 和NaOH溶液生成蓝色沉淀,①正确;根据质量守恒定律判断反应前后
2
氯元素的质量不变,②正确;根据HCl+NaOH=NaCl+HO,CuCl+2NaOH= Cu(OH)↓+2 NaCl判
2 2 2
断反应后溶质质量不断增加,③正确;随着NaOH溶液滴加和反应发生判断反应后溶剂不断
增加,④错误。故选D。
二、填空题(本大题共5小题,共21分)
17、(2019重庆中考A)(3分)某牛奶的营养成分表如右图所示。
(1)表中“钠”和“钙”指的是 (填序号)。A.元素 B.分子 C.原子
(2)该牛奶所含基本营养素中,除水外含量最高的是 。
(3)钠原子的结构示意图为 。
【答案】(1) A ;(2)糖类;(3) 。
【解析】(1)牛奶中营养成分中“钠”和“钙”主要指的是钠元素和钙元素。故选A ;(2)根据
图中信息判断该牛奶所含基本营养素中,除水外含量最高的是糖类,其次是脂肪、蛋白质等;
(3)钠元素为11号元素,其原子结构示意图 。
18、(2019重庆中考A) (4分)空气、水是我们赖以生存的重要资源。
6(1)Cu能与空气中的HO、O 和 反应生成“铜锈”[主要成分为Cu(OH)CO]。
2 2 2 2 3
(2)生活中常用 的方法降低水的硬度。
(3)电解水可制氢气。通电一段时间后,如右图所示。电极X为电源的 极。氢气作为新
能源,其主要优点为 (填序号)。
A.制取成本低 B.燃烧产物无污染 C.制备原料为水,来源广 D.贮存方便,安全
【答案】 (1)CO ; (2)煮沸;(3)正极,BC。
2
【解析】(1)根据“铜锈”的主要成分为Cu(OH)CO 判断其生成原理为Cu能与空气中的HO、
2 2 3 2
O 和CO 反应; (2)煮沸可以把硬水转化为软水;(3)根据电解水原理判断a与正极相连,为
2 2
氧气,b与正极相连,为氢气;电解水正确氢气成本高,氢气燃烧产物无污染且制备原料为水,
来源广;氢气易爆炸,贮存不方便,不安全。故选BC。
(2019重庆中考A)19、(5分)成功着陆月球背面的“嫦娥四号”探测器使用了多种材料。
(1)探测器上的五星红旗含有一种叫聚酸亚胺的有机高分子材料。该材料属于 (填“金
属”或“合成”)材料
(2)探测器使用的铝合金硬度比纯铝的硬度 (填“大”或“小”)
(3)探测器广泛使用了Al、Fe、Cu利用它们完成如下实验
①将未打磨的铝片放入FeSO 溶液中,没有明显现象。
4
②将打磨过的铝片放入FeSO 溶液中,铝片表面有明显变化。
4
③将打磨过的铁片片放入CuSO 溶液中,铁片表面变红
4
实验①中无现象是因为铝片表面有一层致密的 (填化学式)薄膜;
实验②中发生反应的化学方程式为 ;
实验③中铁片足量,充分反应后溶液变为 色。
【答案】(1)合成;(2)大;(3)①AlO ;②2Al+3FeSO=Al(SO4)+3Fe;③浅绿色。
2 3 4 2 3
【解析】(1) 有机高分子材料属于合成材料;(2)合金比组成它的纯金属硬度大,熔点低;(3)
铝常温下与氧气发生氧化反应,其表面生成一层致密氧化铝(AlO)保护膜,阻碍其进一步氧
2 3
化; 铝活动性强于铁,可以与亚铁的盐溶液发生置换反应:2Al+3FeSO=Al(SO4)+3Fe;铝活
4 2 3
动性强于铁,铁与CuSO 溶液反应生成浅绿色FeSO 溶液。
4 4
7(2019重庆中考A)20. (4分)我国科学家研发出由二氧化碳高效转化为甲醇(CHOH)的新技
3
术。
(1) 若该技术广泛应用,可把排放的CO 转化为甲醇,则能缓解 (填序号)。
2
A.酸雨 B.温室效应 C.白色污染
(2) 甲醇可被氧气氧化,其反应为:2CHOH+O 催化剂△2X+2HO,则X的化学式为 。
3 2 2
类比乙醇的燃烧,写出甲醇在空气中完全燃烧的化学方程式 。
(3) 若44gCO 全部转化为CHOH,且反应中其它物质均不含碳元素,可生成CHOH的质量为
2 3 3
g。
【答案】(1) B;(2)CHO 2CHOH+3O==2CO+4HO; (3)32。
2 3 2 2 2
【解析】(1) 该技术把二氧化碳高效转化为甲醇(CHOH),可以缓解温室效应。故选B;(2)根据
质量守恒定律判断该反应方程式:2CHOH+3O==2CO+4HO;(3)根据反应方程式计算44gCO 全
3 2 2 2 2
部转化为32gCHOH。
3
(2019重庆中考A)21. (5分)某化学兴趣小组欲分离KCl和BaCl 混合溶液,得到都含单一
2
溶质的两种溶液。他们设计了如下图所示的实验流程:
供选试剂:KSO 溶液、NaCO 溶液、KCO 溶液、盐酸、稀硫酸
3 4 2 3 2 3
(1) 步骤①中,分离A、B的实验操名称是 ,试剂a是
(2) 沉淀B表面残留少量滤液,需用蒸馏水多次洗涤,为了检验沉淀B是否洗涤干净,可向步
骤②的最后一次洗涤液中加入的试剂是 (双选,填序号)。
A.NaOH溶液 B.CaCl 溶液 C.NaCl溶液 D.AgNO 和HNO 混合溶液
2 3 3
(3) 步骤③中,发生反应的化学方程式为
(4) 要达到预期的日的,还需要改进的方法为
【答案】(1)过滤、KCO 溶液;(2)BD;(3)2HCl+BaCO=BaCl+HO+CO↑;(4)加入过量试剂a改
2 3 3 2 2 2
为适量的试剂a。
【解析】(1)分离固体与液体操作是过滤,根据流程图判断试剂a是KCO 溶液;(2) 要分离
2 3
8KCl和BaCl 混合溶液,且得到都含单一溶质的两种溶液,加入试剂既可以除去BaCl,又能生
2 2
成KCl,不能引入新的杂质,最后还得生成BaCl 溶液。故选BD;(3)步骤③把碳酸钡转化成氯
2
化钡,反应方程式:2HCl+BaCO=BaCl+HO+CO↑;(4)加入过量的KCO 溶液,引入新的杂质
3 2 2 2 2 3
KCO,应改为适量的试剂KCO 溶液。
2 3 2 3
三、实验题(本大题共2小题,共11分)
22. (2019重庆中考A)(5分)制取气体是初中化学实验的重要内容。
(1) 仪器M的名称是
(2) 实验室选用B装置制备氧气,其反应的化学方程式为
(3) C装置中的一处明显错误为 。
(4) 某气体只能用D装置收集,则该气体具有的性质为 (填序号)。
a.能与水反应b.能与空气反应c.密度与空气接近
(5) 若用A、E装置制取H,按气体流向,导管口连接顺序为 (填序号)。
2
【答案】(1)铁架台; (2) ; (3)长颈漏斗未形成液封;
(4)bc;(5)①③②。
【解析】(1) 仪器M是铁架台; (2) 实验室用氯酸钾和二氧化锰加热制取氧气的反应方程式:
; (3) C装置中的长颈漏斗未形成液封,使制取的气体从长
颈漏斗中逸出;(4) D装置是排水法收集气体,满足条件是不能与水反应,能与空气反应和密
度与空气接近。故选bc;(5) 用A、E装置制取H,按气体流向,氢气密度小于空气,用向下排
2
空气法收集,即导管口连接顺序为①③②。
23、(2019重庆中考A) (6分)小李将实验剩余的FeCl 溶液倒入含有HO 的废液缸,立即产
3 2 2
生大量的无色气泡。
(1) 小李根据组成的元素猜测,无色气体可能是H、O、HCl、Cl 中的一种或多种。
2 2 2
【查阅资料】1.Cl 是黄绿色、有刺激性气味的气体 2.FeCl 在水中解离出Fe3+、Cl-
2 3
根据资料,小李可排除的气体为
【实验一】为进一步验证该气体成分,他用燃着的木条伸入收集满该气体的小试管中,只观察
9到木条燃得更旺,则该气体一定含 。
(2) 小李认为上诉过程中FeCl 溶液作了HO 分解的催化剂。
3 2 2
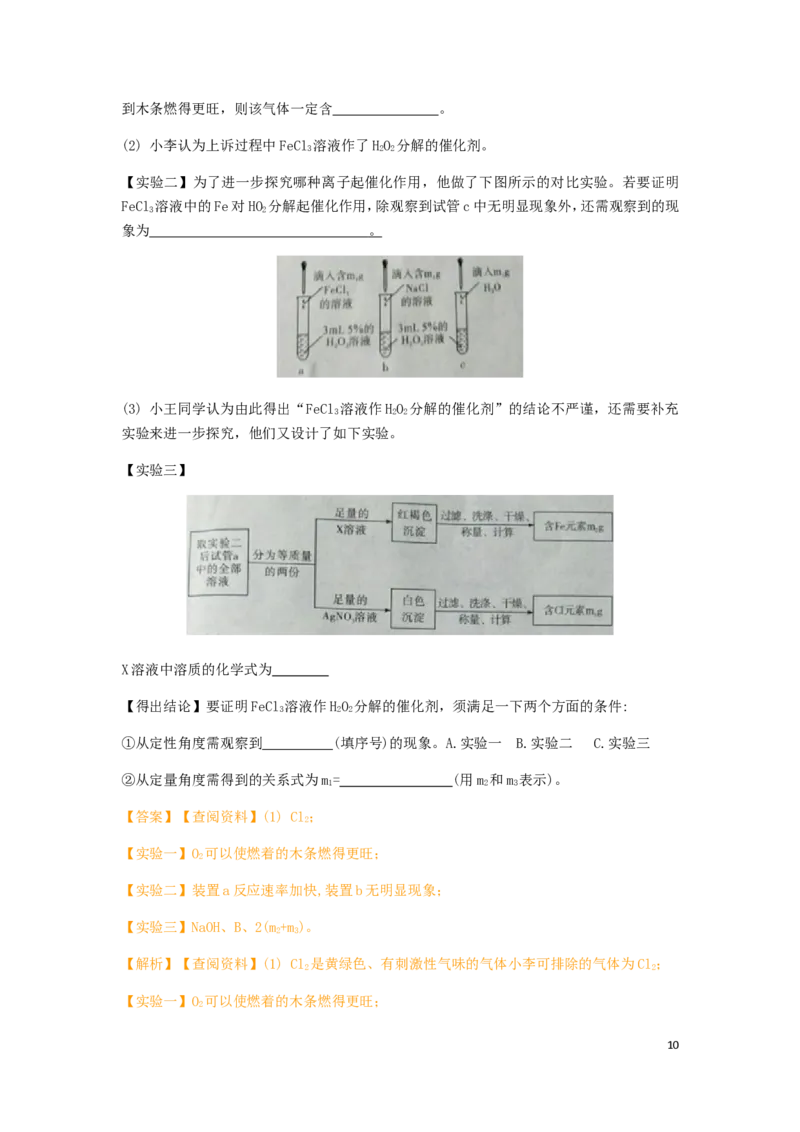
【实验二】为了进一步探究哪种离子起催化作用,他做了下图所示的对比实验。若要证明
FeCl 溶液中的Fe对HO 分解起催化作用,除观察到试管c中无明显现象外,还需观察到的现
3 2
象为 。
(3) 小王同学认为由此得出“FeCl 溶液作HO 分解的催化剂”的结论不严谨,还需要补充
3 2 2
实验来进一步探究,他们又设计了如下实验。
【实验三】
X溶液中溶质的化学式为
【得出结论】要证明FeCl 溶液作HO 分解的催化剂,须满足一下两个方面的条件:
3 2 2
①从定性角度需观察到 (填序号)的现象。A.实验一 B.实验二 C.实验三
②从定量角度需得到的关系式为m= (用m 和m 表示)。
1 2 3
【答案】【查阅资料】(1) Cl;
2
【实验一】O 可以使燃着的木条燃得更旺;
2
【实验二】装置a反应速率加快,装置b无明显现象;
【实验三】NaOH、B、2(m+m)。
2 3
【解析】【查阅资料】(1) Cl 是黄绿色、有刺激性气味的气体小李可排除的气体为Cl;
2 2
【实验一】O 可以使燃着的木条燃得更旺;
2
10【实验二】观察装置a、b、c中现象,即装置a反应速率加快,装置b无明显现象;
【实验三】根据NaOH与FeCl 反应生成红褐色沉淀,实验二可以从定性判断FeCl 溶液所起的
3 3
催化作用。故选B;定量计算:反应前后FeCl 的质量不变, 由于取实验二后试管a中的全部
3
溶液分为等质量的两份,所得FeCl 的质量为(m+m)×2。
3 2 3
三、计算题(本大题包括1个小题,共6分)
23. (2019重庆中考A)(6分)高铁酸钠( NaFeo)是一种新型绿色消毒剂,主要用于饮用水
2 4
处理。某工厂以22.35 kg NaClO固体若干Fe(SO4) 固体和质量分数为20%的NaOH溶液为原
2 3
料生产 NaFeo,反应原理为:3NaClO+Fe(SO4)+10NaOH = 2NaFeo+3NaCl+3NaSO+5HO。假
2 4 2 3 2 4 2 4 2
设反应物均恰好完全反应。试计算:
[已知:相对分子质量为 NaCIO 74.5 Fe(SO) 400 NaFeo 166]
2 4 3 2 4
(1)NaFeO 中质量分数最大的元素是
2 4
(2)制备过程中需加入20%的NaOH溶液的质量是多少?
(3)最后所得溶液中NaFeO 的质量分数是多少?(计算结果精确到0.1%)
2 4
【答案】(1)氧元素;(2) 200kg;(3)12.7%。
【解析】(1)根据NaFeO 化学式计算和判断氧元素是NaFeO 中质量分数最大的元素;
2 4 2 4
(2)解:NaOH的质量为x
3NaClO+Fe(SO4)+10NaOH = 2NaFeo+3NaCl+3NaSO+5HO
2 3 2 4 2 4 2
223.5 400 332
22. 35kg x
20%的NaOH溶液的质量=40kg÷20%=200kg
答:加入20%的NaOH溶液的质量是200kg
(3)解:设Fe(SO4) 的质量为y, NaFeo 的质量z
2 3 2 4
3NaClO+Fe(SO4)+10NaOH=2NaFeo+3NaCl+3NaSO+5HO
2 3 2 4 2 4 2
223.5 400 332
2235kg y z
y=40kg z=33.2kg(1分)
NaFeo 溶液的质量:22.35kg+40kg+200kg(1分)
2 4
11NaFeo 的质量分数12.7%(1分)
2 4
答:最后所得溶液中NaFeo 的质量分数是12.7%。
2 4
12