文档内容
2025-2026 学年高二化学上学期第一次月考卷
(考试时间:90 分钟 试卷满分:100 分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号
填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:选择性必修一第一章(鲁科版)。
5.难度系数:0.65
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Cu 64
第Ⅰ卷(选择题 共 54 分)
一、选择题:本题共 18 个小题,每小题 3 分,共 54 分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.下列设备工作时,将化学能转化为热能的是
A B C D
太阳能集热器 锂离子电池 燃气灶 电风扇
A.A B.B C.C D.D
2.某化学反应由两步反应 A→B→C 构成,A、B、C 分别为三种物质,该反应中能量曲线如图所示,下列
叙述正确的是
A.A→C 为放热反应,所以不需要任何条件
B.A 比 C 更稳定
C.破坏 B 中化学键吸收的能量低于形成 C 中新化学键释放的能量,所以 B→C 为放热反应
D.A→B 中化学能转化为热能
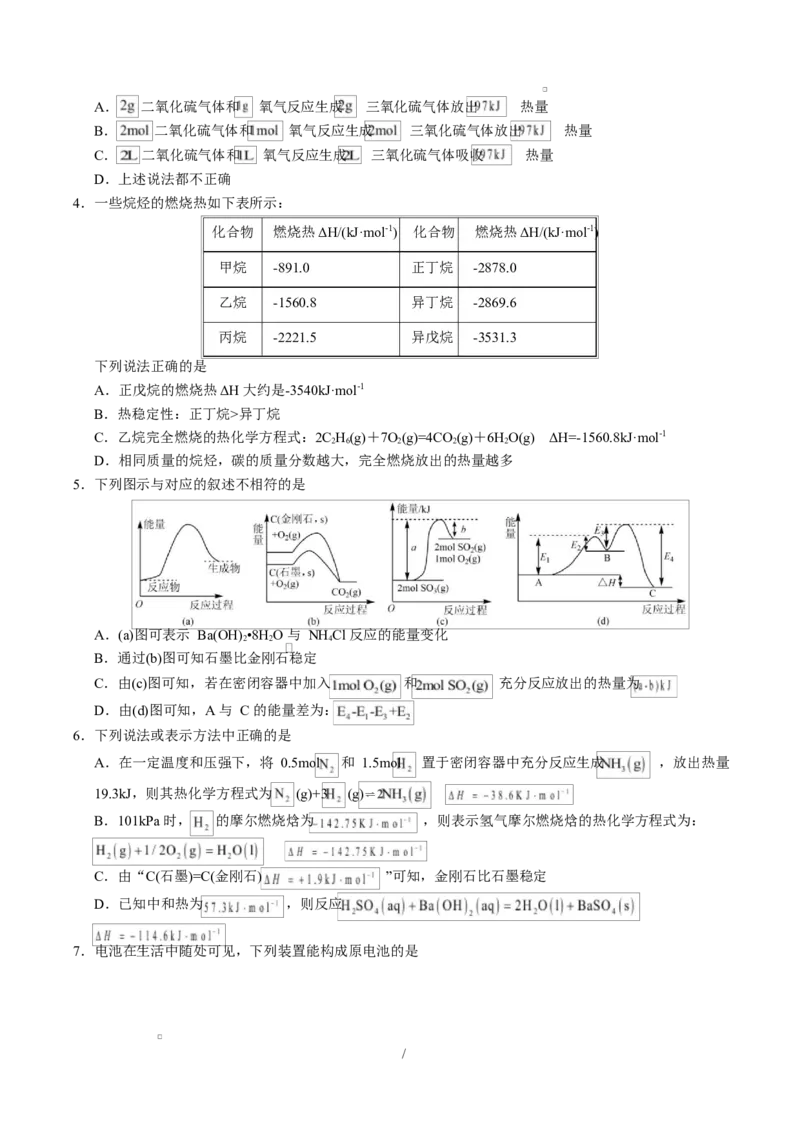
3.热化学方程式 的意义是
/A. 二氧化硫气体和 氧气反应生成 三氧化硫气体放出 热量
B. 二氧化硫气体和 氧气反应生成 三氧化硫气体放出 热量
C. 二氧化硫气体和 氧气反应生成 三氧化硫气体吸收 热量
D.上述说法都不正确
4.一些烷烃的燃烧热如下表所示:
化合物 燃烧热ΔH/(kJ·mol-1) 化合物 燃烧热ΔH/(kJ·mol-1)
甲烷 -891.0 正丁烷 -2878.0
乙烷 -1560.8 异丁烷 -2869.6
丙烷 -2221.5 异戊烷 -3531.3
下列说法正确的是
A.正戊烷的燃烧热ΔH 大约是-3540kJ·mol-1
B.热稳定性:正丁烷>异丁烷
C.乙烷完全燃烧的热化学方程式:2C H(g)+7O(g)=4CO (g)+6HO(g) ΔH=-1560.8kJ·mol-1
2 6 2 2 2
D.相同质量的烷烃,碳的质量分数越大,完全燃烧放出的热量越多
5.下列图示与对应的叙述不相符的是
A.(a)图可表示 Ba(OH) •8H O 与 NH Cl 反应的能量变化
2 2 4
B.通过(b)图可知石墨比金刚石稳定
C.由(c)图可知,若在密闭容器中加入 和 充分反应放出的热量为
D.由(d)图可知,A 与 C 的能量差为:
6.下列说法或表示方法中正确的是
A.在一定温度和压强下,将 0.5mol 和 1.5mol 置于密闭容器中充分反应生成 ,放出热量
19.3kJ,则其热化学方程式为 (g)+3 (g)⇌2
B.101kPa 时, 的摩尔燃烧焓为 ,则表示氢气摩尔燃烧焓的热化学方程式为:
C.由“C(石墨)=C(金刚石) ”可知,金刚石比石墨稳定
D.已知中和热为 ,则反应
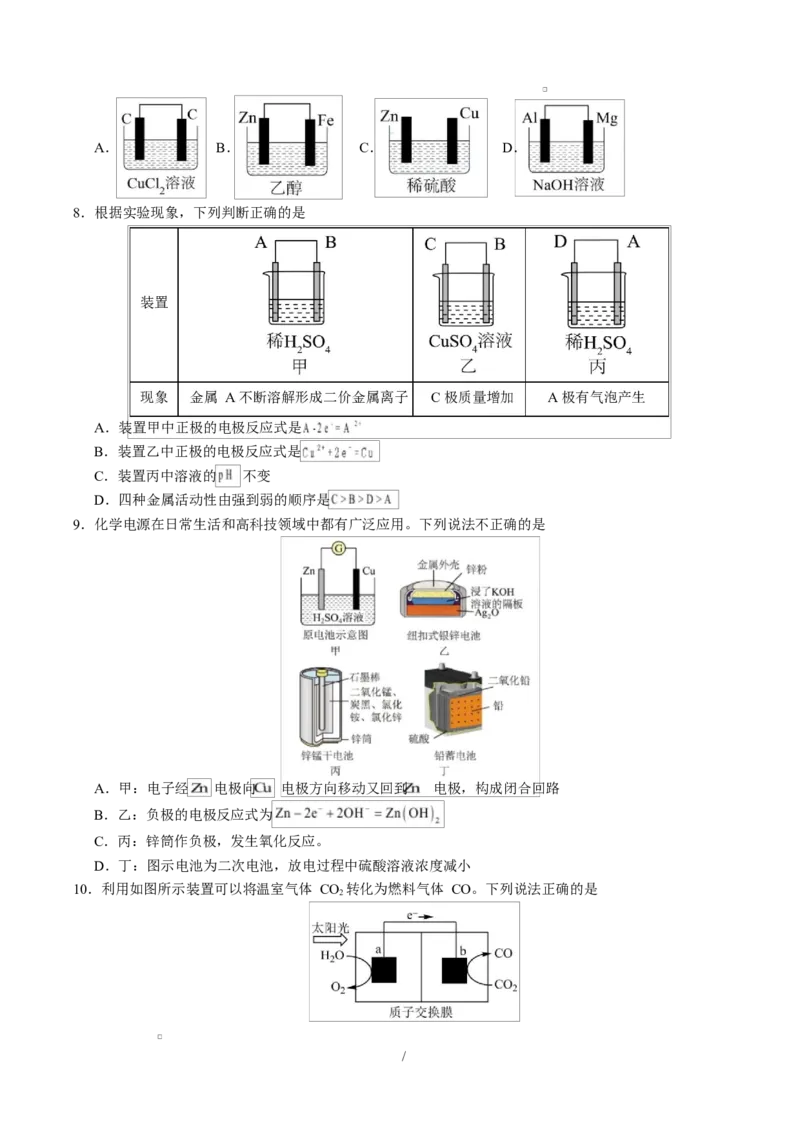
7.电池在生活中随处可见,下列装置能构成原电池的是
/A. B. C. D.
8.根据实验现象,下列判断正确的是
装置
现象 金属 A 不断溶解形成二价金属离子 C 极质量增加 A 极有气泡产生
A.装置甲中正极的电极反应式是
B.装置乙中正极的电极反应式是
C.装置丙中溶液的 不变
D.四种金属活动性由强到弱的顺序是
9.化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是
A.甲:电子经 电极向 电极方向移动又回到 电极,构成闭合回路
B.乙:负极的电极反应式为
C.丙:锌筒作负极,发生氧化反应。
D.丁:图示电池为二次电池,放电过程中硫酸溶液浓度减小
10.利用如图所示装置可以将温室气体 CO 转化为燃料气体 CO。下列说法正确的是
2
/A.电极 a 表面发生反应 2H
2
O-4e-=O
2
+ 4H+
B.电极 b 为电源阴极,发生氧化反应
C.该装置工作时,H+从 b 极区向 a 极区移动
D.该装置中每生成 1 mol CO,同时生成 1 mol O
2
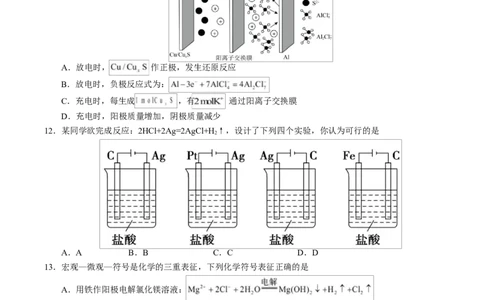
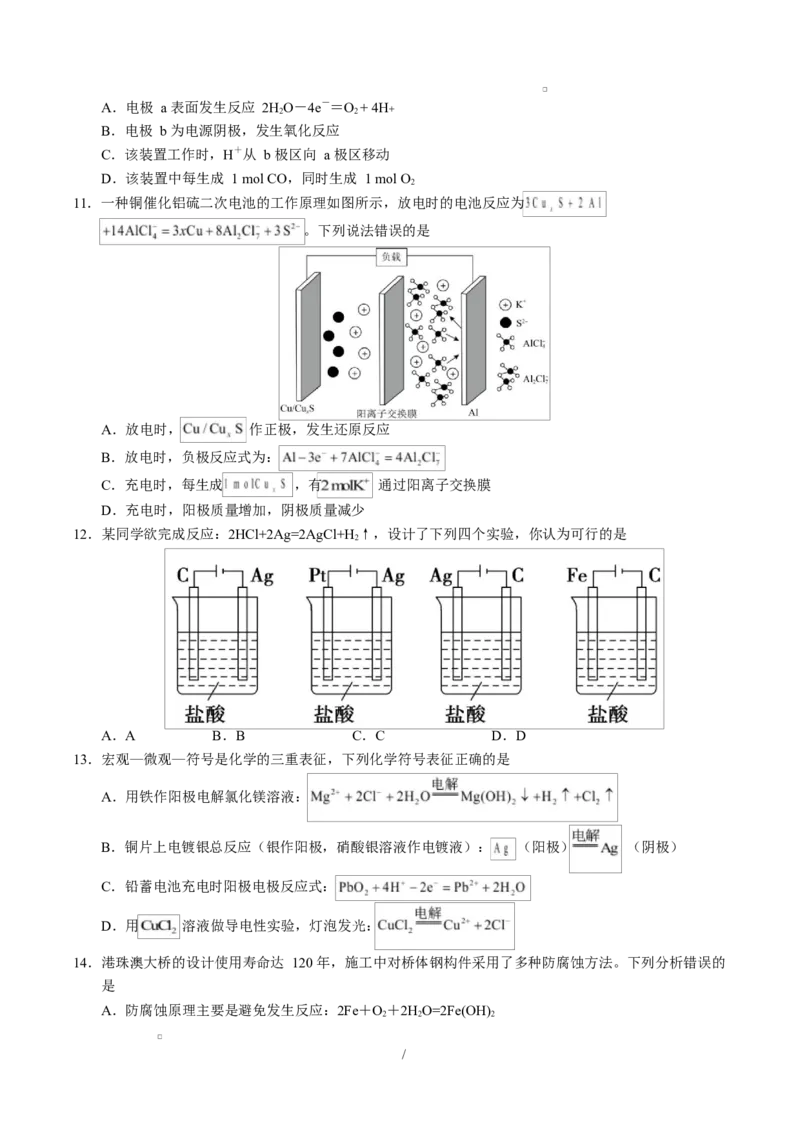
11.一种铜催化铝硫二次电池的工作原理如图所示,放电时的电池反应为
。下列说法错误的是
A.放电时, 作正极,发生还原反应
B.放电时,负极反应式为:
C.充电时,每生成 ,有 通过阳离子交换膜
D.充电时,阳极质量增加,阴极质量减少
12.某同学欲完成反应:2HCl+2Ag=2AgCl+H ↑,设计了下列四个实验,你认为可行的是
2
A.A B.B C.C D.D
13.宏观—微观—符号是化学的三重表征,下列化学符号表征正确的是
A.用铁作阳极电解氯化镁溶液:
B.铜片上电镀银总反应(银作阳极,硝酸银溶液作电镀液): (阳极) (阴极)
C.铅蓄电池充电时阳极电极反应式:
D.用 溶液做导电性实验,灯泡发光:
14.港珠澳大桥的设计使用寿命达 120 年,施工中对桥体钢构件采用了多种防腐蚀方法。下列分析错误的
是
A.防腐蚀原理主要是避免发生反应:2Fe+O+2HO=2Fe(OH)
2 2 2
/B.钢构件表面喷涂环氧树脂涂层,是为了隔绝空气、水等,防止形成原电池
C.采用外加电流阴极保护法时需直接在钢构件上安装锌块
D.钢构件可采用不锈钢材料以减缓电化学腐蚀
15.钢铁在潮湿空气中的电化学腐蚀基本化学原理如下图所示。下列说法不正确的是
A.Fe、C 构成原电池的外电路 B.钢铁表面可发生反应:
C.吸氧腐蚀与析氢腐蚀可先后发生 D.利用电化学腐蚀可测定空气中氧气的含量
16.一种新型高温可充电电池的构造如图所示,其电池活性物质为 Na 和 S。下列说法正确的是
A.放电时石墨 b 上发生的反应为
B.外电路中每通过 1mol 电子,有 0.5molNa+ 通过含 Na+ 的导体
C.放电时,电流的传导方向为石墨 b→外电路→石墨 a→固体电解质→石墨 b
D.闭合 K,可将化学能转化为电能
2
17.下列是冬季使用的某一“暖宝宝”贴的标签。以下叙述错误的是
品名:一次性使用取暖片
成分:铁粉、活性炭、水、木粉、食盐等
用法:使用之前将其真空包装外袋撕开。取出内袋,轻轻揉
搓,贴在内衣外层。
注意事项:1.避免真空塑料包装袋被破坏,造成产品失效。
2.可持续 10 小时均匀放热。
A.暖宝宝发热的原理主要是利用铁生锈放热
B.铁生锈后反应产物的主要成分是四氧化三铁
C.暖宝宝需接触空气才会发热
D.食盐能加快“暖宝宝”中铁生锈的速度
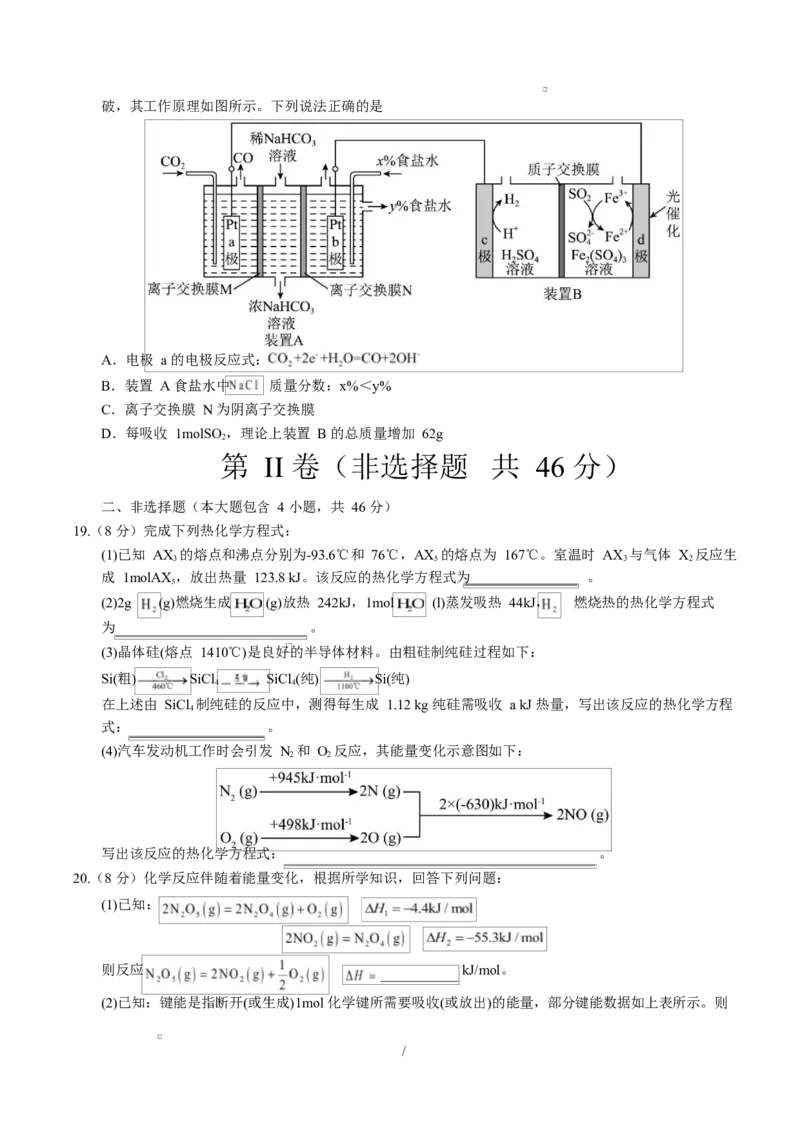
18.我国科学家在光电催化—化学耦合烟气脱硫并实现 CO 的资源化利用与电能储存的研究中取得重大突
2
/破,其工作原理如图所示。下列说法正确的是
A.电极 a 的电极反应式:
B.装置 A 食盐水中 质量分数:x%<y%
C.离子交换膜 N 为阴离子交换膜
D.每吸收 1molSO ,理论上装置 B 的总质量增加 62g
2
第 II 卷(非选择题 共 46 分)
二、非选择题(本大题包含 4 小题,共 46 分)
19.(8 分)完成下列热化学方程式:
(1)已知 AX 的熔点和沸点分别为-93.6℃和 76℃,AX 的熔点为 167℃。室温时 AX 与气体 X 反应生
3 5 3 2
成 1molAX ,放出热量 123.8 kJ。该反应的热化学方程式为 。
5
(2)2g (g)燃烧生成 (g)放热 242kJ,1mol (l)蒸发吸热 44kJ, 燃烧热的热化学方程式
为 。
(3)晶体硅(熔点 1410℃)是良好的半导体材料。由粗硅制纯硅过程如下:
Si(粗) SiCl SiCl (纯) Si(纯)
4 4
在上述由 SiCl 制纯硅的反应中,测得每生成 1.12 kg 纯硅需吸收 a kJ 热量,写出该反应的热化学方程
4
式: 。
(4)汽车发动机工作时会引发 N 和 O 反应,其能量变化示意图如下:
2 2
写出该反应的热化学方程式: 。
20.(8 分)化学反应伴随着能量变化,根据所学知识,回答下列问题:
(1)已知:
则反应 kJ/mol。
(2)已知:键能是指断开(或生成)1mol 化学键所需要吸收(或放出)的能量,部分键能数据如上表所示。则
/△H= 。
化学键 N≡N F—F N—F
键能/(
941.7 154.8 283.0
)
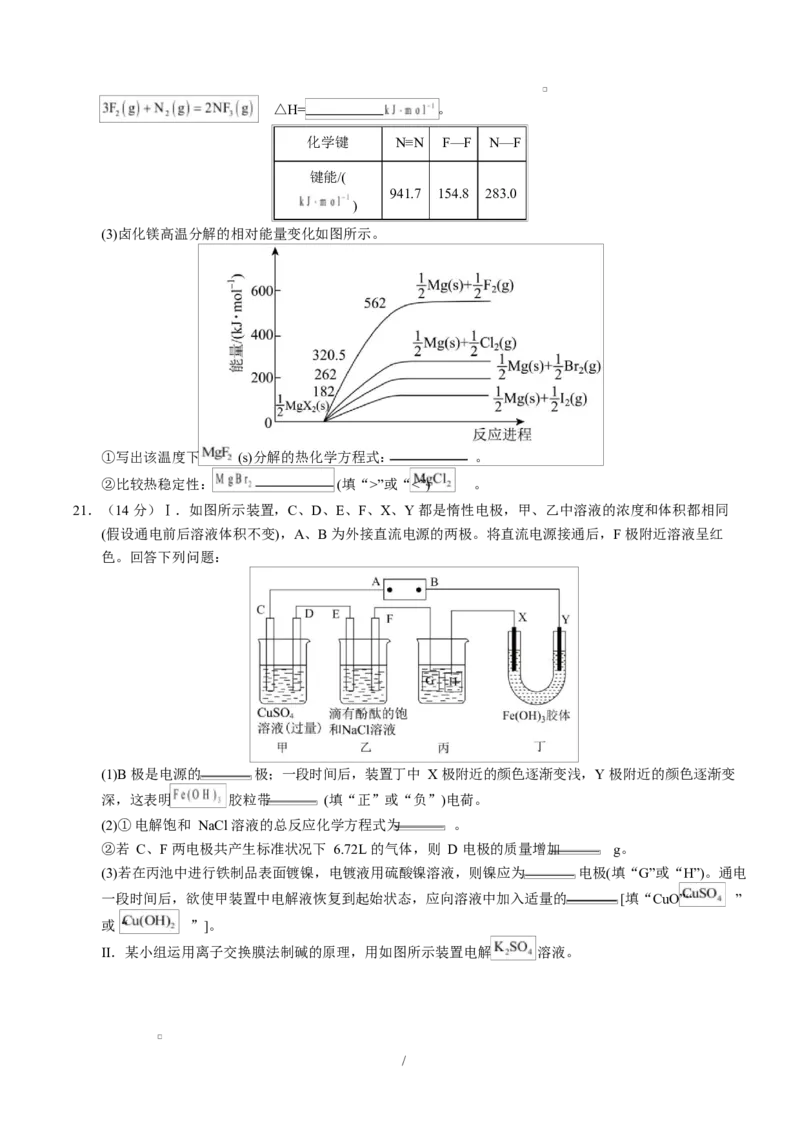
(3)卤化镁高温分解的相对能量变化如图所示。
①写出该温度下 (s)分解的热化学方程式: 。
②比较热稳定性: (填“>”或“<”) 。
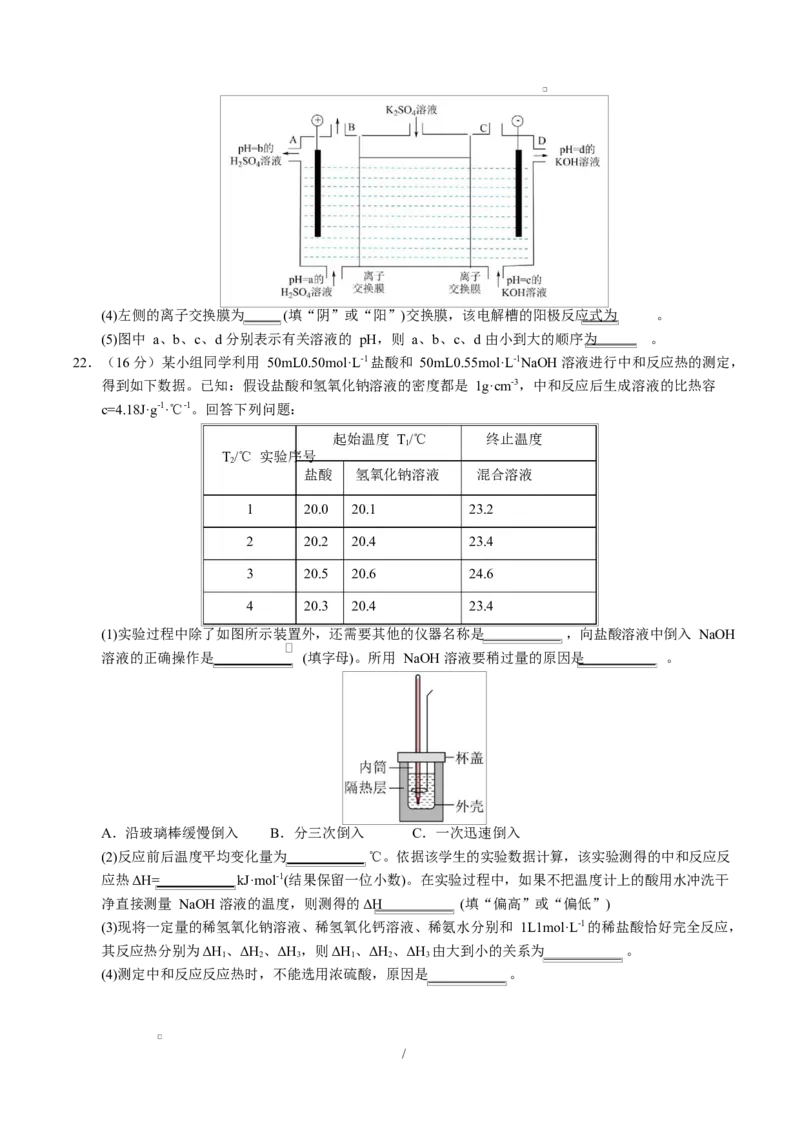
21.(14 分)Ⅰ.如图所示装置,C、D、E、F、X、Y 都是惰性电极,甲、乙中溶液的浓度和体积都相同
(假设通电前后溶液体积不变),A、B 为外接直流电源的两极。将直流电源接通后,F 极附近溶液呈红
色。回答下列问题:
(1)B 极是电源的 极;一段时间后,装置丁中 X 极附近的颜色逐渐变浅,Y 极附近的颜色逐渐变
深,这表明 胶粒带 (填“正”或“负”)电荷。
(2)①电解饱和 NaCl 溶液的总反应化学方程式为 。
②若 C、F 两电极共产生标准状况下 6.72L 的气体,则 D 电极的质量增加 g。
(3)若在丙池中进行铁制品表面镀镍,电镀液用硫酸镍溶液,则镍应为 电极(填“G”或“H”)。通电
一段时间后,欲使甲装置中电解液恢复到起始状态,应向溶液中加入适量的 [填“CuO”“ ”
或“ ”]。
II.某小组运用离子交换膜法制碱的原理,用如图所示装置电解 溶液。
/(4)左侧的离子交换膜为 (填“阴”或“阳”)交换膜,该电解槽的阳极反应式为 。
(5)图中 a、b、c、d 分别表示有关溶液的 pH,则 a、b、c、d 由小到大的顺序为 。
22.(16 分)某小组同学利用 50mL0.50mol·L-1 盐酸和 50mL0.55mol·L-1NaOH 溶液进行中和反应热的测定,
得到如下数据。已知:假设盐酸和氢氧化钠溶液的密度都是 1g·cm-3,中和反应后生成溶液的比热容
c=4.18J·g-1·℃-1。回答下列问题:
起始温度 T/℃ 终止温度
1
T/℃ 实验序号
2
盐酸 氢氧化钠溶液 混合溶液
1 20.0 20.1 23.2
2 20.2 20.4 23.4
3 20.5 20.6 24.6
4 20.3 20.4 23.4
(1)实验过程中除了如图所示装置外,还需要其他的仪器名称是 ,向盐酸溶液中倒入 NaOH
溶液的正确操作是 (填字母)。所用 NaOH 溶液要稍过量的原因是 。
A.沿玻璃棒缓慢倒入 B.分三次倒入 C.一次迅速倒入
(2)反应前后温度平均变化量为 ℃。依据该学生的实验数据计算,该实验测得的中和反应反
应热ΔH= kJ·mol-1(结果保留一位小数)。在实验过程中,如果不把温度计上的酸用水冲洗干
净直接测量 NaOH 溶液的温度,则测得的ΔH (填“偏高”或“偏低”)
(3)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和 1L1mol·L-1 的稀盐酸恰好完全反应,
其反应热分别为ΔH、ΔH、ΔH,则ΔH、ΔH、ΔH 由大到小的关系为 。
1 2 3 1 2 3
(4)测定中和反应反应热时,不能选用浓硫酸,原因是 。
/