文档内容
2025-2026 学年高二化学上学期第一次月考卷
(考试时间:60 分钟,试卷满分:100 分)
注意事项:
1.答题前,考生务必将自己的学校、班级、姓名、准考证号填写清楚,并将条形码粘贴在规定位置。
2.本试卷设试卷和答题纸两部分。试卷包括试题与答题要求;所有答案必须涂或写在答题纸上;做在
试卷上一律不得分。答题纸与试卷在试题编号上是一一对应的,答题时应特别注意,不能错位。
3.选择类试题中,标注“不定项”的试题,每小题有 1~2 个正确选项,只有 1 个正确选项的,多选不给
分,有 2 个正确选项的,漏选一个给一半分,错选不给分;未特别标注的试题,每小题只有一个正确选项。
4.测试范围:沪科版 2020 选择性必修 1 第一、二章。
5.考试结束后,将本试卷和答题卡一并交回。
6.难度系数:0.72。
可能用到的相对原子质量:H-1;C-12;O-16;Na-23;Mg-24;Al-27;Cu-64;Fe-56;Mn-55;Fe-56;
Cl-35.5;
一、治理温室气体(20 分)
CO、CH 和 NO 是地球大气中的主要温室气体,相同量的 NO 的增温潜能是 CO 的 289 倍,研究温
2 4 2 2 2
室气体对环境保护有重要意义。
I. CH 与 CO 的处理:
4 2
通过下列反应,可将 CH 与 CO 转化:CH(g)+CO(g) 2CO(g)+2H(g) ΔH>0。
4 2 4 2 2
(1)该反应的自发性为_______。
A.高温下自发 B.低温下自发 C.任何温度下均自发 D.任何温度下均不自发
(2)能判断该反应达到平衡状态的是_______(不定项)。
A.v (CH)=v (CO) B.CH、CO 的分子数之比为 1:1
正 4 逆 4 2
C.CH、CO、CO、H 的浓度相等 D.恒容容器中气体的平均摩尔质量不变
4 2 2
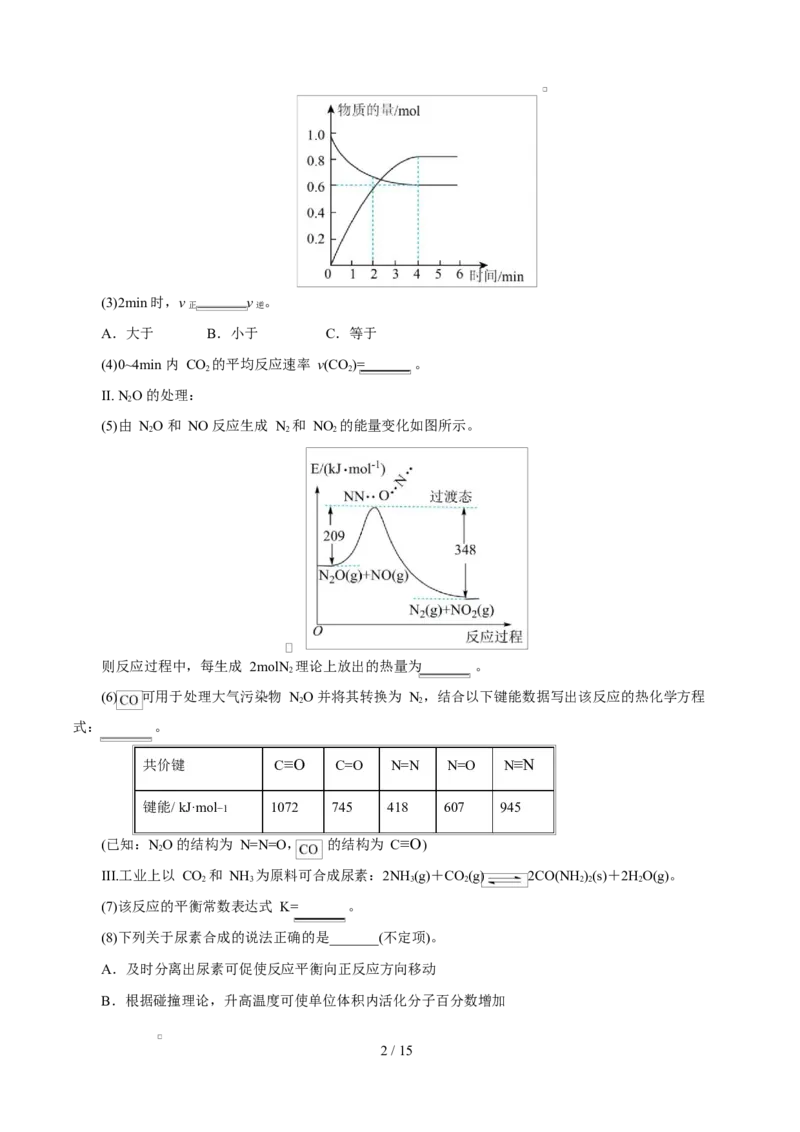
一定温度下,在 密闭容器中充入 1molCH (g)和 1mol CO(g),发生上述反应,测得两种气体的物质
4 2
的量随时间变化关系如图所示:
1 / 15(3)2min 时,v v 。
正 逆
A.大于 B.小于 C.等于
(4)0~4min 内 CO 的平均反应速率 v(CO)= 。
2 2
II. N O 的处理:
2
(5)由 NO 和 NO 反应生成 N 和 NO 的能量变化如图所示。
2 2 2
则反应过程中,每生成 2molN 理论上放出的热量为 。
2
(6) 可用于处理大气污染物 NO 并将其转换为 N,结合以下键能数据写出该反应的热化学方程
2 2
式: 。
共价键 C≡O C=O N=N N=O N≡N
键能/ kJ·mol−1 1072 745 418 607 945
(已知:NO 的结构为 N=N=O, 的结构为 C≡O)
2
III.工业上以 CO 和 NH 为原料可合成尿素:2NH (g)+CO(g) 2CO(NH)(s)+2HO(g)。
2 3 3 2 2 2 2
(7)该反应的平衡常数表达式 K= 。
(8)下列关于尿素合成的说法正确的是_______(不定项)。
A.及时分离出尿素可促使反应平衡向正反应方向移动
B.根据碰撞理论,升高温度可使单位体积内活化分子百分数增加
2 / 15C.保持容积不变,充入惰性气体增大压强,可提高总反应的反应速率
D.更换催化剂,不能改变 NH 的平衡转化率
3
IV.还可用于工业制“碱”。
(9)制“碱”的基本原理为:向饱和食盐水中先通入氨气,再通入过量 CO,制得氯化铵和 。(填物
2
质名称)
(10)简述检验“碱”中是否含有 Cl-的方法: 。
【答案】(1)A(2 分)
(2)AD(2 分)
(3)A(2 分)
(4)0.05 mol·L-1·min-1(2 分)
(5)278kJ(2 分)
(6) CO(g)+NO(g)=N (g)+CO(g) ΔH=-338kJ·mol−1(2 分)
2 2 2
(7) (2 分)
(8)BD(2 分)
(9)碳酸氢钠(2 分)
(10)取少量碱于试管溶解,加入硝酸,再滴入硝酸银,若有白色沉淀说明有氯离子,反之不含(2 分)
【解析】(1)由方程式可知该反应是气体物质的量增多的熵增反应,且ΔH>0,由ΔG=ΔH-TΔS<0 可知
该反应仅在高温下自发,故选 A;
(2)A 项,正逆反应速率相等,说明反应达到平衡状态,A 正确;B 项,分子数之比不能说明反应达到
平衡状态,B 错误;C 项,浓度相等不能说明反应达到平衡状态,C 错误;D 项,反应前后气体的质量不变,
物质的量是变量,恒容容器中气体的平均摩尔质量不变,说明反应达到平衡状态,D 正确; 故选 AD。
(3)2min 之后反应物的物质的量降低、生成物的物质的量增加,反应正向进行,对应的速率关系是 v(正)
>v(逆),故选 A;
(4)4min 时浓度不再改变,即达到平衡状态,1mol CO(g)参加反应,
2
;
(5)根据能量变化图可知,热化学方程式:NO(g)+NO(g)=N (g)+NO (g) ΔH=-139kJ·mol−1,则生成
2 2 2
2molN 理论放出热量为 278kJ;
2
(6)CO 可用于处理大气污染物 NO 并将其转换为 N 方程式 CO+NO=N+CO ,
2 2 2 2 2
3 / 15,热化学方程式为 CO(g)+NO
2
(g)=N(g)+CO(g) ΔH=-338kJ·mol−1;
2 2
(7)根据平衡常数的定义结合反应方程式 2NH (g)+CO(g) 2CO(NH)(s)+2HO(g)可知,该反应
3 2 2 2 2
的平衡常数表达式 ;
(8)A 项,由题干方程式可知,尿素为固体,故及时分离出尿素,尿素的浓度不变,正、逆反应速率不
变仍然相等,化学平衡不移动,A 错误;B 项,升高温度,使单位体积内活化分子百分数增加,有效碰撞
次数增多,反应速率加快,B 正确;C 项,保持容积不变,充入惰性气体增大压强,反应体系中各组分的浓
度保持不变,正逆反应速率不变,C 错误;D 项,改变催化剂,只能改变反应速率,而不能使平衡发生移动,
即不能改变 NH 的平衡转化率,D 正确;故选 BD。
3
(9)制“碱”的基本原理为 NaCl+NH +CO +H O=NaHCO ↓+NHCl:向饱和食盐水中先通入氨气,再通入
3 2 2 3 4
过量 CO,制得氯化铵和碳酸氢钠;
2
(10)简述检验“碱”中是否含有 Cl-的方法:取少量碱于试管溶解,加入硝酸,再滴入硝酸银,若有白色
沉淀说明有氯离子,反之不含。
二、工业合成氨(22 分)
运用化学反应原理研究合成氨反应有重要意义。合成氨的工业生产主要包括造气、净化与合成三个步
骤。
(1)生产氢气:将水蒸气通过红热的炭即产生水煤气:C(s)+HO(g) CO(g)+H(g) ΔH=131.3kJ·
2 2
mol−1, ΔS=133.7J·mol-1·K-1。
该反应在常温下 (填“能”或“不能”)自发进行。
(2)水煤气转化反应 CO(g)+HO(g) CO(g)+H(g)在一定温度下达到化学平衡。现将不同量的 CO
2 2 2
(g)和 HO(g)分别通入到体积为 2L 的恒容密闭容器中进行反应,得到如下两组数据:
2
起始量/mol 平衡量/mol
实验编号 温度/℃ 达到平衡所需时间/min
CO HO H CO
2 2
1 650 4 2 1.6 2.4 5
2 900 2 1 0.4 1.6 3
①平衡常数 K(650℃) K(900℃)(填“大于”,“小于”或“等于”)
②若将实验 2 中 CO 和 HO 的物质的量加倍,则平衡时 H 物质的量浓度为 mol·L-1。
2 2
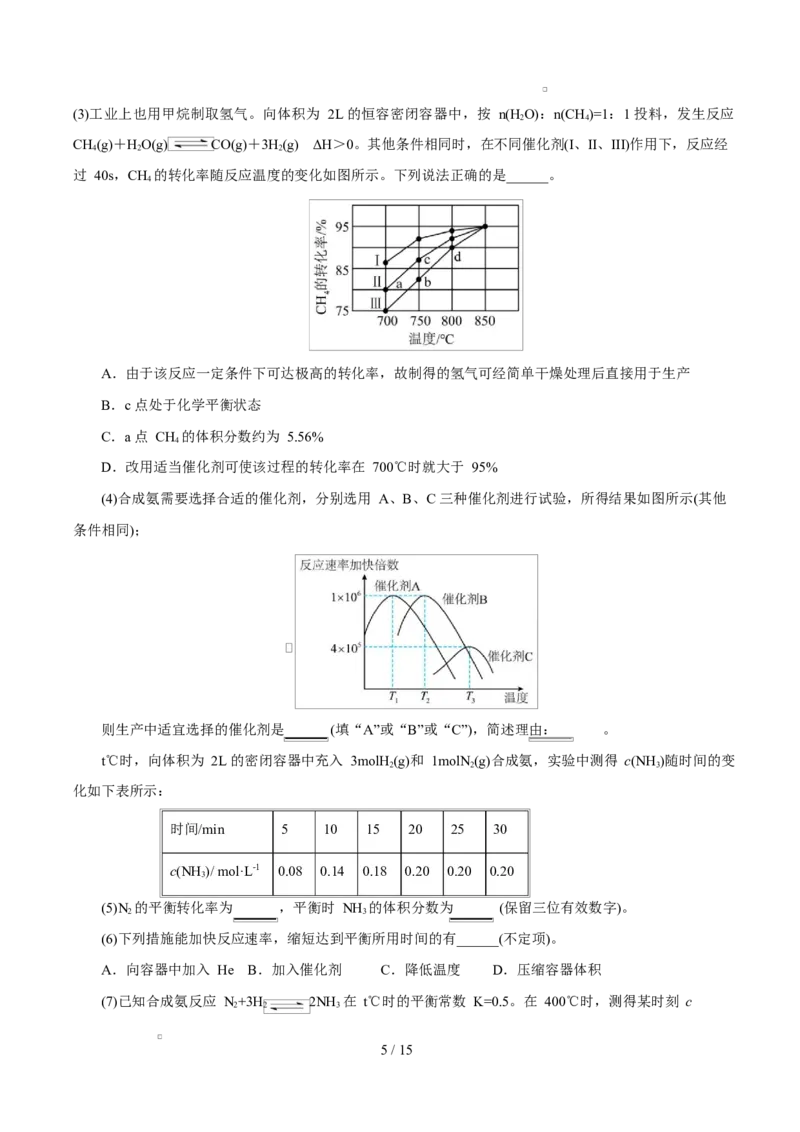
4 / 15(3)工业上也用甲烷制取氢气。向体积为 2L 的恒容密闭容器中,按 n(H O):n(CH)=1:1 投料,发生反应
2 4
CH(g)+HO(g) CO(g)+3H(g) ΔH>0。其他条件相同时,在不同催化剂(I、II、III)作用下,反应经
4 2 2
过 40s,CH 的转化率随反应温度的变化如图所示。下列说法正确的是______。
4
A.由于该反应一定条件下可达极高的转化率,故制得的氢气可经简单干燥处理后直接用于生产
B.c 点处于化学平衡状态
C.a 点 CH 的体积分数约为 5.56%
4
D.改用适当催化剂可使该过程的转化率在 700℃时就大于 95%
(4)合成氨需要选择合适的催化剂,分别选用 A、B、C 三种催化剂进行试验,所得结果如图所示(其他
条件相同);
则生产中适宜选择的催化剂是 (填“A”或“B”或“C”),简述理由: 。
t℃时,向体积为 2L 的密闭容器中充入 3molH (g)和 1molN (g)合成氨,实验中测得 c(NH )随时间的变
2 2 3
化如下表所示:
时间/min 5 10 15 20 25 30
c(NH )/ mol·L-1 0.08 0.14 0.18 0.20 0.20 0.20
3
(5)N 的平衡转化率为 ,平衡时 NH 的体积分数为 (保留三位有效数字)。
2 3
(6)下列措施能加快反应速率,缩短达到平衡所用时间的有______(不定项)。
A.向容器中加入 He B.加入催化剂 C.降低温度 D.压缩容器体积
(7)已知合成氨反应 N+3H 2NH 在 t℃时的平衡常数 K=0.5。在 400℃时,测得某时刻 c
2 2 3
5 / 15(N )=2mol·L-1 c(H )=2mol·L-1、c(NH )=mol·L-1,此时刻该反应的 v v (填“>”“=”或“<”)。
2 2 3 正 逆
(8)关于合成氨工业的说法,错误的是______。
A.可通过热交换器有效利用反应产生的热量,预热反应前的 N 和 H
2 2
B.选择 500℃左右的温度进行,可使催化剂活性好,但高温不利于提高平衡转化率
C.从合成塔中出来的气体中氨含量低,通过分离氨后,将未反应的气体循环使用,提高原料气体的利
用率
D.反应物 H 和 N 物质的量之比维持在 2.8~2.9,以便让平衡混合物中氨的含量最大
2 2
【答案】(1)不能(2 分)
(2)大于(2 分) 0.4(2 分)
(3)C(2 分)
(4)A (2 分) 催化剂效率高,且活性温度低,低温有利于平衡正向移动(2 分)
(5)20% (2 分) 11.1%(2 分)
(6)BD(2 分)
(7)< (2 分)
(8)D(2 分)
【解析】(1)①△G=△H−T△S=131.3kJ/mol−T×133.7×10-3kJ/(kmol),在低温下,该值一定是大于 0 的,
所以不能在低温下自发进行; ⋅
(2)对于 CO(g)+HO(g) CO(g)+H(g),根据题中信息 650℃氢气物质的量为 1.6mol,则二氧化
2 2 2
碳物质的量为 1.6mol,CO 物质的量为 2.4mol,水蒸气物质的量为 0.4mol,平衡常数为 K= ;
900℃氢气物质的量为 0.4mol,则二氧化碳物质的量为 0.4mol,CO 物质的量为 1.6mol,水蒸气物质的量为
0.6mol,平衡常数为 K= ,则平衡常数 K(650℃) 大于 K(900℃);
若将实验 2 中 CO 和的物质的量加倍,相当于将两个容器压缩到一个容器中,加压,平衡不移动,浓
度变为原来二倍,因此平衡时的物质的量浓度为 ;
(3)A 项,制得的氢气中有 CO 和未反应完的甲烷、水,不能只经过简单干燥直接用于生产,A 错误;B
项,c 点在 750℃,使用催化剂 I 甲烷的转化率更高,c 点一定不在化学平衡状态,B 错误;C 项,a 点时
CH 的转化率为 80%,设 n(CH)=n(HO)=1mol,转化的甲烷和水都是 0.8mol,生成 CO 为 0.8mol,HO 为
4 4 2 2
6 / 152.4mol,甲烷的体积分数为 ,C 正确;D 项,催化剂只能改变化学
反应速率,不能改变平衡移动,700℃时温度低,甲烷的转化率应该低于 850℃时的平衡转化率,D 错误;
故选 C;
(4)由图可知,使用催化剂 A 反应速率加快倍数高,且催化剂活性温度低,合成氨反应是放热反应,温
度低有利于平衡正向移动,可以提高平衡转化率,因此生产中适宜选择催化剂 A;
(5)平衡时氨气的物质的量为 0.20mol/L×2L=0.4mol,反应的 N 的物质的量为 0.2mol,反应的 H 的物质
2 2
的量为 0.6mol,N 的转化率为 ;平衡时 NH 的体积分数为
2 3
;
(6)A 项,容器体积不变加入 He,反应物和生成物浓度均不变,反应速率不变,A 不符合;B 项,加入
催化剂可以加快反应速率,缩短达到平衡所用的时间,B 符合;C 项,降低温度使反应速率减慢,C 不符合;
D 项,压缩容器的体积,增大反应物浓度,反应速率加快,可以缩短达到平衡的时间,D 符合;故选 BD;
(7)Q= >K,反应逆向进行,v < v ;
正 逆
(8)A 项,通过热交换器有效利用反应产生的热量,预热反应前的 N 和 H,可以节约能源,降低成本,
2 2
A 正确;B 项,合成氨反应是放热反应,选择 500℃左右的温度进行,可使催化剂活性好,但高温不利于提
高平衡转化率,B 正确;C 项,分离氨后,将未反应的气体循环使用,可以提高原料气体的利用率,C 正确;
D 项,反应物的物质的量之比等于方程式中系数之比时,平衡后生成物含量最高,反应物 H 和 N 物质的
2 2
量之比维持在 2.8~2.9,增加 N 的浓度,可以提高氢气的转化率,D 错误;故选 D。
2
三、砷与其重要化合物(20 分)
砷元素广泛存在于自然界,砷与其化合物被运用在农药、除草剂、杀虫剂等。
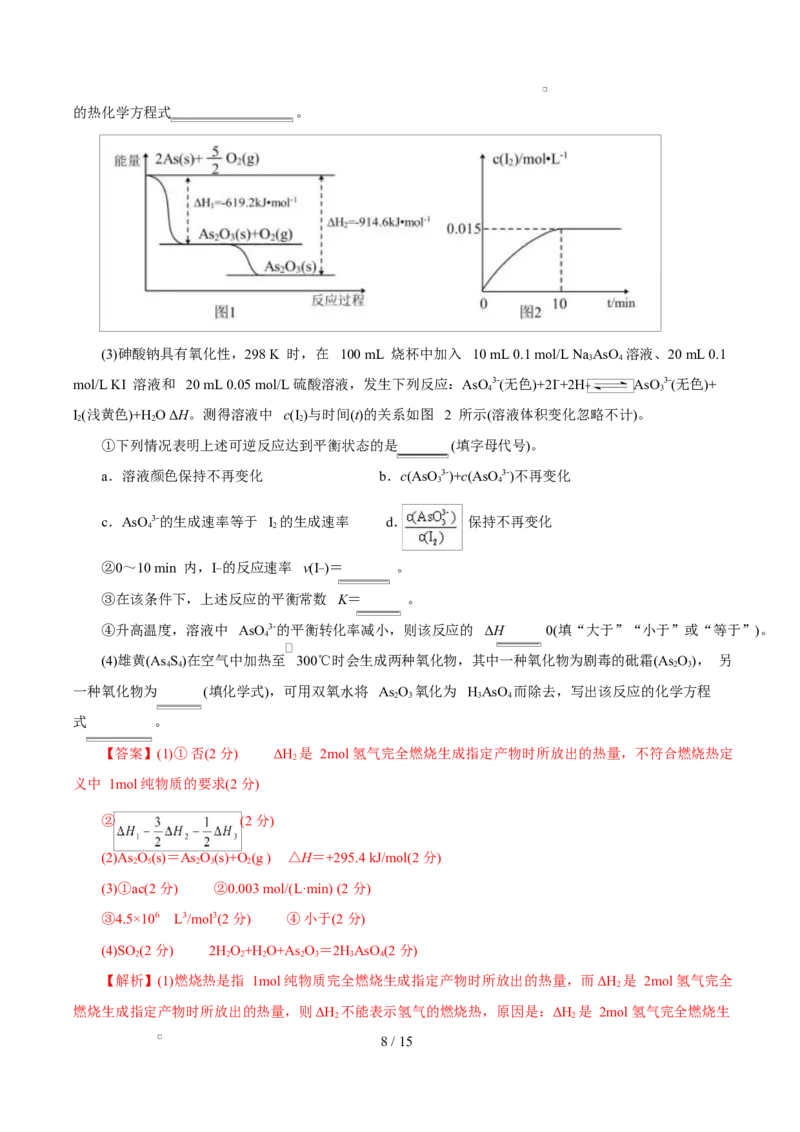
(1)已知:2As(s)+4O(g)+3H(g)=2HAsO (s) ΔH
2 2 3 4 1
2H(g)+O(g)=2HO(l) ΔH
2 2 2 2
4As(s)+5O(g)=2As O(s) ΔH
2 2 5 3
①ΔH (选填“是”或“否”)为 H 的燃烧热,原因是 。
2 2
②反应 As O(s)+ 3H O(l)=2HAsO (s)的ΔH= 。(用ΔH、ΔH、ΔH 表示)
2 5 2 3 4 1 2 3
(2)砷的常见氧化物有 As O 和 As O,其中 As O 热稳定性差。根据图 1 写出 As O 分解为 As O
2 3 2 5 2 5 2 5 2 3
的热化学方程式 。
(2)砷的常见氧化物有 As O 和 As O,其中 As O 热稳定性差。根据图 1 写出 As O 分解为 As O
2 3 2 5 2 5 2 5 2 3
7 / 15的热化学方程式 。
(3)砷酸钠具有氧化性,298 K 时,在 100 mL 烧杯中加入 10 mL 0.1 mol/L Na AsO 溶液、20 mL 0.1
3 4
mol/L KI 溶液和 20 mL 0.05 mol/L 硫酸溶液,发生下列反应:AsO
4
3-(无色)+2I-+2H+ AsO
3
3-(无色)+
I(浅黄色)+H O ΔH。测得溶液中 c(I)与时间(t)的关系如图 2 所示(溶液体积变化忽略不计)。
2 2 2
①下列情况表明上述可逆反应达到平衡状态的是 (填字母代号)。
a.溶液颜色保持不再变化 b.c(AsO3-)+c(AsO3-)不再变化
3 4
c.AsO 3-的生成速率等于 I 的生成速率 d. 保持不再变化
4 2
②0~10 min 内,I− 的反应速率 v(I−)= 。
③在该条件下,上述反应的平衡常数 K= 。
④升高温度,溶液中 AsO 3-的平衡转化率减小,则该反应的 ΔH 0(填“大于”“小于”或“等于”)。
4
(4)雄黄(As S)在空气中加热至 300℃时会生成两种氧化物,其中一种氧化物为剧毒的砒霜(As O), 另
4 4 2 3
一种氧化物为 (填化学式),可用双氧水将 As O 氧化为 HAsO 而除去,写出该反应的化学方程
2 3 3 4
式 。
【答案】(1)①否(2 分) ΔH 是 2mol 氢气完全燃烧生成指定产物时所放出的热量,不符合燃烧热定
2
义中 1mol 纯物质的要求(2 分)
② (2 分)
(2)As O(s)=As O(s)+O(g ) △H=+295.4 kJ/mol(2 分)
2 5 2 3 2
(3)①ac(2 分) ②0.003 mol/(L·min) (2 分)
③4.5×106 L3/mol3(2 分) ④小于(2 分)
(4)SO (2 分) 2HO+H O+As O=2HAsO (2 分)
2 2 2 2 2 3 3 4
【解析】(1)燃烧热是指 1mol 纯物质完全燃烧生成指定产物时所放出的热量,而ΔH 是 2mol 氢气完全
2
燃烧生成指定产物时所放出的热量,则ΔH 不能表示氢气的燃烧热,原因是:ΔH 是 2mol 氢气完全燃烧生
2 2
8 / 15成指定产物时所放出的热量,不符合燃烧热定义中 1mol 纯物质的要求;①2As(s)+4O
2
(g)+3H(g)=2HAsO (s) ΔH;②2H(g)+O(g)=2HO(l) ΔH;③4As(s)+5O(g)=2As O(s) ΔH;由
2 3 4 1 2 2 2 2 2 2 5 3
可得反应:As O(s)+ 3H O(l)=2HAsO (s),则该反应的 ;
2 5 2 3 4
(2)由图象可知,As O 分解为 As O 需要吸收的热量为-619kJ/mol-(-914.6kJ/mol) =+295.4 kJ•mol-1,则
2 5 2 3
热化学方程式 As O(s)=As O(s)+O(g) △H=+295.4 kJ•mol-1;
2 5 2 3 2
(3)①AsO
4
3-(无色)+2I-+2H+ AsO
3
3-(无色)+I
2
(浅黄色)+H
2
O。a.溶液颜色不再变化,说明碘的浓度
不变,反应达到平衡状态,故 a 正确;b.根据原子守恒可知,c(AsO3-)+c(AsO3-)始终不变,不能说明反应
3 4
达到平衡状态,故 b 错误;c.AsO 3-的生成速率等于 I 的生成速率,说明正逆反应速率相等,反应达到平
4 2
衡状态,故 c 正确;d.根据方程式,AsO 3-和 I 的物质的量相同, =1,始终保持不变,不能说明
3 2
反应达到平衡状态,故 d 错误;故选 ac;
②图 2 可知,I 浓度变化为 0.015mol/L,I-浓度变化 0.03mol/L,0-10min,v(I-)= =0.003mol/
2
(L•min);③
K═ =4.5×106 L3/mol3;④升高温度,AsO 3-的平衡转化率减小,说明平衡逆向进行,
4
正反应为放热反应,△H 小于 0;
(4)雄黄在空气中加热至 300℃时会 两种氧化物,其中的一种氧化物为剧毒的砒霜(As O),由原子守恒
2 3
可知反应为 As S+7O 2As O+4SO,另一种氧化物为二氧化硫,双氧水将 As O 氧化为 HAsO
4 4 2 2 3 2 2 3 3 4
而除去,氧化还原反应中过氧化氢中氢元素化合价-1 价变化为-2 价,As 元素化合价+3 价变化为+5 价,结
合电子守恒和原子守恒写出该反应的化学方程式为 2HO+H O+As O=2H AsO 。
2 2 2 2 3 3 4
四、钼及其化合物(20 分)
MoS 可用于制取钼的化合物、润滑添加剂、氢化反应和异构化反应的催化剂等。
2
已知反应:
①MoS (s) Mo(s)+S(g) ΔH ②MoO (s) +3H (g) Mo(s)+3HO(g) ΔH
2 2 1 3 2 2 2
③S(g)+2O(g) 2SO (g) ΔH ④2H(g)+O(g) 2HO(g) ΔH
2 2 2 3 2 2 2 4
(1) 的原子序数为 42,下列相关描述正确的是_______(不定项)。
9 / 15A.位于第六周期 B.属于 族 C.核外单电子 6 个 D.属于过渡金属
(2)MoS 纳米粒子具有类似于石墨的层状结构,具有优异的润滑性能,原因是 。
2
(3)2MoS (s)+7O(g) 2MoO (s)+4SO (g)的ΔH= (用含ΔH、ΔH、ΔH、ΔH 的代数式表示)。
2 2 3 2 1 2 3 4
恒温恒容条件下,仅发生反应 MoO (s) +3H (g) Mo(s)+3HO(g) ΔH>0
3 2 2
该反应的速率表达式为 和 ,测得 和浓度的关系如下表:
c(H )/ mol·L-1 v (mol·L-1·s-1)
2 正
1 0.2 1.2×10-8
2 0.4 9.6×10-8
3 0.6 3.24×10-7
(4)下列说法正确的是_______。(不定项)
A.当 n(H ):n(H O)不再变化,说明反应达到了平衡状态
2 2
B.平衡后,再通入 H,平衡正向移动,H 的转化率升高
2 2
C.该反应的活化能
D.移走 Mo,反应速率减慢,平衡正向移动
(5)n=_______。
A.1 B.2 C.3 D.4
(6)该温度下,平衡时 的体积分数为 20%,则 。
A.> B.< C.=
该温度下,向某恒容密闭容器中充入 1.5molH 和 1.5mol H O(g),此时反应 进行。
2 2
A.正向 B.逆向
(7)该反应分两步进行:
第 I 步 MoO (s) +H (g) MoO (s)+HO(g) ΔH
3 2 2 2 5
第Ⅱ步 MoO (s) +2H (g) Mo(s)+2HO(g) ΔH
2 2 2 6
其反应过程能量变化示意图如图所示,决定该反应速率的步骤是 。
10 / 15A.I B.Ⅱ
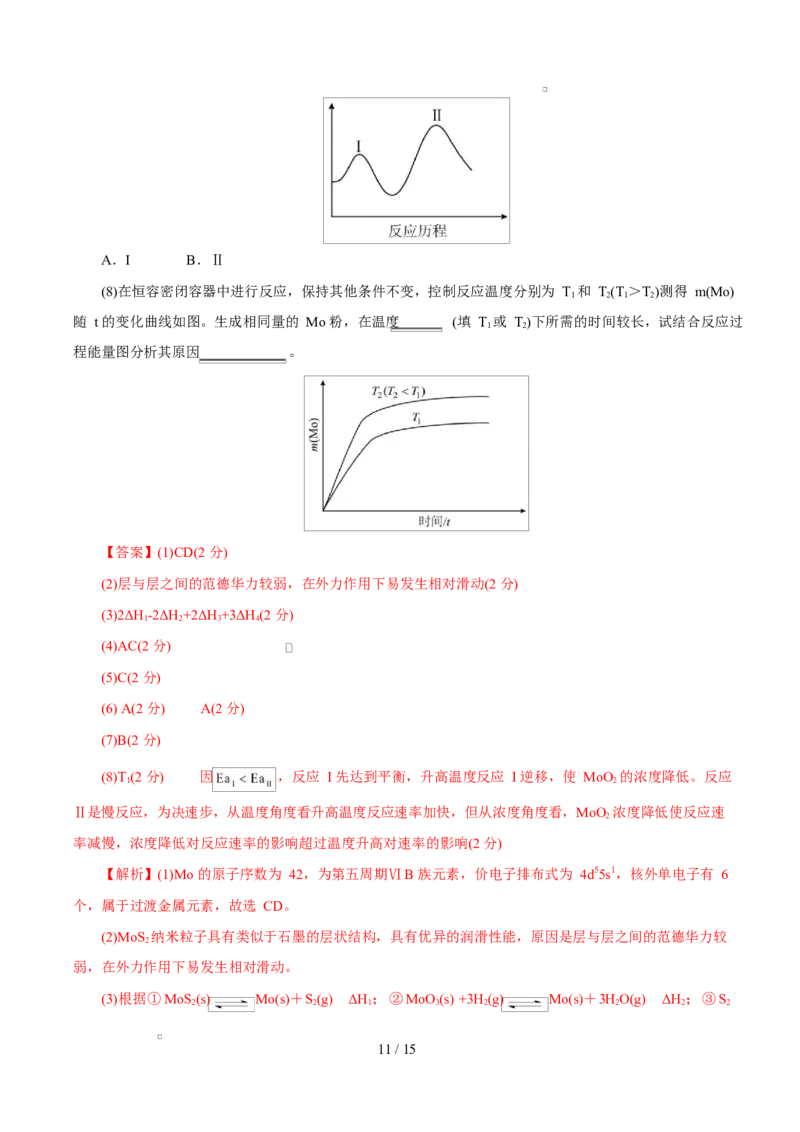
(8)在恒容密闭容器中进行反应,保持其他条件不变,控制反应温度分别为 T 和 T(T >T)测得 m(Mo)
1 2 1 2
随 t 的变化曲线如图。生成相同量的 Mo 粉,在温度 (填 T 或 T)下所需的时间较长,试结合反应过
1 2
程能量图分析其原因 。
【答案】(1)CD(2 分)
(2)层与层之间的范德华力较弱,在外力作用下易发生相对滑动(2 分)
(3)2ΔH -2ΔH +2ΔH +3ΔH (2 分)
1 2 3 4
(4)AC(2 分)
(5)C(2 分)
(6) A(2 分) A(2 分)
(7)B(2 分)
(8)T (2 分) 因 ,反应 I 先达到平衡,升高温度反应 I 逆移,使 MoO 的浓度降低。反应
1 2
Ⅱ是慢反应,为决速步,从温度角度看升高温度反应速率加快,但从浓度角度看,MoO 浓度降低使反应速
2
率减慢,浓度降低对反应速率的影响超过温度升高对速率的影响(2 分)
【解析】(1)Mo 的原子序数为 42,为第五周期ⅥB 族元素,价电子排布式为 4d55s1,核外单电子有 6
个,属于过渡金属元素,故选 CD。
(2)MoS 纳米粒子具有类似于石墨的层状结构,具有优异的润滑性能,原因是层与层之间的范德华力较
2
弱,在外力作用下易发生相对滑动。
(3)根据①MoS (s) Mo(s)+S(g) ΔH;②MoO (s) +3H (g) Mo(s)+3HO(g) ΔH;③S
2 2 1 3 2 2 2 2
11 / 15(g)+2O(g) 2SO (g) ΔH;④2H(g)+O(g) 2HO(g) ΔH;由盖斯定律 2×①-2×②+2×③+3×
2 2 3 2 2 2 4
④可得 2MoS (s)+7O(g) 2MoO (s)+4SO (g)的ΔH=2ΔH-2ΔH +2ΔH +3ΔH 。
2 2 3 2 1 2 3 4
(4)A 项,当 n(H ):n(H O)不再变化,说明其浓度不变,反应达到了平衡状态,A 正确;B 项,平衡后,
2 2
再通入 H,平衡正向移动,但是 H 的转化率不变,B 错误;C 项,该反应为吸热反应,活化能
2 2
,C 正确;D 项,Mo 为固体,移走 Mo,不影响反应速率,平衡不移动,D 错误;故选 AC。
(5)由表格数据, ,解得 n=3,故选 C。
(6)该温度下,平衡时 H 的体积分数为 20%,则 HO 体积分数为 80%,氢气和 HO 浓度比为 1:4,则
2 2 2
, > ,故选 A;该温度下,向某恒容密闭容器中充入 1.5molH 和 1.5mol
2
HO(g),Q=1<64,未达到平衡,此时反应正向进行,故选 A。
2
(7)活化能大的步骤为决速步骤,第Ⅱ步的活化能大于第 I 步,反应Ⅱ是慢反应,决定该反应速率的步
骤是Ⅱ,故选 B。
(8)由图可知,生成相同量的 Mo 粉,在温度 T 下所需的时间较长,结合反应过程能量图,分析其原因
1
为:因 ,反应 I 先达到平衡,升高温度反应 I 逆移,使 MoO 的浓度降低。反应Ⅱ是慢反应,为
2
决速步,从温度角度看升高温度反应速率加快,但从浓度角度看,MoO 浓度降低使反应速率减慢,浓度降
2
低对反应速率的影响超过温度升高对速率的影响。
五、合成尿素(18 分)
尿素[CO(NH)]是首个由无机物(氨气和二氧化碳)人工合成的有机物,由此,打破了无机物和有机物的
2 2
界限。以下图装置,利用浓氨水与生石灰反应制备少量氨气。
(1)盛放浓氨水的仪器名称为 。
A.恒压滴液漏斗 B.冷凝管 C.分液漏斗 D.容量瓶
(2)选取该仪器盛放浓氨水的优点为 。
12 / 15(3)尿素和丙醇的相对分子质量相同,但是,在常温常压下,尿素呈固态,丙醇呈液态,其主要原因
是 。
氨气和二氧化碳合成尿素的反应原理为:2NH (g)+CO(g) CO(NH)(s)+HO(l) ΔH<0。
3 2 2 2 2
(4)该反应在 条件下可自发进行。
A.低温 B.高温 C.任意温度
研究发现,上述反应分两步完成:
反应Ⅰ:2NH (g)+CO(g) 2NH COONH(s) ΔH<0
3 2 2 4 1
反应Ⅱ:2NH COONH(s) CO(NH)(s)+HO(l) ΔH>0
2 4 2 2 2 2
(5)下图中能正确表示尿素合成过程中能量变化的曲线是 。
A. B. C. .
(6)下列说法正确的是 (不定项)。
A.NH COONH 为合成尿素反应的中间产物
2 4
B.恒压,降低氨碳比 ,反应Ⅰ中 的平衡转化率会降低
C.反应Ⅰ是吸热反应,反应Ⅱ是放热反应
D.平衡后移走产物 CO(NH),平衡会向正反应方向移动
2 2
(7)若向某恒温恒容的密闭容器中加入等物质的量 NH 和 CO 合成尿素,下列能说明反应已经达到平衡
3 2
状态的是 (不定项)。
A.CO 的体积分数不再变化 B.化学平衡常数 K 不变
2
C.2v (NH )=v (CO) D.体系中气体的密度不变
正 3 逆 2
(8)向上题平衡后体系中,保持温度和容器体积不变,再充入 1molNH 和 1molCO ,达到新平衡时,CO
3 2 2
平衡转化率将 。
A.增大 B.减小 C.不变
研究发现尿素 CO(NH) 水溶液吸收氮氧化物是一种减少大气污染物的方法。反应原理为:NO+NO +
2 2 2
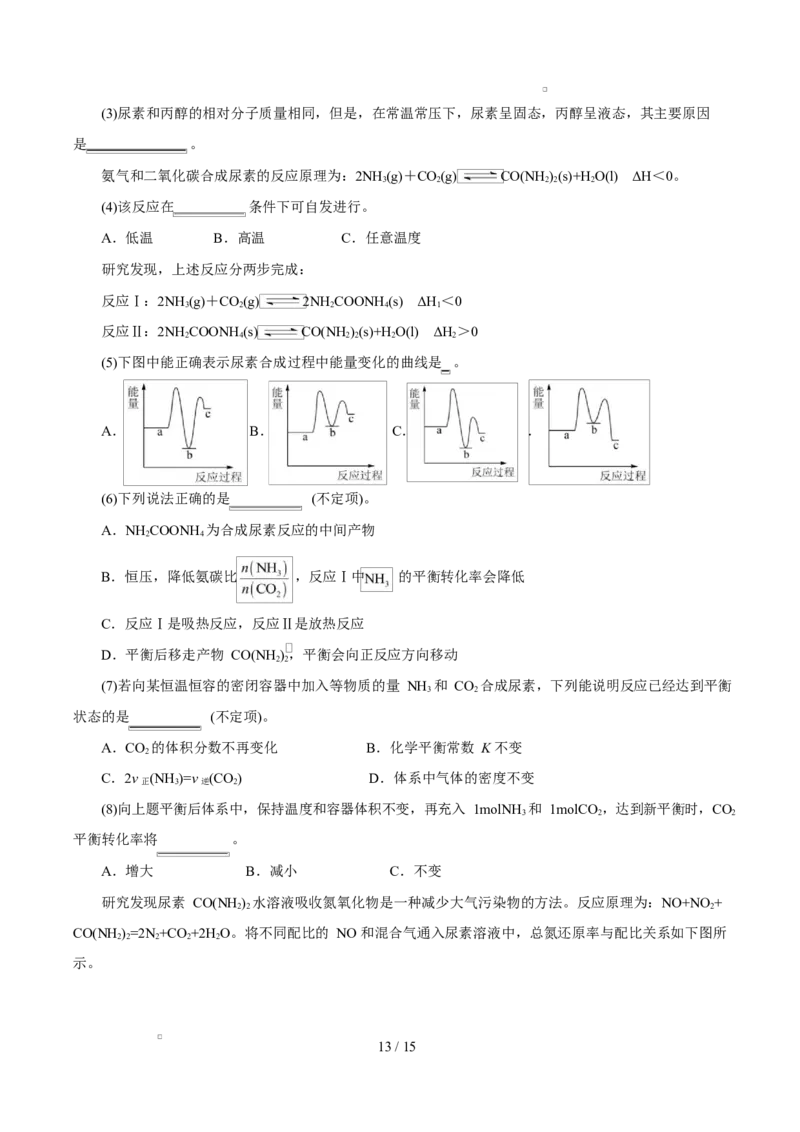
CO(NH)=2N +CO +2H O。将不同配比的 NO 和混合气通入尿素溶液中,总氮还原率与配比关系如下图所
2 2 2 2 2
示。
13 / 15(9)随 NO 和 NO 比例的提高,总氮还原率降低的主要原因是 。
2
【答案】(1)A(2 分)
(2)能够平衡气压,便于液体顺利流下(2 分)
(3)尿素分子中有两个-NH ,比丙醇的分子间氢键更强,熔点更高(2 分)
2
(4)A(2 分)
(5)C(2 分)
(6)A(2 分)
(7)AD(2 分)
(8)A(2 分)
(9)NO 难溶于水,难与尿素接触反应,未参与反应的 NO 增多,总氮还原率降低(2 分)
【解析】浓氨水滴入生石灰上,利用生石灰的吸水性,同时放出热量,促使氨气的挥发,制取氨气,
恒压滴液漏斗能够平衡压强,保证溶液顺利流下。
(1)盛放浓氨水的仪器名称为:恒压滴液漏斗,故选 A;
(2)该仪器盛放浓氨水的优点为:能够平衡压强,便于液体顺利流下;
(3)尿素和丙醇都是分子晶体,尿素分子中有两个-NH ,比丙醇的分子间氢键更多、更强,分子间作用
2
力尿素大于丙醇,熔点高于丙醇;
(4)反应 2NH (g)+CO(g) CO(NH)(s)+HO(l) ΔH<0,△S<0,自发进行的条件是△G=△H-T△
3 2 2 2 2
S<0,低温下可以自发进行,故选 A;
(5)反应Ⅰ:2NH (g)+CO(g) 2NH COONH(s) ΔH<0 为放热反应;
3 2 2 4 1
反应Ⅱ:2NH COONH(s) CO(NH)(s)+HO(l) ΔH>0 为吸热反应;
2 4 2 2 2 2
总反应:2NH (g)+CO(g) CO(NH)(s)+HO(l) ΔH<0 为放热反应;
3 2 2 2 2
放热反应是反应物能量高于生成物能量,吸热反应是反应物能量低于生成物能量。
A 项,总反应为吸热反应,不符合;B 项,总反应为吸热反应,不符合;C 项,第一步放热反应,第二
步吸热反应,总反应为放热反应,C 符合;D 项,第一步是吸热反应,第二步是放热反应,总反应是放热
14 / 15反应,D 不符合;故选 C;
(6)A 项,根据反应Ⅰ:2NH (g)+CO(g) 2NH COONH(s) ΔH<0;反应Ⅱ:2NH COONH(s)
3 2 2 4 1 2 4
CO(NH)(s)+HO(l) ΔH>0;可知,NH COONH 为合成尿素反应的中间产物,A 正确;B 项,恒
2 2 2 2 2 4
压,降低氨碳比 ,CO 的物质的量增加,反应Ⅰ中 NH 的平衡转化率会升高,B 错误;C 项,反
2 3
应ⅠΔH<0 是放热反应,反应ⅡΔH>0 是吸热反应,C 错误;D 项,CO(NH) 是固体,改变固体的量。
1 2 2 2
平衡不移动,D 错误;故选 A;
(7)A 项,体系中各反应物或生成物的体积分数不再变化,说明反应达到平衡状态,CO 的体积分数不再变
2
化,说明反应达到平衡状态,A 符合;B 项,温度不变,化学平衡常数 K 不变,K 值不变,反应不一定是
平衡状态,B 不符合;C 项,速率之比等于方程式中系数之比,v (NH )=2v (CO)时,反应达到平衡状态,
正 3 逆 2
C 不符合;D 项,尿素是固体,反应过程中体系中气体的密度为变量,当体系中气体的密度不变,说明反
应达到平衡状态,D 符合;故选 AD;
(8)保持温度和容器体积不变,再充入 1molNH 和 1mol CO,相当于增大压强,平衡正向移动,达到新
3 2
平衡时,CO 平衡转化率将增大,故选 A;
2
(9)NO 难溶于水,难与尿素接触反应,随 NO 和 NO 比例的提高,未参与反应的 NO 增多,总氮还原
2
率降低。
15 / 15