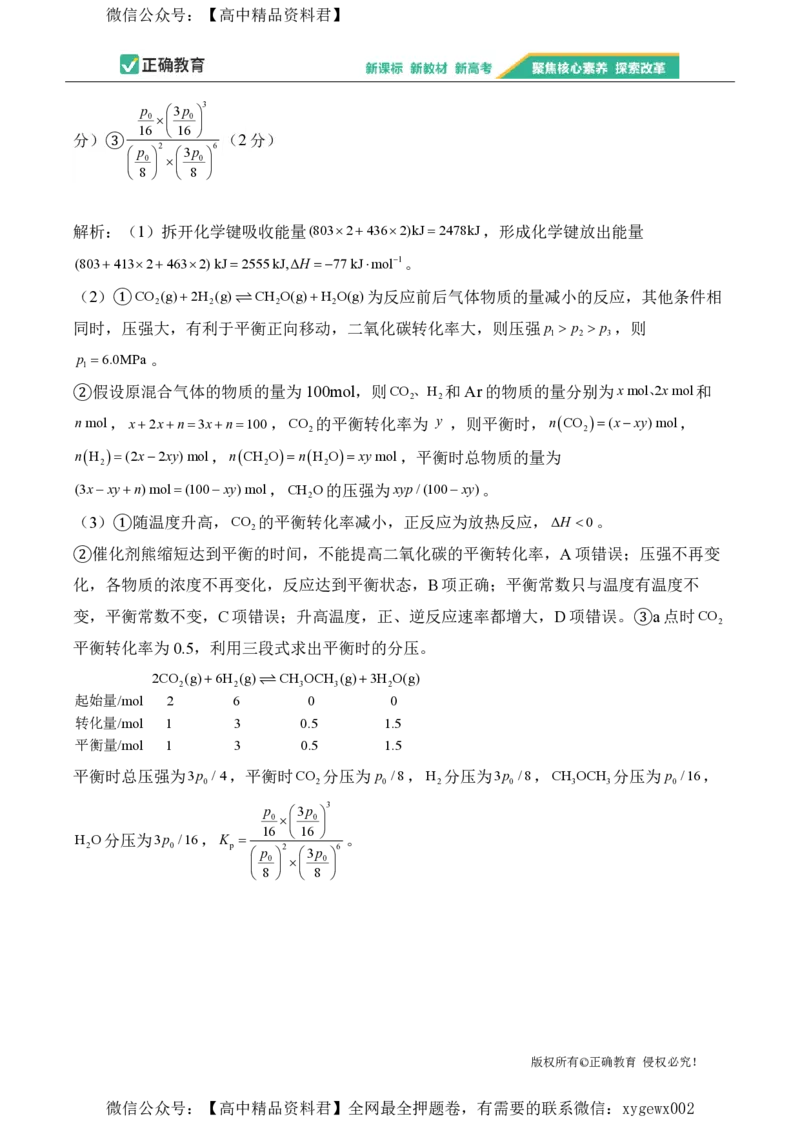文档内容
微信公众号:【高中精品资料君】
2024 届明日之星高考化学精英模拟卷 【湖北版】
可能用到的相对原子质量:C-12、O-16、Mn-55
一、单项选择题:本题共 15 小题,每小题 3 分,共 45 分。在每小题给出的四个选项中,只
有一项是符合题目要求的。
1.化学渗透在社会生活的各个方面。下列叙述正确的是( )
A.核辐射废水中氘含量较高,氚是氢的一种放射性同位素
B.微粒直径为1~100 nm的物质,具有丁达尔效应
C.我国自主研发的大丝束碳纤维被称为“新材料之王”,碳纤维属于有机高分子材料
D.煤的液化、蛋白质的颜色反应、焰色试验都涉及化学变化
2.根据元素周期律和元素周期表,下列推断合理的是( )
A.价电子排布式为2s2和3s23p5的两原子能形成离子化合物
B.与K同周期且基态原子未成对电子数相同的元素还有 4种
C.第84号元素的最高化合价是+7
D.同一周期中,ⅡA与ⅢA族元素原子的核电荷数都相差1
3.湖北随州出土的曾侯乙编钟是迄今发现的最完整、最大、保存最好的一套青铜编钟。铜锈
(俗称铜绿)在一定程度上能提升青铜器的艺术价值,铜锈成分复杂,考古学家将铜锈分为
有害锈和无害锈,原理如图所示。下列说法正确的是( )
A.青铜比纯铜的熔点高
B.Cu (OH) CO 属于无害锈,可以保护青铜器
2 2 3
C.埋在地下的青铜器中的Cu可能发生吸氧腐蚀和析氢腐蚀
D.黄铜矿经冶炼可以直接得到纯度为99.9%的铜
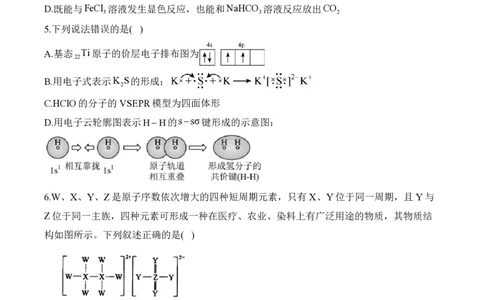
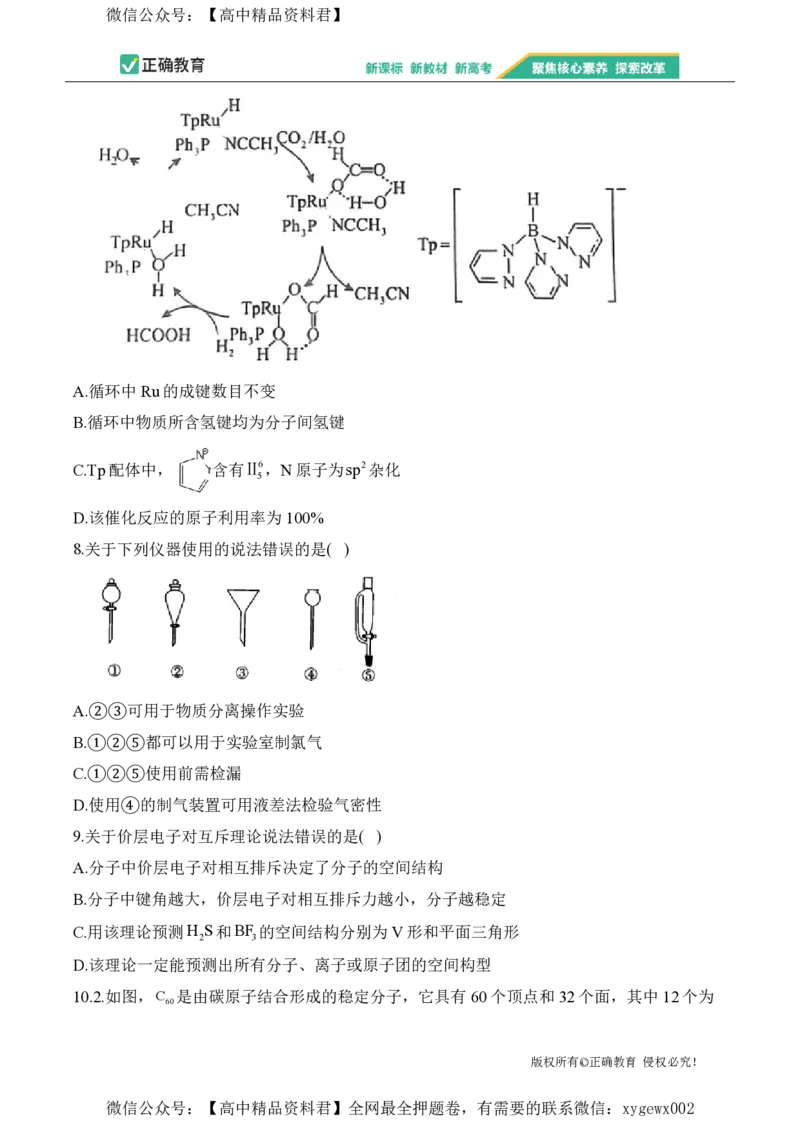
4.我国科研人员发现中药有效成分W能明显抑制新冠病毒的活性,其结构简式如图所示。下
列关于中药有效成分W的说法错误的是( )
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
A.W分子中含有三种含氧官能团
B.1 mol W最多能与4 mol NaOH反应
C.W的分子式是C H O ,含有一个手性碳原子
19 18 7
D.既能与FeCl 溶液发生显色反应,也能和NaHCO 溶液反应放出CO
3 3 2
5.下列说法错误的是( )
A.基态 Ti原子的价层电子排布图为
22
B.用电子式表示K S的形成:
2
C.HClO的分子的 VSEPR模型为四面体形
D.用电子云轮廓图表示HH的ssσ键形成的示意图:
6.W、X、Y、Z是原子序数依次增大的四种短周期元素,只有 X、Y位于同一周期,且Y与
Z位于同一主族,四种元素可形成一种在医疗、农业、染料上有广泛用途的物质,其物质结
构如图所示。下列叙述正确的是( )
A.原子半径:Z>Y>X>W
B.等物质的量浓度的X和Z的含氧酸的酸性:Z>X
C.W、X、Z均可与Y形成多种化合物
D.简单氢化物的还原性:Y>Z
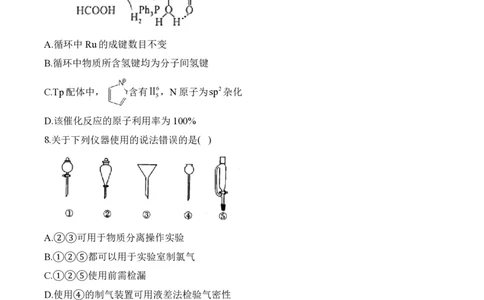
7.含Tp配体的钉(Ru)配合物催化氢化CO 生成甲酸的机理如图所示。下列叙述错误的是
2
( )
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
A.循环中Ru的成键数目不变
B.循环中物质所含氢键均为分子间氢键
C.Tp配体中, 含有Ⅱ6,N原子为sp2杂化
5
D.该催化反应的原子利用率为100%
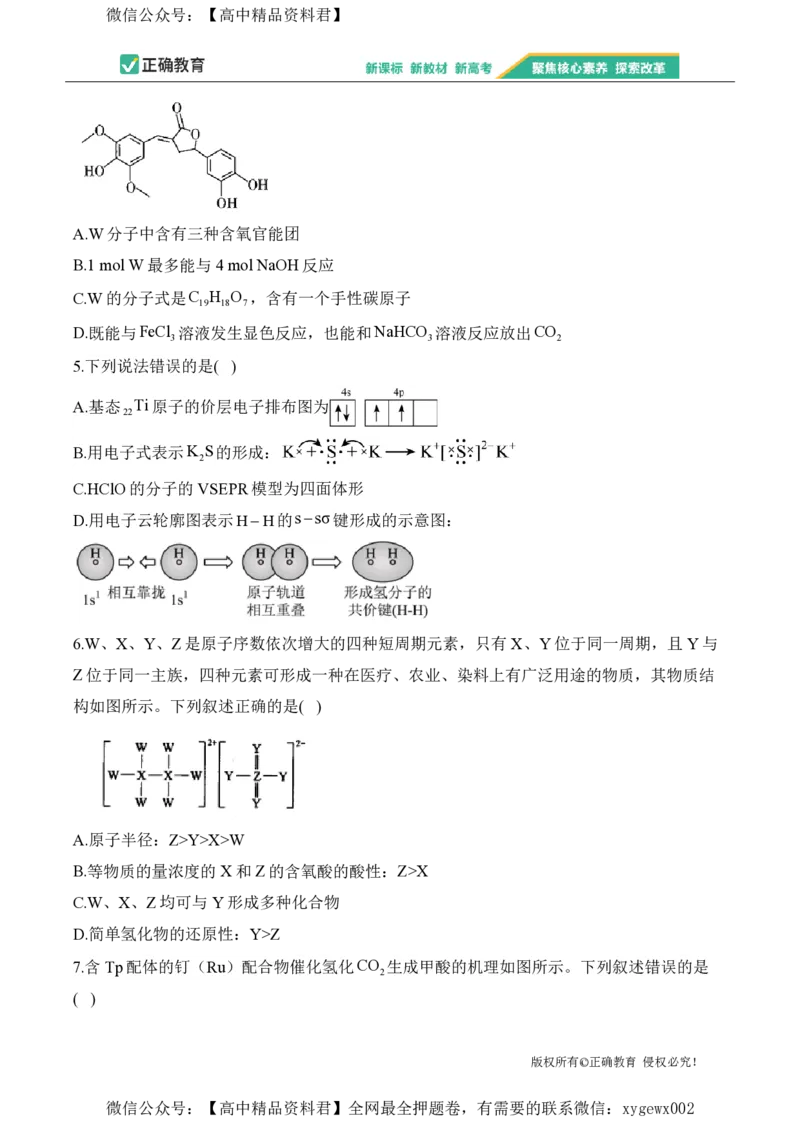
8.关于下列仪器使用的说法错误的是( )
A.②③可用于物质分离操作实验
B.①②⑤都可以用于实验室制氯气
C.①②⑤使用前需检漏
D.使用④的制气装置可用液差法检验气密性
9.关于价层电子对互斥理论说法错误的是( )
A.分子中价层电子对相互排斥决定了分子的空间结构
B.分子中键角越大,价层电子对相互排斥力越小,分子越稳定
C.用该理论预测H S和BF 的空间结构分别为V形和平面三角形
2 3
D.该理论一定能预测出所有分子、离子或原子团的空间构型
10.2.如图,C 是由碳原子结合形成的稳定分子,它具有60个顶点和32个面,其中12个为
60
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
正五边,20个为正六边形。科研人员用电子计算机模拟出类似C 的新物质N ,下列有关 N
60 60
篚叙述正确的是()
A.N 分子中含有键和π键
60
B.N 属于原子晶体
60
C.N 分子是非极性分子
60
D.N 的熔点比C 的低
60 60
11.燃料电池近几年发展迅速,如图是科学家利用页岩气设计的一种固态(熔盐)燃料电池工
作示意图。下列说法错误的是( )
A.电极材料采用石墨烯,吸附甲烷的电极为负极,发生氧化反应
B.通入氧气的电极上电极反应式为O 2CO 4e 2CO2
2 2 3
C.电池工作时,CO2向通甲烷的电极一侧移动
3
D.该电池的优点是二氧化碳可循环利用,不会释放温室气体
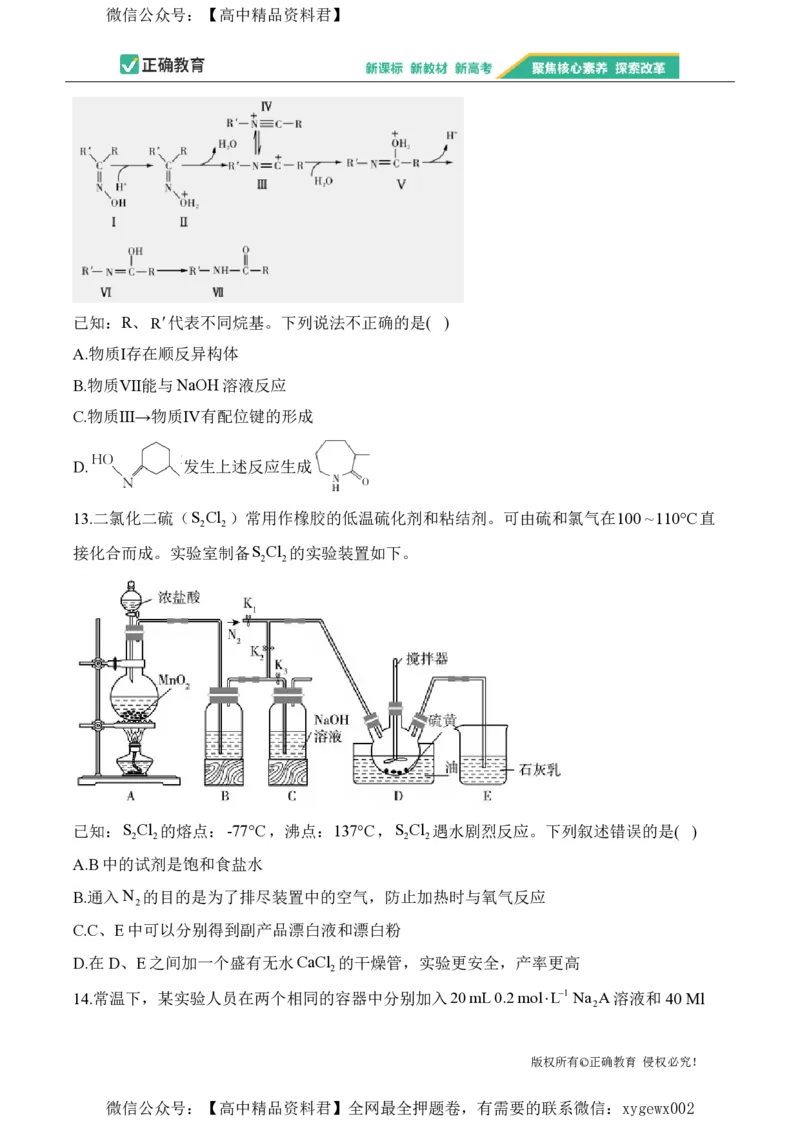
12.Beckmann重排是酮肟在一定条件下生成酰胺的反应,机理中与羟基处于反位的基团迁移
到缺电子的氮原子上,具体反应历程如图所示:
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
已知:R、R代表不同烷基。下列说法不正确的是( )
A.物质Ⅰ存在顺反异构体
B.物质Ⅶ能与NaOH溶液反应
C.物质Ⅲ→物质Ⅳ有配位键的形成
D. 发生上述反应生成
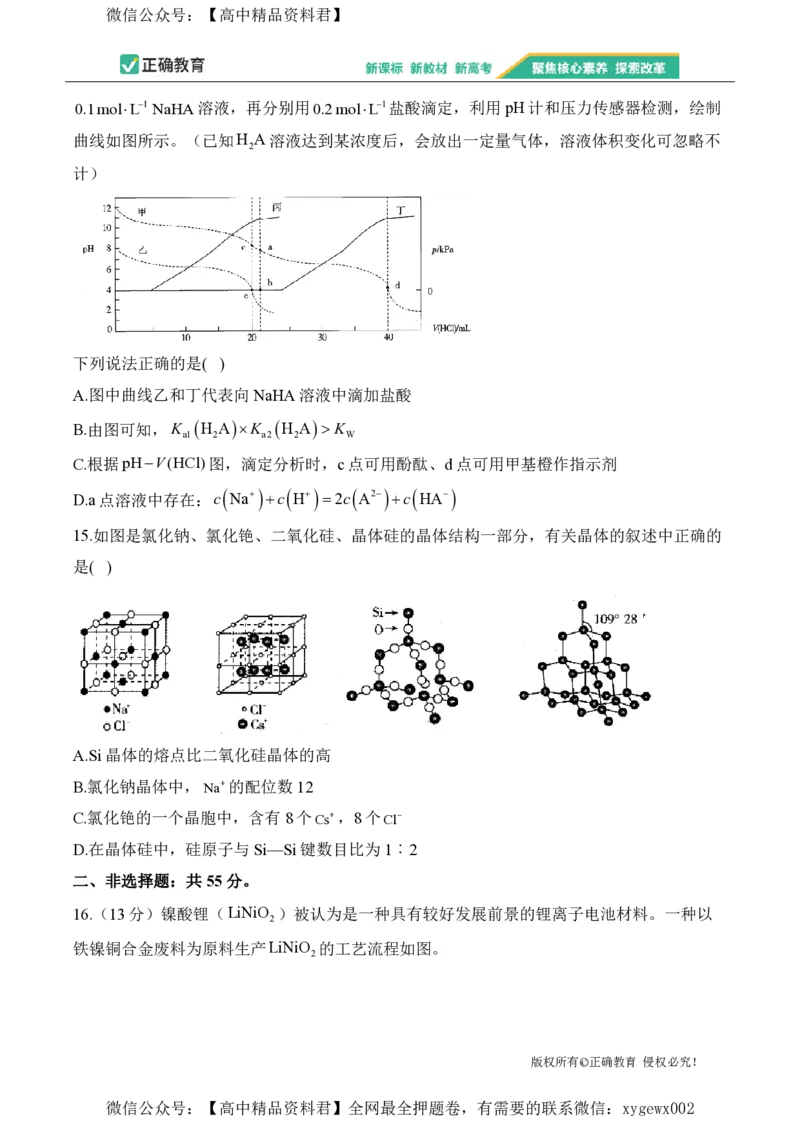
13.二氯化二硫(S Cl )常用作橡胶的低温硫化剂和粘结剂。可由硫和氯气在100~110C直
2 2
接化合而成。实验室制备S Cl 的实验装置如下。
2 2
已知:S Cl 的熔点:-77C,沸点:137C,S Cl 遇水剧烈反应。下列叙述错误的是( )
2 2 2 2
A.B中的试剂是饱和食盐水
B.通入N 的目的是为了排尽装置中的空气,防止加热时与氧气反应
2
C.C、E中可以分别得到副产品漂白液和漂白粉
D.在D、E之间加一个盛有无水CaCl 的干燥管,实验更安全,产率更高
2
14.常温下,某实验人员在两个相同的容器中分别加入20mL0.2 molL1 Na A溶液和40 Ml
2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
0.1 molL1 NaHA溶液,再分别用0.2 molL1盐酸滴定,利用 pH计和压力传感器检测,绘制
曲线如图所示。(已知H A溶液达到某浓度后,会放出一定量气体,溶液体积变化可忽略不
2
计)
下列说法正确的是( )
A.图中曲线乙和丁代表向NaHA溶液中滴加盐酸
B.由图可知,K H AK H A K
a1 2 a2 2 W
C.根据pHV(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂
D.a点溶液中存在:c
Na
c
H
2c
A2
c
HA
15.如图是氯化钠、氯化铯、二氧化硅、晶体硅的晶体结构一部分,有关晶体的叙述中正确的
是( )
A.Si晶体的熔点比二氧化硅晶体的高
B.氯化钠晶体中,Na+的配位数12
C.氯化铯的一个晶胞中,含有8个Cs+,8个Cl
D.在晶体硅中,硅原子与Si—Si键数目比为1︰2
二、非选择题:共 55 分。
16.(13分)镍酸锂(LiNiO )被认为是一种具有较好发展前景的锂离子电池材料。一种以
2
铁镍铜合金废料为原料生产LiNiO 的工艺流程如图。
2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
已知:①K Ni(OH) 21015,K Fe(OH) 41038,K Cu(OH) 51020,
sp 2 sp 3 sp 2
K (CuS)1.01036,K (NiS)1.01021,K (FeS)6.31018;lg20.3。
sp sp sp
②常温下,有关金属阳离子开始沉淀和沉淀完全的pH如表。
金属阳离子 Fe3 Fe2 Cu2 Ni2
开始沉淀的pH 2.2 5.8 4.2 6.7
沉淀完全
(
x 8.8 7.7 9.3
c1.0105 molL1
)的pH
回答下列问题:
(1)“酸溶”后,废料中的铁、镍和铜完全溶于混酸中,所得溶液中的溶质为
Fe SO 、FeSO 、NiSO 、CuSO 及过量的H SO ,则尾气的主要成分为_________。
2 4 3 4 4 4 2 4
(2)“氧化”是将“酸溶”后溶液中的少量Fe2氧化,适当升高温度会加快“氧化”速率,但温度
高于60 ℃时,“氧化”速率会降低,其原因为___________。
(3)“除铁”后滤渣的主要成分为__________(写化学式),表格中的x_____。
(4)“沉铜”时,加入的试剂X可能为________(填字母)。
a.NaOH溶液 b.H S气体 c.Na S溶液 d.FeS
2 2
(5)“沉镍”析出NiCO 沉淀,则滤液中的溶质主要为_______(填化学式);在空气中“煅
3
烧”的化学方程式为______。
(6)若1.0 t铁镍铜合金废料(含镍质量分数为59.0%)经过上述流程制得0.88tLiNiO ,则
2
LiNiO 的产率为_______%(结果保留3位有效数字)。
2
17.(14分)奥昔布宁是具有解痉和抗胆碱作用的药物,G是合成奥昔布宁的中间体。G的一
种合成路线如图。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
已知:
回答下列问题:
(1)A是芳香族化合物,其名称为___________。
(2)B的结构简式是___________,B→C的反应类型是___________。
(3)G中官能团的名称为___________。
(4)E→F的化学方程式是___________。
(5)同时满足下列条件的F的同分异构体有___________种,其中核磁共振氢谱有5组峰的
结构简式为___________。(不考虑立体异构)
①能与FeCl 溶液发生显色反应;
3
②能与碳酸氢钠溶液反应;
③分子中除苯环外不含其他的环。
(6)补充完整由苯乙烯合成E的合成路线 _________(其他无机试剂
任选)。
18.(14分)高纯碳酸锰广泛应用于电子工业,是制备高性能磁性材料的原料。某化学小组在
实验室模拟用软锰矿粉(主要成分为MnO )制备MnCO 回答下列问题:
2 3
(1)制备MnSO 溶液:将mg 软锰矿粉经除杂后制得MnO 浊液,向MnO 浊液中通入
4 2 2
SO ,制得MnSO 溶液,实验装置如图所示(夹持和加热装置略)。
2 4
①通过装置A可观察通入SO ,与N 的快慢,则 A中加入的最佳试剂是_________。
2 2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
②MnO 转化为MnO 的离子方程式为___________。
2 2
③实验中若将N 换成空气,将导致SO2浓度明显大于Mn2浓度,原因是___________。
2 4
(2)制备MnCO 固体:在搅拌下向MnSO 溶液中缓慢滴加NH HCO 溶液,有浅红色的沉
3 4 4 3
淀生成,过滤、洗涤、干燥,得到高纯碳酸锰。生成MnCO 的离子方程式为___________。
3
检验沉淀是否洗涤干净的方法是___________。
(3)测定碳酸锰产品的纯度:称取0.2500 g碳酸锰产品于锥形瓶中,加12.50 L磷酸,加热
后,立即加入1 g硝酸铵,充分反应后,碳酸锰全部转化为MnPO 3 ,多余的硝酸铵全
4 2
部分解,除去氮氧化物后,冷却至室温。将上述所得溶液加水稀释至50 mL,滴加2~3滴指
示剂,然后用0.2000 molL1的硫酸亚铁铵
NH
4
2
FeSO
4
2
标准溶液滴定[反应为
MnPO 3 Fe2 Mn2 Fe3 2PO3 ]。重复操作3次,记录数据如表:
4 2 4
0.2000 molL1硫酸亚铁铵标准溶液读数(mL)
滴定次数
滴定前 滴定后
1 0.10 10.20
2 0.22 11.32
3 1.05 10.95
则产品的纯度为__________。若滴定终点时俯视读数,则测得的碳酸锰产品的纯度
__________(填“偏高”“偏低”或“无影响”)。
19.(14分)二氧化碳的大量排放,严重破坏了地球环境,合理利用二氧化碳造福人类成为科
学家研究的热点。请回答下列问题:
(1)在催化剂作用下,二氧化碳发生反应:CO (g)2H (g) CH O(g)H O(g)。已知几种化
2 2 2 2
学键的键能如表所示,则该反应的ΔH ________________kJ mol1。
化学键 C=O H一H C一H O一H
键能
803 436 413 463
kJ
mol1
(2)①将一定量的CO (g)、H (g)和N (g)的混合气体通入到一定体积的密闭容器中发生反应
2 2 2
CO (g)2H (g) CH O(g)H O(g),在1.0MPa、3.0MPa和6.0MPa压强下,CO 平衡转化率
2 2 2 2 2
α随温度 T 的变化如图所示。则压强 p ________________,判断的依据是
1
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
________________。
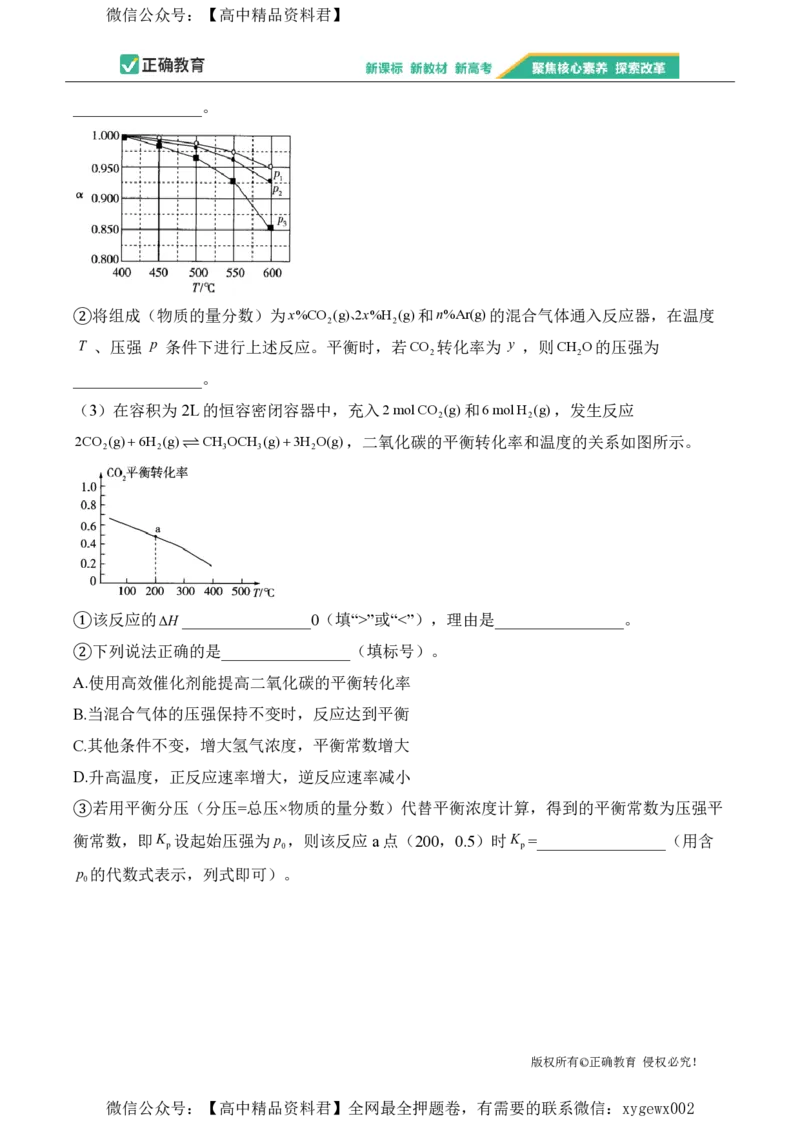
②将组成(物质的量分数)为x%CO (g)、2x%H (g)和n%Ar(g)的混合气体通入反应器,在温度
2 2
T 、压强 p 条件下进行上述反应。平衡时,若CO 转化率为 y ,则CH O的压强为
2 2
________________。
(3)在容积为2L的恒容密闭容器中,充入2molCO (g)和6molH (g),发生反应
2 2
2CO (g)6H (g) CH OCH (g)3H O(g),二氧化碳的平衡转化率和温度的关系如图所示。
2 2 3 3 2
①该反应的ΔH________________0(填“>”或“<”),理由是________________。
②下列说法正确的是________________(填标号)。
A.使用高效催化剂能提高二氧化碳的平衡转化率
B.当混合气体的压强保持不变时,反应达到平衡
C.其他条件不变,增大氢气浓度,平衡常数增大
D.升高温度,正反应速率增大,逆反应速率减小
③若用平衡分压(分压=总压×物质的量分数)代替平衡浓度计算,得到的平衡常数为压强平
衡常数,即K 设起始压强为 p ,则该反应 a点(200,0.5)时K =________________(用含
p 0 p
p 的代数式表示,列式即可)。
0
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
答案以及解析
1.答案:A
解析:氚(3H)是氢的一种放射性同位素,A项正确;微粒直径为 1~100 nm的物质可能为
纯净物,不一定是胶体,B项错误;碳纤维的主要成分是碳单质,不属于有机高分子材料,
C项错误;煤的液化、蛋白质的颜色反应属于化学变化,焰色试验属于物理变化,D项错
误。
2.答案:B
解析:价电子排布式为2s2和3s23p5的两原子分别为Be和Cl,BeCl 为共价化合物,A项错
2
误;基态钾原子有1个未成对电子,第4周期中与基态钾原子未成对电子数相同的元素还有
钪元素(Sc)、铜元素(Cu)镓元素(Ga)溴元素(B)4种元素,B项正确;第84号元素
位于第6周期第ⅥA族,为钋元素(Po),由于最高正价等于主族序数,所以该元素最高化
合价是+6,C项错误;短周期同周期的ⅡA族与ⅢA族元素的原子序数一定相差1,4、5周期
由于存在过渡金属,所以相差11,6、7周期由于过渡金属中又出现镧系锕系,则相差25,
D项错误。
3.答案:B
解析:青铜是合金,其熔点比组分金属的低,A错误;Cu (OH) CO 为致密结构,可以防止
2 2 3
潮湿空气进入内部进一步腐蚀铜,从而保护青铜器,属于无害锈,B正确;铜的金属活动性
比H弱,不会发生析氢腐蚀,C错误;黄铜矿经过冶炼得到粗铜,电解精炼粗铜,粗铜作阳
极,可以得到纯度为99.9%的铜,D错误。
4.答案:D
解析:W分子中含有酚羟基(—OH)、酯基(—COO—)、醚键(—O—)三种含氧官能
团,A正确;一个W分子中含有三个酚羟基、一个酯基,所以1 mol该化合物最多能与4
mol NaOH反应,B正确;根据W的结构简式可以推出W的分子式是C H O ,且在五元环
19 18 7
上有一个手性碳原子,C正确;该物质含有酚羟基,能与FeCl 溶液发生显色反应,但无羧
3
基,不能和NaHCO 溶液反应放出CO ,D错误。
3 2
5.答案:A
解析:A.基态 Ti原子的价层电子排布式为3d24s2,价层电子排布图为
22
,故A错误;
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
B.K S中钾原子失去电子,硫原子得到电子形成离子键,其电子式表示的形成过程规范正
2
确,B正确;
1
C.HClO的分子中心原子价层电子对数为2+ 62=4,VSEPR模型为四面体形,C正确;
2
D.每个H原子核外1s能级的电子经过“头碰头”方式结合形成ssσ键,D正确;
故选A。
6.答案:C
解析:由W、X、Y、Z是原子序数依次增大的四种短周期元素,只有 X、Y位于同一周期,
可知W位于第 1周期,即W是氢元素;X、Y位于第 2周期,Z位于第3周期,根据题给物
质结构中X、Y、Z的成键特点可知,X为氮元素、Y为氧元素、Z为硫元素。原子半径:
S>N>O>H,A错误;由于 S和N均能形成多种含氧酸,所以无法比较等物质的量浓度的 X
和Z的含氧酸的酸性强弱,B错误;H、N、S均可与O形成多种化合物,C正确;简单氢化
物的还原性:H OH S,D错误。
2 2
7.答案:B
解析:B由图可知,生成CH CN的同时生成的另一种中间产物存在分子内氢键,故B错误。
3
8.答案:B
解析:②是分液漏斗,可以分离互不相溶的液体,是分液操作的仪器;③是普通漏斗,可以
用作过滤操作的仪器,A说法正确。②是分液操作的装置,不能用作实验室制取氯气中添加
盐酸的装置,B说法错误。①②⑤都有旋塞和上盖,需要检查该部分装置是否紧密,故使用
前需检漏,C说法正确。④为长颈漏斗,使用长颈漏斗制备气体,检查气密性时,可从长颈
漏斗加入水形成段液柱,静置,观察液面,液面不下降,则气密性良好,D说法正确。
9.答案:D
612
解析:H S的中心原子为S,S有2个σ键电子对,孤电子对数 2,VSEPR模型
2 2
为四面体形,H S的空间结构为V形;BF 的中心原子为B,B有3个σ键电子对,孤电子对
2 3
313
数 0,VSEPR模型为平面三角形,BF 的空间结构为平面三角形,C正确。该理
2 3
论并不能预测所有分子或离子的空间结构,比如许多过渡金属化合物的空间结构不能用
VSEPR模型解释,D错误。
10.答案:C
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
解析:C解析:本题考查N 分子的结构与性质。N 是由非极性键(N一N)构成的,为非
60 60
极性分子,不含有π键 N 是分子晶体,A,B两项均错误;N 和C 都是非极性分子,N 的分
60 60 60 60
子量更大,范德华力更大,熔点更高,D项错误
11.答案:D
解析:依题意,甲烷发生氧化反应生成二氧化碳,吸附甲烷的电极为负极,A项正确;
O 、CO 共同参与反应,电极反应式为O 2CO 4e 2CO2,B项正确;
2 2 2 2 3
根据原电池工作原理阴离子向负极移动,C项正确;
电池总反应为CH 2O CO 2H O,会释放出二氧化碳,D项错误。
4 2 2 2
12.答案:D
解析:A.物质I存在顺反异构体,如图 ,故A正确;
B.物质Ⅶ含有酰胺基,能与NaOH溶液反应,故B正确;
C.物质Ⅲ中碳正离子上有空轨道,N原子提供孤电子对形成配位键,故物质Ⅲ→物质Ⅳ有配
位键的形成,故C正确;
D. 发生Beckmann重排可以得到 或 ,不能生成
,故D错误;故选D。
13.答案:A
解析:装置A中二氧化锰和浓盐酸共热生成氯气,经 B装置干燥后进入D与硫磺在
100~110℃化合生成S Cl ,为避免硫磺与装置中空气中的氧气发生副反应,可提前通入N ,
2 2 2
以排尽装置中的空气,最后的尾气氯气用石灰乳吸收即可。A. S Cl 遇水剧烈反应,所以需
2 2
制得干燥的氯气,装置B的试剂为浓硫酸,A符合题意;B.硫与装置中空气中的氧气加热时
容易发生副反应生成二氧化硫气体,故通入N 以排尽装置中的空气,B不符合题意;C.进入
2
到C中的氯气和氢氧化钠溶液反应生成氯化钠和次氯酸钠,得到副产品漂白液,进入到E中
的氯气和石灰乳反应生成氯化钙和次氯酸钙,得到副产品漂白粉,C不符合题意;D.由于
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
S Cl 遇水反应,在D、E之间可加一个盛有无水CaCl 的干燥管,避免E中的水蒸气进入D
2 2 2
中,实验更安全,产率更高,D不符合题意;故选 A。
14.答案:C
解析:根据上述分析,曲线乙和丙代表向NaHA溶液中滴加盐酸,A错误;若
K
K H AK H A K ,则K H A W ,即K H A K A2 ,但由图可
al 2 a2 2 W a2 2 K H A a2 2 b2
a1 2
知,NaHA溶液显碱性,说明HA的水解程度大于其电离程度,即K A2 K H A,B
h2 a2 2
错误;根据pHV(HCl)图,滴定分析时,c点溶液的pH在8.5左右,在酚酞的变色范围内,
故可用酚酞作指示剂,d点溶液的pH在4左右,在甲基橙的变色范围内,故可用甲基橙作指
示剂,C正确;a点时,溶液溶质为NaHA、H A和 NaCl,存在电荷守恒
2
c
Na
c
H
2c
A2
c
HA
c
Cl
c
OH
,D错误。
15.答案:D
解析: Si晶体与二氧化硅晶体都属于共价晶体, Si—O的键长比Si—Si的键长短,故Si—O
的键能比Si—Si的键能大,二氧化硅晶体比 Si晶体的熔点高,A错误;氯化钠晶体中钠离子
位于顶点和面心,氯离子位于棱心和体心,则每个Na+周围紧邻的Cl共有 6个,B错误;氯
化铯是体心立方晶胞,图示结构实际是8个氯化铯晶胞,则氯化铯一个晶胞中含有1个Cs+,
1个Cl,故 C错误;在硅晶体中,每个硅原子形成2个Si—Si键,所以Si原子与Si—Si键
数目比为1︰2,D正确。
16.(13分)答案:(1)NO(1分)
(2)温度高于60 ℃,H O 会分解(1分)
2 2
(3)Fe(OH) (1分);3.2(2分)
3
(4)bc(2分)
煅烧
(5)Na SO (2分);4NiCO 2Li CO O 4LiNiO 6CO (2分)
2 4 3 2 3 3 2 2
(6)89.8(2分)
解析:(1)分析题给信息可知,稀硝酸与合金反应产生NO,能溶解铜的物质是稀硝酸或生
成的Fe3,稀硫酸不与金属反应产生H ,故尾气的主要成分为NO。
2
(2)温度高于60 ℃,H O 会分解,H O 溶液浓度降低,使“氧化”速率降低。
2 2 2 2
(3)“除铁”时加入NaOH溶液生成Fe(OH) 沉淀,根据表格中数据知Fe3完全沉淀时,
3
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
c Fe3 1.0105 molL1,则有c3 OH K Fe(OH) /c Fe3
sp 3
41038 / 1.0105 mol3L3 41033 mol3L3,c OH 41/31011 molL1,则
2
pOH11 lg210.8,pH1410.83.2。
3
(4)由“沉铜”的产物为CuS可知,应加入硫化物,虽然FeS也可“沉铜”,但转化为CuS沉
淀后,滤液中又引入杂质Fe2,会对后续“沉镍”造成干扰,故只能选 bc。
(5)根据流程图分析,滤液中的溶质主要为Na SO ;“煅烧”的反应物有NiCO、Li CO ,
2 4 3 2 3
生成物有LiNiO ,镍元素化合价升高,说明NiCO 被氧化,故空气中煅烧的氧气参与反应,
2 3
煅烧
化学方程式为4NiCO 2Li CO O 4LiNiO 6CO 。
3 2 3 3 2 2
(6)第一步:列关系式。根据镍原子守恒可得NiLiNiO 。第二步:计算理论上生成
2
LiNiO 的质量。理论上生成LiNiO 的质量为1.0 t59.0% 59 gmol1 98 gmol1 0.98 t。
2 2
0.88t
第三步:计算LiNiO 的产率。LiNiO 的产率是 100%89.8%。
2 2 0.98t
17.(14分)答案:(1)苯酚(1分)
(2) (1分);取代反应(1分)
(3)羟基、酯基(1分)
(4) H O(2分)
2
(5)16(2分); (2分)
(6)
(4分)。
解析:(1)综上分析,A是苯酚。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(2)B为环己醇,结构简式为 ;环己醇与浓HCl在加热条件下反应生成C,
B→C的反应类型是取代反应。
(3)根据G的结构简式( )可知,分子中的官能团名称是羟基、酯基。
(4)E( )与甲醇在浓硫酸、加热的条件下发生酯化反应制得F,故
E→F的化学方程式为
H O。
2
(5)能与FeCl 溶液发生显色反应,说明含有酚羟基,能与碳酸氢钠溶液反应,说明含有羧
3
基,由F的结构简式可知,还有2个碳原子和一个不饱和度,分子中除苯环外不含其他的
环,则还有一个碳碳双键。若苯环上有2个取代基,则为—OH、— CH CH— COOH或—
OH、 ,在苯环上有邻、间、对三种位置关系,共6种;若苯环上有3个取代
基,则为—OH、— CH CH 和—COOH,在苯环上有 10种位置关系,则符合要求的同分异
2
构体有16种,其中核磁共振氢谱有5组峰的结构简式为 。
(6)对比E的结构简式 和苯乙烯的结构简式 可知,苯
乙烯与Br 发生加成反应后再水解,最后氧化可得E,合成路线为
2
。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
18.(14分)答案:(1)①饱和亚硫酸氢钠溶液(2分)
②MnO SO Mn2 SO2(2分)
2 2 4
③在溶液中,二氧化硫会被氧气氧化为硫酸根离子(2分)
(2)Mn2 2HCO MnCO H OCO (2分);取少量最后一次洗涤液放入试管
3 3 2 2
中,滴加盐酸酸化的BaCl 溶液,若无白色沉淀产生,则说明沉淀洗涤干净,反之则未洗干
2
净(2分)
(3)92%(2分);偏低(2分)
解析:(1)①通过观察 A中气泡的快慢来调节气体的通入速率,故 A中加入的试剂不能和
二氧化硫、氮气反应,最佳试剂是饱和亚硫酸氢钠溶液。②MnO 和二氧化硫反应生成硫酸
2
锰,反应的离子方程式为MnO SO Mn2 SO2。③实验中若将N 换成空气,则在溶
2 2 4 2
液中,空气中的氧气可以将一氧化硫氧化生成SO2,导致SO2浓度明显大Mn2浓度。
4 4
(2)MnCO 沉淀表面会附着SO2,取最后一次洗涤液少许于试管中,滴加盐酸酸化的
3 4
BaCl 溶液,无沉淀生成,说明已洗净,反之说明未洗干净。
2
(3)测定碳酸锰产品的纯度时,3次滴定操作中的第2次误差过大,实验数据不能采用,由
10.10 mL9.90 mL
此可得出两次有效滴定所用标准溶液的平均体积为 10.00 mL,由原子守
2
恒及题给反应可得出如下关系式:MnCO NH FeSO ,nMnCO
3 4 2 4 2 3
n
NH
4
2
FeSO
4
2
0.2000 molL10.010 L2103 mol,则产品的纯度
2103 mol115 gmol1
100%92%。若滴定终点时俯视读数,则读出的硫酸亚铁铵标准
0.2500g
溶液的体积偏小,测得的碳酸锰产品的纯度偏低。
19.(14分)答案:(1)-77(1分)
(2)①6.0MPa(1分);其他条件不变,增大压强,平衡正向移动,CO 转化率增大(2
2
分)
②xyp/(100xy)(2分)
(3)①<(2分);随温度升高,CO 平衡转化率降低,正反应为放热反应(2分)②B(2
2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
p 3p 3
0 0
16 16
分)③ (2分)
p 2 3p 6
0 0
8 8
解析:(1)拆开化学键吸收能量(80324362)kJ2478kJ,形成化学键放出能量
(80341324632)kJ2555kJ,ΔH 77kJmol1。
(2)①CO (g)2H (g) CH O(g)H O(g)为反应前后气体物质的量减小的反应,其他条件相
2 2 2 2
同时,压强大,有利于平衡正向移动,二氧化碳转化率大,则压强 p p p ,则
1 2 3
p 6.0MPa。
1
②假设原混合气体的物质的量为 100mol,则CO 、H 和 Ar的物质的量分别为xmol、2xmol和
2 2
nmol,x2xn3xn100,CO 的平衡转化率为 y ,则平衡时,nCO (xxy)mol,
2 2
nH (2x2xy)mol,nCH OnH Oxymol,平衡时总物质的量为
2 2 2
(3xxyn)mol(100xy)mol,CH O的压强为xyp/(100xy)。
2
(3)①随温度升高,CO 的平衡转化率减小,正反应为放热反应,ΔH 0。
2
②催化剂熊缩短达到平衡的时间,不能提高二氧化碳的平衡转化率,A项错误;压强不再变
化,各物质的浓度不再变化,反应达到平衡状态,B项正确;平衡常数只与温度有温度不
变,平衡常数不变,C项错误;升高温度,正、逆反应速率都增大,D项错误。③a点时CO
2
平衡转化率为0.5,利用三段式求出平衡时的分压。
2CO (g)6H (g) CH OCH (g)3H O(g)
2 2 3 3 2
起始量/mol 2 6 0 0
转化量/mol 1 3 0.5 1.5
平衡量/mol 1 3 0.5 1.5
平衡时总压强为3p /4,平衡时CO 分压为 p /8,H 分压为3p /8,CH OCH 分压为 p /16,
0 2 0 2 0 3 3 0
p 3p 3
0 0
16 16
H O分压为3p /16,K 。
2 0 p p 2 3p 6
0 0
8 8
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002