文档内容
广安中学2026高考冲刺月测卷一
化学试卷
一、单选题
1.下列有关物质变化的说法正确的是
A.二氧化硫是非电解质,所以二氧化硫的水溶液不能导电
B.一种单质和一种化合物发生的反应一定是置换反应
C.碳酸钠粉末遇水生成含有结晶水的Na CO ⋅10H O是物理变化
2 3 2
D.通过化学反应,可由NaCO 一步转化生成NaOH
2 3
2.下列说法中正确的是
A.价电子排布为3d104s1的元素位于第四周期第IA族,是s区元素
B.SO 分子和O 分子的立体构型均为V形
2 3
C.有机物CH=CH―CH 分子中有1个π键、2个σ键
2 3
D.由于氢键的存在,水分子的稳定性好,高温下也很难分解
3.物质的性质决定用途,下列物质的用途及原理正确的是
A.瓷坩埚耐高温,可用于加热分解石灰石
B.铝粉与NaOH溶液反应放热,可用于厨卫管道疏通
C.K FeO 具有强氧化性,可用于除去硬水中的Ca2+、Mg2+
2 4
D.钛合金具有高强韧性,可用于制造载人潜水器的耐压舱
4.实验室用盐酸和NaOH溶液反应来测定中和反应的反应热。下列说法正确的是
A.用同一温度计测量酸液温度后立即测量碱液温度
B.为使两物质充分反应,添加NaOH溶液时应遵循少量多次原则
C.实验中需要稍过量的NaOH溶液以保证实验数据的准确性
D.为防止玻璃搅拌器损坏,可用铁质材料替代
5.当光束通过下列分散系时,能观察到丁达尔效应的是( )
A.CuSO 溶液 B.硫酸
4
C.NaCl 溶液 D.Fe(OH) 胶体
3
6.离子化合物A B由四种原子序数依次增大的短周期主族元素W、X、Y、Z组成,其中阴、阳离子均由两
2
种元素组成且均呈正四面体形。四种元素的原子序数之和为21,且W、Z元素的基态原子核外均只有1个
未成对电子。下列说法错误的是
A.第一电离能:Y>Z>X
B.原子半径:X>Y>Z
C.键角:YW >YZ
3 3
D. 的化学式:
A B (YW ) XZ
2 4 2 4
7.下列元素性质的递变规律中正确的是
A.原子半径:Be<B<C<N
B.第一电离能:B<Be<Mg<Na
C.电负性:O>N>S>P
D.气态氢化物的稳定性:NH<PH<SiH
3 3 48.下列物质之间的转化都能一步实现的
① ❑ ❑ ② ❑ ❑ ③ ❑ ❑
S→SO →H SO Si→SiO →H SiO NH →NO →HNO
3 2 4 2 2 3 3 2 3
❑
④Na O → ❑ Na CO → ❑ NaOH ⑤CaCl → ❑ CaCO → ❑ CO ⑥H 2 O 2 (aq)→H 2
2 2 2 3 2 3 2 MnO
2
⑦ ❑ ❑ ❑ - ❑ ❑ ⑧ ❑
Al→Al O →Al(OH) →[Al(OH) ] →Al(OH) →AlCl NaCl(aq)→NaNO (aq)
2 3 3 4 3 3 3
❑ ❑ ❑ ❑
⑨CuO(s)→Cu(s)→CuS(s) ⑩Cu(s) → Fe(s)→FeS(s)
S Fe(SO ) ❑
2 43
A.2个 B.3个 C.4个 D.5个
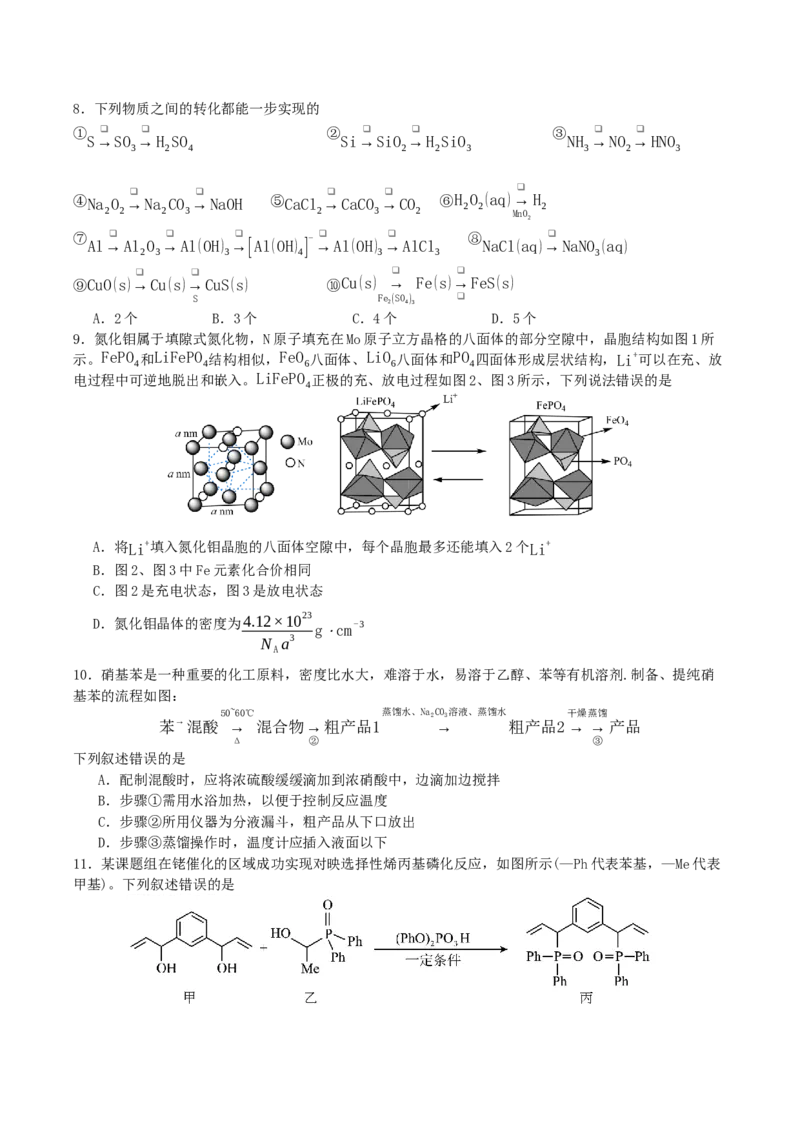
9.氮化钼属于填隙式氮化物,N原子填充在Mo原子立方晶格的八面体的部分空隙中,晶胞结构如图1所
示。FePO 和LiFePO 结构相似,FeO 八面体、LiO 八面体和PO 四面体形成层状结构,Li+可以在充、放
4 4 6 6 4
电过程中可逆地脱出和嵌入。LiFePO 正极的充、放电过程如图2、图3所示,下列说法错误的是
4
A.将Li+填入氮化钼晶胞的八面体空隙中,每个晶胞最多还能填入2个Li+
B.图2、图3中Fe元素化合价相同
C.图2是充电状态,图3是放电状态
D.氮化钼晶体的密度为4.12×1023
g⋅cm-3
N a3
A
10.硝基苯是一种重要的化工原料,密度比水大,难溶于水,易溶于乙醇、苯等有机溶剂.制备、提纯硝
基苯的流程如图:
50~60℃ 蒸馏水、Na 2 CO 3 溶液、蒸馏水 干燥蒸馏
苯→混酸 → 混合物→粗产品1 → 粗产品2→ →产品
Δ ② ③
下列叙述错误的是
A.配制混酸时,应将浓硫酸缓缓滴加到浓硝酸中,边滴加边搅拌
B.步骤①需用水浴加热,以便于控制反应温度
C.步骤②所用仪器为分液漏斗,粗产品从下口放出
D.步骤③蒸馏操作时,温度计应插入液面以下
11.某课题组在铑催化的区域成功实现对映选择性烯丙基磷化反应,如图所示(—Ph代表苯基,—Me代表
甲基)。下列叙述错误的是A.甲分子中所有碳原子可能共平面
B.甲和乙发生加成反应生成丙
C.乙的分子式为C H OP
14 15 2
D.丙与足量H 反应生成丁,丁分子中最多含4个手性碳原子
2
12.纤维电池是可以为可穿戴设备提供电能的便携二次电池。一种纤维钠离子电池放电的总反应为
Na MnO +NaTi (PO ) =Na MnO +Na Ti (PO ) ,其结构简图如图,下列说法正确的是
0.44 2 2 4 3 0.44-x 2 1+x 2 4 3
A.放电时甲为正极
B.放电时负极的电极反应式为
NaTi (PO ) -xe-+xNa+=Na Ti (PO )
2 4 3 1+x 2 4 3
C.充电时,若转移1mole-,甲电极将减少23xg
D.充电时Na+从乙极迁移到甲极
13.下列物质:①BeCl②CS③白磷④BF⑤NF⑥HO,其中含极性键的非极性分子是
2 2 3 3 2 2
A.①④⑥ B.②③⑥ C.①②④ D.③④⑤
14.下列说法正确的是
A.NaCO 溶液:c(OH-)=c(H+)+c( )+2c(HCO)
2 2 4 HC O- 2 2 4
2 4
B.常温下pH为3.75的KHSO 溶液中,c( )c(CN-),则a一定小于b
D.将pH均为a的氢氧化钠溶液和氨水分别加水稀释100倍,pH变为b和c,则a、b、c的大小关系是:
b>c>a
15.某同学以大小相同的铜片和锌片为电极研究水果电池,得到的实验数据如表所示:
电流/
实验编号 水果种类 电极间距离/cm
μA
① 番茄 1 98.7
② 番茄 2 72.5
③ 苹果 2 27.2
下列说法错误的是
A.电流从铜片经外电路流向锌片
B.实验②和③探究的是水果种类对电流的影响
C.实验①和③探究的是电极间距离对电流的影响
D.锌片上发生氧化反应,锌片作水果电池的负极
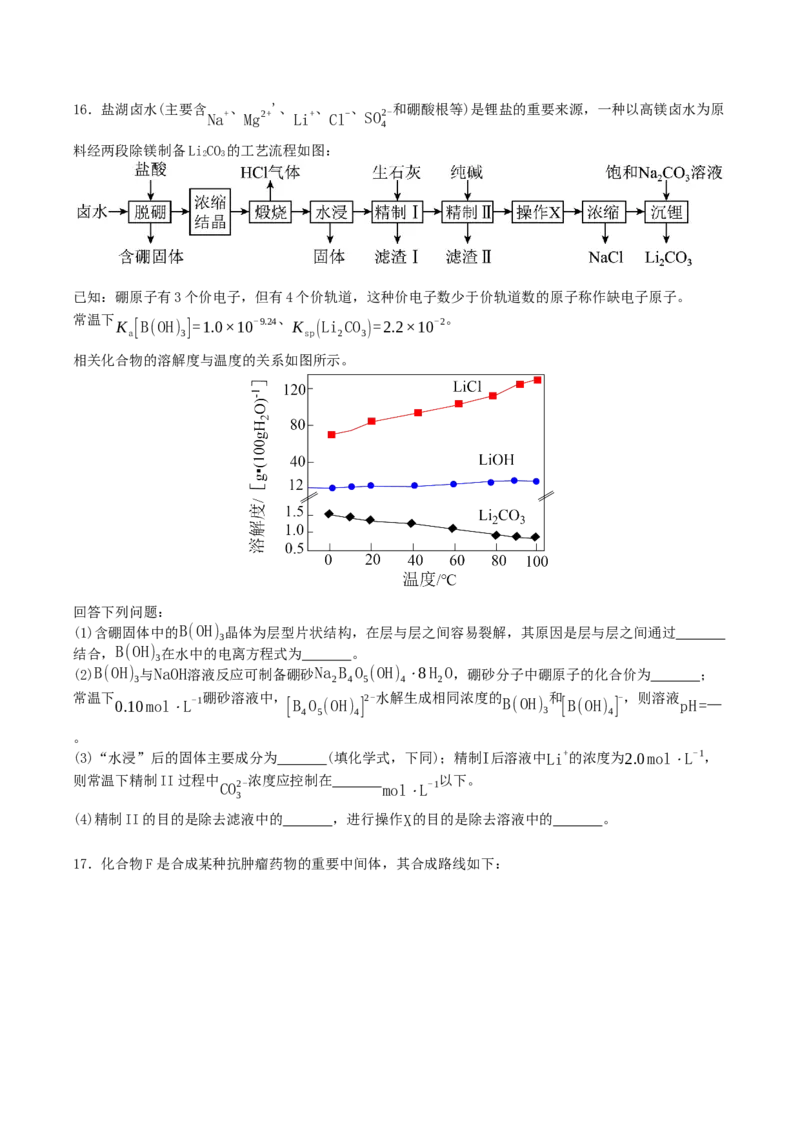
二、解答题16.盐湖卤水(主要含 、 '、 、 、 和硼酸根等)是锂盐的重要来源,一种以高镁卤水为原
Na+ Mg2+ Li+ Cl- SO2-
4
料经两段除镁制备LiCO 的工艺流程如图:
2 3
已知:硼原子有3个价电子,但有4个价轨道,这种价电子数少于价轨道数的原子称作缺电子原子。
常温下 K [B(OH) ]=1.0×10-9.24 、 K (Li CO )=2.2×10-2 。
a 3 sp 2 3
相关化合物的溶解度与温度的关系如图所示。
回答下列问题:
(1)含硼固体中的B(OH) 晶体为层型片状结构,在层与层之间容易裂解,其原因是层与层之间通过
3
结合,B(OH) 在水中的电离方程式为 。
3
(2)B(OH) 与NaOH溶液反应可制备硼砂Na B O (OH) ⋅8H O,硼砂分子中硼原子的化合价为 ;
3 2 4 5 4 2
常温下
0.10mol⋅L-1
硼砂溶液中,
[B O (OH) ]
2-水解生成相同浓度的
B(OH)
和
[B(OH) ]
-,则溶液
pH=
4 5 4 3 4
。
(3)“水浸”后的固体主要成分为 (填化学式,下同);精制I后溶液中Li+的浓度为2.0mol⋅L-1,
则常温下精制II过程中 浓度应控制在 以下。
CO2- mol⋅L-1
3
(4)精制II的目的是除去滤液中的 ,进行操作X的目的是除去溶液中的 。
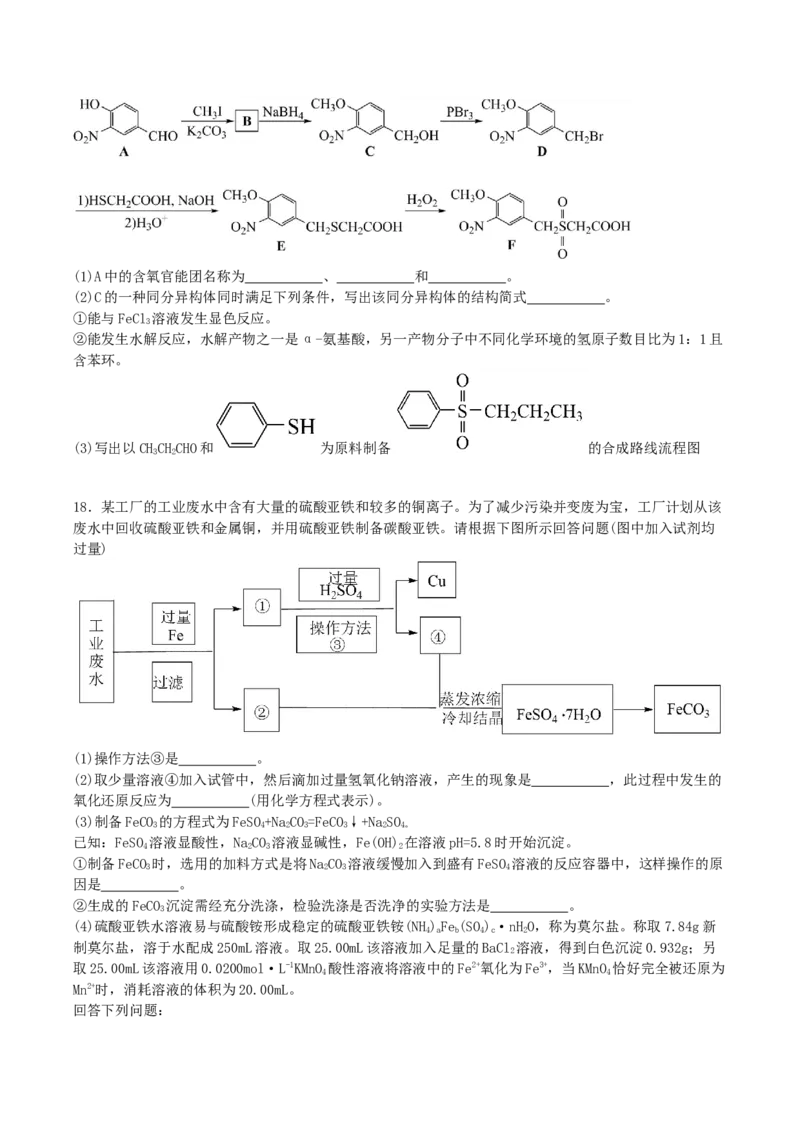
17.化合物F是合成某种抗肿瘤药物的重要中间体,其合成路线如下:(1)A中的含氧官能团名称为 、 和 。
(2)C的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式 。
①能与FeCl 溶液发生显色反应。
3
②能发生水解反应,水解产物之一是α-氨基酸,另一产物分子中不同化学环境的氢原子数目比为1:1且
含苯环。
(3)写出以CHCHCHO和 为原料制备 的合成路线流程图
3 2
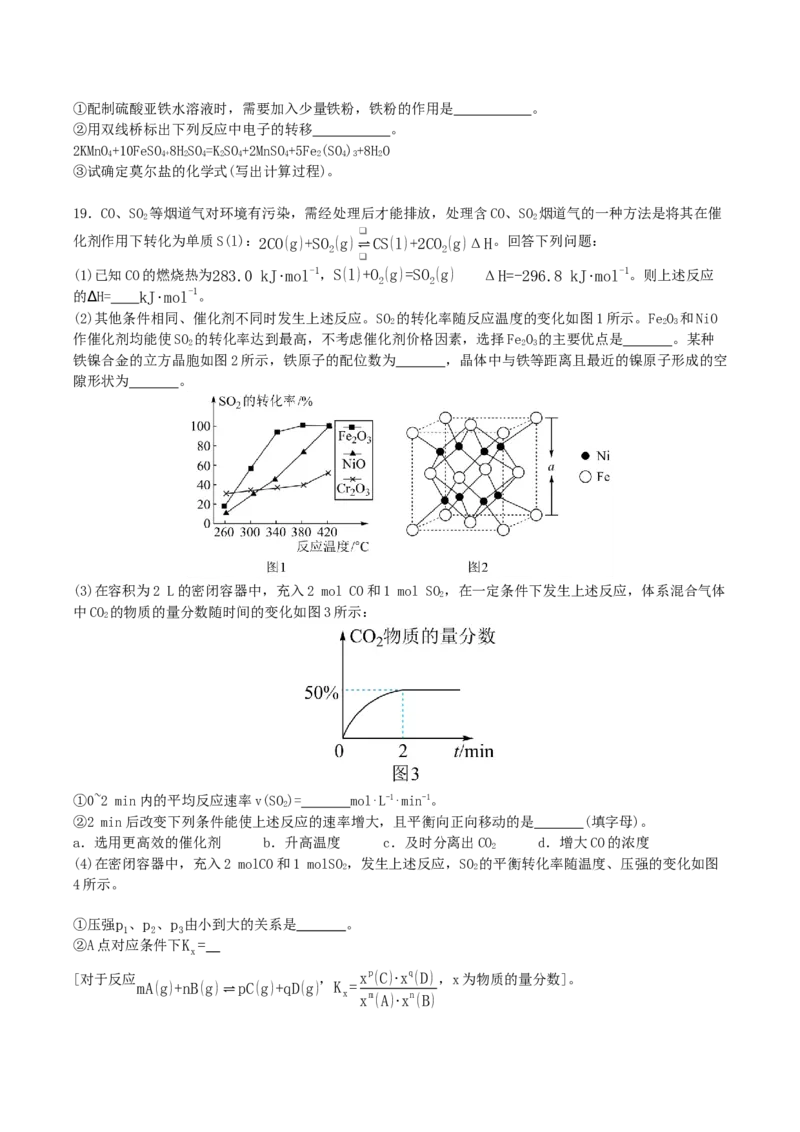
18.某工厂的工业废水中含有大量的硫酸亚铁和较多的铜离子。为了减少污染并变废为宝,工厂计划从该
废水中回收硫酸亚铁和金属铜,并用硫酸亚铁制备碳酸亚铁。请根据下图所示回答问题(图中加入试剂均
过量)
(1)操作方法③是 。
(2)取少量溶液④加入试管中,然后滴加过量氢氧化钠溶液,产生的现象是 ,此过程中发生的
氧化还原反应为 (用化学方程式表示)。
(3)制备FeCO 的方程式为FeSO+NaCO=FeCO↓+NaSO
3 4 2 3 3 2 4。
已知:FeSO 溶液显酸性,NaCO 溶液显碱性,Fe(OH) 在溶液pH=5.8时开始沉淀。
4 2 3 2
①制备FeCO 时,选用的加料方式是将NaCO 溶液缓慢加入到盛有FeSO 溶液的反应容器中,这样操作的原
3 2 3 4
因是 。
②生成的FeCO 沉淀需经充分洗涤,检验洗涤是否洗净的实验方法是 。
3
(4)硫酸亚铁水溶液易与硫酸铵形成稳定的硫酸亚铁铵(NH)Fe(SO)·nHO,称为莫尔盐。称取7.84g新
4 a b 4 c 2
制莫尔盐,溶于水配成250mL溶液。取25.00mL该溶液加入足量的BaCl 溶液,得到白色沉淀0.932g;另
2
取25.00mL该溶液用0.0200mol·L-1KMnO 酸性溶液将溶液中的Fe2+氧化为Fe3+,当KMnO 恰好完全被还原为
4 4
Mn2+时,消耗溶液的体积为20.00mL。
回答下列问题:①配制硫酸亚铁水溶液时,需要加入少量铁粉,铁粉的作用是 。
②用双线桥标出下列反应中电子的转移 。
2KMnO+10FeSO 8HSO=KSO+2MnSO+5Fe(SO)+8HO
4 4+ 2 4 2 4 4 2 4 3 2
③试确定莫尔盐的化学式(写出计算过程)。
19.CO、SO 等烟道气对环境有污染,需经处理后才能排放,处理含CO、SO 烟道气的一种方法是将其在催
2 2
❑
化剂作用下转化为单质S(l):2CO(g)+SO (g)⇌ CS(l)+2CO (g)ΔH。回答下列问题:
2 2
❑
(1)已知CO的燃烧热为283.0 kJ·mol-1,S(l)+O (g)=SO (g) ΔH=-296.8 kJ·mol-1。则上述反应
2 2
的∆H= kJ·mol-1。
(2)其他条件相同、催化剂不同时发生上述反应。SO 的转化率随反应温度的变化如图1所示。FeO 和NiO
2 2 3
作催化剂均能使SO 的转化率达到最高,不考虑催化剂价格因素,选择FeO 的主要优点是 。某种
2 2 3
铁镍合金的立方晶胞如图2所示,铁原子的配位数为 ,晶体中与铁等距离且最近的镍原子形成的空
隙形状为 。
(3)在容积为2 L的密闭容器中,充入2 mol CO和1 mol SO,在一定条件下发生上述反应,体系混合气体
2
中CO 的物质的量分数随时间的变化如图3所示:
2
①0~2 min内的平均反应速率v(SO)= mol⋅L-1⋅min-1。
2
②2 min后改变下列条件能使上述反应的速率增大,且平衡向正向移动的是 (填字母)。
a.选用更高效的催化剂 b.升高温度 c.及时分离出CO d.增大CO的浓度
2
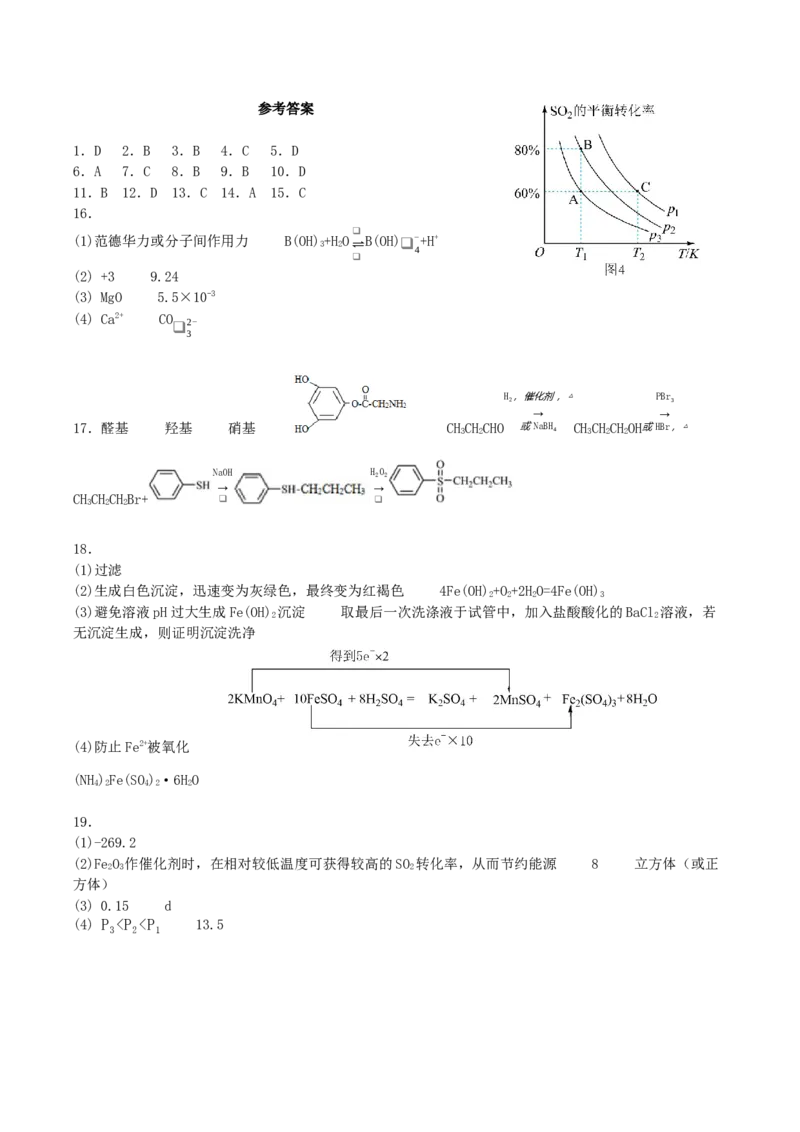
(4)在密闭容器中,充入2 molCO和1 molSO,发生上述反应,SO 的平衡转化率随温度、压强的变化如图
2 2
4所示。
①压强p 、p 、p 由小到大的关系是 。
1 2 3
②A点对应条件下K =
x
[对于反应 , xp (C)·xq (D) ,x为物质的量分数]。
mA(g)+nB(g)⇌ pC(g)+qD(g) K
x
=
xm (A)·xn (B)参考答案
1.D 2.B 3.B 4.C 5.D
6.A 7.C 8.B 9.B 10.D
11.B 12.D 13.C 14.A 15.C
16.
❑
(1)范德华力或分子间作用力 B(OH)+HO B(OH) -+H+
3 2 ⇌ ❑
4
❑
(2) +3 9.24
(3) MgO 5.5×10-3
(4) Ca2+ CO
2-
❑
3
H,催化剂,△ PBr
2 3
→ →
17.醛基 羟基 硝基 CHCHCHO 或NaBH CHCHCHOH或HBr,△
3 2 4 3 2 2
NaOH H O
2 2
→ →
CH 3 CH 2 CH 2 Br+ ❑ ❑
18.
(1)过滤
(2)生成白色沉淀,迅速变为灰绿色,最终变为红褐色 4Fe(OH)+O+2HO=4Fe(OH)
2 2 2 3
(3)避免溶液pH过大生成Fe(OH) 沉淀 取最后一次洗涤液于试管中,加入盐酸酸化的BaCl 溶液,若
2 2
无沉淀生成,则证明沉淀洗净
(4)防止Fe2+被氧化
(NH)Fe(SO)·6HO
4 2 4 2 2
19.
(1)-269.2
(2)FeO 作催化剂时,在相对较低温度可获得较高的SO 转化率,从而节约能源 8 立方体(或正
2 3 2
方体)
(3) 0.15 d
(4) P