文档内容
高途高中·化学
点睛卷
2024
福建省-------------------------------- 高途高中化学点睛卷 -----------------------------------
绝密 启用前
【高途】2024 年福建省普通高中学业水平选择性考试模拟测试卷
化学
本试卷共 8页,18小题,满分100分,考试用时 75分钟。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Si-28 Cl-35.5 Fe-56 Zn-65 Br-80
一、选择题:本题共 10小题,每小题 4分,共40分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.“中国名片”、“中国制造”发展在众多领域受到世界瞩目,它们与化学有着密切联系。下列不正确的是
A.新型核潜艇“长征18”可以在海底潜伏数月之久,运用Na O 作供氧剂
2 2
B.“福建舰”采用富锌涂层具有防水、隔氧等作用
C.C919大型客机使用了大量先进碳纤维复合材料、铝锂合金等,铝锂合金可减轻机身自重
D.五彩缤纷的烟花利用了焰色试验的原理,焰色反应是化学变化
2.青蒿素及其相关产品在抗疟疾方面有显著的疗效,几乎不溶于水,沸点为216℃,热稳定性差,结构如
图所示,下列说法不正确的是
A.青蒿素不能用热的溶剂进行萃取 B.青蒿素分子中含有7个手性碳原子
C.1mol青蒿琥酯可以消耗1molNaOH D.青蒿琥酯的水溶性优于青蒿素
3.下列离子组能大量共存且加入(或通入)试剂发生反应的离子方程式正确的是
选项 离子组 试剂 离子方程式
足量铁氰化钾
A Fe2、Fe3、Cl 溶液 Fe2 K 3 FeCN 6 KFe FeCN 6 2K
B K、SO2、Cl 少量Cl 3SO2Cl H O2ClSO22HSO
3 2 3 2 2 4 3
C H、Fe2、SO2 少量BaNO Ba2 SO2 BaSO
4 3 2 4 4
D C H CHO、OH-、NH 足量银氨溶液
C
2
H
5
CHO2
AgNH
3
2
2OH
2 5 4 C H COONH2Ag3NH
2 5 4 3
A.A B.B C.C D.D
1-------------------------------- 高途高中化学点睛卷 -----------------------------------
4.设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.1mol硝基(NO )与46g NO 所含电子数均为23N
2 2 A
B.1mol Na O 分别与足量的CO 和SO 反应转移的电子数均为2N
2 2 2 2 A
C.1mol基态碳原子核外电子占据的原子轨道数目为3N
A
D.28g硅晶体中含有SiSi数目为4N
A
5.一种用作锂离子电池电解液的锂盐结构如图所示,X、Y、Z、W为原子序数依次增大的短周期主族元素,
基态W原子的s和p能级电子数之比为2:3,下列说法错误的是
A.电负性:Y>X
B.第一电离能:Z>W
C.简单离子半径:Y>Z
D.Y、Z分别与H 化合生成氢化物的沸点Z的高
2
6.油画创作通常需要用到多种无机颜料。研究发现,在不同的空气湿度和光照条件下,颜料雌黄As S 褪
2 3
色的主要原因是发生了以下两种化学反应:
下列说法正确的是
A.反应I和II中,元素As和S都被氧化
B.反应I和II中,氧化1molAsS 转移的电子数之比为1:2
3
C.AsO3和SO2的空间结构都是正四面体形
4 4
nO
D.反应I和II中,参加反应的 2 :I13
主要形式 VO V O VO VO3
2 2 5 3 4
备注 多钒酸盐在水中溶解度较小
已知:①“焙烧”的主要反应之一为:CaCO (s)=CaO(s)+CO (g);
3 2
②在焙烧过程中产生Ca V O ;其中,Ca V O 在水中的溶解度小,易溶于稀硫酸和碱溶液。
2 2 7 2 2 7
(1)Ca V O 中V的化合价为 ,写出在焙烧过程中产生Ca V O 的化学方程式 。
2 2 7 2 2 7
(2)“稀H SO 调pH”后钒元素主要以VO存在,生成VO的离子方程式为 。
2 4 2 2
(3)“滤渣2”的主要成分是 。利用上述表格数据,计算Fe(OH) 的K = 。
3 sp
(4)“调pH值至6~8.5”时控制温度不超过40℃,原因是 。
(5)已知“沉钒”得到NH VO ,该环节通常需要加入过量 (NH ) SO ,其原因是 。
4 3 4 2 4
(6)有机卤化铅晶体具有独特的光电性能,下图为其晶胞结构示意图。
1 1 1
① 原子坐标参数A 为(0,0,0);B为( , , ),则X 为 。若该晶胞的边长为anm,则最近的
1 2
2 2 2
两个Cl-中心间的距离是 。
② 在该晶胞的另一种表达方式中,若图中Pb2+处于顶点位置,则Cl-处于 位置。
A.顶点 B.面心 C.体心 D.棱心
4-------------------------------- 高途高中化学点睛卷 -----------------------------------
12.(14分)CuCl是一种难溶于水和乙醇的白色固体,可溶于浓盐酸或者浓氨水(形成络合物),易被氧化为
高价绿色铜盐,见光受热易分解。在催化领域广泛应用,纺织工业中常作脱色剂,可利用如图装置(夹持装
置略去)将SO 通入新制氢氧化铜悬浊液中制备CuCl。
2
实验步骤及现象:①向C中先加入10.00mL0.5mol•L-1CuCl 溶液,再加入30mL0.6mol•L-1NaOH溶液;
2
②取下A中分液漏斗上的玻璃塞,然后打开分液漏斗的活塞,产生SO 气体至过量,直至C中出现较多的
2
白色沉淀,上层是淡绿色的溶液;
③将C中混合物过滤,依次用水和乙醇洗涤低温晾干,精确称量所得固体质量为0.398g。
回答下列问题:
(1)试剂a为浓硫酸,反应过程中表现的是浓硫酸的 性和 性。
(2)装置B中长颈漏斗的作用是 。
(3)将SO 通入C中,与新制氢氧化铜悬浊液反应,产生白色固体的离子方程式为 。
2
(4)装置C的规格最好选用 (填字母)。
A.50mL B.100mL C.150mL D.200mL
(5)针对步骤2中的现象查阅资料得知:
i.白色沉淀为CuCl;
ii.上层淡绿色溶液中的主要溶质为NaCl和少量Cu(HSO ) 。
3 2
结论:本实验中较多量的新制氢氧化铜与二氧化硫发生了氧化还原反应,少量与之发生了复分解反应,二
者为竞争关系。检验淡绿色溶液中含有HSO的操作方法是 。
3
(6)产品需要避光保存在阴凉的环境中,其原因是 。
(7)计算该实验中CuCl的产率为 %。
稀释
(8)已知:Cu O+2H+=Cu+Cu2++H O,CuCl+HCl=HCuCl ,HCuCl CuCl↓+HCl。若所得CuCl固体中混有
2 2 2 2
少量Cu O,请补充完整除去Cu O的实验方案:
2 2
①向产物中滴加试剂 ,使固体充分溶解,再过滤出杂质;.
②向滤液中加水稀释至不再产生沉淀为止;
③过滤、洗涤、干燥,可得到除去Cu O后的CuCl固体。
2
5-------------------------------- 高途高中化学点睛卷 -----------------------------------
13.(14分)甲醇是一种重要的化工原料,又是一种可再生能源,具有广阔的开发利用前景。工业上通过CO
2
制甲醇的主要反应如下:
i.CO(g)+3H(g)CH OH(g)+H O(g)ΔH =-49.4kJmol-1
2 2 3 2 1
ii.CO(g)+H(g)CO(g)+H O(g)ΔH =41.2kJmol-1
2 2 2 2
(1)研究发现,在单原子Cu/ZrO 催化时,反应i的历程如下
2
第一步CO +H HCOO*+H*(慢)
2 2
第二步HCOO*+2H CH O*+H O(快)
2 3 2
第三步CH O*+H* CH OH(快)
3 3
下列说法正确的是_______。
A.任何温度下,反应i均可自发进行
B.升高温度时,三步反应速率均加快
C.用不同催化剂催化反应可以改变反应历程,提高平衡转化率
D.反应历程中,第一步反应的活化能最高,是反应的决速步
(2)绝热条件下,将H 、CO 以体积比2:1充入恒容密闭容器中,若只发生反应ⅱ,下列不可以作为反应ⅱ
2 2
达到平衡的判据是_______。
A.c(CO )与c(CO)比值不变 B.容器内气体密度不变
2
c(CO)c(H O)
C.容器内气体压强不变 D. 2 不变
c(H)c(CO)
2 2
(3)将H 、CO 以体积比3:1充入恒容密闭容器中,在催化剂存在下发生反应i和反应ii。CO 的平衡转化
2 2 2
率及CH OH的选择性(生成目标产物所消耗的反应物的物质的量与参与反应的反应物的物质的量之比)随温
3
度变化曲线如图所示:
CO 加氢制甲醇, 温(填“高”或“低”,下同)有利于提高反应速率, 温 压有利于提高平
2
衡时CH OH的产率。结合上图阐述实际选用约312℃作为反应温度的原因 。
3
(4)温度为T℃时,在一个刚性容器中模拟工业上合成CH OH,往容器中通入1molCO 、3molH 进行反应
3 2 2
i和反应ii,反应过程中容器内的压强随着时间变化如下表所示。
时间/min 0 10 20 30 40 50
压强/MPa 120 105 95 90 88 88
计算反应开始至40min时,CH OH的平均反应速率是 MPa/min,平衡时n(CH OH)是n(CO)的4倍,
3 3
则H 的平衡分压是 MPa(分压=总压×气体物质的量分数);CO 的平衡转化率是 (最后结果保
2 2
留两位小数)。
6-------------------------------- 高途高中化学点睛卷 -----------------------------------
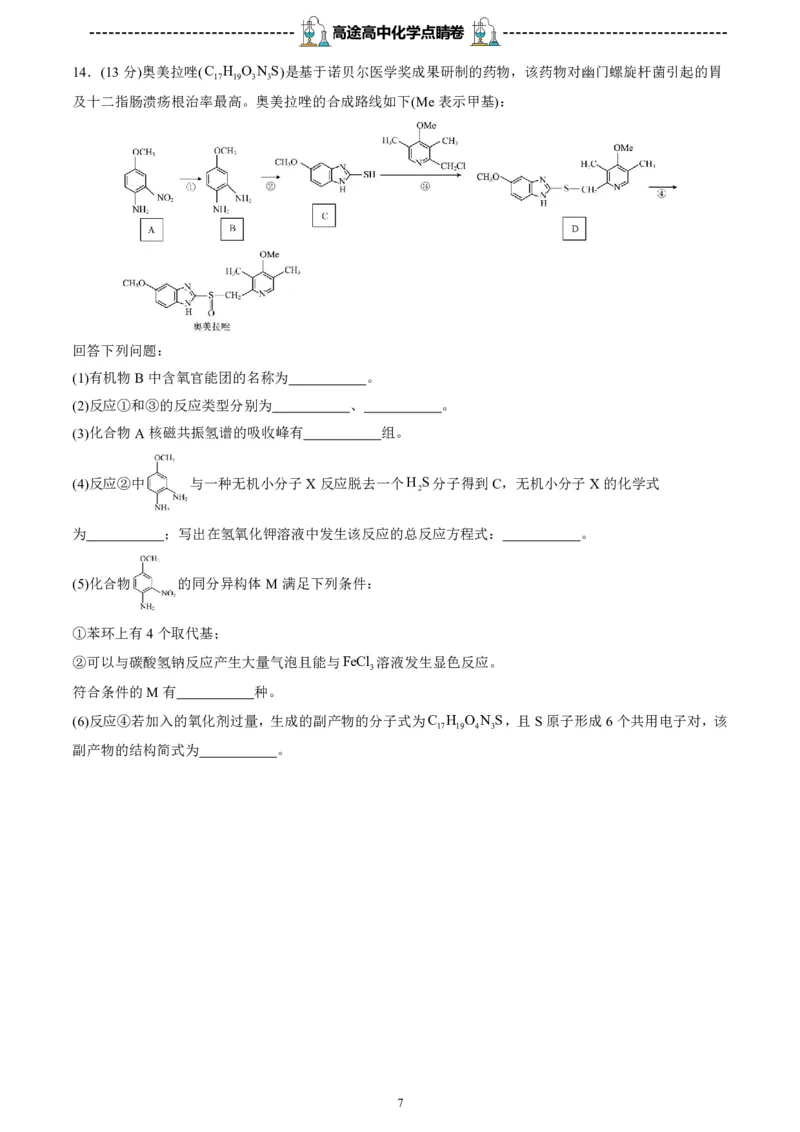
14.(13分)奥美拉唑(C H O NS)是基于诺贝尔医学奖成果研制的药物,该药物对幽门螺旋杆菌引起的胃
17 19 3 3
及十二指肠溃疡根治率最高。奥美拉唑的合成路线如下(Me表示甲基):
回答下列问题:
(1)有机物B中含氧官能团的名称为 。
(2)反应①和③的反应类型分别为 、 。
(3)化合物A核磁共振氢谱的吸收峰有 组。
(4)反应②中 与一种无机小分子X反应脱去一个H S分子得到C,无机小分子X的化学式
2
为 ;写出在氢氧化钾溶液中发生该反应的总反应方程式: 。
(5)化合物 的同分异构体M满足下列条件:
①苯环上有4个取代基;
②可以与碳酸氢钠反应产生大量气泡且能与FeCl 溶液发生显色反应。
3
符合条件的M有 种。
(6)反应④若加入的氧化剂过量,生成的副产物的分子式为C H O N S,且S原子形成6个共用电子对,该
17 19 4 3
副产物的结构简式为 。
7-------------------------------- 高途高中化学点睛卷 -----------------------------------
【高途】2024 年福建省普通高中学业水平选择性考试模拟测试卷
化学参考答案
1.【答案】D
【详解】A.Na O 能分别与H O、CO 反应生成O ,可用作供氧剂,A正确;
2 2 2 2 2
B.富锌涂层能形成保护层,具有防水、隔氧等作用,B正确;
C.铝、锂相对原子质量较小,铝锂合金密度低,强度高,可减轻飞机机身自重,C正确;
D.焰色试验属于物理变化,D错误;故选D。
2.【答案】C
【详解】A.青蒿素沸点低,因此不能用热的溶剂进行萃取,故A正确;
B.青蒿素分子中含有7个手性碳原子,用“*”表示 ,故B正确;
C.1mol青蒿琥酯含有1mol羧基和1mol酯基,则消耗2molNaOH,故C错误;
D.青蒿琥酯含有羧基,亲水基团,因此其水溶性优于青蒿素,故D正确。综上所述,答案为C。
3.【答案】B
【详解】A.该组离子互不反应可大量共存,其中Fe2与铁氰化钾反应生成蓝色沉淀,离子方程式:
Fe2 K FeCN 3 KFeFeCN ,故A错误;
6 6
B.该组离子互不反应可大量共存,通少量氯气后反应离子方程式为:
3SO2Cl H O2ClSO22HSO,故B正确;
3 2 2 4 3
C.加入少量BaNO 离子方程式为:3Fe2+NO+4H+2Ba22SO2 2BaSO 3Fe3+NO2H O,
3 2 3 4 4 2
故C错误;
D.OH-与NH不能大量共存,加入足量银氨溶液共热,离子方程式:
4
C
2
H
5
CHO2
AgNH
3
2
2OH C
2
H
5
COONH
4
2Ag3NH
3
H
2
O,故D错误;故选B。
4.【答案】A
【详解】A.硝基(NO )是电中性,1个硝基(NO )含有23个电子,1mol硝基(NO )含电子数为23N ,
2 2 2 A
46g NO 是1mol,所含电子数也为23N ,A正确;
2 A
B.过氧化钠与二氧化碳反应的化学方程式为:2Na O +2CO =2Na CO +O ,Na O 中O的化合价为-1价,反
2 2 2 2 3 2 2 2
应后生成0价O ,则1molNa O 参与反应电子转移1mol(即N ),B错误;
2 2 2 A
C.碳为6号元素,基态C原子核外电子排布图为 ;则1mol基态碳原子核外电子占据的原
子轨道数目为4N ,C错误;
A
8-------------------------------- 高途高中化学点睛卷 -----------------------------------
D.硅晶体中1个硅原子周围与4个硅原子形成共价键,平均1个硅原子形成2个共价键,28g硅晶体是1mol,
平均有SiSi数目是2N ,D错误;答案选A。
A
5.【答案】D
【分析】X、Y、Z、W为原子序数依次增大的短周期主族元素,基态W原子的s和p能级电子数之比为2:3,
则W的电子排布式为1s22s22p63s23p3,W为P元素;由锂盐结构图式,可确定Y形成2对共用电子,最外层电
子数为6,其为O元素;X形成4对共用电子,最外层电子数为4,其为C元素;Z形成1对共用电子,最外层电
子数为7,其为F元素。从而得出X、Y、Z、W分别为C、O、F、P。
【详解】A.X、Y分别为C、O元素,二者同周期,非金属性O>C,则电负性:O>C,A正确;
B.Z、W分别为F、P,第一电离能F>N>P,则第一电离能:F>P,B正确;
C.Y、Z分别为O、F,O2-与F-的电子层结构相同,但核电荷数O<F,故简单离子半径:O2->F-,C正确;
D.Y、Z分别与H 化合生成的氢化物分别为H O、HF,常温常压下,前者呈液态,后者呈气态,所以沸点
2 2
H O比HF高,D错误;故选D。
2
6.【答案】C
【详解】A.反应Ⅰ中As元素化合价不变,未发生氧化还原反应,故A错误;
B.反应Ⅰ的化学方程式:2As S +6O +3H O=2As O +3H S O ,电子转移总数24e-,氧化1molAs S ,转移电
2 3 2 2 2 3 2 2 3 2 3
子物质的量12mol,反应Ⅱ的化学方程式:2As S +14O +12H O=4H AsO +6H SO ,电子转移数56e-,氧化
2 3 2 2 3 4 2 4
1molAs S ,转移电子物质的量28mol,反应Ⅰ和Ⅱ中,氧化1molAs S 转移的电子数之比=12:28=3:7,故B
2 3 2 3
错误;
1
C.AsO3的价电子对数=4+ 5342 =4,结构中相当于一个氧原子被一个硫原子代替,空间结构是四
4 2
1
面体结构,SO2的价电子对数=4+ 6242 =4,无孤对电子,空间结构是正四面体形,故C正确;
4 2
D.反应Ⅰ的化学方程式:2As S +6O +3H O=2As O +3H S O ,反应Ⅱ的化学方程式:
2 3 2 2 2 3 2 2 3
nO
2As S +14O +12H O=4H AsO +6H SO ,参加反应的 2 :Ⅰ>Ⅱ,故D错误;故选C。
2 3 2 2 3 4 2 4 nH O
2
7.【答案】D
【详解】A.高温煅烧时硫酸锶反应的方程式为SrSO 4C4COSrS,1mol硫酸锶参与反应,生成4molCO
4
,但是C与其它氧化物也会发生反应生成CO,所以会大于4∶1,A正确;
B.酸浸生成的气体为硫化氢,硫化氢通入硫酸铜溶液会产生硫化铜黑色沉淀,B正确;
C.氢氧化钙的溶解度随温度的升高而降低,而氢氧化锶的溶解度随温度的升高而升高,所以“除镁钙”时控
制温度95℃~100℃是为了降低氢氧化钙的溶解度,保证除钙效果,C正确;
D.“沉锶”的离子反应方程式为Sr22OHNH+HCO SrCO H ONH H O,D错误;故选D。
4 3 3 2 3 2
9-------------------------------- 高途高中化学点睛卷 -----------------------------------
8.【答案】B
【详解】A.由题干图示信息可知,操作1分离固体和液体,故该操作为过滤,则用到的主要玻璃仪器有普
通漏斗、烧杯、玻璃棒,A正确;
B.杯酚与C 分子两分子之间的作用力为分子间作用力,而不是共价键,B错误;
60
C.由题干图示信息可知,杯酚可溶于氯仿循环使用,C正确;
D.杯酚晶体是通过分子通过分子间作用力形成的分子晶体,D正确;故答案为:B。
9.【答案】B
【详解】A.由题意知,Cu Se填充碳纳米管作为正极材料,钠较为活泼,钠为负极材料。据“均摊法”,
2x
1 1
每个Cu Se晶胞中含8 +6 4个Se,则晶胞内铜离子、亚铜离子和为42x个,设铜离子、亚铜
2x
8 2
离子分别为a、b,则ab42x,由化合价代数和为零可知,2ab42,解得a4x,b88x,
A错误;
B.放电时,正极Cu Se得到电子发生还原反应生成零价铜,电极反应式为
2x
Cu 2x Se2Na 2e Na Se2xCu ,B正确;
2
C.充电时外电路中转移1mol电子,阳极释放出1mol钠离子,质量减小23g,阴极生成1mol钠,质量增加23g
,两极质量变化差为46g,C错误;
41251030
D.晶胞中Na有8个,Se2有4个,故在计算个数时要乘4,正确答案为 g/cm3,D错误;故选B。
a3N
A
10.【答案】D
c(H)c(A) 103103
【分析】从图中可以看出,当V(NaOH)=0时,pH=3,c(H+)=10-3mol/L,此时Ka= = =10-5
c(HA) 0.1
。随着NaOH的不断滴入,溶液的pH不断增大,δ(HA)不断减小,δ(A-)不断增大,则δ(HA)为不断下降的曲
线,δ(A-)为不断上升的曲线。
c(H)c(A)
【详解】A.x点时,δ(HA)=δ(A-),则c(HA)=c(A-),Ka= =c(H+)=10-5mol/L,对应溶液的pH约为
c(HA)
5,A正确;
B.p点对应的溶液中,V(NaOH)=10时,反应后溶液中,n(HA)=n(A-),依据物料守恒,2c(Na+)=c(A-)+c(HA)
,依据电荷守恒,c(H+)+c(Na+)=c(A-)+c(OH-),则2c H cHA 2c OH c A ,B正确;
C.p→q对应的溶液中,起初以HA的电离为主,抑制水电离,后来以A-的水解为主,促进水电离,所以水
的电离程度一直增大,C正确;
D.n点对应的溶液pH=7,此时NaA、HA共存,c(H+)=c(OH-),依据电荷守恒,可得出c(Na+)=c(A-),由
Ka=
107 c(A)
=10-5,可得出c(A-)=100c(HA),所以存在:c
Na
c
A>cHA,D错误;故选D。
c(HA)
10-------------------------------- 高途高中化学点睛卷 -----------------------------------
11.(20分)【答案】(1) +5 2CaO+V O +O =Ca V O
2 3 2 2 2 7
(2)Ca V O +6H++2SO2 =2VO +2CaSO +3H O
2 2 7 4 2 4 2
(3) Fe(OH) 10-37.4
3
(4)高于40℃,氨气逸出导致Fe3+沉淀反应速率下降
(5)利用同离子效应,促进NH VO 尽可能析出完全
4 3
1 1 2
(6) (1, , ) anm D
2 2 2
【分析】钒渣(主要成分为V O 、FeO、SiO 及少量MgO、CaO、Al O ),在空气中焙烧,CaCO (s)=CaO(s)
2 3 2 2 3 3
+CO (g),产生Ca V O 、Fe O ;加稀硫酸调pH<1,SiO 此过程中不反应,过滤得滤渣1为硫酸钙、SiO ,
2 2 2 7 2 3 2 2
据信息知,所得滤液中含有VO+外,还有Mg2+、Al3+、Fe3+、SO2-,滤液中加入氨水调节pH=6~8.5,VO+沉
2 4 2
淀为V O ,根据表2信息, Fe3+、Al3+完全转化为Fe(OH) 、Al(OH) 沉淀,过滤,滤渣2中含Fe(OH) 、Al(OH)
2 5 3 3 3 3
,滤渣2中加入NaOH使Al(OH) 转化为NaAlO ,则滤渣3的主要成分为Fe(OH) ;滤液含VO-,加硫酸铵 “
3 2 3 3
沉钒”得到NH VO ,煅烧纯净的NH VO 得到V O ;
4 3 4 3 2 5
【详解】(1)Ca V O 中V的化合价为+5,在焙烧过程V O 被O 氧化产生Ca V O ,化学方程式为2CaO+V O
2 2 7 2 3 2 2 2 7 2 3
+O =Ca V O 。
2 2 2 7
(2)已知Ca V O 在水中的溶解度小,易溶于稀硫酸,“稀H SO 调pH”后钒元素主要以VO存在,则生成VO
2 2 7 2 4 2 2
的离子方程式为Ca V O +6H++2SO2 =2VO +2CaSO +3H O。
2 2 7 4 2 4 2
(3)据分析“滤渣2”的主要成分是Fe(OH) 。利用上述表格数据,0.01mol·L−1Fe3+形成氢氧化物沉淀时的pH=2.2
3
,则常温下K FeOH c Fe3 c3 OH =0.01 1.01011.83 =1.01037.4。
sp
3
(4)已知氨水易挥发,则用氨水“调pH值至6~8.5”时控制温度不超过40℃,原因是:高于40℃,氨气逸出导致
Fe3+沉淀反应速率下降。
(5)已知“沉钒”得到NH VO NH VO 存在沉淀溶解平衡:NH VO (s) NH+ (aq)+VO- (aq),“沉钒”中加
4 3 4 3 4 3 4 3
入过量(NH ) SO ,则增大c(NH+),有利于NH VO 结晶析出,故答案为:利用同离子效应,促进NH VO
4 2 4 4 4 3 4 3
尽可能析出完全。
1 1 1 1 1
(6)① 由图可知,原子坐标参数A 为(0,0,0);B为( , , ),则X 为(1, , )。若该晶胞的边长为a
1 2
2 2 2 2 2
2
nm,则最近的两个Cl-中心间的距离是晶胞边长一半的 2倍,即为 anm。
2
②图中Pb2+处于2个Cl-的中点,则在该晶胞的另一种表达方式中,若图中Pb2+处于顶点位置,则Cl-处于2个Pb2+
的中点,故Cl-处于棱心位置,选D。
12.(14分)【答案】(1) 酸 强氧化
(2)安全装置
(3)2C1SO 2CuOH 2CuClSO22H O
2 2 4 2
(4)B
11-------------------------------- 高途高中化学点睛卷 -----------------------------------
(5)取少量淡绿色溶液于试管中,滴入少量BaCl 溶液,无明显现象,再滴加稀HCl,若产生无色有刺激性气
2
味的气体,且该气体能使品红褪色,证明溶液中含有HSO
3
(6)产品见光受热易分解
(7)80
(8)浓HCl
【分析】本实验利用Zn与浓硫酸产生的SO 与新制的氢氧化铜悬浊液反应得到CuCl,利用CuCl是一种难溶于
2
水和乙醇的白色固体这一物理性质进行过滤、洗涤、干燥之后得到产品,
【详解】(1)Zn与浓硫酸反应产生还原产物SO 说明浓硫酸具有强氧化性,同时硫酸转化为了硫酸盐,体现了
2
硫酸的酸性。
(2)装置B中长颈漏斗可以避免装置内气压过大引发安全事故,可通过长颈漏斗内液面上升情况判断装置内气
压情况。
(3)SO 通入C中,与新制氢氧化铜悬浊液反应生成CuCl,根据价态规律可知二氧化硫被氧化为SO2,故离子
2 4
方程式为2C1SO 2CuOH 2CuClSO22H O 。
2 2 4 2
(4)三颈烧瓶加热时液体不超过2/3,而烧瓶内液体实际体积为40mL,据此可知烧瓶应选择比60mL大一点的
规格。故选B。
(5)检验淡绿色溶液中含有HSO的具体操作为取少量淡绿色溶液于试管中,滴入少量BaCl 溶液,无明显现
3 2
象,再滴加稀HCl,若产生无色有刺激性气味的气体,且该气体能使品红褪色,证明溶液中含有HSO-。
3
(6)题干信息可知CuCl易被氧化为高价绿色铜盐,见光受热易分解,产品需要避光保存在阴凉的环境中。
(7)10.00mL0.5mol•L-1CuCl
2
溶液经计算理论上n(CuCl)=n(CuCl
2
)=10.00mL×0.5mol•L-1=5103mol,故产率为
0.398g
100%80%。
5103mol6435.5g·mol1
(8)根据已知信息及CuCl可溶于浓盐酸且稀释后重新得到CuCl可知,若所得CuCl固体中混有少量Cu O,先加
2
浓盐酸将CuCl溶解并将Cu O转化为Cu与Cu2+,过滤之后对滤液进行稀释可以重新得到CuCl。
2
13.(14分)【答案】(1)BD;(2)B;
(3)高;低;高;温度低,反应速率太慢,且CO 转化率低;温度太高,甲醇的选择性低;
2
(4)0.4;38;66.67%
【详解】(1)反应i,ΔS<0,0,低温条件下可自发进行,故A错误;
升高温度时,所有反应反应速率均加快,故B正确;
催化剂不改变反应历程,加快反应速率,但不影响平衡移动,不能提高平衡转化率,故C错误;
第一步反应为慢反应,而活化能越高,反应速率越慢,则第一步反应的活化能最高,慢反应为总反应的决
速步,故D正确;
(2)A.反应过程中c(CO )减小,c(CO)浓度增大,则c(CO )与c(CO)比值减小,故比值不变,能判断反应达到
2 2
平衡状态,故A正确;
B.容器容积不变,混合气体的总质量不变,则气体的密度始终不变,故容器内气体密度不变,不能判断反
应达到平衡状态,故B错误;
12-------------------------------- 高途高中化学点睛卷 -----------------------------------
C.反应前后气体物质的量不变,但是容器绝热,温度降低,压强减小,故容器内气体压强不变,能判断反
应达到平衡状态,故C正确;
c(CO)c(H O)
D.容器绝热,温度降低,降温平衡逆向移动,平衡常数减小,故K= 2 不变,能判断反应
c(H)c(CO)
2 2
达到平衡状态,故D正确;故选B。
(3)CO 加氢制甲醇,升温反应速率加快,故高温有利于提高反应速率,反应i为放热反应,降温平衡正向移
2
动,故低温有利于提高平衡时CH OH的产率。实际选用300-320℃反应温度的原因:温度低,反应速率太慢
3
,且CO 转化率低,温度高,甲醇选择性低。
2
(4)反应i为气体分子数减小的反应,导致总压强减小;反应ii为气体分子数不变的反应,不会导致压强的变
化;故反应开始到40min时,减小的压强120MPa-88MPa=32MPa为反应i进行导致;由三段式可知:
CO(g) +3H(g) CH OH(g) +H O(g)
2 2 3 2
物质的量 1 3 1 1 13112
16MPa 32MPa
16MPa
则CH OH的平均反应速率是 =0.4MPa/min;
3
40min
容器中通入1molCO 、3molH 进行反应i和反应ii,初始压强为120MPa,则初始CO 、H 的分压分别为30MPa
2 2 2 2
、90MPa;由图表可知,反应开始至40min时,反应达到平衡,由三段式可知:
CO (g) +3H (g) CH OH(g) +H O(g)
2 2 3 2
开始(MPa) 30 90 0 0
变化(MPa) x 3x x x
CO (g) +H (g) CO(g) +H O(g)
2 2 2
开始(MPa) 0 0
变化(MPa) y y y y
平衡时CO 、H 、CH OH、H O、CO的分压分别为(30-x-y)MPa、(90-3x-y)MPa、xMPa、(x+y)MPa、yMPa
2 2 3 2
,总压强为88MPa,则(30-x-y)+(90-3x-y)+x+(x+y)+y=88,得120-2x=88;平衡时n(CH OH)是n(CO)的4倍,
3
根据气体压强之比等于物质的量之比,则x=4y,联立解得:y=4MPa,x=16MPa;故H 的平衡分压是90
2
(16+4)MPa
MPa-3×16MPa-4MPa=38MPa;CO 的平衡转化率= 100%66.7%。
2
30MPa
14.(13分)【答案】(1)醚键;(2)还原反应;取代反应;(3)5
(4)CS +CS +2KOH→ +K S+2H O;(5)16;(6)
2; 2 2 2
【分析】有机物A中硝基经还原后生成有机物B,B中两个氨基的H原子被取代并成环生成有机物C,C中S-H
键的H原子被取代后生成有机物D,D中S原子氧化后引入S=O键生成最后产物,据此答题。
【详解】(1)有机物B中含氧官能团结构为C-O-C,名称为醚键。
(2)反应①为硝基转化为氨基,属于还原反应。反应②是氨基上的H原子被取代的反应,属于取代反应。
(3)化合物A不具有对称性,共有5种不同化学环境的氢,故核磁共振氢谱的吸收峰有5组。
13-------------------------------- 高途高中化学点睛卷 -----------------------------------
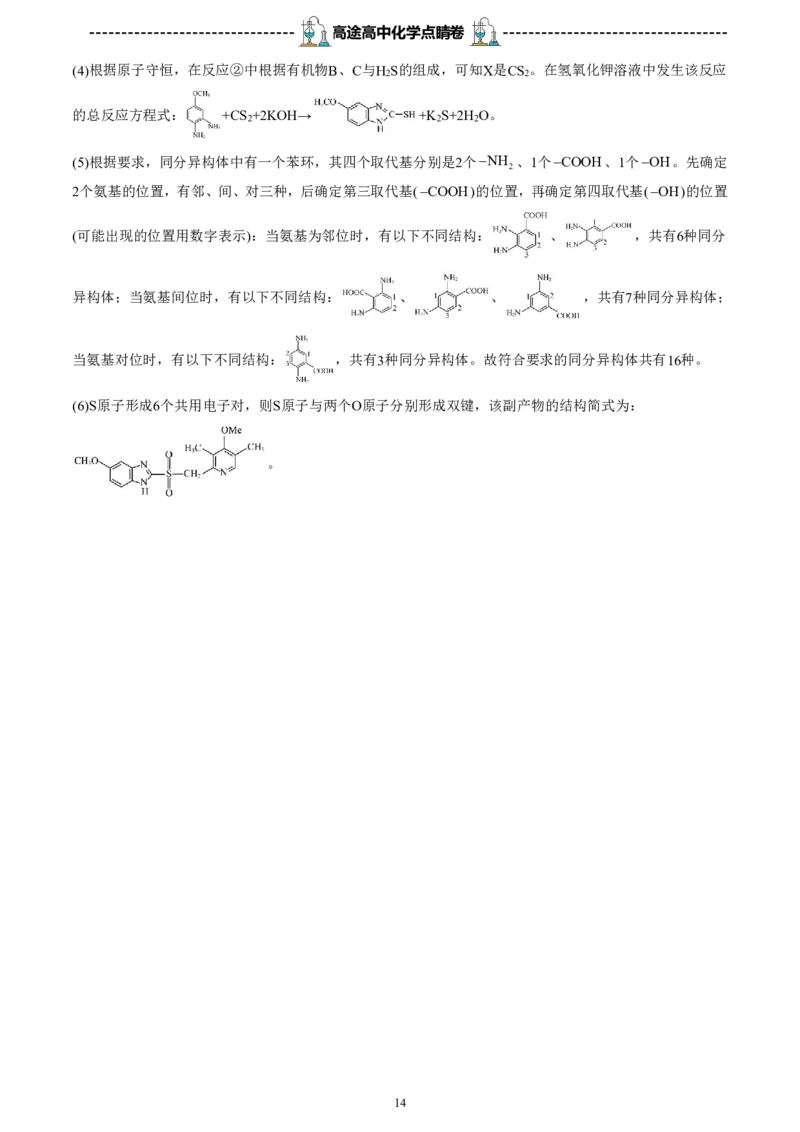
(4)根据原子守恒,在反应②中根据有机物B、C与H S的组成,可知X是CS 。在氢氧化钾溶液中发生该反应
2 2
的总反应方程式: +CS +2KOH→ +K S+2H O。
2 2 2
(5)根据要求,同分异构体中有一个苯环,其四个取代基分别是2个NH 、1个COOH、1个OH。先确定
2
2个氨基的位置,有邻、间、对三种,后确定第三取代基(COOH)的位置,再确定第四取代基(OH)的位置
(可能出现的位置用数字表示):当氨基为邻位时,有以下不同结构: 、 ,共有6种同分
异构体;当氨基间位时,有以下不同结构: 、 、 ,共有7种同分异构体;
当氨基对位时,有以下不同结构: ,共有3种同分异构体。故符合要求的同分异构体共有16种。
(6)S原子形成6个共用电子对,则S原子与两个O原子分别形成双键,该副产物的结构简式为:
。
14