文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题 01 质量守恒定律的应用
【题型一】推断未知物质的化学式
[例题1] (2023秋•兴文县期末)载人航天飞船使用铝粉与高氯酸铵的固体混合物作燃料,
高温
点燃时高氯酸铵发生以下反应:2NH 4 ClO 4 ¯ N 2 ↑+Cl 2 ↑+2O 2 ↑+4X,则X的化学式为(
❑
)
A.Cl B.ClO C.H O D.H
2 2 2 2
【解答】解:反应前后氮原子都是2个,氯原子都是2个,反应前氢原子是8个,反应后应该是
8个,包含在未知物质中,反应前氧原子是8个,反应后应该是8个,其中4个包含在未知物质
中,X的化学式是H O。
2
故选:C。
[例题2] (2024•西平县一模)抗击“新型冠状病毒”,学以致用。“84消毒液”和洁厕
灵混合使用时,会生成有毒气体X,反应的化学方程式为:NaClO+2HCl═NaCl+X↑+H O,X
2
的化学式为( )
A.Cl B.Cl C.H D.CO
2 2
【解答】解:由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式,反
应前钠、氯、氧、氢原子个数分别为1、3、1、2,反应后的生成物中钠、氯、氧、氢原子个数
分别为1、1、1、2,根据反应前后原子种类、数目不变,则每个X分子由2个氯原子构成,则
物质X的化学式为Cl 。
2
故选:B。
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
判断未知化学式应根据化学反应前后原子的种类和数目不变进行分析
【题型二】微观反应示意图
[例题3] (2024•黄州区校级开学)甲醛(CH O)是一种无色、有刺激性气味的气体,室
2
内装修残留的甲醛对人体健康影响很大。如图是利用催化剂除去甲醛的微观示意图,下列有关
说法正确的是( )
A.反应物的分子个数比为3:2
B.反应前后原子个数改变
C.反应的生成物是H O和CO
2 2
D.利用该反应不会对环境造成任何影响
催化剂
【解答】解:由微观反应示意图可知,该反应的化学方程式为CH O+O CO +H O。
2 2 2 2
¯
❑
A、由化学方程式可知,反应物的分子个数比为1:1,说法错误;
B、由质量守恒定律可知,反应前后原子的个数不变,说法错误;
C、由化学方程式可知,反应的生成物是H O和CO ,说法正确;
2 2
D、该反应会生成二氧化碳气体,空气中二氧化碳的含量过高会加剧温室效应,说法错误。
故选:C。
[例题4] (2024•绥化模拟)清华大学的研究人员成功研制出一种纳米纤维催化剂,可将
二氧化碳转化为甲醇,该反应的微观示意图如图所示。下列说法错误的是( )
A.甲、乙、丙、丁都属于化合物
B.反应前后原子的种类和数目均不变
C.反应生成的丙和丁的质量比为16:9
D.参加反应的甲和乙的分子个数比为1:3
【解答】解:由反应的微观示意图和质量守恒定律可知,反应物是二氧化碳和氢气,生成物是
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
催化剂
甲醇和水,反应的方程式是:CO +3H CH OH+H O。
2 2 3 2
¯
❑
A、由物质的组成可知,甲、丙、丁分别是二氧化碳、甲醇和水,都是化合物,乙是氢气,是一
种单质,故A说法错误;
B、由质量守恒定律可知,反应前后原子的种类和数目均不变,故B说法正确;
C、由化学方程式的意义可知,反应生成甲醇和水的质量比为32:18=16:9,故C说法正确;
D、由化学方程式的意义可知,参加反应的甲和乙的分子个数比为1:3,故D说法正确。
故选:A。
1.先对应表示出反应的化学方程式。
2.根据书写的化学方程式判断反应物或生成物的分子个数比与质量比、判断所属反应的基本反应类
型。
3.根据质量守恒定律:化学反应前后元素种类不变,原子种类、数目不变;分子个数可能改变
【题型三】密闭容器中数据分析
[例题5] (2023秋•织金县期末)密闭容器内有甲、乙、丙、丁四种物质,在一定条件下
充分反应,测得反应前后各物质的质量如下。下列说法不正确的是( )
物质 甲 乙 丙 丁
反应前质量/g 6 10 0 50
反应后质量/g 14 10 17 x
A.丁一定是化合物,丙可能是单质
B.该反应的基本类型为化合反应
C.发生变化的甲与丙的质量比为8:17
D.x的值为25
【解答】解:A、反应是丁→甲+丙,丁一定是化合物,丙可能是单质,选项正确;
B、该反应的反应物是丁,生成物是甲和丙,符合“一变多”的形式,属于分解反应,故选项说
法错误。
C、发生变化的甲与丙的质量比为8:17,故选项说法正确。
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D、x的数值为25,故选项说法正确。
故选:B。
[例题6] (2023秋•楚雄市期末)某密闭容器中有甲、乙、丙、丁四种物质,在一定条件
下发生化学反应,测得反应前及反应一段时间后各物质的质量变化如图所示,下列说法正确的
是( )
A.乙一定是该反应的催化剂
B.该反应可能是实验室用氯酸钾制取氧气
C.甲、丙相对分子质量比为4:15
D.若继续反应至丙为55g,丙刚好是丁质量的5倍
【解答】解:A、乙反应前后质量不变,可能是该反应的催化剂,故选项不正确。
B、a=21+8+40+30﹣17﹣8﹣25=49,甲、丙反应后质量增大,是生成物,丁反应后质量减小,
是反应物,该反应是分解反应,反应的丁、甲、丙的质量比是(49g﹣30g):(21g﹣17g):
(40g﹣25g)=19:4:15,氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气,氯酸钾、
氯化钾、氧气质量比是245:149:96,因此该反应不是实验室用氯酸钾制取氧气,故选项不正
确。
C、不知道化学计量数,不能确定甲、丙相对分子质量比,故选项不正确。
D、反应的丙、丁的质量比是(40g﹣25g):(49﹣30)=15:19,若继续反应至丙为55g,则
又生成15g丙,同时反应的丁的质量是 19g,丁质量是 30g﹣19g=11g,丙刚好是丁质量的
55g÷11g=5倍,故选项正确。
故选:D。
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
1. 根据反应前后各物质的质量总和不变,计算未知物的质量。
2. 反应后质量减小→反应物;
反应后质量增大→生成物;
反应后质量不变→催化剂或不参与反应的杂质。
1. (2023秋•南召县期末)偏二甲肼(C H N )与N O 反应放出的能量能把火箭送入
2 8 2 2 4
太空,化学方程式为C H N +2N O ═2X↑+3N ↑+4H O↑。下列说法正确的是( )
2 8 2 2 4 2 2
A.X的化学式为CO
B.偏二甲肼中碳元素质量分数为40%
C.该反应属于分解反应
D.反应中不存在元素化合价的改变
【解答】解:A、反应前碳原子是2个,反应后应该是2个,包含在未知物质中,反应前后氢原
子都是8个,氮原子都是6个,反应后氧原子是8个,反应后应该是8个,其中4个包含在未知
物质中,X的化学式为CO ,该选项说法不正确;
2
24
B、偏二甲肼中碳的质量分数为: ×100%=40%,该选项说法正确;
60
C、反应物是两种,不是分解反应,该选项说法不正确;
D、反应中有单质生成,故反应中一定存在元素化合价的改变,该选项说法不正确。
故选:B。
2. (2023秋•剑阁县期末)下列归纳或推理正确的是( )
A.根据质量守恒定律,1g木炭与1g氧气充分反应生成2g二氧化碳
B.氧化物中含氧元素,所以含有氧元素的化合物就是氧化物
C.点燃H 与O 的混合气体可能发生爆炸,则点燃CH 与O 的混合气体也可能发生爆炸
2 2 4 2
D.单质是由一种元素组成,所以由一种元素组成的物质一定是单质
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【解答】解:A、碳与氧气反应生成二氧化碳的质量比为3:8,不是1:1,故错误;
B、氧化物由两种元素组成,其中一种是氧元素的化合物,氧化物中含氧元素,但含有氧元素的
化合物不一定是氧化物,如硫酸;错误;
C、点燃可燃性气体与空气或与氧气的混合物容易发生爆炸,氢气和甲烷都具有可燃性;正确;
D、单质由一种元素组成,由一种元素组成的物质不一定是单质;错误;
故选:C。
3. (2024•正阳县一模)已知Fe(OH) 和稀硝酸发生如下反应,3Fe(OH) +10HNO
2 2 3
=3X+NO↑+8H O。下列关于物质X的说法错误的是( )
2
A.物质X属于盐
B.物质X的溶液有大量Fe2+
C.物质X的溶液呈黄色
D.物质X由三种元素组成
【解答】解:A、由分析可知,X的化学式为Fe(NO ) ,它是由金属阳离子和酸根阴离子构
3 3
成的化合物,属于盐,故选项说法正确。
B、由分析可知,X的化学式为Fe(NO ) ,则物质X的溶液中有大量的Fe3+,故选项说法错
3 3
误。
C、由分析可知,X的化学式为Fe(NO ) ,铁离子在溶液中呈黄色,则物质X的溶液呈黄色,
3 3
故选项说法正确。
D、由分析可知,X的化学式为Fe(NO ) ,则物质X由铁、氮、氧三种元素组成,故选项说
3 3
法正确。
故选:B。
4. (2024•新邵县一模)一定条件下,密闭容器中发生了某一化学反应,涉及的物质为
甲、乙、丙、丁,如图为各物质在反应前和反应后某时刻的质量关系。下列说法不正确的是(
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
)
A.x的值是31
B.甲、丁的相对分子质量之比为7:11
C.丙可能为催化剂
D.反应中消耗甲和乙的质量比为7:4
【解答】解:A、由表中数据可知,x=20+20+20+20﹣13﹣16﹣20=31,故选项说法正确。
B、甲、丁的质量变化比为7g:11g=7:11,若甲、丁的化学计量数相同,则甲、丁的相对分子
质量之比可能为7:11,否则不是,故选项说法不正确。
C、反应前后丙的质量不变,则丙可能是该反应的催化剂,也可能是没有参加反应的物质,故选
项说法正确。
D、反应中消耗甲和乙的质量比为7g:4g=7:4,故选项说法正确。
故选:B。
5. (2023秋•林芝市期末)三氧化铬(CrO )常用于金属镀铬.工业上制造三氧化铬的
3
化学方程式为:Na Cr O +X═2CrO +Na SO +H O,其中X的化学式是 ( )
2 2 7 3 2 4 2
A.H S B.H SO C.H SO D.SO
2 2 3 2 4 2
【解答】解:根据质量守恒定律,反应前后原子种类和个数都不变,由化学方程式
Na Cr O +X═2CrO +Na SO +H O可知:反应前钠原子的个数是2个,反应后是2个;
2 2 7 3 2 4 2
反应前铬原子的个数是2个,反应后是2个;
反应前氧原子的个数是7个,反应后是11个,则其中4个包含在X中;
反应前氢原子的个数是0个,反应后是2个;
反应前硫原子的个数是0个,反应后1个;
由分析可知,每个X中含有4个氧原子、2个氢原子,1个硫原子,故化学式H SO 。
2 4
故选:C。
6. (2024•雁塔区校级二模)乙醇是一种重要的化工原料。科学家以金(Au)纳米粒子
和二氧化钛(TiO )作催化在一定条件下制取乙醇的微观示意图如图。
2
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
关于该反应的说法正确的是( )
A.反应前后金和二氧化钛的质量及性质均不变
B.参加反应的氢气与二氧化碳的质量比为3:22
C.反应前后原子和分子的数目均没有增减
D.乙醇由2个碳原子、6个氢原子、1个氧原子构成
Au
【解答】解:由反应的微观示意图可知,该反应的化学方程式为:6H +2CO
2 2 ¯
TiO
2
C H OH+3H O。
2 5 2
A、金和二氧化钛是该反应的催化剂,由催化剂的定义可知,反应前后金和二氧化钛的质量及化
学性质均不变,但物理性质可能发生改变,故选项说法错误;
B、由化学方程式的意义可知,参加反应的氢气与二氧化碳的质量比为(6×2):(2×44)=3:
22,故选项说法正确;
C、由反应的化学方程式可知,反应前后原子的数目均没有改变,但每8个分子变化成了4个分
子,分子的数目发生了改变,故选项说法错误;
D、乙醇是由乙醇分子构成,一个乙醇分子由2个碳原子,6个氢原子、1个氧原子构成,故选
项说法错误;
故选:B。
7. (2024•重庆二模)科学家研制出一种新型的催化剂,可以去除装修残留的甲醛
(CH O),反应过程的微观示意图如下,说法错误的是( )
2
A.分子在化学变化中可再分
B.反应前后分子数目发生改变
C.反应前后原子的数目没有改变
D.生成物均是氧化物
【解答】解:A、分子在化学变化中可再分,原子不可再分;故A正确;
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
B、由分析可知,反应前后的分子数目均为2,没有发生改变,故B错误;
C、化学反应前后原子的种类和数目均不改变,故C正确;
D、氧化物是由两种元素组成,其中一种为氧元素的化合物,该反应的生成物为二氧化碳和水,
均属于氧化物,故D正确;
故选:B。
8. (2024•碑林区校级模拟)如图表示甲转化为丙的微观过程。下列有关说法不正确的
是( )
A.转化②中的物质都属于氧化物
B.转化①中甲与O 的分子个数比为2:3
2
C.丙的化学式可以表示为H SO
2 4
D.整个转化过程中硫元素化合价升高
【解答】解:A、硫酸不是氧化物,该选项不正确。
B、转化①中硫化氢与O 的分子个数比为2:3,该选项正确。
2
C、丙的化学式可以表示为H SO ,该选项正确。
2 4
D、整个转化过程中硫元素化合价升高,由﹣2转化成+4,再转化成+6,该选项正确。
故选:A。
9. (2024•榆树市校级一模)模型认知是重要的科学方法,分析下列各图回答有关问题。
(1)元素周期表中氮元素的某些信息如图 1 所示,由图 1 可知,氮的相对原子质量为
。
(2)图2表示“氮元素的价类二维图”,请回答下列问题。
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
①N 属于单质,是因为 。
2
②写出图中B点对应物质的化学式 。
(3)神舟十六号载人飞船于2023年5月30日发射成功,其使用的燃料中的一种燃烧时发生化
学 反 应 的 微 观 示 意 图 如 图 3 所 示 , 请 写 出 该 反 应 的 化 学 方 程 式
点燃 (提示:甲在常温常压下为气体)。
O +2N H ¯ 3N +4H O
2 4 2 4 ❑ 2 2
【解答】解:(1)元素周期表中氮元素的某些信息如图1所示,由图1可知,氮的相对原子质
量为14.01。
(2)①N 属于单质,是因为氮气是由氮元素组成的纯净物。
2
②图中B点对应物质的化学式是HNO 。
3
(3)该反应的化学方程式是 点燃 。
N O +2N H ¯ 3N +4H O
2 4 2 4 ❑ 2 2
故答案为:(1)14.01。
(2)①氮气是由一种元素组成的纯净物。
②HNO 。
3
(3) 点燃 。
N O +2N H ¯ 3N +4H O
2 4 2 4 ❑ 2 2
10. (2023•蒙阴县一模)“宏观﹣微观﹣符号”三重表征是化学独特的表示物质及其变
化的方法。某化学反应的微观示意图如图所示,回答下列问题。
(1)写出该反应的化学方程式为 ;
(2)从微观角度分析,反应前后 不变;(写出一点即可)
(3)该反应前后共涉及 种分子。
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【解答】解:(1)由反应的微观示意图可知,该反应是一氧化氮和一氧化碳在催化剂的作用下
生成二氧化碳和氮气,反应的化学方程式为:2NO+2CO 催化剂 2CO +N 。
2 2
¯
❑
(2)从微观角度分析,反应前后原子的种类、数目和质量不变。
(3)由反应的微观示意图可知,该反应前后共涉及一氧化氮、一氧化碳、二氧化碳和氮气 4种
分子。
故答案为:
(1)2NO+2CO 催化剂 2CO +N ;
2 2
¯
❑
(2)原子的种类;
(3)4。
11. (2023•双台子区校级模拟)化学在疫情防控中的价值。
(1)疫情防控期间常用的消毒剂有75%的酒精溶液、过氧乙酸溶液和84消毒液。在室内喷洒
高 浓 度 的 酒 精 消 毒 极 易 引 发 火 灾 , 酒 精 完 全 燃 烧 的 化 学 反 应 方 程 式 为 :
点燃 。84消毒液主要有效成分为次氯酸钠(NaClO),其
H OH+3O ¯ 2CO +3H O
2 5 2 ❑ 2 2
中氯元素的化合价为 。制备次氯酸钠的一种方法为:X+2NaOH═NaCl+NaClO+H O,
2
X的化学式为 ,其判断依据为 。
(2)中医药在抗击新冠肺炎中起重要作用,传统的煎煮方法提炼出来的中药中的有效成分偏低;
通过乙醚浸泡,水浴蒸发浓缩的提炼方法可使有效成分的提炼得以提高,水浴加热的优点:
。根据以上描述可以得知中药中的有效成分在水中的溶解能力比在乙醚中的溶解能力 。
【 解 答 】 解 : ( 1 ) 酒 精 完 全 燃 烧 生 成 二 氧 化 碳 和 水 , 化 学 方 程 式 为 :
点燃 ;次氯酸钠(NaClO)中钠元素通常显+1价,氧元素通
C H OH+3O ¯ 2CO +3H O
2 5 2 ❑ 2 2
常显﹣2价,设次氯酸钠(NaClO)氯元素化合价为x,根据化合物中正、负化合价的代数和为
零,(+1)+x+(﹣2)=0,x=+1,故氯元素的化合价为+1价;根据化学方程式:反应前
2Na、2O、2H,反应后2Na、2Cl、2O、2H,根据质量守恒定律,化学反应前后原子种类、数目
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
不变,X中含2Cl,为Cl ;
2
(2)水浴加热的优点可控制加热的温度或受热均匀等,传统的煎煮方法提炼出来的中药中的有
效成分偏低;通过乙醚浸泡,水浴蒸发浓缩的提炼方法可使有效成分的提炼得以提高,根据以
上描述可以得知中药中的有效成分在水中的溶解能力比在乙醚中的溶解能力小或弱。
故答案为:(1) 点燃 ;+1;Cl ;质量守恒定律。
2
C H OH+3O ¯ 2CO +3H O
2 5 2 ❑ 2 2
(2)可控制加热的温度或受热均匀等;小。
12. (2023•秀英区校级模拟)海南五指山少数民族地区的酒文化源远流长,民间常有
“以酒会客”的习俗,其中家酿的“山兰酒”还拥有“茅台”的美称,称之为“biang”,是
采用所居山区一种旱糯稻山兰稻酿制,是真正的绿色酒类。请你回答下列问题:
(1)旱糯稻山兰稻酿制成酒属于 变化,“山兰酒”开瓶十里香,这表明分子具有
的性质;
(2)“山谷酒”的主要成分之一是乙醇(化学式为C H OH),乙醇中C、H、O三种元素的质
2 5
量比为 ;
(3)“开车不喝酒,喝酒不开车”。国家对“酒驾”给予了更严厉的处罚。交警用“酒精检测
仪”很快可以检测出司机的饮酒程度,其化学反应原理是:C H OH+4X+6H SO ═2Cr (SO )
2 5 2 4 2 4
3
+2CO
2
↑+9H
2
O,化学方程式中X的化学式是 。
【解答】解:(1)旱糯稻山兰稻酿制成酒过程有新物质生成,属于化学变化;“山兰酒”开瓶
十里香,这表明分子具有不断运动的性质。
(2)乙醇中C、H、O三种元素的质量比为:(12×2):(1×6):(16×1)=12:3:8。
(3)根据化学反应前后各原子种类和数目不变,反应物中除X外C、H、O、S原子的数目分别
为2、18、25、6,生成物中C、H、O、S、Cr原子的数目分别为2、18、37、6、4,X的化学计
量数为4,所以一个X分子中有1个原子和3个氧原子,X的化学式为CrO 。
3
故答案为:(1)化学;不断运动。
(2)12:3:8。
(3)CrO 。
3
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
13. (2023•温县三模)丙烷(C H )是液化石油气的主要成分之一,将44g丙烷与一定
3 8
量的氧气在密闭容器中引燃,恰好完全反应。已知生成CO 和CO的质量比为22:7,则生成
2
H O的质量为 ,反应中消耗O 的质量为 。
2 2
12×3
【解答】解:44gC H 中含碳元素的质量为44g× ×100%=36g,则C H 中氢元
3 8 12×3+1×8 3 8
8g
=72g
素的质量为44g﹣36g=8g,则生成的水的质量为 2 ;已知生成CO 和CO的质
×100% 2
18
量比为 22:7,设生成的二氧化碳的质量为 22x,则生成的一氧化碳的质量为 7x;
12 12
22x× ×100%+7x× ×100%=36g,x=4g,则生成的二氧化碳的质量为22×4g=88g,
44 28
生成的一氧化碳的质量为7×4g=28g;根据质量守恒定律,化学反应前后物质的总质量不变,则
消耗的氧气的质量为88g+28g+72g﹣44g=144g。故答案为:72g;144g。
14. (2023•驿城区校级三模)5.2gC H 在点燃时能与 14.4gO 反应,得到13.2gCO 和
2 2 2 2
mgCO等,则m为 ,该反应的化学方程式为 。
24
【解答】解:乙炔中碳元素的质量为:5.2g× ×100%=4.8g,氢元素的质量为5.2g﹣4.8g=
26
12
0.4g,二氧化碳中碳元素的质量为:13.2g× ×100%=3.6g,一氧化碳的质量为:
44
4.8g−3.6g
= 2
12 2.8g,水的质量为:0.4g× ×100%=3.6g;故乙炔、氧气、二氧化碳、一氧化
×100% 18
28
5.2g 14.4g 13.2g 2.8g 3.6g
碳、水的化学计量数之比是: : : : : =4:9:6:2:4;
26 32 44 28 18
点燃
故 m 为 2.8,化学方程式为 4C H +9O 6CO +2CO+4H O。故答案为:2.8;4C H +9O
2 2 2 2 2 2 2 2
¯
❑
点燃6CO +2CO+4H O。
2 2
¯
❑
15. (2023•夏邑县模拟)某化合物4.8g在氧气中充分燃烧,生成6.6g二氧化碳和5.4g水,
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
消耗氧气的质量为 g;若该化合物的相对分子质量为32,该反应的化学方程式为
。
【解答】解:根据质量守恒定律可知,化学反应前后物质的总质量保持不变,故消耗氧气的质
量为6.6g+5.4g﹣4.8g=7.2g;该化合物的化学式用X表示,由各物质的质量和相对分子质量可知,
反应中各物质的分子个数(用 n 表示)比为 n(X):n(O ):n(CO ):n(H O)
2 2 2
4.8g 7.2g 6.6g 5.4g 2:3:2:4,故该反应的化学方程式可表示为2X+3O 点燃
= : : : = 2
¯
32 32 44 18
❑
2CO +4H O,因为化学反应前后,原子的种类和数目保持不变,反应后共有2个碳原子、8个氧
2 2
原子和8个氢原子,反应前已有6个氧原子,则2X中含有2个碳原子、8个氢原子和2个氧原
点燃
子,故该化合物为CH O,因此该反应的化学方程式为2CH O+3O 2CO +4H O。
4 4 2 2 2
¯
❑
点燃
故答案为:7.2;2CH O+3O 2CO +4H O。
4 2 2 2
¯
❑
16. (2023•枣阳市二模)几十年来,从“东方红”唱响到“神舟”逐梦,从“北斗”指
路到“嫦娥”揽月,从“祝融”探火到“天宫”遨游……中国航天一次次的非凡突破,让中国
印记闪耀星空。
点燃
(1)20世纪以前,黑火药作为火箭推进剂,其反应为:2KNO +S+3C K S+N +3X,X的
3 2 2
¯
❑
化学式为 。
(2)1970年,中国第一颗人造卫星发射升空,其推进剂为偏二甲肼(C H N )和四氧化二氮,
2 8 2
偏二甲肼中氮、氢元素的质量比为 。
(3)2022年中国空间站全面建成.通电分解水是空间站供氧的一种方法,氧气可以从电源的
极获得。
【解答】解:(1)根据质量守恒定律,化学反应前后原子的种类和数目不变,由反应的化学方
点燃
程式2KNO +S+3C K S+N +3X可知,反应物中含K、N、O、S、C的个数分别是2、2、
3 2 2
¯
❑
6、1、3,生成物中含K、N、O、S、C的个数分别是2、2、0、1、0,则3X中含有6个O、3
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
个C,所以X的化学式为:CO 。
2
(2)偏二甲肼(C H N )中氮、氢元素的质量比为(14×2):8=7:2。
2 8 2
(3)通电分解水是空间站供氧的一种方法,在电解水实验中,“正氧负氢”,则氧气可以从电
源的正极获得。
故答案为:
(1)CO ;
2
(2)7:2;
(3)正。
17. (2023•昂仁县二模)2012年6月24日,中国载人航天工程实现新突破,神舟九号航
天员成功驾驶飞船与天宫一号目标飞行器对接,这标志着中国成为世界上第三个完整掌握空间
交会对接技术的国家。四氧化二氮(N O )是运载神舟九号的长征2号F运载火箭的推进剂之
2 4
一。在室温、101kPa时,四氧化二氮是无色气体,易转化为二氧化氮(NO )。二氧化氮有毒,
2
在紫外线的作用下能破坏臭氧层。因此,我国将于2014年投入使用的长征5号运载火箭将全
部使用无毒无污染的新型环保燃料。
(1)二氧化氮(NO )中氮元素的化合价为 ;
2
(2)四氧化二氮(N O )中氮元素与氧元素的质量比为 ;
2 4
(3)液态四氧化二氮的化学性质与气态四氧化二氮相同,请从微观的角度分析其原因
;
(4)为减少二氧化氮对环境的污染,可用氢氧化钠溶液进行吸收处理,其反应的化学方程式为;
2NO
2
+2NaOH=NaNO
3
+X+H
2
O,其中X的化学式为 。
【解答】解:(1)NO 中,氧元素化合价为﹣2价,设氮元素化合价为x,根据化合价原则,化
2
合物中各元素化合价代数和为零,则x+(﹣2)×2=0,解得x=+4,所以二氧化氮(NO )中氮
2
元素的化合价为+4。
(2)N O 中氮元素与氧元素的质量比为(14×2):(16×4)=7:16。
2 4
(3)液态四氧化二氮的化学性质与气态四氧化二氮相同,从微观的角度分析其原因是:气态四
氧化二氮和液态四氧化二氮由同种分子构成。
(4)根据质量守恒定律,化学反应前后原子的种类和数目不变,由反应的化学方程式
2NO +2NaOH=NaNO +X+H O可知,等号左边有2个氮原子、2个钠原子、2个氢原子和6个氧
2 3 2
原子,等号右边除X外,有1个钠原子、1个氮原子、2个氢原子和4个氧原子,则X中含有1
个钠原子、1个氮原子和2个氧原子,所以X的化学式为NaNO 。
2
故答案为:
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)+4;
(2)7:16;
(3)气态四氧化二氮和液态四氧化二氮由同种分子构成;
(4)NaNO 。
2
18. (2023•岱岳区二模)2023年4月20日,“中国龙芯之母”黄令仪同志因病抢救无效
去世。她所参与研发的“龙芯1号”的问世,打破了国产计算机无芯可用的困局!半导体材料
的不断发展,加快了智能芯片的不断革新。
(1)第一代半导体材料为硅材料、锗材料。
Ⅰ.锗的化学性质与硅相似,如图1是两者在元素周期表中的信息,下列说法正确的是 。
A.硅和锗元素都属于非金属元素
B.硅、锗原子的质子数相等
C.锗的相对原子质量为72.61
D.硅、锗原子的最外层电子数都是4
Ⅱ.工业制备高纯硅的方法为:氢气与四氯化硅(SiCl ) 在高温下发生置换反应,请写出该反应
4
的化学方程式 。
(2)第二代半导体材料以砷化镓、磷化铟为主。铟原子、磷原子的原子结构示意图如图2所示。
Ⅰ.铟元素在第 周期。X的数值应为 。
Ⅱ.磷化铟的化学式为 。
(3)第三代半导体材料为碳化硅和氮化镓等。
一定条件
Ⅰ.氮化镓的制备方法为GaCl +NH GaN+3X,则X的化学式为 。
3 3
¯
❑
Ⅱ.碳化硅(SiC)中Si的化合价为+4价,则SiC中C的化合价为 。
【解答】解:(1)Ⅰ.A.硅元素属于非金属元素,锗元素属于金属元素,故A错误;
B.硅、锗元素属于不同元素,.硅、锗原子的质子数不相等,故B错误;
16关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.锗的相对原子质量为72.64,故C错误;
D.硅、锗原子的最外层电子数相等,都是4,故D正确。
故选:D。
高温
Ⅱ.氢气与四氯化硅(SiCl ) 在高温下发生置换反应,该反应的化学方程式为2H +SiCl
4 2 4
¯
❑
Si+4HCl。
(2)Ⅰ.铟原子核外有5个电子层,故铟元素在第5周期。在原子中,质子数=核外电子数,49
=2+X+18+18+3,X的数值应为8。
Ⅱ.磷元素的化合价为﹣3价,铟元素的化合价为+3价,根据化合物中,正、负化合价的代数和
为零,故磷化铟的化学式为InP。
(3)Ⅰ.根据质量守恒定律可知,化学反应前后原子的种类和数目不变,氮化镓的制备方法为
一定条件
GaCl +NH GaN+3X,则X的化学式为HCl。
3 3
¯
❑
Ⅱ.碳化硅(SiC)中Si的化合价为+4价,根据化合物中,正、负化合价的代数和为零,则SiC
中C的化合价为﹣4。
19. (2023•潍坊一模)质量守恒定律是化学变化中的一个基本规律。请根据图示回答下
列问题。
17关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
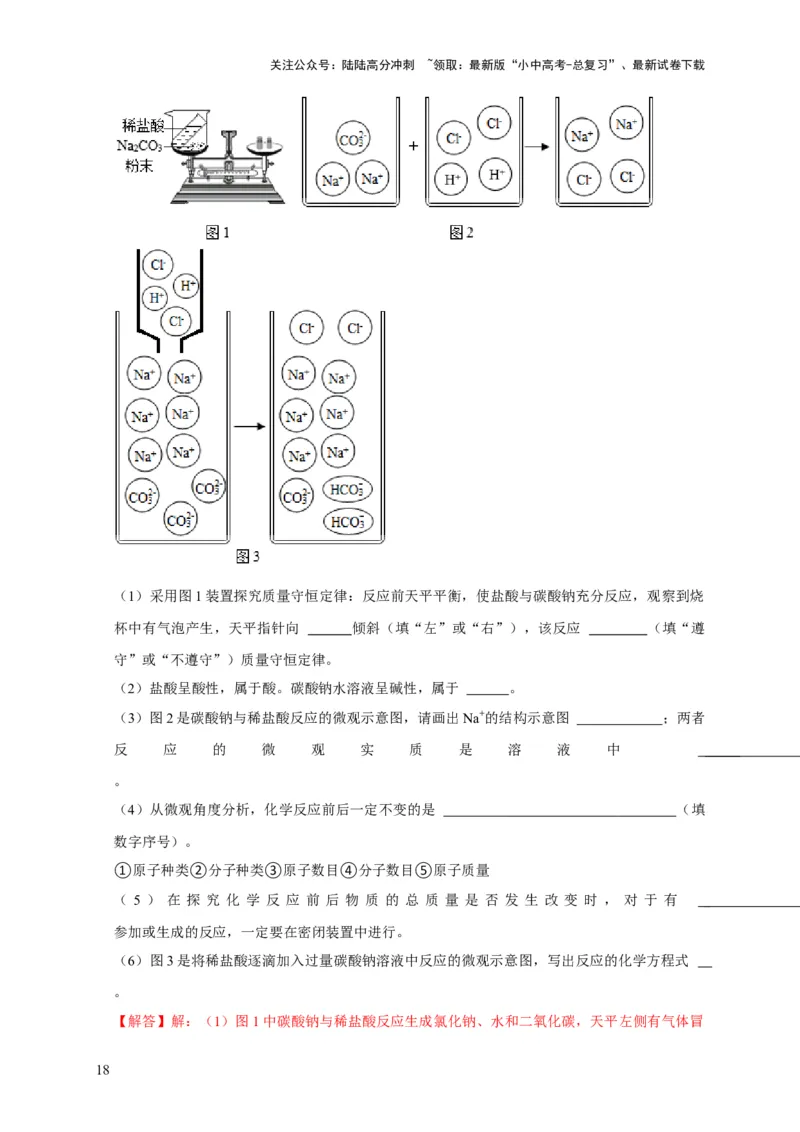
(1)采用图1装置探究质量守恒定律:反应前天平平衡,使盐酸与碳酸钠充分反应,观察到烧
杯中有气泡产生,天平指针向 倾斜(填“左”或“右”),该反应 (填“遵
守”或“不遵守”)质量守恒定律。
(2)盐酸呈酸性,属于酸。碳酸钠水溶液呈碱性,属于 。
(3)图2是碳酸钠与稀盐酸反应的微观示意图,请画出Na+的结构示意图 ;两者
反 应 的 微 观 实 质 是 溶 液 中
。
(4)从微观角度分析,化学反应前后一定不变的是 (填
数字序号)。
①原子种类②分子种类③原子数目④分子数目⑤原子质量
( 5 ) 在 探 究 化 学 反 应 前 后 物 质 的 总 质 量 是 否 发 生 改 变 时 , 对 于 有
参加或生成的反应,一定要在密闭装置中进行。
(6)图3是将稀盐酸逐滴加入过量碳酸钠溶液中反应的微观示意图,写出反应的化学方程式
。
【解答】解:(1)图1中碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳,天平左侧有气体冒
18关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
出,左边质量减轻,故天平指针向右倾斜,反应后,右侧砝码质量=左侧质量+冒出的气体质量,
该反应遵守质量守恒定律。
(2)碳酸钠溶液虽然是碱性,但碳酸钠由金属离子钠离子和酸根离子碳酸根离子构成,属于盐;
(3)钠离子由钠原子失去一个电子形成,核电荷数为11,核外电子数为10,结构示意图为:
;图2所示钠离子和氯离子反应前后没有发生变化,而碳酸根离子和氢离子发生反应
生成水和二氧化碳;
(4)根据质量守恒定律,化学反应前后原子种类、原子数目、原子质量一定不变,分子种类一
定变化、分子数目可能变化;
(5)在探究化学反应前后物质的总质量是否发生改变时,为防止与外界有物质交换,对于有气
体参加或生成的反应,一定要在密闭装置中进行。
(6)根据图3,碳酸钠与稀盐酸反应生成碳酸氢钠和氯化钠,化学方程式为:Na CO +HCl=
2 3
NaHCO +NaCl。
3
19