文档内容
江苏省苏州市2025-2026学年第一学期高三期初学情调研测试化学试题
(考试时间:75分钟 满分:100分)
可能用到的相对原子质量: H-1 C-12 N-14 O-16 Na-23 V-51 Sr-88
1. 我国科学家在月壤中发现一种新矿物———嫦娥石[Ca₈YFe(PO₄)₇]。下列元素不属于主族元素的是
A. P B. Ca C. Fe D. O
2. 反应 2NH +NaClO=NaCl+N H +H O可用于制备肼(N₂H₄)。下列说法正确的是
3 2 4 2
A. NH₃是非极性分子 B. NaClO 既含有离子键又含有共价键
C. CT的结构示意图为 D. N₂H₄的结构式为
3. 实验室利用氨气和氯气反应制备氯化铵,下列实验装置和操作不能达到实验目的的是
4. CO(NH₂)₂是常用氮肥。下列说法不正确的是
A. 原子半径:r(C)>r(N)>r(O) B. 稳定性: CH >NH >H O
4 3 2
C. 第一电离能:I₁(N)>I₁(O)>I₁(C) D. 电负性: x(O)>x(N)>x(C)
阅读下列资料,完成5~7题:
周期表中IVA 族元素及其化合物应用广泛,甲烷具有较大的燃烧热(890. 3kJ·mol⁻¹), Si、Ge是重要
的半导体材料,硅晶体表面 SiO₂能与氢氟酸(HF,弱酸)反应生成 H SiF (H SiF 在水中完全电离为
2 6 2 6
H⁺和SiF²⁻);1885年德国化学家将硫化锗(GeS₂)与H₂共热制得了门捷列夫预言的类硅⁻锗;Si₃N₄是一
种高强度耐高温材料,可由 SiO₂、C、N₂高温反应制得,同时生成CO。Pb,PbO₂是铅蓄电池的电极
材料。
5. 下列说法正确的是
A. CH₄空间构型为平面正方形 B. Si₃N₄为分子晶体
C. Ge基态核外价层电子排布式: [Ar]4s24p2 D. HF 能形成分子间氢键
6. 下列化学反应表示不正确的是
高温
3SiO +6C+2N
A. 制备氮化硅: 2 2_______
Si N +6CO¿
¿ 3 4
B. 铅蓄电池放电时负极反应: Pb−2e−+SO2− =PbSO
4 4
C. 电解水制氢的阳极反应: 2H O−2e−=H +2OH−
2 2
D. 甲烷的燃烧: CH (g)+2O (g)=CO (g)+2H O(l)△H=−890. 3kJ·mo l−1
4 2 2 27. 下列物质结构与性质或物质性质与用途具有对应关系的是
A. 甲烷具有还原性,可用作燃料 B. 石墨能导电、可用作润滑剂
C. 含铅化合物颜色丰富,可用作电极材料 D. SiO₂为酸性氧化物,可用作光导纤维
催化剂
4NH (g)+5O (g)
8. 对于反应 3 2 _________ 下列说法正确的是
4NO(g)+6H O(g);△H<0。¿
¿ 2
A. 该反应的△S<0
c4 (NO)
B. 该反应的平衡常数 K=
c4 (NH )c2 (O )
3 2
C. 催化剂能降低该反应的焓变
D. 该反应中每消耗1molNH₃,转移电子数约为 5×6. 02×1023
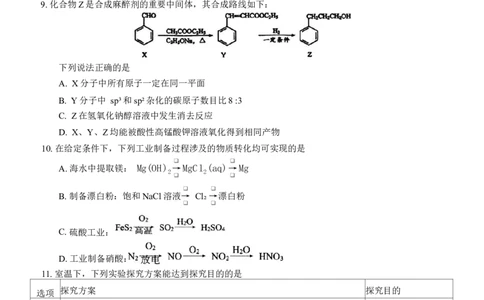
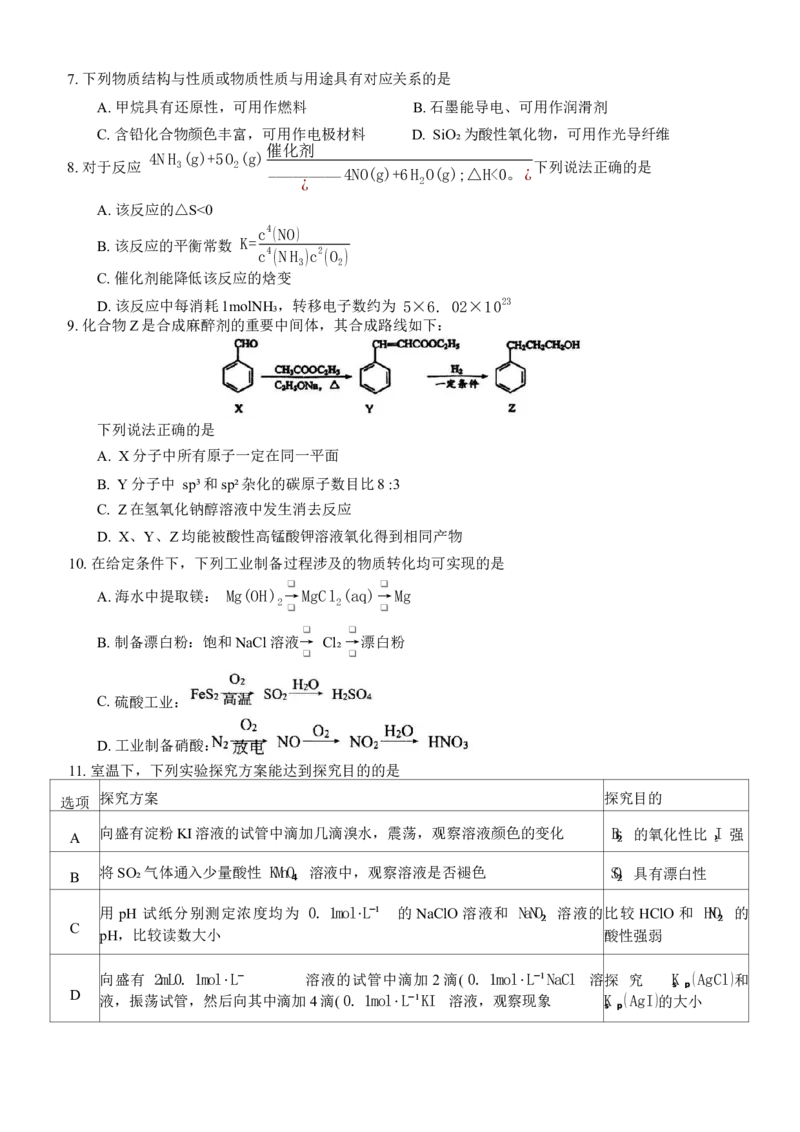
9. 化合物Z是合成麻醉剂的重要中间体,其合成路线如下:
下列说法正确的是
A. X分子中所有原子一定在同一平面
B. Y 分子中 sp³和sp²杂化的碳原子数目比8 :3
C. Z在氢氧化钠醇溶液中发生消去反应
D. X、Y、Z均能被酸性高锰酸钾溶液氧化得到相同产物
10. 在给定条件下,下列工业制备过程涉及的物质转化均可实现的是
❑ ❑
A. 海水中提取镁: Mg(OH) →MgCl (aq)→Mg
2 2
❑ ❑
❑ ❑
B. 制备漂白粉:饱和NaCl溶液→ Cl₂ →漂白粉
❑ ❑
C. 硫酸工业:
D. 工业制备硝酸:
11. 室温下,下列实验探究方案能达到探究目的的是
选项 探究方案 探究目的
A 向盛有淀粉KI溶液的试管中滴加几滴溴水,震荡,观察溶液颜色的变化 Br₂ 的氧化性比 ₂I 强
B 将SO₂气体通入少量酸性 KMnO₄ 溶液中,观察溶液是否褪色 SO₂ 具有漂白性
用pH 试纸分别测定浓度均为 0. 1mol⋅L⁻¹ 的NaClO溶液和 NaNO₂ 溶液的比较 HClO 和 HNO₂ 的
C
pH,比较读数大小 酸性强弱
向盛有 2mL0. 1mol⋅L⁻ 溶液的试管¹中Ag滴NO加₃ 2滴( 0. 1mol⋅L⁻¹NaCl 溶探 究 Kₛ ₚ(AgCl)和
D
液,振荡试管,然后向其中滴加4滴( 0. 1mol⋅L⁻¹KI 溶液,观察现象 Kₛ ₚ(AgI)的大小12. 室温下, 通过下列实验探究NaHCO₃、Na₂CO₃溶液的性质。
实验1:用pH 试纸测量( 0. 1mol⋅ L−1NaHCO 溶液的pH,测得pH约为8
3
实验2:将 0. 1mol⋅ L−1NaHCO 溶液与 0. 1mol⋅ L−1CaCl 溶液等体积混合,产生白色沉淀
3 2
实验3:向饱和 Na₂CO₃溶液中通入CO₂,溶液pH从12下降到约为9
下列说法正确的是
A. NaHCO₃溶液中: c(CO2−)+c(H+)=c(H CO )+c(OH−)
3 2 3
B. 由实验1可得出: c(CO2−)>c(H CO )
3 2 3
C. 实验2中两溶液混合时有: c(Ca2+)⋅c(CO2−)=K (CaCO )
3 sp 3
D. 实验3 中发生反应的化学方程式为: 2Na++CO2− +H O+CO =2NaHCO ↓
3 2 2 3
13. 二氧化碳加氢制甲烷过程中的主要反应为
反应 ICO
2
(g)+4H
2
(g)=CH
4
(g)+2H
2
O(g) △H₁
反应Ⅰ ICO
2
(g)+H
2
(g)=CO(g)+H
2
O(g) △H₂
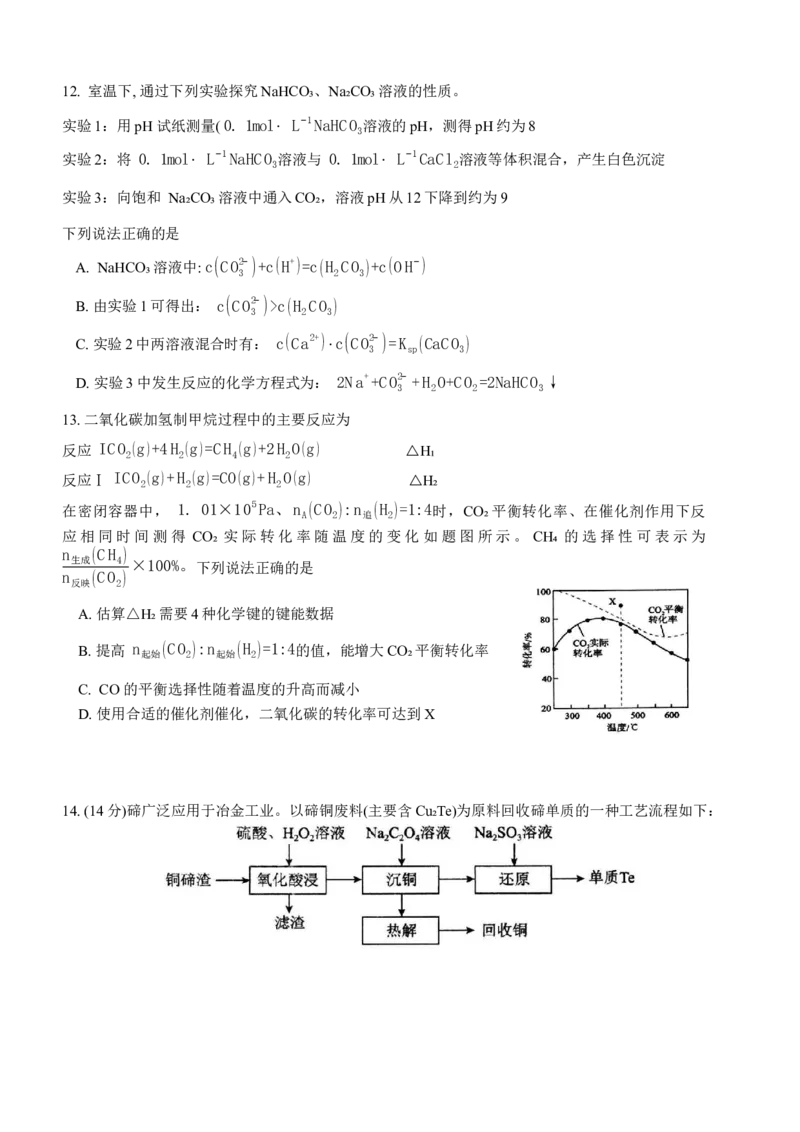
在密闭容器中, 1. 01×105Pa、n (CO ):n (H )=1:4时,CO₂平衡转化率、在催化剂作用下反
A 2 追 2
应相同时间测得 CO₂ 实际转化率随温度的变化如题图所示。 CH₄ 的选择性可表示为
n (CH )
生成 4 ×100%。下列说法正确的是
n (CO )
反映 2
A. 估算△H₂需要4种化学键的键能数据
B. 提高 n (CO ):n (H )=1:4的值,能增大CO₂平衡转化率
起始 2 起始 2
C. CO 的平衡选择性随着温度的升高而减小
D. 使用合适的催化剂催化,二氧化碳的转化率可达到X
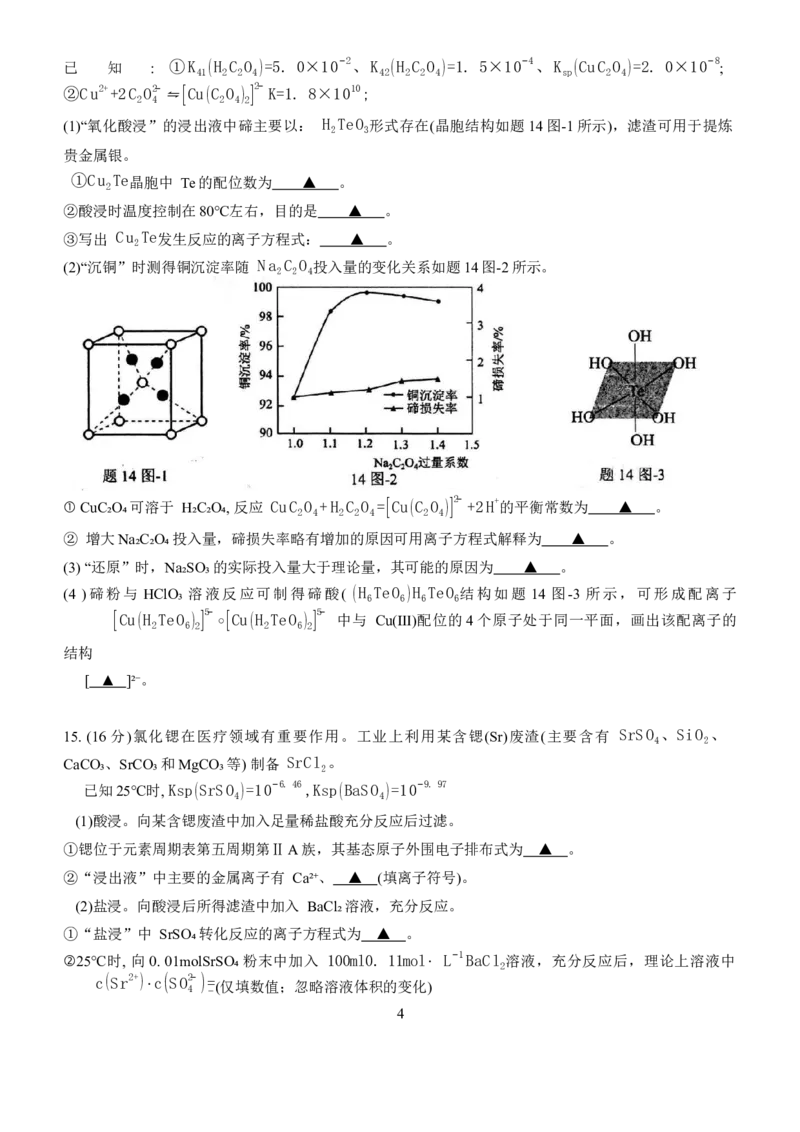
14. (14分)碲广泛应用于冶金工业。以碲铜废料(主要含Cu₂Te)为原料回收碲单质的一种工艺流程如下:已 知 : ①K (H C O )=5. 0×10−2、K (H C O )=1. 5×10−4、K (CuC O )=2. 0×10−8 ;
41 2 2 4 42 2 2 4 sp 2 4
②Cu2++2C O2− ⇋[Cu(C O ) ] 2− K=1. 8×1010;
2 4 2 4 2
(1)“氧化酸浸”的浸出液中碲主要以: H TeO 形式存在(晶胞结构如题14图-1所示),滤渣可用于提炼
2 3
贵金属银。
①Cu Te晶胞中 Te的配位数为 ▲ 。
2
②酸浸时温度控制在80℃左右,目的是 ▲ 。
③写出 Cu Te发生反应的离子方程式: ▲ 。
2
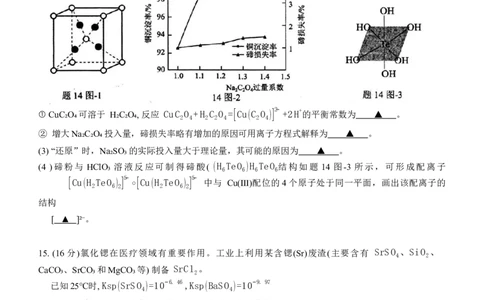
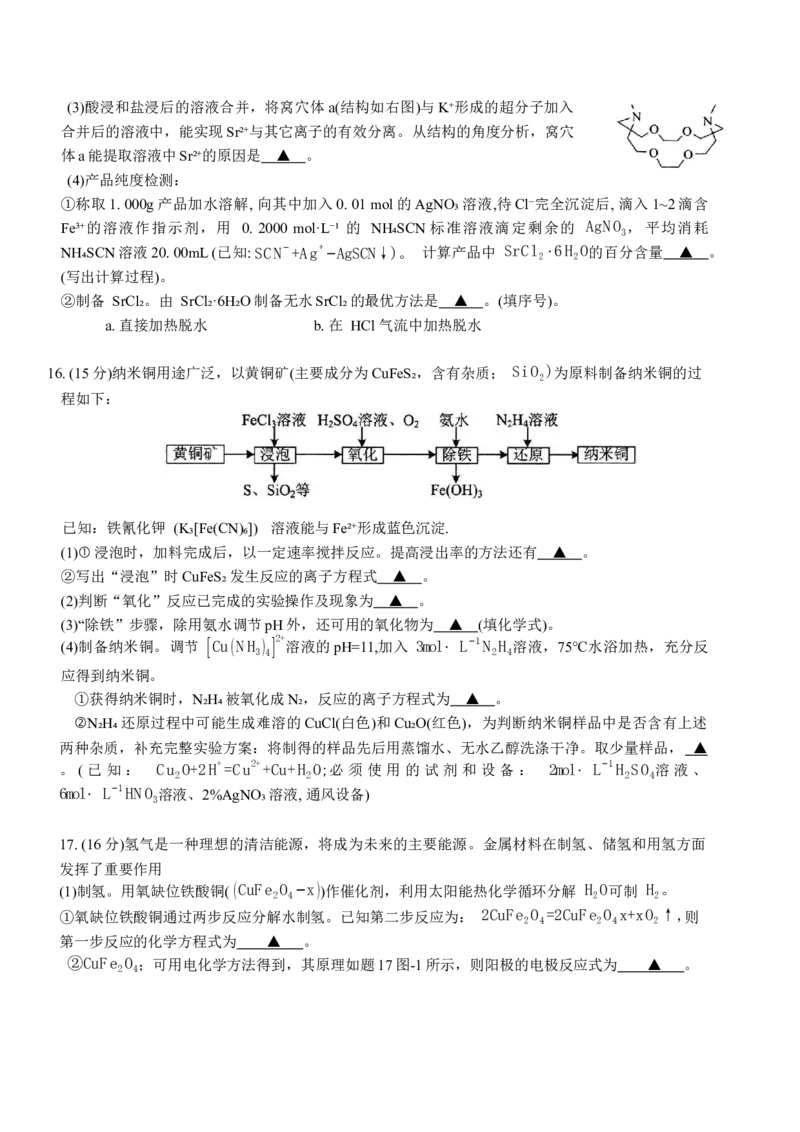
(2)“沉铜”时测得铜沉淀率随 Na C O 投入量的变化关系如题14图-2所示。
2 2 4
① CuC₂O₄可溶于 H₂C₂O₄, 反应 CuC O +H C O =[Cu(C O )] 2− +2H+的平衡常数为 ▲ 。
2 4 2 2 4 2 4
② 增大Na₂C₂O₄投入量,碲损失率略有增加的原因可用离子方程式解释为 ▲ 。
(3) “还原”时,Na₂SO₃的实际投入量大于理论量,其可能的原因为 ▲ 。
(4 )碲粉与 HClO₃ 溶液反应可制得碲酸( (H TeO )H TeO 结构如题 14 图-3 所示,可形成配离子
6 6 6 6
[Cu(H TeO ) ]
5−
∘[Cu(H TeO ) ]
5−
中与 Cu(Ⅲ)配位的4个原子处于同一平面,画出该配离子的
2 6 2 2 6 2
结构
[ ▲ ]²⁻。
15. (16 分)氯化锶在医疗领域有重要作用。工业上利用某含锶(Sr)废渣(主要含有 SrSO 、SiO 、
4 2
CaCO₃、SrCO₃和MgCO₃等) 制备 SrCl 。
2
已知25℃时, Ksp(SrSO )=10−6. 46,Ksp(BaSO )=10−9. 97
4 4
(1)酸浸。向某含锶废渣中加入足量稀盐酸充分反应后过滤。
①锶位于元素周期表第五周期第ⅡA 族,其基态原子外围电子排布式为 ▲ 。
②“浸出液”中主要的金属离子有 Ca²⁺、 ▲ (填离子符号)。
(2)盐浸。向酸浸后所得滤渣中加入 BaCl₂溶液,充分反应。
①“盐浸”中 SrSO₄转化反应的离子方程式为 ▲ 。
②25℃时, 向0. 01molSrSO₄粉末中加入 100ml0. 11mol⋅ L−1BaCl 溶液,充分反应后,理论上溶液中
2
c(Sr2+)⋅c(SO2
4
−)=
(仅填数值;忽略溶液体积的变化)
¯
4(3)酸浸和盐浸后的溶液合并,将窝穴体a(结构如右图)与K⁺形成的超分子加入
合并后的溶液中,能实现Sr²⁺与其它离子的有效分离。从结构的角度分析,窝穴
体a能提取溶液中Sr²⁺的原因是 ▲ 。
(4)产品纯度检测:
①称取1. 000g产品加水溶解, 向其中加入0. 01 mol的AgNO₃溶液,待Cl⁻完全沉淀后, 滴入1~2滴含
Fe³⁺的溶液作指示剂,用 0. 2000 mol·L⁻¹ 的 NH₄SCN 标准溶液滴定剩余的 AgNO , 平均消耗
3
NH₄SCN溶液20. 00mL (已知: SCN−+Ag+ −AgSCN↓)。 计算产品中 SrCl ⋅6H O的百分含量 ▲ 。
2 2
(写出计算过程)。
②制备 SrCl₂。由 SrCl₂·6H₂O制备无水SrCl₂的最优方法是 ▲ 。(填序号)。
a. 直接加热脱水 b. 在 HCl 气流中加热脱水
16. (15分)纳米铜用途广泛,以黄铜矿(主要成分为CuFeS₂,含有杂质; SiO )为原料制备纳米铜的过
2
程如下:
已知:铁氰化钾 (K₃[Fe(CN)₆]) 溶液能与Fe²⁺形成蓝色沉淀.
(1)①浸泡时,加料完成后,以一定速率搅拌反应。提高浸出率的方法还有 ▲ 。
②写出“浸泡”时CuFeS₂发生反应的离子方程式 ▲ 。
(2)判断“氧化”反应已完成的实验操作及现象为 ▲ 。
(3)“除铁”步骤,除用氨水调节pH外,还可用的氧化物为 ▲ (填化学式)。
(4)制备纳米铜。调节 [Cu(NH ) ] 2+ 溶液的pH=11,加入 3mol⋅ L−1N H 溶液,75℃水浴加热,充分反
3 4 2 4
应得到纳米铜。
①获得纳米铜时,N₂H₄被氧化成N₂,反应的离子方程式为 ▲ 。
②N₂H₄还原过程中可能生成难溶的CuCl(白色)和Cu₂O(红色),为判断纳米铜样品中是否含有上述
两种杂质,补充完整实验方案:将制得的样品先后用蒸馏水、无水乙醇洗涤干净。取少量样品, ▲
。 ( 已 知 : Cu O+2H+=Cu2++Cu+H O;必 须 使 用 的 试 剂 和 设 备 : 2mol⋅ L−1H SO 溶 液 、
2 2 2 4
6mol⋅ L−1HNO 溶液、2%AgNO₃溶液, 通风设备)
3
17. (16分)氢气是一种理想的清洁能源,将成为未来的主要能源。金属材料在制氢、储氢和用氢方面
发挥了重要作用
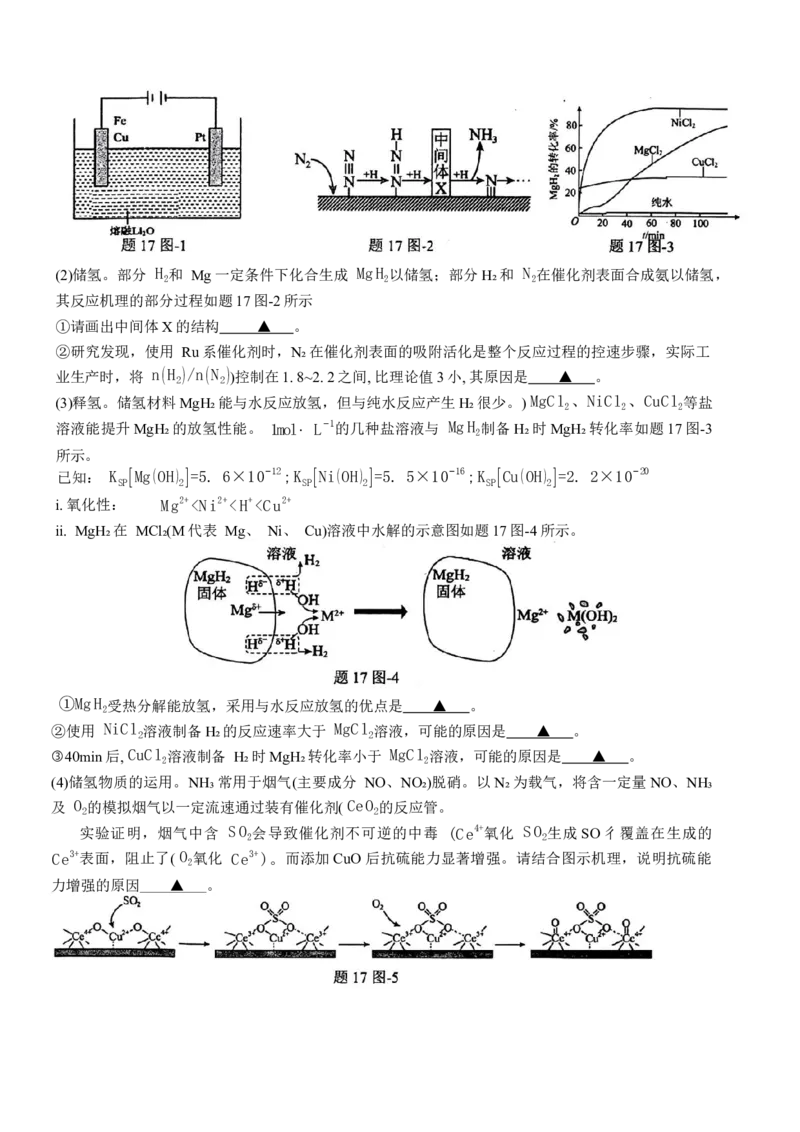
(1)制氢。用氧缺位铁酸铜( (CuFe O −x))作催化剂,利用太阳能热化学循环分解 H O可制 H 。
2 4 2 2
①氧缺位铁酸铜通过两步反应分解水制氢。已知第二步反应为: 2CuFe O =2CuFe O x+xO ↑,则
2 4 2 4 2
第一步反应的化学方程式为 ▲ 。
②CuFe O ;可用电化学方法得到,其原理如题17图-1所示,则阳极的电极反应式为 ▲ 。
2 4(2)储氢。部分 H 和 Mg一定条件下化合生成 MgH 以储氢;部分H₂和 N 在催化剂表面合成氨以储氢,
2 2 2
其反应机理的部分过程如题17图-2所示
①请画出中间体X的结构 ▲ 。
②研究发现,使用 Ru系催化剂时,N₂在催化剂表面的吸附活化是整个反应过程的控速步骤,实际工
业生产时,将 n(H )/n(N ))控制在1. 8~2. 2之间, 比理论值3小, 其原因是 ▲ 。
2 2
(3)释氢。储氢材料MgH₂能与水反应放氢,但与纯水反应产生H₂很少。) MgCl 、NiCl 、CuCl 等盐
2 2 2
溶液能提升MgH₂的放氢性能。 1mol⋅ L−1的几种盐溶液与 MgH
2
制备H₂时MgH₂转化率如题17图-3
所示。
已知: K [Mg(OH) ]=5. 6×10−12;K [Ni(OH) ]=5. 5×10−16;K [Cu(OH) ]=2. 2×10−20
SP 2 SP 2 SP 2
i. 氧化性: Mg2+