文档内容
绝密★考试结束前
2025 学年第一学期浙南名校联盟十月联考
高三年级化学学科 试题
命题学校:瓯海中学 陈耀斌 审题学校:龙湾中学 项彩虹 平阳中学 廖蒙蒙
考生须知:
1.本卷共6页,满分100分,考试时间90分钟。
2.答题前,在答题卷指定区域填写班级、姓名、考场号、座位号及准考证号并填涂相应数字。
3.所有答案必须写在答题纸上,写在试卷上无效。
4.考试结束后,只需上交答题纸。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Ca-40
选择题部分
一、选择题(本大题共16小题,每小题3分,共48分。每小题只有一个选项符合题意,不选、多
选、错选均不得分)
1. 下列属于共价化合物的是
A.NaOH B.Na O C.N D.CH
2 2 2 4
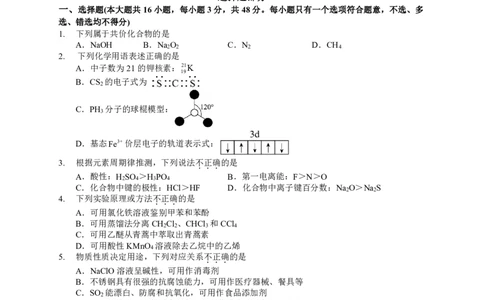
2. 下列化学用语表述正确的是
A.中子数为21的钾核素:21K
19
B.CS 的电子式为
2
C.PH 分子的球棍模型:
3
D.基态Fe3+价层电子的轨道表示式:
3. 根据元素周期律推测,下列说法不 . 正 . 确 . 的是
A.酸性:H SO >H PO B.第一电离能:F>N>O
2 4 3 4
C.化合物中键的极性:HCl>HF D.化合物中离子键百分数:Na O>Na S
2 2
4. 下列实验原理或方法不 . 正 . 确 . 的是
A.可用氯化铁溶液鉴别甲苯和苯酚
B.可用蒸馏法分离CH Cl 、CHCl 和CCl
2 2 3 4
C.可用乙醚从青蒿中萃取出青蒿素
D.可用酸性KMnO 溶液除去乙烷中的乙烯
4
5. 物质性质决定用途,下列对应关系不 . 正 . 确 . 的是
A.NaClO溶液呈碱性,可用作消毒剂
B.不锈钢具有很强的抗腐蚀能力,可用作医疗器械、餐具等
C.SO 能漂白、防腐和抗氧化,可用作食品添加剂
2
D.乙二醇的水溶液凝固点很低,可用作汽车发动机的防冻液
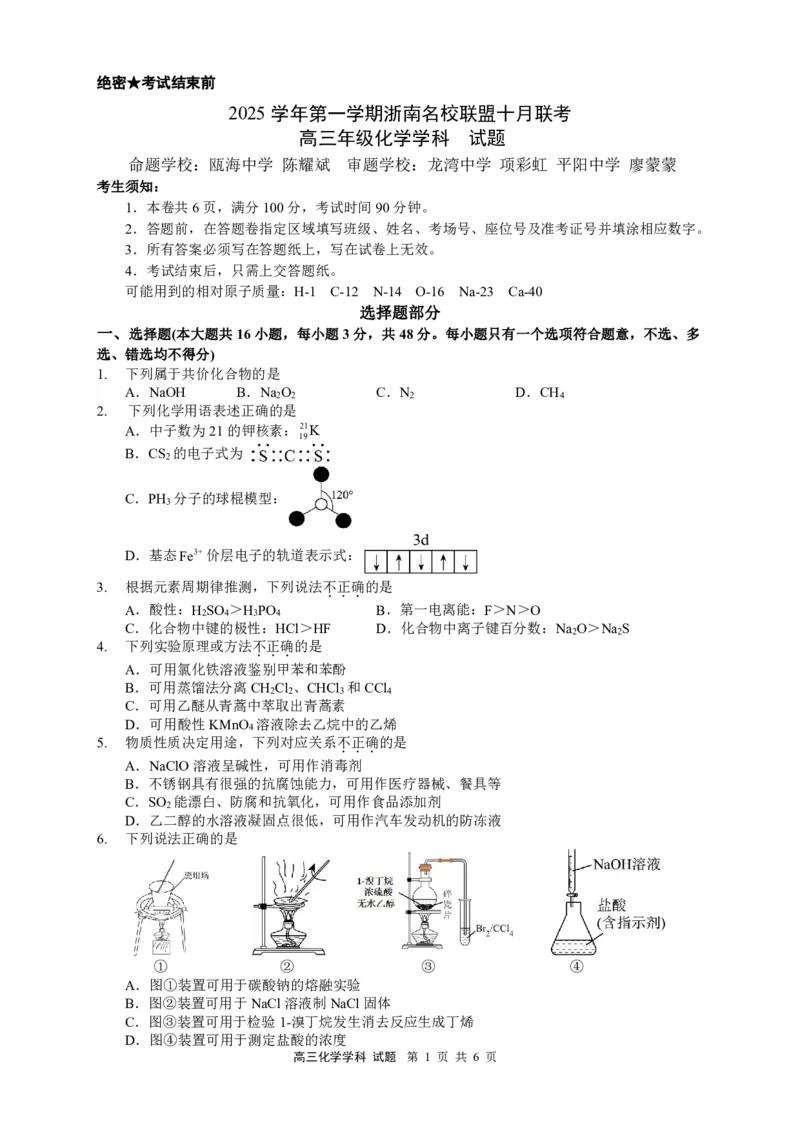
6. 下列说法正确的是
① ② ③ ④
A.图①装置可用于碳酸钠的熔融实验
B.图②装置可用于NaCl溶液制NaCl固体
C.图③装置可用于检验1-溴丁烷发生消去反应生成丁烯
D.图④装置可用于测定盐酸的浓度
高三化学学科 试题 第 1 页 共 6 页
{#{QQABaYE8wggQgNaACB4LAQmiCkkQkIOjJaoMBUATOAQCSIFIBIA=}#}7. 可根据物质结构推测其性质,下列推测的性质不 . 合 . 理 . 的是
选项 结构 性质
A NH NO 和CH NH NO 都含有离子键 两者的熔点相近
4 3 3 3 3
B 金刚石中共价键键能大 金刚石硬度高
C
聚丙烯酸钠具有高吸水性
聚丙烯酸钠的结构是
D 臭氧极性微弱 臭氧在CCl 中溶解度高于在水中溶解度
4
8. 下列反应的离子方程式书写不 . 正 . 确 . 的是
A.用Na O 和水制备少量O :2Na O +2H O=4Na++4OH-+O ↑
2 2 2 2 2 2 2
B.用KClO 和浓盐酸制备Cl :ClO -+5Cl-+6H+=3Cl ↑+3H O
3 2 3 2 2
C.用稀盐酸浸泡氧化银:Ag O+2H++2Cl-=2AgCl+H O
2 2
D.向NaHCO 溶液中通入少量Cl :2HCO -+Cl =2CO ↑+Cl-+ClO-+H O
3 2 3 2 2 2
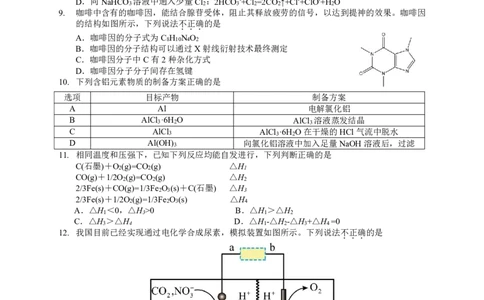
9. 咖啡中含有的咖啡因,能结合腺苷受体,阻止其释放疲劳的信号,以达到提神的效果。咖啡因
的结构如图所示,下列说法不正确的是
...
A.咖啡因的分子式为C H N O
8 10 4 2
B.咖啡因的分子结构可以通过X射线衍射技术最终测定
C.咖啡因分子中C有2种杂化方式
D.咖啡因分子分子间存在氢键
10. 下列含铝元素物质的制备方案正确的是
选项 目标产物 制备方案
A Al 电解氯化铝
B AlCl 3 ·6H 2 O AlCl 3 溶液蒸发结晶
C AlCl 3 AlCl 3 ·6H 2 O在干燥的HCl气流中脱水
D Al(OH)
3
向氯化铝溶液中加入足量NaOH溶液后,过滤
11. 相同温度和压强下,已知下列反应均能自发进行,下列判断正确的是
C(石墨)+O (g)=CO (g) △H
2 2 1
CO(g)+1/2O (g)=CO (g) △H
2 2 2
2/3Fe(s)+CO(g)=1/3Fe O (s)+C(石墨) △H
2 3 3
2/3Fe(s)+1/2O (g)=1/3Fe O (s) △H
2 2 3 4
A.△H <0,△H >0 B.△H >△H
1 3 1 2
C.△H >△H D.△H -△H -△H +△H =0
3 4 1 2 3 4
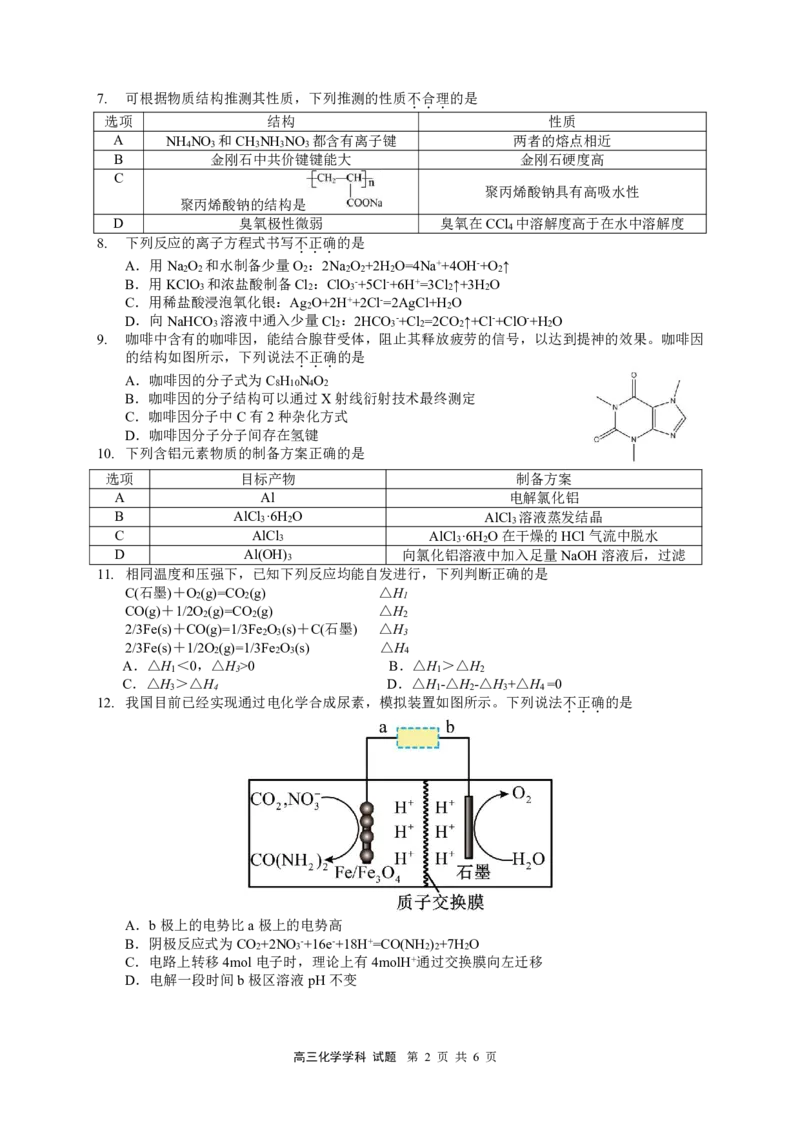
12. 我国目前已经实现通过电化学合成尿素,模拟装置如图所示。下列说法不 . 正 . 确 . 的是
A.b极上的电势比a极上的电势高
B.阴极反应式为CO +2NO -+16e-+18H+=CO(NH ) +7H O
2 3 2 2 2
C.电路上转移4mol电子时,理论上有4molH+通过交换膜向左迁移
D.电解一段时间b极区溶液pH不变
高三化学学科 试题 第 2 页 共 6 页
{#{QQABaYE8wggQgNaACB4LAQmiCkkQkIOjJaoMBUATOAQCSIFIBIA=}#}13. 氟氢化钾(KHF 2 ),晶体结构与NaCl类似,工业上可用于制氟气,下列说法不 . 正 . 确 . 的是
A.KHF 晶体中每个K+紧邻的K+有6个
2
B.KHF 中阴阳离子个数比是1:1
2
电解
C.电解熔融KHF 制F :2KHF 2KF+H ↑+F ↑
2 2 2 2 2
D.KHF 中的作用力有离子键、氢键、共价键
2
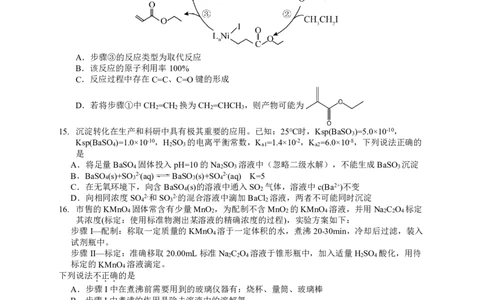
14. CO /C H 耦合反应制备丙烯酸乙酯的机理如图所示。下列说法正确的是
2 2 4
A.步骤③的反应类型为取代反应
B.该反应的原子利用率100%
C.反应过程中存在C=C、C=O键的形成
D.若将步骤①中CH =CH 换为CH =CHCH ,则产物可能为
2 2 2 3
15. 沉淀转化在生产和科研中具有极其重要的应用。已知:25℃时,Ksp(BaSO )=5.0×10-10,
3
Ksp(BaSO )=1.0×10-10,H SO 的电离平衡常数,K =1.4×10-2,K =6.0×10-8,下列说法正确的
4 2 3 a1 a2
是
A.将足量BaSO 固体投入pH=10的Na SO 溶液中(忽略二级水解),不能生成BaSO 沉淀
4 2 3 3
B.BaSO (s)+SO 2-(aq) BaSO (s)+SO 2-(aq) K=5
4 3 3 4
C.在无氧环境下,向含BaSO (s)的溶液中通入SO 气体,溶液中c(Ba2+)不变
4 2
D.向相同浓度SO 2-和SO 2-的混合溶液中滴加BaCl 溶液,两者不可能同时沉淀
4 3 2
16. 市售的KMnO 固体常含有少量MnO ,为配制不含MnO 的KMnO 溶液,并用Na C O 标定
4 2 2 4 2 2 4
其浓度(标定:使用标准物测出某溶液的精确浓度的过程),实验方案如下:
步骤I—配制:称取一定质量的KMnO 溶于一定体积的水,煮沸20-30min,冷却后过滤,装入
4
试剂瓶中。
步骤II—标定:准确移取20.00mL标准Na C O 溶液于锥形瓶中,加入适量H SO 酸化,用待
2 2 4 2 4
标定的KMnO 溶液滴定。
4
下列说法不正确的是
...
A.步骤I中在煮沸前需要用到的玻璃仪器有:烧杯、量筒、玻璃棒
B.步骤I中煮沸的作用是除去溶液中的溶解氧
C.步骤II的标定不需要加入指示剂
D.实验II中,滴定时发现一段时间后溶液中产生气泡速率突然加快,可能是Mn2+的催化作用
非选择题部分
二、非选择题(本大题共4小题,共52分)
17. (16分)锌和硫在工业中都有重要作用,也是人体必需元素。回答下列问题:
(1)下列说法正确的是 。
A.基态锌原子的价电子排布式为:4s2
B.碱性:[Zn(NH ) ]2+<NH
3 4 3
C.基态硫原子核外电子占据的原子轨道数为8
D.同周期元素中第一电离能大于硫元素的有三种
高三化学学科 试题 第 3 页 共 6 页
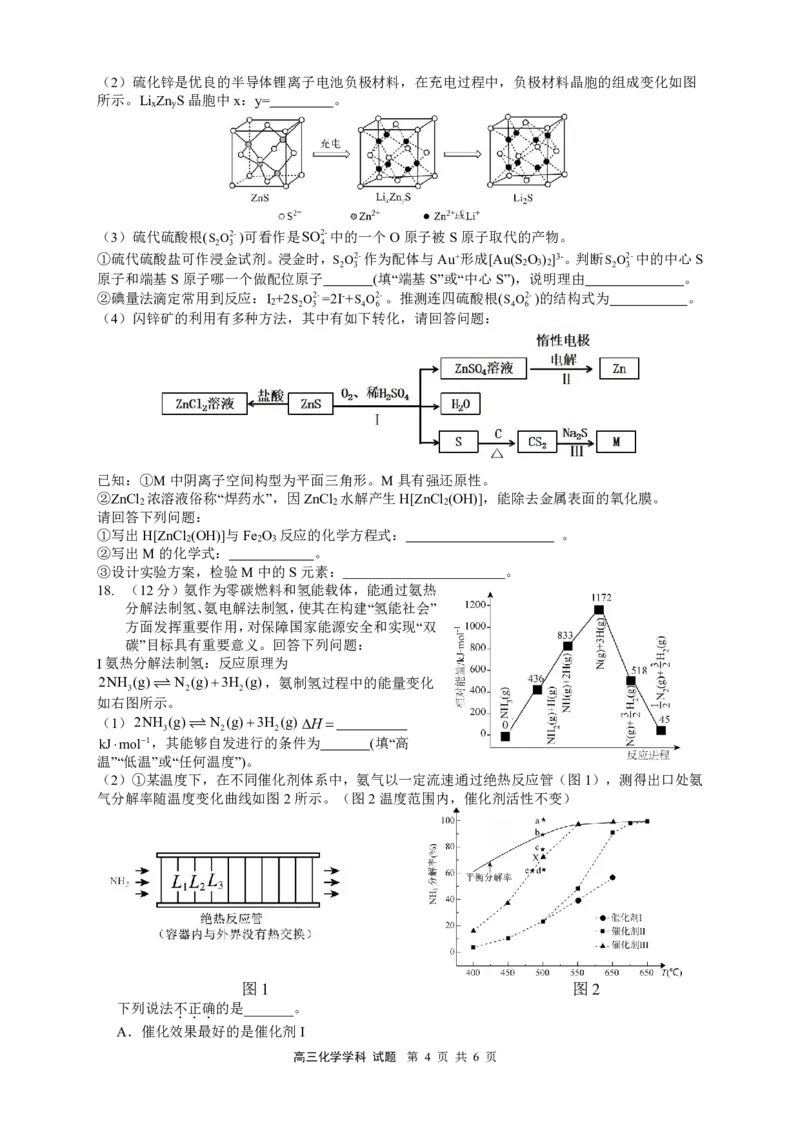
{#{QQABaYE8wggQgNaACB4LAQmiCkkQkIOjJaoMBUATOAQCSIFIBIA=}#}(2)硫化锌是优良的半导体锂离子电池负极材料,在充电过程中,负极材料晶胞的组成变化如图
所示。Li Zn S晶胞中x:y= 。
x y
(3)硫代硫酸根(S O2-)可看作是SO2-中的一个O原子被S原子取代的产物。
2 3 4
①硫代硫酸盐可作浸金试剂。浸金时,S 2 O 3 2-作为配体与Au+形成[Au(S 2 O 3 ) 2 ]3-。判断S 2 O 3 2-中的中心S
原子和端基S原子哪一个做配位原子 (填“端基S”或“中心S”),说明理由 。
②碘量法滴定常用到反应:I 2 +2S 2 O 3 2-=2I-+S 4 O 6 2-。推测连四硫酸根(S 4 O 6 2-)的结构式为 。
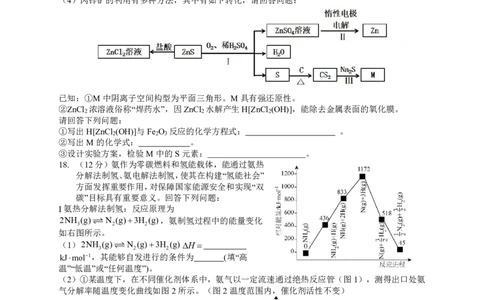
(4)闪锌矿的利用有多种方法,其中有如下转化,请回答问题:
已知:①M中阴离子空间构型为平面三角形。M具有强还原性。
②ZnCl 浓溶液俗称“焊药水”,因ZnCl 水解产生H[ZnCl (OH)],能除去金属表面的氧化膜。
2 2 2
请回答下列问题:
①写出H[ZnCl (OH)]与Fe O 反应的化学方程式: 。
2 2 3
②写出M的化学式: 。
③设计实验方案,检验M中的S元素: 。
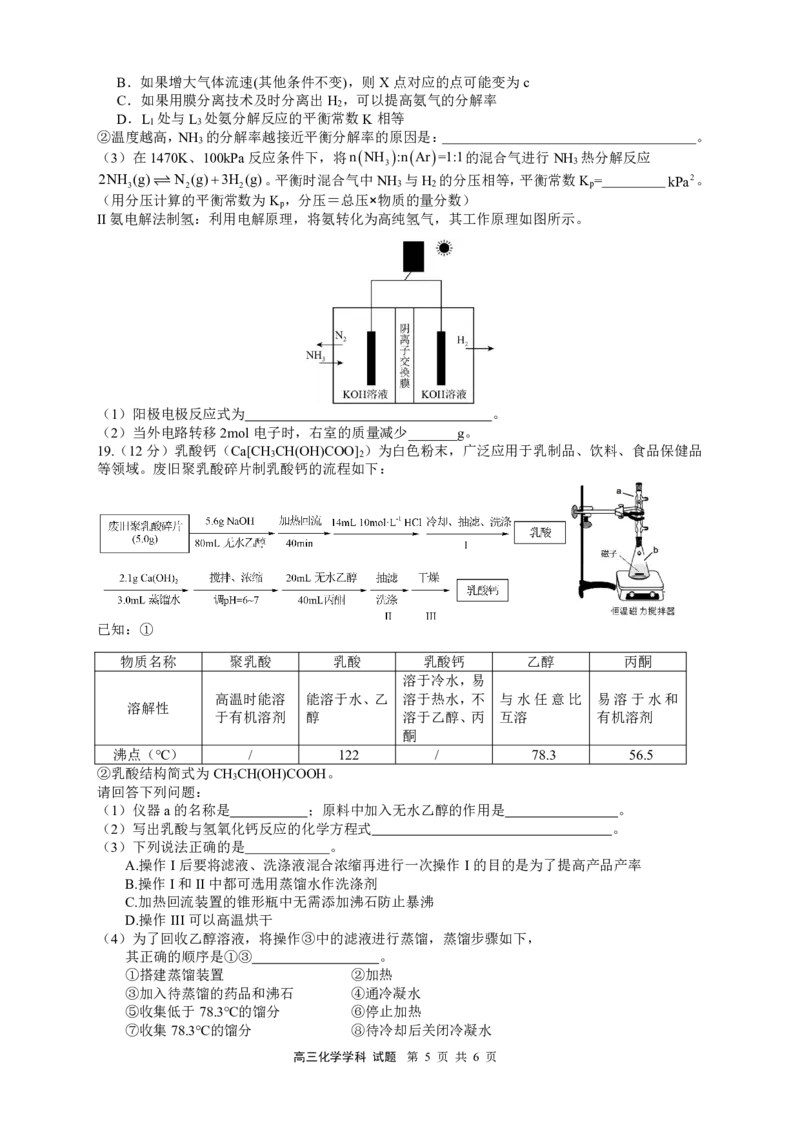
18. (12分)氨作为零碳燃料和氢能载体,能通过氨热
分解法制氢、氨电解法制氢,使其在构建“氢能社会”
方面发挥重要作用,对保障国家能源安全和实现“双
碳”目标具有重要意义。回答下列问题:
I氨热分解法制氢:反应原理为
2NH (g)N (g)3H (g),氨制氢过程中的能量变化
3 2 2
如右图所示。
(1)2NH (g)N (g)3H (g) H
3 2 2
kJmol1,其能够自发进行的条件为 (填“高
温”“低温”或“任何温度”)。
(2)①某温度下,在不同催化剂体系中,氨气以一定流速通过绝热反应管(图1),测得出口处氨
气分解率随温度变化曲线如图2所示。(图2温度范围内,催化剂活性不变)
图1 图2
下列说法不
.
正
.
确
.
的是_______。
A.催化效果最好的是催化剂I
高三化学学科 试题 第 4 页 共 6 页
{#{QQABaYE8wggQgNaACB4LAQmiCkkQkIOjJaoMBUATOAQCSIFIBIA=}#}B.如果增大气体流速(其他条件不变),则X点对应的点可能变为c
C.如果用膜分离技术及时分离出H ,可以提高氨气的分解率
2
D.L 处与L 处氨分解反应的平衡常数K相等
1 3
②温度越高,NH 的分解率越接近平衡分解率的原因是: 。
3
(3)在1470K、100kPa反应条件下,将nNH :nAr=1:1的混合气进行NH 热分解反应
3 3
2NH
3
(g)N
2
(g)3H
2
(g)。平衡时混合气中NH
3
与H
2
的分压相等,平衡常数K
p
= kPa2。
(用分压计算的平衡常数为K ,分压=总压×物质的量分数)
p
II氨电解法制氢:利用电解原理,将氨转化为高纯氢气,其工作原理如图所示。
(1)阳极电极反应式为 。
(2)当外电路转移2mol电子时,右室的质量减少_______g。
19.(12分)乳酸钙(Ca[CH CH(OH)COO] )为白色粉末,广泛应用于乳制品、饮料、食品保健品
3 2
等领域。废旧聚乳酸碎片制乳酸钙的流程如下:
已知:①
物质名称 聚乳酸 乳酸 乳酸钙 乙醇 丙酮
溶于冷水,易
高温时能溶 能溶于水、乙 溶于热水,不 与水任意比 易溶于水和
溶解性
于有机溶剂 醇 溶于乙醇、丙 互溶 有机溶剂
酮
沸点(℃) / 122 / 78.3 56.5
②乳酸结构简式为CH CH(OH)COOH。
3
请回答下列问题:
(1)仪器a的名称是 ;原料中加入无水乙醇的作用是 。
(2)写出乳酸与氢氧化钙反应的化学方程式 。
(3)下列说法正确的是 。
A.操作I后要将滤液、洗涤液混合浓缩再进行一次操作I的目的是为了提高产品产率
B.操作I和II中都可选用蒸馏水作洗涤剂
C.加热回流装置的锥形瓶中无需添加沸石防止暴沸
D.操作III可以高温烘干
(4)为了回收乙醇溶液,将操作③中的滤液进行蒸馏,蒸馏步骤如下,
其正确的顺序是①③ 。
①搭建蒸馏装置 ②加热
③加入待蒸馏的药品和沸石 ④通冷凝水
⑤收集低于78.3℃的馏分 ⑥停止加热
⑦收集78.3℃的馏分 ⑧待冷却后关闭冷凝水
高三化学学科 试题 第 5 页 共 6 页
{#{QQABaYE8wggQgNaACB4LAQmiCkkQkIOjJaoMBUATOAQCSIFIBIA=}#}(5)通过以下方法测定产品纯度:取 ag 乳酸钙样品溶解,加入缓冲溶液调节 pH,加入 bmL
cmol·L-1EDTA溶液。然后加入指示剂,用dmol·L-1的标准锌溶液滴定过量的EDTA溶液,实验消耗
标准锌溶液emL。
已知:Ca2+和Zn2+与EDTA反应的化学计量数之比均为1:1。M(乳酸钙)=218g·mol-1。
①计算乳酸钙的纯度为 (用相应的字母表示)。
②下列操作可能使测得的结果偏高的是___________。
A.盛装标准锌溶液的滴定管没有润洗
B.锥形瓶残留有蒸馏水
C.开始时仰视读数,终点时俯视读数
D.滴定管在滴定前无气泡,滴定后有气泡
20.(12分)氨氯地平主要用于高血压和心绞痛的治疗,是作为治疗高血压病的首选药物。其合成
路线如图所示
已知:
(1)化合物G中含氧官能团的名称是_______________;化合物A的结构简式是__________。
(2)下列说法不正确的是_____________。
A.化合物B中所有原子共平面 B.1mol化合物D最多能消耗4molNaOH
C.反应①为氧化反应,反应②为取代反应 D.化合物F中含有2个手性碳原子
(3)写出C→D的化学方程式_________________________________。
(4)A→B的过程中有副产物生成,写出副产物的结构简式____________(其分子式为C H O 且
8 6 4
含有苯环)。
(5)化合物C有多种同分异构体,写出满足下列条件的同分异构体____________。
①1H-NMR谱和IR谱检测表明:分子中共有4种氢原子,含碳氧双键,且无 结构。
②含有苯环和含N五元杂环,且共用一条边。
(6)化合物ClCH COCH COOCH CH 可由CH COCH COOCH CH 制得,请以乙烯为原料,设计
2 2 2 3 3 2 2 3
合成CH COCH COOCH CH 的路线____________(用流程图表示,无机试剂、有机溶剂任选)。
3 2 2 3
高三化学学科 试题 第 6 页 共 6 页
{#{QQABaYE8wggQgNaACB4LAQmiCkkQkIOjJaoMBUATOAQCSIFIBIA=}#}2025 年学年第一学期浙南名校联盟十月联考
高三年级化学学科参考答案
命题:瓯海中学 陈耀斌
一、选择题答案(本大题共16小题,每小题3分,共48分)
题号 1 2 3 4 5 6 7 8 9 10
答案 D B C D A B A D D C
题号 11 12 13 14 15 16
答案 C D A D C B
二、非选择题(本大题共4小题,共52分)
17.(16分)(1)BD(2分,错选不得分,少选给1分) (2)6:1(2分)
(3)① 端基S(2分) 端基S原子含有孤电子对,能做配位原子(2分,答到孤电子对就给
分)
② 或 (2分,有错不得分)
(4)①6H[ZnCl (OH)]+Fe O =2Fe[ZnCl (OH)] +3H O(2分,配平占1分)
2 2 3 2 3 2
②Na CS (2分,有错不得分)
2 3
③取少许M于试管中,加水溶解,加入足量双氧水,若有黄色沉淀生成,说明有S元素。(2分,
其他合理答案得分)
18.(12分)I (1) +90 (1分,“+”可不写) 高温(1分)
(2)①ABD (2分) ② 温度升高,反应速率加快,转化率接近平衡转化率(2分,答到速率加
快就给分)
625
(3) (2分)
3
II(1)2NH +6OH--6e-=N +6H O(2分,配平占1分) (2)36(2分)
3 2 2
19.(12分)(1)(球形)冷凝管(1分);增大反应物的接触面积,加快反应速率(1分。答到增大接
触面积就给分)
(2)2CH CH(OH)COOH+Ca(OH) ==Ca[CH CH(OH)COO] +2H O(2分,配平占1分)
3 2 3 2 2
(3)AC(2分,少选给1分,有错不给分)
(4)④②⑤⑦⑥⑧(2分,全对才给分)
0.218(bc-de)
(5)① ×100%(2分,100%可不写) ②CD(2分,少选给1分,有错不给分)
a
20.(12分)
(1)酯基、醚键(1分); (1分)
(2)BD(2分,少选给1分,有错不给分)
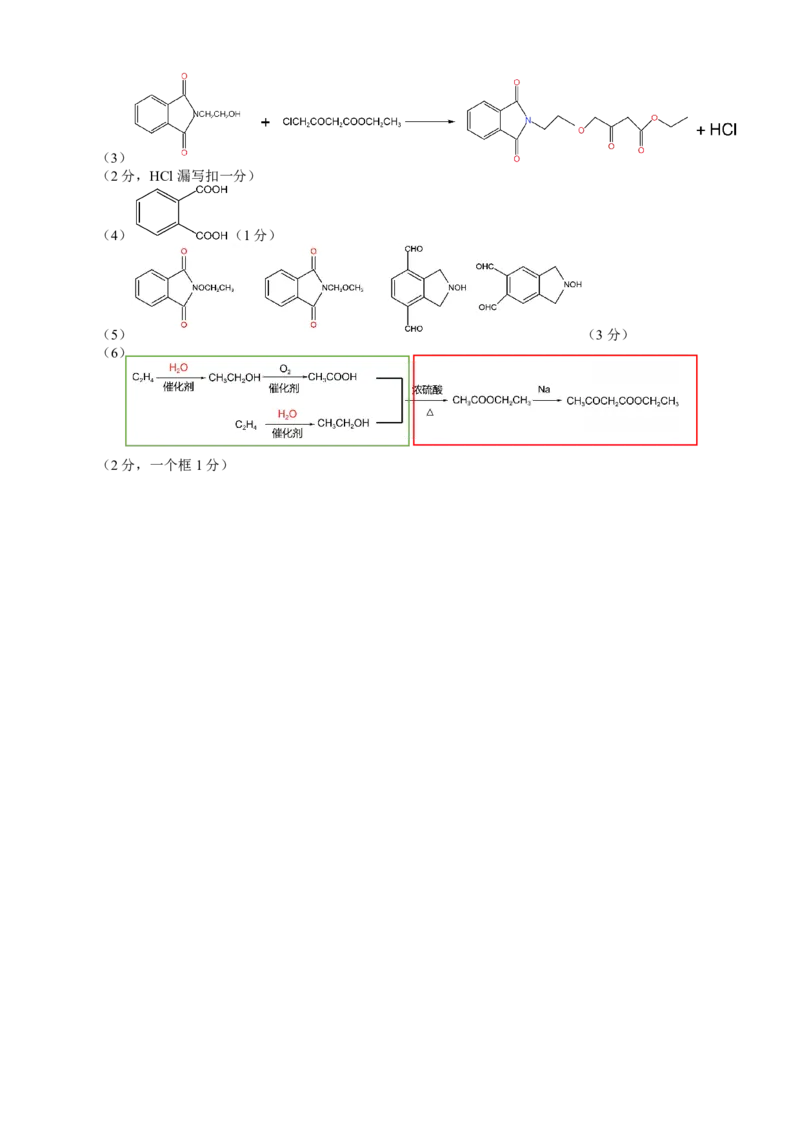
{#{QQABaYE8wggQgNaACB4LAQmiCkkQkIOjJaoMBUATOAQCSIFIBIA=}#}(3)
(2分,HCl漏写扣一分)
(4) (1分)
(5) (3分)
(6)
(2分,一个框1分)
{#{QQABaYE8wggQgNaACB4LAQmiCkkQkIOjJaoMBUATOAQCSIFIBIA=}#}