文档内容
清远一中2025-2026学年度高三10月期中考试
化学试卷
一、选择题(本大题共15小题,每小题3分,共45分。在每小题给出的四个选项中,
只有一项符合题目要求)
1.已知某脂肪酸(用R表示)有以下实验记录:
则以下关于R的结论肯定不正确的是( )
A. R是一元羧酸 B. R分子在烃基为C H —
17 31
C. R的相对分子质量为280 D. R分子含一个碳碳双键
2.下列表示正确的是( )
A. 醛基的电子式:
B. CO 的空间填充模型:
2
C. 氯气的共价键电子云轮廓图:
D. 基态Co2+的价层电子排布图:
3.NaH与水反应的化学方程式为NaH+HO NaOH+H↑,在该反应中NaH ( )
2 2
A. 是氧化剂 B. 是还原剂
C. 既是氧化剂又是还原剂 D. 既不是氧化剂又不是还原剂
4.有机物靛蓝是一种蓝色染料,其结构如图所示。下列有关靛蓝的说法正确的是( )
A. 属于芳香烃 B. 分子式为C H N O
16 10 2 2
C. 含有的官能团为苯基、氨基、酮羰基 D. 苯环上的一氯代物有2种
5.下列分子中,既含有σ键又含有π键的是( )
A. CH B. NH C. CO D. F
4 3 2 2
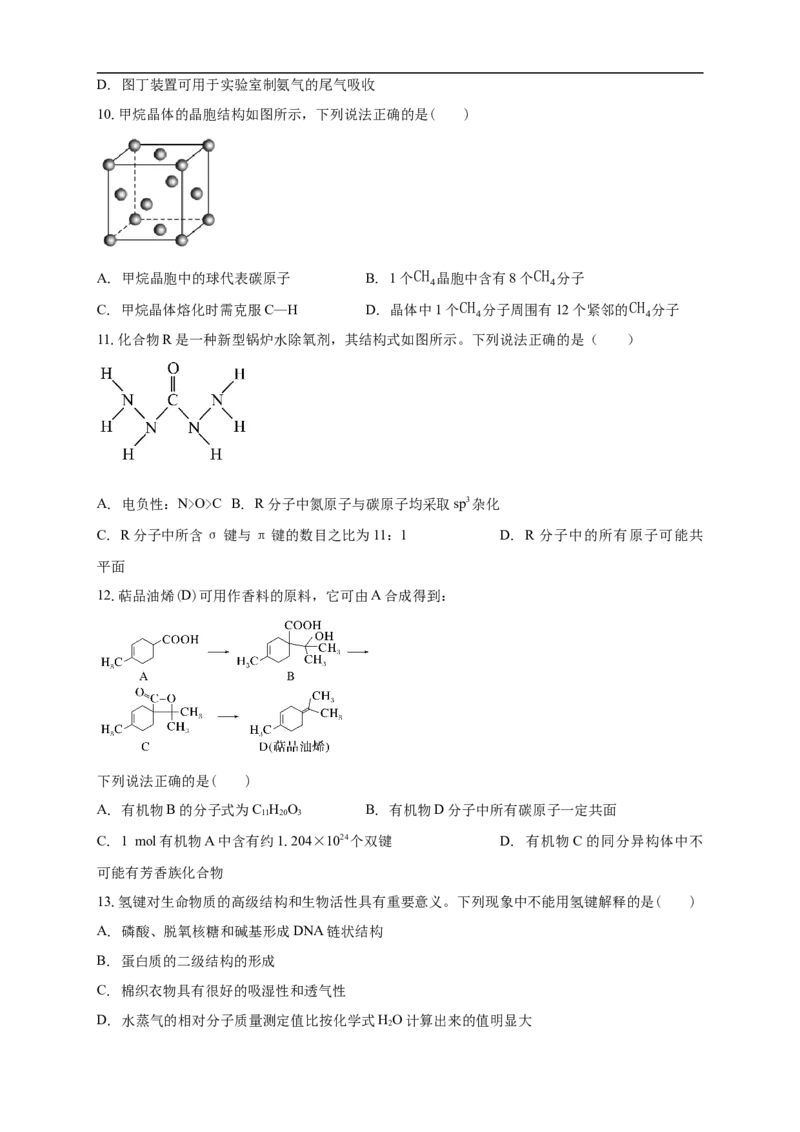
6.Li S属立方晶体,晶胞边长为d pm,晶胞截面图如图所示。则下列关于该晶胞的描述错误的是
2( )
A. 每个晶胞中含有的S2−数目为4
B. 与Li+距离最近且相等的S2−有8个
❑√3
C. 该晶胞中两个距离最近的Li+和S2−的核间距的计算表达式为 dpm
4
184
D. Li S晶体的密度为 ×1030g⋅cm−3
2 d3N
A
7.如图为氢原子的电子云图,下列说法正确的是( )
A. 电子云图中小黑点的密度越小,电子数目越少
B. 电子云图中小黑点的密度越大,单位体积内电子出现的概率越大
C. 所有电子云轮廓图都是球形
D. 电子云图中小黑点的密度小,表示电子在该区域内运动的速率慢
8.关于周期表中ⅥA族的元素O、S、Se,下列说法正确的是( )
A. 原子半径:r(O)>r(S)>r(Se) B. 第一电离能:I (O)χ(S)>χ(Se)
2 2 2
9.1935年,在中国化学家侯德榜的领导下,中国建成了第一座生产合成氨、硝酸等的联合企业
——永利制碱厂。该企业首先合成氨,氨再经铂铑催化剂催化氧化得到 NO,将NO、水和空气通
入吸收塔中得到硝酸。如图为NH 的制备,收集及催化氧化实验,下列说法正确的是( )
3
A. 图甲装置除了混合氢气和氮气之外还可以干燥气体及观察氢气和氮气的流速
B. 将氨气通入图乙装置中,锥形瓶口出现红棕色气体,说明氨被直接氧化为NO
2
C. 图丙为实验室制取氨气的正确装置D. 图丁装置可用于实验室制氨气的尾气吸收
10.甲烷晶体的晶胞结构如图所示,下列说法正确的是( )
A. 甲烷晶胞中的球代表碳原子 B. 1个CH 晶胞中含有8个CH 分子
4 4
C. 甲烷晶体熔化时需克服C—H D. 晶体中1个CH 分子周围有12个紧邻的CH 分子
4 4
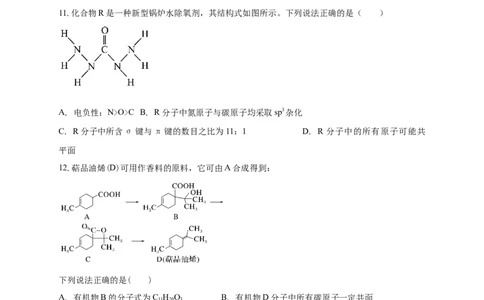
11.化合物R是一种新型锅炉水除氧剂,其结构式如图所示。下列说法正确的是( )
A. 电负性:N>O>C B. R分子中氮原子与碳原子均采取sp3杂化
C. R分子中所含σ键与π键的数目之比为11:1 D. R分子中的所有原子可能共
平面
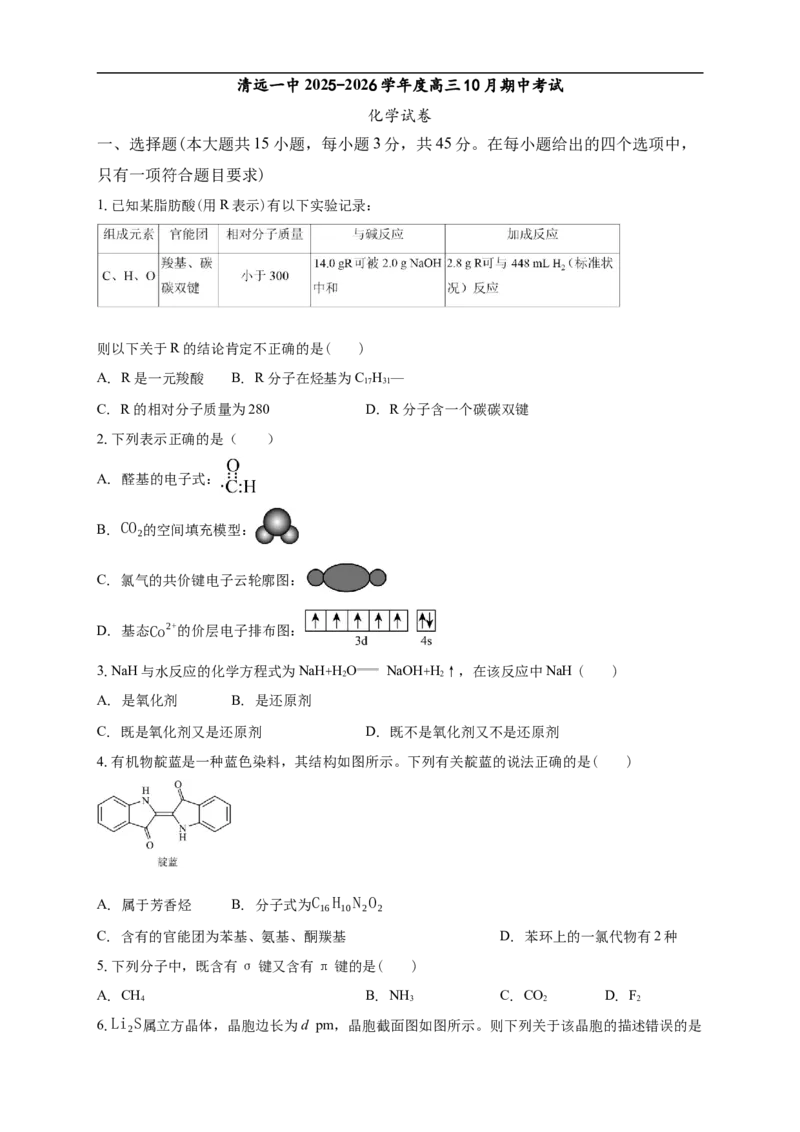
12.萜品油烯(D)可用作香料的原料,它可由A合成得到:
下列说法正确的是( )
A. 有机物B的分子式为C H O B. 有机物D分子中所有碳原子一定共面
11 20 3
C. 1 mol有机物A中含有约1.204×1024个双键 D. 有机物C的同分异构体中不
可能有芳香族化合物
13.氢键对生命物质的高级结构和生物活性具有重要意义。下列现象中不能用氢键解释的是( )
A. 磷酸、脱氧核糖和碱基形成DNA链状结构
B. 蛋白质的二级结构的形成
C. 棉织衣物具有很好的吸湿性和透气性
D. 水蒸气的相对分子质量测定值比按化学式HO计算出来的值明显大
214.a、b、c、d、e、f 为六种短周期元素, a、b、e 、f 位于同一周期,c、d 也是同一周期, 且
d、e 同一主族,原子半径 d<e,a、b、c、d、f原子最外层电子依次增多,则下列说法中正确的
是( )
A. e 的非金属性比 f 强 B. d 元素可能是第一周期元素
C. 六种元素中,a 元素最高价氧化物对应水化物碱性最强 D. a、b、c、d 的原子序数逐渐
增大
15.我们生活的衣食住行都离不开有机化合物,下列说法不正确的是( )
A. 甲烷是一种清洁能源,是天然气的主要成分
B. 用KMnO 溶液浸泡过的藻土可使水果保鲜,是利用了乙烯的还原性
4
C. 乙炔用于焊接或切割金属,是因为乙炔燃烧时放出大量的热
D. 聚氯乙烯(PVC)塑料,可用于制作食品包装袋
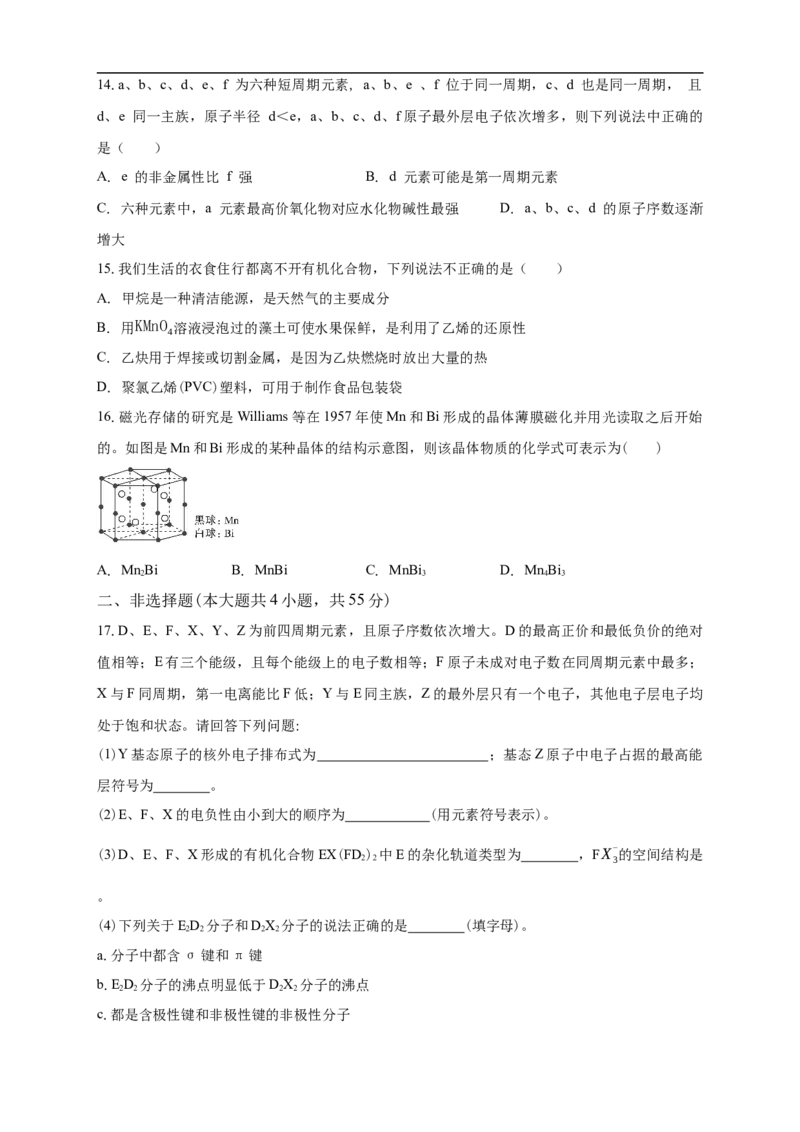
16.磁光存储的研究是Williams等在1957年使Mn和Bi形成的晶体薄膜磁化并用光读取之后开始
的。如图是Mn和Bi形成的某种晶体的结构示意图,则该晶体物质的化学式可表示为( )
A. MnBi B. MnBi C. MnBi D. MnBi
2 3 4 3
二、非选择题(本大题共4小题,共55分)
17.D、E、F、X、Y、Z为前四周期元素,且原子序数依次增大。D的最高正价和最低负价的绝对
值相等;E有三个能级,且每个能级上的电子数相等;F原子未成对电子数在同周期元素中最多;
X与F同周期,第一电离能比F低;Y与E同主族,Z的最外层只有一个电子,其他电子层电子均
处于饱和状态。请回答下列问题:
(1)Y基态原子的核外电子排布式为 ;基态Z原子中电子占据的最高能
层符号为 。
(2)E、F、X的电负性由小到大的顺序为 (用元素符号表示)。
(3)D、E、F、X形成的有机化合物EX(FD ) 中E的杂化轨道类型为
,FX-
的空间结构是
2 2 3
。
(4)下列关于ED 分子和DX 分子的说法正确的是 (填字母)。
2 2 2 2
a.分子中都含σ键和π键
b.ED 分子的沸点明显低于DX 分子的沸点
2 2 2 2
c.都是含极性键和非极性键的非极性分子18.甲、乙、丙三种有机物的结构简式如图,按要求填空。
(1)甲、乙、丙属于________(填字母)。
A.同系物 B.同位素
C.同分异构体 D.同素异形体
(2)甲中共平面的原子最多有________个。
(3)与乙分子式相同的有机物,且属于炔烃有________种。
(4)乙发生加聚反应的化学方程式为_________________________________________________。
(5)丙的二氯代物有________种。
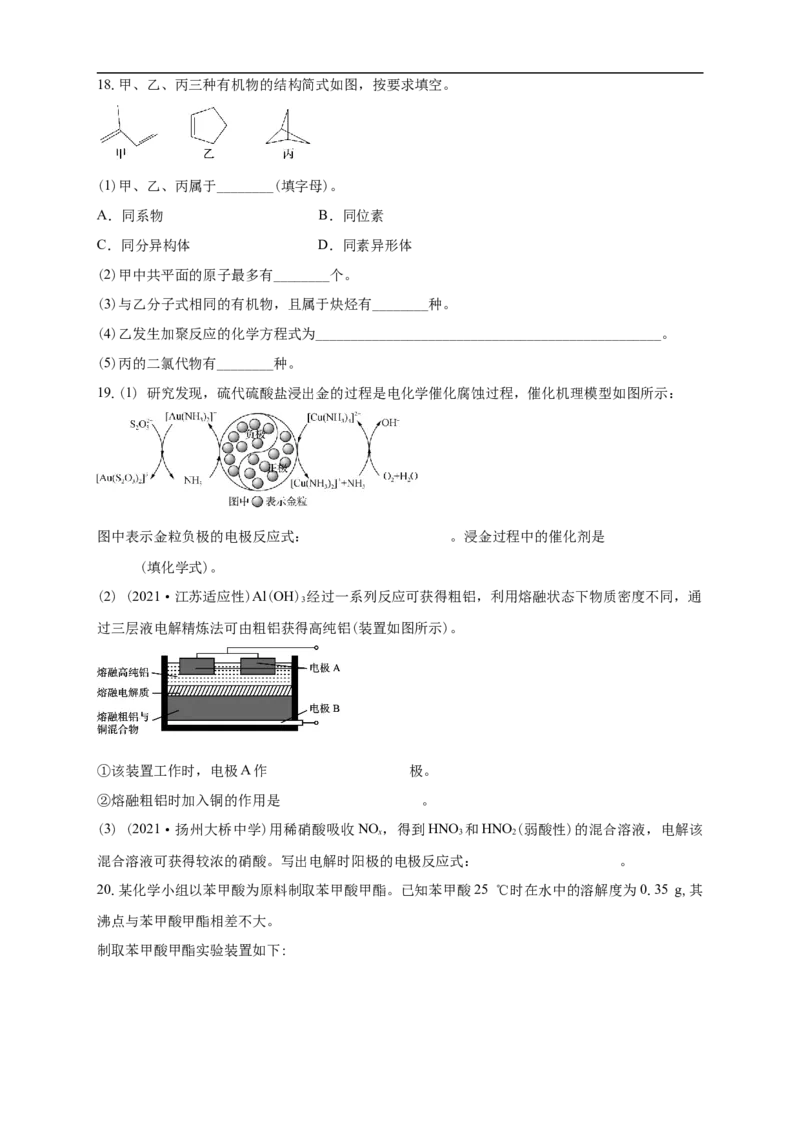
19.(1) 研究发现,硫代硫酸盐浸出金的过程是电化学催化腐蚀过程,催化机理模型如图所示:
图中表示金粒负极的电极反应式: 。浸金过程中的催化剂是
(填化学式)。
(2) (2021·江苏适应性)Al(OH) 经过一系列反应可获得粗铝,利用熔融状态下物质密度不同,通
3
过三层液电解精炼法可由粗铝获得高纯铝(装置如图所示)。
①该装置工作时,电极A作 极。
②熔融粗铝时加入铜的作用是 。
(3) (2021·扬州大桥中学)用稀硝酸吸收NO,得到HNO 和HNO(弱酸性)的混合溶液,电解该
x 3 2
混合溶液可获得较浓的硝酸。写出电解时阳极的电极反应式: 。
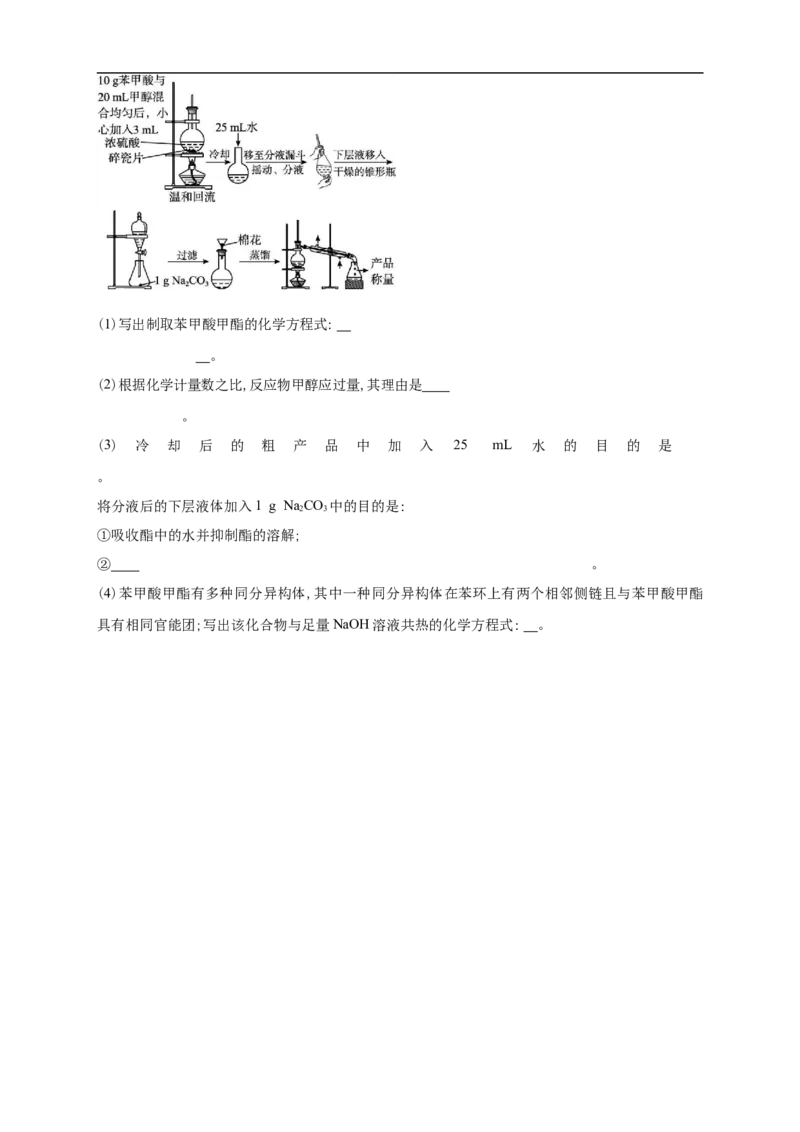
20.某化学小组以苯甲酸为原料制取苯甲酸甲酯。已知苯甲酸25 ℃时在水中的溶解度为0.35 g,其
沸点与苯甲酸甲酯相差不大。
制取苯甲酸甲酯实验装置如下:(1)写出制取苯甲酸甲酯的化学方程式:
。
(2)根据化学计量数之比,反应物甲醇应过量,其理由是
。
(3) 冷 却 后 的 粗 产 品 中 加 入 25 mL 水 的 目 的 是
。
将分液后的下层液体加入1 g NaCO 中的目的是:
2 3
①吸收酯中的水并抑制酯的溶解;
② 。
(4)苯甲酸甲酯有多种同分异构体,其中一种同分异构体在苯环上有两个相邻侧链且与苯甲酸甲酯
具有相同官能团;写出该化合物与足量NaOH溶液共热的化学方程式: 。