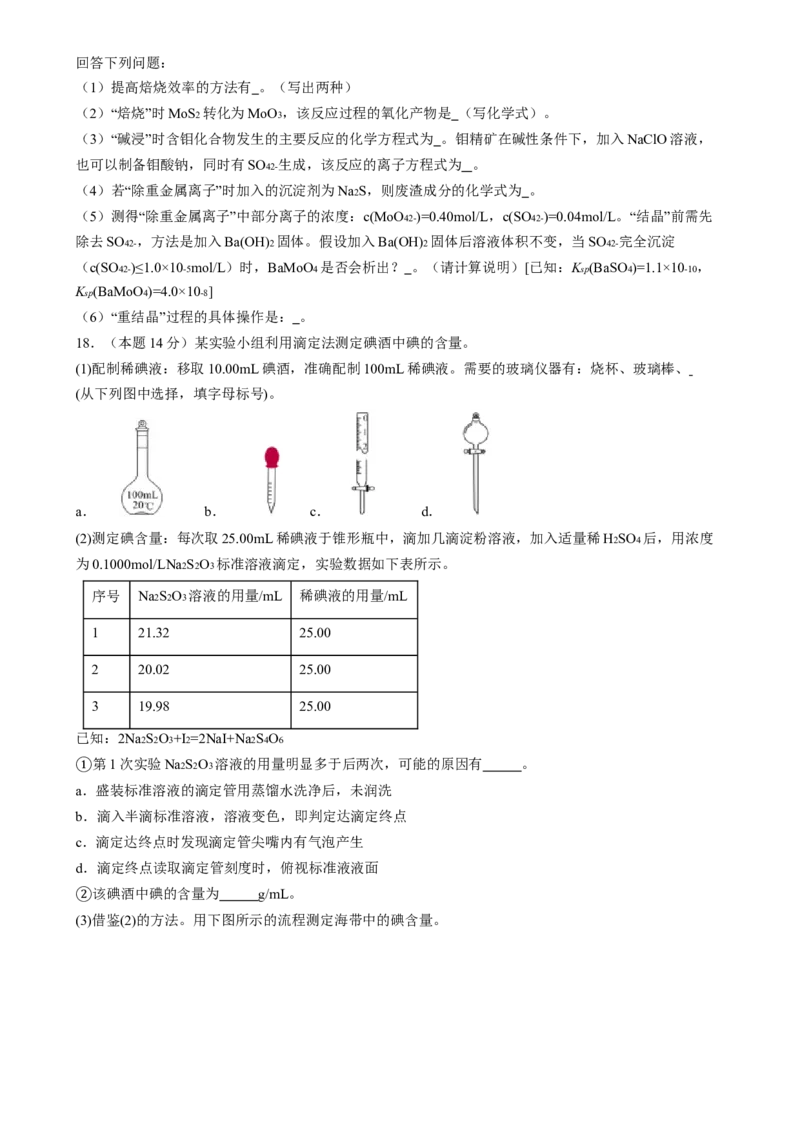文档内容
2024年高三上学期化学月考试卷
一、单选题(每题3分,共48分)
1.下列有关化学用语使用正确的是
A.氢氧化钠的电子式: B.S原子的结构示意图:
C.离子半径: D. 分子的结构式:
2.下列工业制备流程正确的是
A.海水提镁:海水 Mg(OH)2 MgO Mg
B.制备漂白粉:饱和食盐水 氯气 漂白粉
C.工业制硝酸:N2 NO NO2 HNO3
D.工业制高纯硅:石英砂 粗硅 SiHCl3 高纯硅
3.下列有关几种试纸使用的描述中,不正确的是
A.用湿润的红色石蕊试纸检验某种气体是否是NH3
B.某种有色溶液可使淀粉-KI试纸变蓝色,则该溶液中可能含有Fe3+
C.用玻璃棒蘸取溶液点在用蒸馏水湿润过的pH试纸上可测量该溶液的pH
D.将湿润的蓝色石蕊试纸片粘在玻璃棒上置于氯气中,试纸先变红后褪色
4.下列过程对应的离子反应方程式或化学反应方程式书写错误的是
A.碘化亚铁溶液与等物质的量的氯气:
B.用Na2SO3 溶液吸收少量Cl2 :
C.丙烯醛(CH2=CHCHO)与足量溴水反应:CH2=CHCHO+Br2→CH2BrCHBrCHO
D.以NaCl溶液为电解质溶液通过电解法制备Fe(OH)2 时,阳极的电极反应:Fe-2e-=Fe2+
5.某化合物通过界面埋入可以实现钙钛矿太阳能电池的高稳定性,其结构如图。X、Y、Z、W、M是原
子序数依次增大的前四周期主族元素,X与Z的原子序数之和与W的原子序数相等。下列说法正确的是
A.分子极性:
B.简单氢化物的沸点:Z>Y>X
C. 和 的VSEPR模型名称相同
D.与M的原子最外层电子数相同的同周期元素还有2种
6.下列实验仪器、试剂、操作均正确,且能达到实验目的的是A.用NaOH溶液吸收尾气中的
B.由乙醇制乙烯并检验乙烯的性质
Cl2
C.分离苯酚和碳酸氢钠溶液 D.除去SO2 中少量的CO2
A.A B.B C.C D.D
7.下表中的各组物质之间通过一步反应就能实现如图所示转化的是
编号 a b c d
Na
①
Al
②
Fe
③
Mg
④ A. B. C. D.
8.下列实验操作和现象所得结论正确的是
②④ ①④ ②③ ③④
操作 现象 结论
向0.1 mol·L-1 NaHCO3 溶液中滴加饱和的
A 溶液变浑浊 Ca(HCO3)2 难溶于水
CaCl2 溶液
向0.1 mol·L-1 K2S溶液中滴加少量等浓
B 度的ZnSO4 溶液,再滴加少量等浓度的 先产生白色沉淀,后产生黑色沉淀 Ksp(ZnS)>Ksp(CuS)
CuSO4 溶液
在N2 氛围中高温加热FeSO4 固体使其分
Ba(NO3)2 溶液中产生白色沉淀,品红溶 FeSO4 分解的气体产物中
C 解,将气体产物依次通Ba(NO3)2 溶液、
液不褪色 有SO3 没有SO2
品红溶液D 将蘸有浓氨水的玻璃棒靠近某试剂瓶瓶口 试剂瓶瓶口有白烟生成 该试剂不一定是挥发性酸
A.A B.B C.C D.D
9.把浓盐酸分别滴入点滴板上的各种溶液中,现象如下:
实验 现象
中溶液变蓝
①
中溶液产生胶状沉淀
②
中生成沉淀
③
中产生刺激性气体
下列分析不正确的是 ④
A. 中溶液变蓝,体现了浓盐酸的氧化性
B.①中产生白色胶状沉淀:2H+ + =H2SiO3↓
C. 中产生沉淀的原因可用平衡移动原理解释
②
D.③中产生刺激性气体:2H+ + =SO2↑+H2O
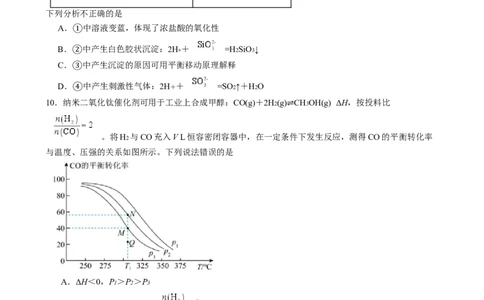
10.纳米
④
二氧化钛催化剂可用于工业上合成甲醇:CO(g)+2H2(g) CH3OH(g) ΔH,按投料比
⇌
。将H2 与CO充入V L恒容密闭容器中,在一定条件下发生反应,测得CO的平衡转化率
与温度、压强的关系如图所示。下列说法错误的是
A.ΔH<0,P1 >P2 >P3
B.达到平衡后,再按照 加入气体,平衡后CO的体积分数减小
C.恒温恒容下,向M点容器中再加入2mol CH3OH、3molCO,则平衡移动
D.T1 、P3 压强下,Q点对应的v正 >v逆
11.下列表达方式或说法正确的是
℃
A.基态到激发态产生的光谱是发射光谱
B.氯化铵的电子式:
C.Ca原子的电子排布式为1s22s22p63s23p63d2
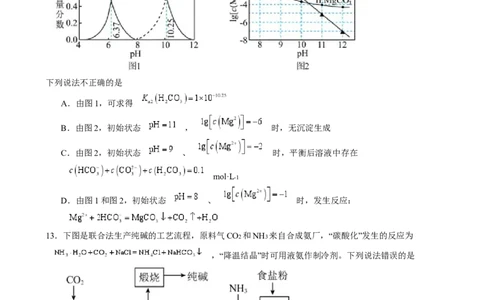
D.NH3 、H2O、CO2 、HCl四分子中孤电子对数最多的是CO212.室温下, 体系中各含碳微粒的物质的量分数与pH的关系如图1所示。在
mol·L-1 的体系中,研究 在不同pH时的可能产物, 与pH
的关系如图2所示,曲线Ⅰ的离子浓度关系符合; ,曲线Ⅱ的离
子浓度关系符合: 。
下列说法不正确的是
A.由图1,可求得
B.由图2,初始状态 , 时,无沉淀生成
C.由图2,初始状态 、 时,平衡后溶液中存在
mol·L-1
D.由图1和图2,初始状态 、 时,发生反应:
13.下图是联合法生产纯碱的工艺流程,原料气CO2 和NH3 来自合成氨厂,“碳酸化”发生的反应为
,“降温结晶”时可用液氨作制冷剂。下列说法错误的是
A.“煅烧”产生的气体可以循环使用 B.母液I通NH3 的主要目的是增大
C.液氨制冷与液氨分子间氢键有关 D.母液II用于吸氨可以提高NaCl的利用率
14.2-乙酰氧基苯甲酸在医疗上可用作血小板聚集的抑制剂,其结构简式如图所示。下列关于该有机物的
说法错误的是A.分子式为C9H8O4
B.苯环上的一氯代物有4种(不考虑立体异构)
C.分子中所有原子可能共平面
D.能与NaHCO3 溶液反应生成CO2
15.7.5g镁铝合金完全溶解于100mL密度为1.40g/mL、质量分数为63%的浓硝酸中得到NO2 和NO的混
合气体11.2L(标准状况),向反应后的溶液中加入3.0mol/LNaOH溶液,当金属离子恰好完全沉淀时,
得到19.4g沉淀,下列说法不正确的是
A.该合金中铝与镁的物质的量之比是2:1
B.该浓硝酸中HNO3 的物质的量浓度是14.0mol/L
C.NO2 和NO的混合气体中,NO的体积分数是20%
D.得到19.4g沉淀时,加入NaOH溶液的体积是300mL
16. 可充电电池的工作原理示意图如图,其中锂离子交换膜只允许 通过,电池反
应为: 。下列说法正确的是
A. 电解质与 溶液可互换
B.放电时, 电极发生 脱嵌,充电时发生 嵌入
C.充电时,阴极反应为:
D.充电时,当转移0.1mol电子时,左室中电解质的质量减轻1.3g
二、解答题(共52分)
17.(本题12分)钼酸钠晶体(Na2MoO4·2H2O)常用于制造阻燃剂和无公害冷水系统的金属抑制剂。如
图是利用钼精矿(主要成分是MoS2 ,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图:回答下列问题:
(1)提高焙烧效率的方法有 。(写出两种)
(2)“焙烧”时MoS2 转化为MoO3 ,该反应过程的氧化产物是 (写化学式)。
(3)“碱浸”时含钼化合物发生的主要反应的化学方程式为 。钼精矿在碱性条件下,加入NaClO溶液,
也可以制备钼酸钠,同时有SO42- 生成,该反应的离子方程式为 。
(4)若“除重金属离子”时加入的沉淀剂为Na2S,则废渣成分的化学式为 。
(5)测得“除重金属离子”中部分离子的浓度:c(MoO42-)=0.40mol/L,c(SO42-)=0.04mol/L。“结晶”前需先
除去SO42- ,方法是加入Ba(OH)2 固体。假设加入Ba(OH)2 固体后溶液体积不变,当SO42- 完全沉淀
(c(SO42-)≤1.0×10-5mol/L)时,BaMoO4 是否会析出? 。(请计算说明)[已知:Ksp(BaSO4)=1.1×10-10 ,
Ksp(BaMoO4)=4.0×10-8]
(6)“重结晶”过程的具体操作是: 。
18.(本题14分)某实验小组利用滴定法测定碘酒中碘的含量。
(1)配制稀碘液:移取10.00mL碘酒,准确配制100mL稀碘液。需要的玻璃仪器有:烧杯、玻璃棒、
(从下列图中选择,填字母标号)。
a. b. c. d.
(2)测定碘含量:每次取25.00mL稀碘液于锥形瓶中,滴加几滴淀粉溶液,加入适量稀H2SO4 后,用浓度
为0.1000mol/LNa2S2O3 标准溶液滴定,实验数据如下表所示。
序号 Na2S2O3 溶液的用量/mL 稀碘液的用量/mL
1 21.32 25.00
2 20.02 25.00
3 19.98 25.00
已知:2Na2S2O3+I2=2NaI+Na2S4O6
第1次实验Na2S2O3 溶液的用量明显多于后两次,可能的原因有 。
a.盛装标准溶液的滴定管用蒸馏水洗净后,未润洗
①
b.滴入半滴标准溶液,溶液变色,即判定达滴定终点
c.滴定达终点时发现滴定管尖嘴内有气泡产生
d.滴定终点读取滴定管刻度时,俯视标准液液面
该碘酒中碘的含量为 g/mL。
(3)借鉴(2)的方法。用下图所示的流程测定海带中的碘含量。
②加入H2O2 溶液发生的离子反应方程式为 。
预测达到滴定终点的实验现象为 ,然而,在实验时却发现溶液变色片刻后,恢复滴定前的颜色。
①
②
继续滴加Na2S2O3 溶液变色片刻后再一次恢复原色。
(4)探究异常现象产生的原因。
该学习小组通过设计对照实验,发现空气中的氧气并不能较快地氧化待测液中的I- 。
提出猜想:过量的H2O2 将生成的I- 重新氧化成碘单质。
验证猜想:将10mL待测液、8滴0.lmol/LH2SO4 溶液、2滴淀粉溶液和 混合,用
Na2S2O3 溶液滴定,若待测液变为无色后又反复变色,则证明猜想不成立。
提出疑问:什么物质反复氧化碘离子?
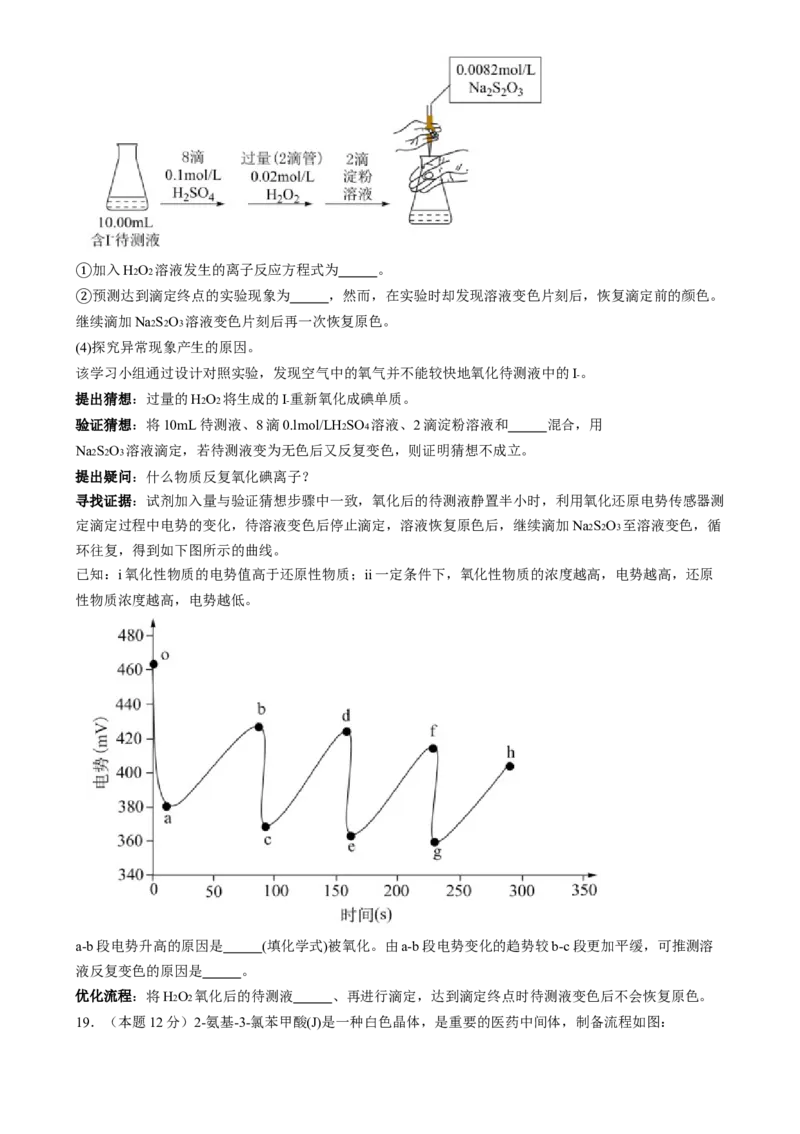
寻找证据:试剂加入量与验证猜想步骤中一致,氧化后的待测液静置半小时,利用氧化还原电势传感器测
定滴定过程中电势的变化,待溶液变色后停止滴定,溶液恢复原色后,继续滴加Na2S2O3 至溶液变色,循
环往复,得到如下图所示的曲线。
已知:i氧化性物质的电势值高于还原性物质;ii一定条件下,氧化性物质的浓度越高,电势越高,还原
性物质浓度越高,电势越低。
a-b段电势升高的原因是 (填化学式)被氧化。由a-b段电势变化的趋势较b-c段更加平缓,可推测溶
液反复变色的原因是 。
优化流程:将H2O2 氧化后的待测液 、再进行滴定,达到滴定终点时待测液变色后不会恢复原色。
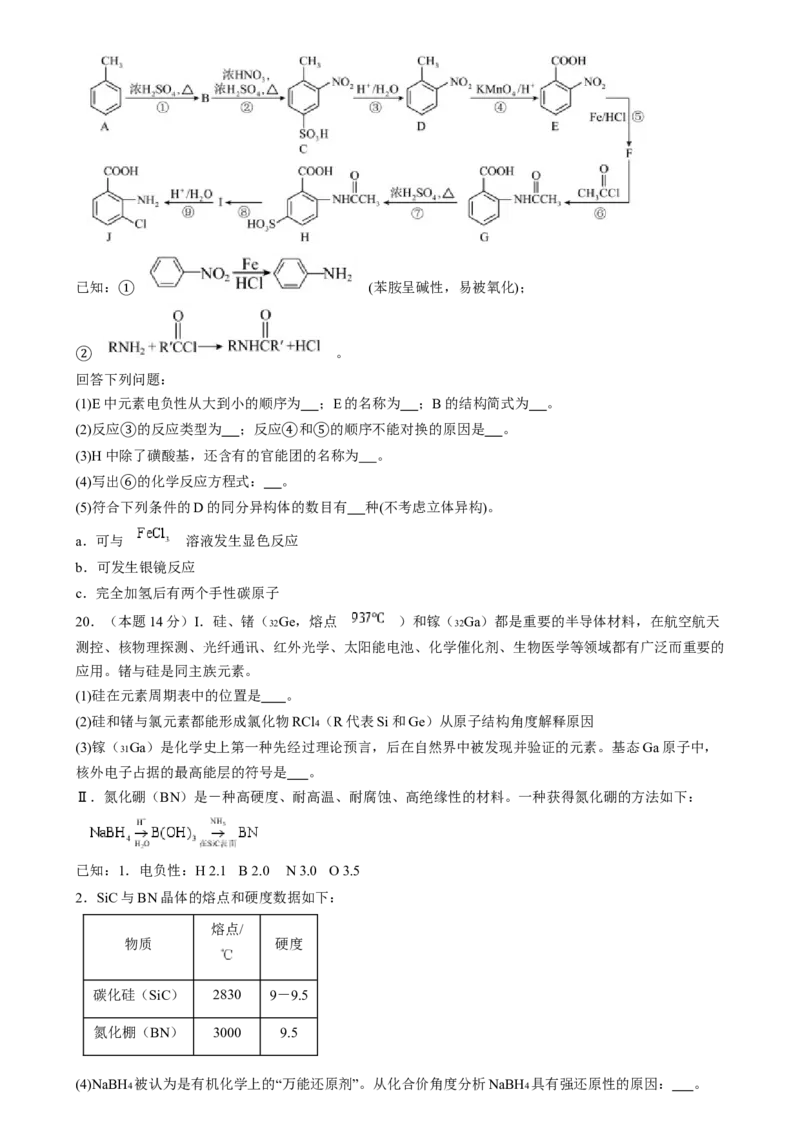
19.(本题12分)2-氨基-3-氯苯甲酸(J)是一种白色晶体,是重要的医药中间体,制备流程如图:已知: (苯胺呈碱性,易被氧化);
①
。
回答下列问题:
②
(1)E中元素电负性从大到小的顺序为 ;E的名称为 ;B的结构简式为 。
(2)反应 的反应类型为 ;反应 和 的顺序不能对换的原因是 。
(3)H中除了磺酸基,还含有的官能团的名称为 。
③ ④ ⑤
(4)写出 的化学反应方程式: 。
(5)符合下列条件的D的同分异构体的数目有 种(不考虑立体异构)。
⑥
a.可与 溶液发生显色反应
b.可发生银镜反应
c.完全加氢后有两个手性碳原子
20.(本题14分)I.硅、锗( 32Ge,熔点 )和镓( 32Ga)都是重要的半导体材料,在航空航天
测控、核物理探测、光纤通讯、红外光学、太阳能电池、化学催化剂、生物医学等领域都有广泛而重要的
应用。锗与硅是同主族元素。
(1)硅在元素周期表中的位置是 。
(2)硅和锗与氯元素都能形成氯化物RCl4 (R代表Si和Ge)从原子结构角度解释原因
(3)镓( 31Ga)是化学史上第一种先经过理论预言,后在自然界中被发现并验证的元素。基态Ga原子中,
核外电子占据的最高能层的符号是 。
Ⅱ.氮化硼(BN)是-种高硬度、耐高温、耐腐蚀、高绝缘性的材料。一种获得氮化硼的方法如下:
已知:1.电负性:H 2.1 B 2.0 N 3.0 O 3.5
2.SiC与BN晶体的熔点和硬度数据如下:
熔点/
物质 硬度
碳化硅(SiC) 2830 9-9.5
氮化棚(BN) 3000 9.5
(4)NaBH4 被认为是有机化学上的“万能还原剂”。从化合价角度分析NaBH4 具有强还原性的原因: 。(5)硼酸的化学式为B(OH)
3
是一元弱酸。
硼酸产生H+ 过程为:
硼酸分子的空间构型为 。
①
硼酸具有弱酸性是由于B与水中的OH- 形成配位键,描述配位键的形成过程 。
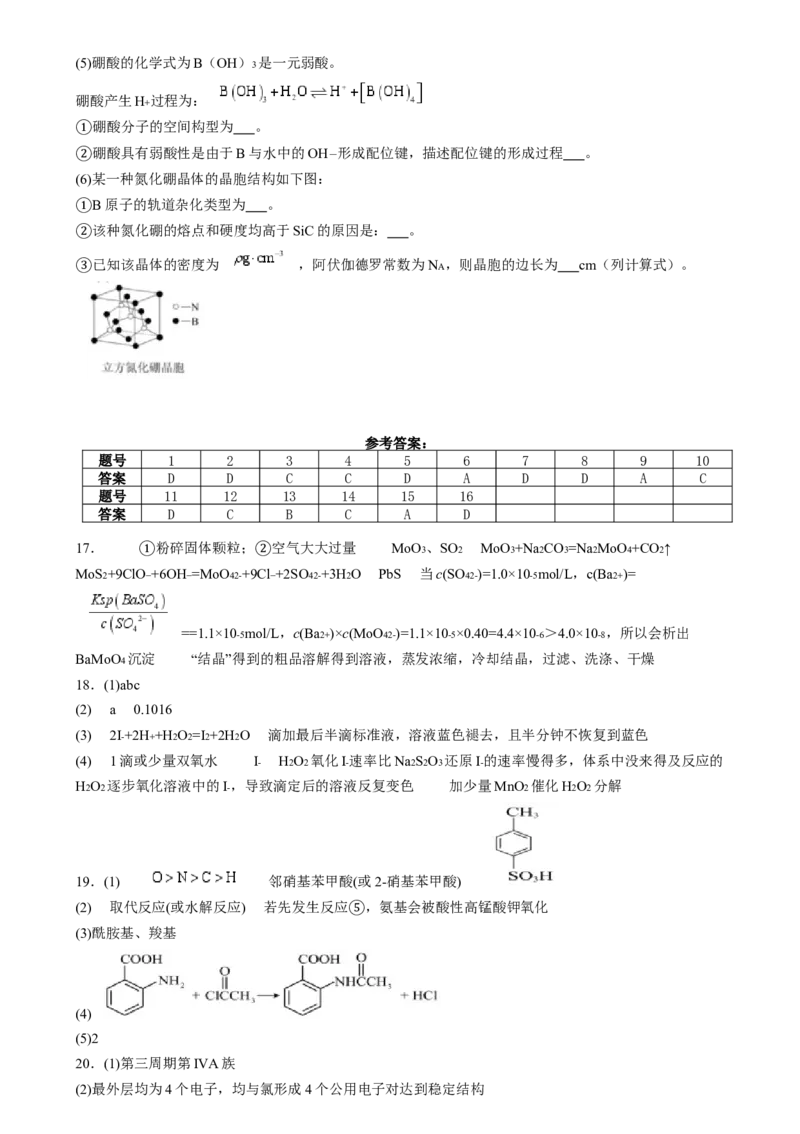
(6)某一种氮化硼晶体的晶胞结构如下图:
②
B原子的轨道杂化类型为 。
该种氮化硼的熔点和硬度均高于SiC的原因是: 。
①
②已知该晶体的密度为 ,阿伏伽德罗常数为NA ,则晶胞的边长为 cm(列计算式)。
③
参考答案:
题号 1 2 3 4 5 6 7 8 9 10
答案 D D C C D A D D A C
题号 11 12 13 14 15 16
答案 D C B C A D
17. 粉碎固体颗粒; 空气大大过量 MoO3 、SO2 MoO3+Na2CO3=Na2MoO4+CO2↑
MoS2+9ClO ①−+6OH−=MoO42-+9
②
Cl−+2SO42-+3H2O PbS 当c(SO42-)=1.0×10-5mol/L,c(Ba2+)=
==1.1×10-5mol/L,c(Ba2+)×c(MoO42-)=1.1×10-5×0.40=4.4×10-6 >4.0×10-8 ,所以会析出
BaMoO4 沉淀 “结晶”得到的粗品溶解得到溶液,蒸发浓缩,冷却结晶,过滤、洗涤、干燥
18.(1)abc
(2) a 0.1016
(3) 2I-+2H++H2O2=I2+2H2O 滴加最后半滴标准液,溶液蓝色褪去,且半分钟不恢复到蓝色
(4) 1滴或少量双氧水 I- H2O2 氧化I- 速率比Na2S2O3 还原I- 的速率慢得多,体系中没来得及反应的
H2O2 逐步氧化溶液中的I- ,导致滴定后的溶液反复变色 加少量MnO2 催化H2O2 分解
19.(1) 邻硝基苯甲酸(或2-硝基苯甲酸)
(2) 取代反应(或水解反应) 若先发生反应 ,氨基会被酸性高锰酸钾氧化
(3)酰胺基、羧基
⑤
(4)
(5)2
20.(1)第三周期第IVA族
(2)最外层均为4个电子,均与氯形成4个公用电子对达到稳定结构(3)N
(4)H为-1价
(5) 平面三角形 B原子提供空轨道,OH- 中的氧原子提供孤电子对,形成配位键
(6) sp3 均属共价晶体,结构相似,B-N键长比Si-C键短,键能更大