文档内容
清远一中2025-2026学年度高三10月期中考试
化学试卷
一、选择题(本大题共15小题,每小题3分,共45分。在每小题给出的四个选项中,
只有一项符合题目要求)
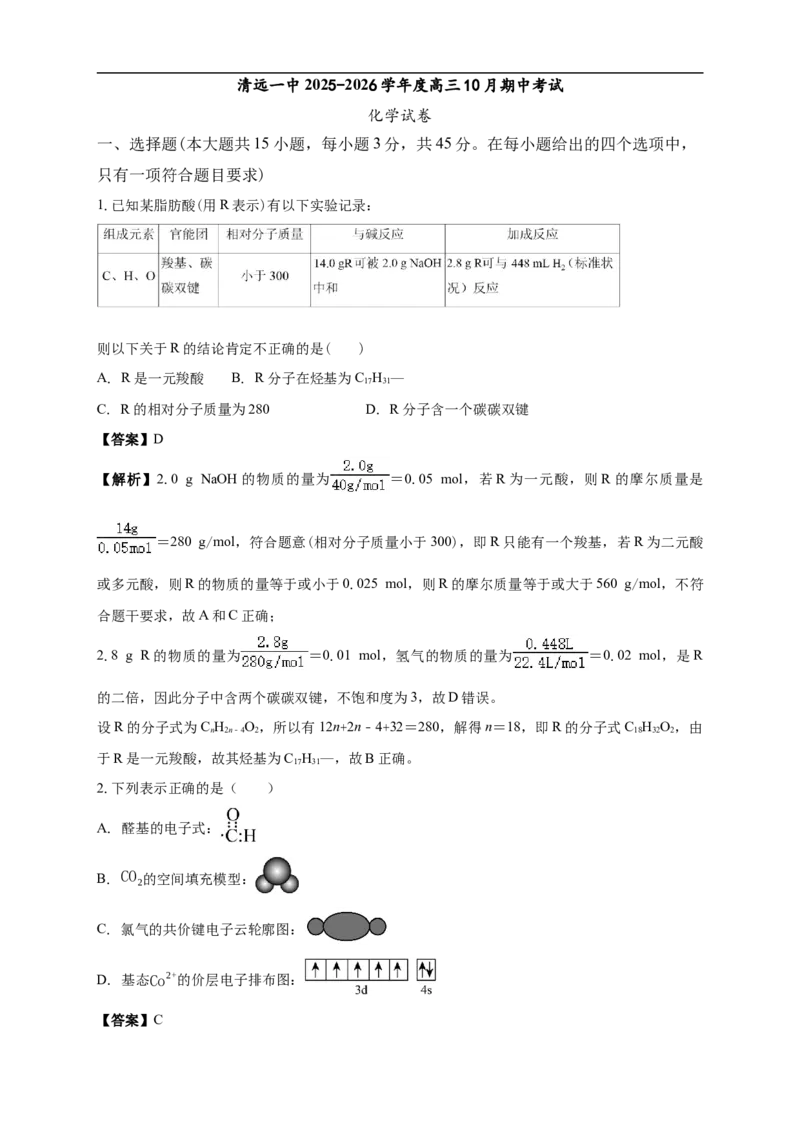
1.已知某脂肪酸(用R表示)有以下实验记录:
则以下关于R的结论肯定不正确的是( )
A. R是一元羧酸 B. R分子在烃基为C H —
17 31
C. R的相对分子质量为280 D. R分子含一个碳碳双键
【答案】D
【解析】2.0 g NaOH的物质的量为 =0.05 mol,若R为一元酸,则R的摩尔质量是
=280 g/mol,符合题意(相对分子质量小于300),即R只能有一个羧基,若R为二元酸
或多元酸,则R的物质的量等于或小于0.025 mol,则R的摩尔质量等于或大于560 g/mol,不符
合题干要求,故A和C正确;
2.8 g R的物质的量为 =0.01 mol,氢气的物质的量为 =0.02 mol,是R
的二倍,因此分子中含两个碳碳双键,不饱和度为3,故D错误。
设R的分子式为C H O ,所以有12n+2n﹣4+32=280,解得n=18,即R的分子式C H O ,由
n 2n﹣4 2 18 32 2
于R是一元羧酸,故其烃基为C H —,故B正确。
17 31
2.下列表示正确的是( )
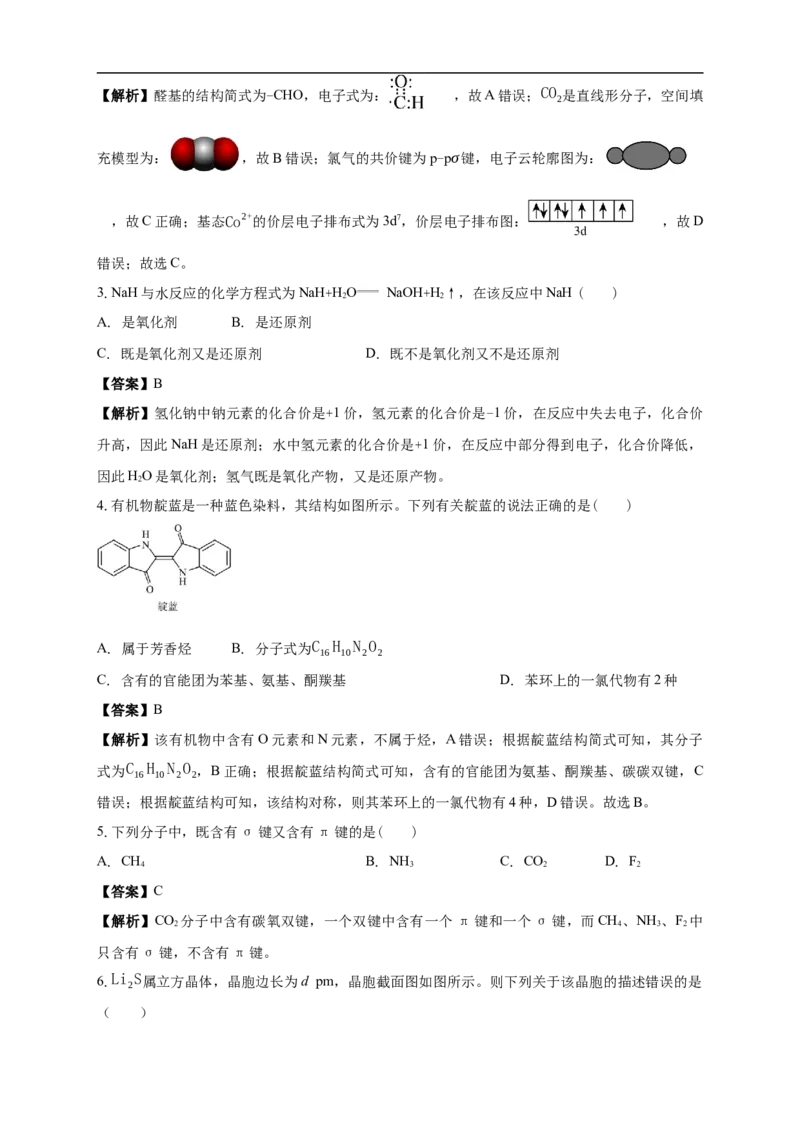
A. 醛基的电子式:
B. CO 的空间填充模型:
2
C. 氯气的共价键电子云轮廓图:
D. 基态Co2+的价层电子排布图:
【答案】C【解析】醛基的结构简式为-CHO,电子式为: ,故A错误;CO 是直线形分子,空间填
2
充模型为: ,故B错误;氯气的共价键为p-pσ键,电子云轮廓图为:
,故C正确;基态Co2+的价层电子排布式为3d7,价层电子排布图: ,故D
错误;故选C。
3.NaH与水反应的化学方程式为NaH+HO NaOH+H↑,在该反应中NaH ( )
2 2
A. 是氧化剂 B. 是还原剂
C. 既是氧化剂又是还原剂 D. 既不是氧化剂又不是还原剂
【答案】B
【解析】氢化钠中钠元素的化合价是+1价,氢元素的化合价是-1价,在反应中失去电子,化合价
升高,因此NaH是还原剂;水中氢元素的化合价是+1价,在反应中部分得到电子,化合价降低,
因此HO是氧化剂;氢气既是氧化产物,又是还原产物。
2
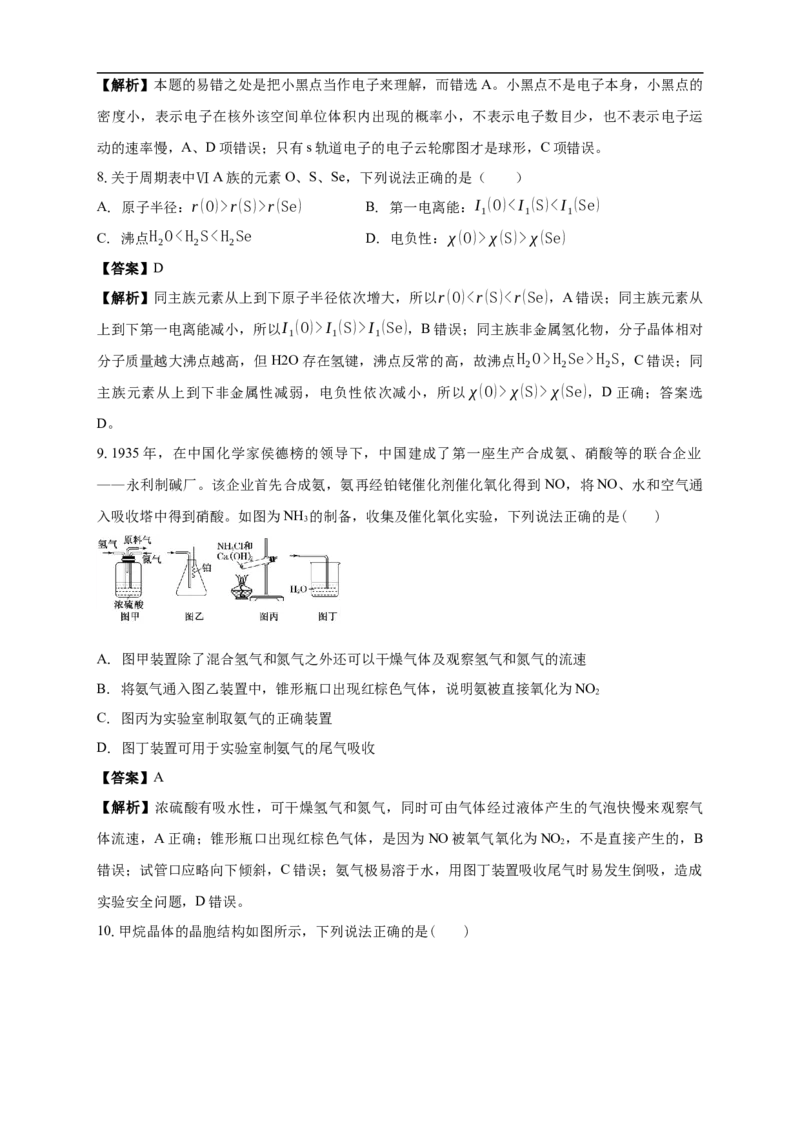
4.有机物靛蓝是一种蓝色染料,其结构如图所示。下列有关靛蓝的说法正确的是( )
A. 属于芳香烃 B. 分子式为C H N O
16 10 2 2
C. 含有的官能团为苯基、氨基、酮羰基 D. 苯环上的一氯代物有2种
【答案】B
【解析】该有机物中含有O元素和N元素,不属于烃,A错误;根据靛蓝结构简式可知,其分子
式为C H N O ,B正确;根据靛蓝结构简式可知,含有的官能团为氨基、酮羰基、碳碳双键,C
16 10 2 2
错误;根据靛蓝结构可知,该结构对称,则其苯环上的一氯代物有4种,D错误。故选B。
5.下列分子中,既含有σ键又含有π键的是( )
A. CH B. NH C. CO D. F
4 3 2 2
【答案】C
【解析】CO 分子中含有碳氧双键,一个双键中含有一个 π键和一个σ键,而CH 、NH 、F 中
2 4 3 2
只含有σ键,不含有π键。
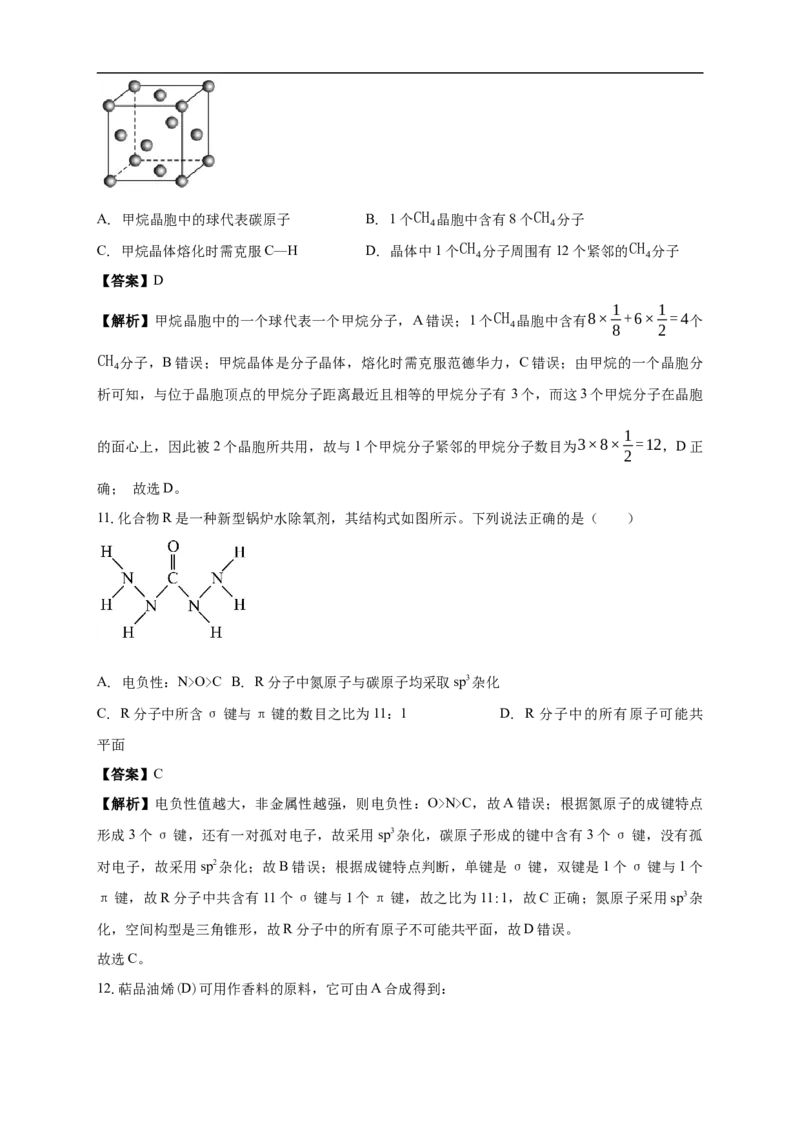
6.Li S属立方晶体,晶胞边长为d pm,晶胞截面图如图所示。则下列关于该晶胞的描述错误的是
2
( )A. 每个晶胞中含有的S2−数目为4
B. 与Li+距离最近且相等的S2−有8个
√3
C. 该晶胞中两个距离最近的Li+和S2−的核间距的计算表达式为 dpm
4
184
D. Li S晶体的密度为 ×1030g⋅cm−3
2 d3N
A
【答案】B
【解析】根据图示,延y轴叠加后构成立方晶胞,S2-位于晶胞的顶点和面心,Li+位于晶胞体内,
1 1
利用均摊法计算,一个晶胞内含有S2-个数 ×8+ ×6=4,Li+的个数为8;
8 2
据分析,每个晶胞中含有的S2-数目为4,A正确;据分析,Li+位于立方晶胞体对角线四分之一处,
与其最近且等距离的S2-位于对应近距离顶点及该顶点所在三个面的面心,有 4个,B错误;据分
析,该晶胞中两个距离最近的Li+和S2-的核间距恰好为该立方晶胞体对角线的四分之一,该晶胞边
√3
长为dpm,则计算表达式为 d pm,C正确;据分析,一个晶胞中含有4个S2-和8个Li+,晶胞
4
32×4+7×8 184
边长为d×10-10cm,LiS晶体的密度为
g/cm3= ×1030g/cm3
,D正确。
2 N (d×10−10 ) 3 dN
A A
7.如图为氢原子的电子云图,下列说法正确的是( )
A. 电子云图中小黑点的密度越小,电子数目越少
B. 电子云图中小黑点的密度越大,单位体积内电子出现的概率越大
C. 所有电子云轮廓图都是球形
D. 电子云图中小黑点的密度小,表示电子在该区域内运动的速率慢
【答案】B【解析】本题的易错之处是把小黑点当作电子来理解,而错选A。小黑点不是电子本身,小黑点的
密度小,表示电子在核外该空间单位体积内出现的概率小,不表示电子数目少,也不表示电子运
动的速率慢,A、D项错误;只有s轨道电子的电子云轮廓图才是球形,C项错误。
8.关于周期表中ⅥA族的元素O、S、Se,下列说法正确的是( )
A. 原子半径:r(O)>r(S)>r(Se) B. 第一电离能:I (O)χ(S)>χ(Se)
2 2 2
【答案】D
【解析】同主族元素从上到下原子半径依次增大,所以r(O)I (S)>I (Se),B错误;同主族非金属氢化物,分子晶体相对
1 1 1
分子质量越大沸点越高,但H2O存在氢键,沸点反常的高,故沸点H O>H Se>H S,C错误;同
2 2 2
主族元素从上到下非金属性减弱,电负性依次减小,所以χ(O)>χ(S)>χ(Se),D正确;答案选
D。
9.1935年,在中国化学家侯德榜的领导下,中国建成了第一座生产合成氨、硝酸等的联合企业
——永利制碱厂。该企业首先合成氨,氨再经铂铑催化剂催化氧化得到 NO,将NO、水和空气通
入吸收塔中得到硝酸。如图为NH 的制备,收集及催化氧化实验,下列说法正确的是( )
3
A. 图甲装置除了混合氢气和氮气之外还可以干燥气体及观察氢气和氮气的流速
B. 将氨气通入图乙装置中,锥形瓶口出现红棕色气体,说明氨被直接氧化为NO
2
C. 图丙为实验室制取氨气的正确装置
D. 图丁装置可用于实验室制氨气的尾气吸收
【答案】A
【解析】浓硫酸有吸水性,可干燥氢气和氮气,同时可由气体经过液体产生的气泡快慢来观察气
体流速,A正确;锥形瓶口出现红棕色气体,是因为NO被氧气氧化为NO ,不是直接产生的,B
2
错误;试管口应略向下倾斜,C错误;氨气极易溶于水,用图丁装置吸收尾气时易发生倒吸,造成
实验安全问题,D错误。
10.甲烷晶体的晶胞结构如图所示,下列说法正确的是( )A. 甲烷晶胞中的球代表碳原子 B. 1个CH 晶胞中含有8个CH 分子
4 4
C. 甲烷晶体熔化时需克服C—H D. 晶体中1个CH 分子周围有12个紧邻的CH 分子
4 4
【答案】D
1 1
【解析】甲烷晶胞中的一个球代表一个甲烷分子,A错误;1个CH 晶胞中含有8× +6× =4个
4 8 2
CH 分子,B错误;甲烷晶体是分子晶体,熔化时需克服范德华力,C错误;由甲烷的一个晶胞分
4
析可知,与位于晶胞顶点的甲烷分子距离最近且相等的甲烷分子有 3个,而这3个甲烷分子在晶胞
1
的面心上,因此被2个晶胞所共用,故与1个甲烷分子紧邻的甲烷分子数目为3×8× =12,D正
2
确; 故选D。
11.化合物R是一种新型锅炉水除氧剂,其结构式如图所示。下列说法正确的是( )
A. 电负性:N>O>C B. R分子中氮原子与碳原子均采取sp3杂化
C. R分子中所含σ键与π键的数目之比为11:1 D. R分子中的所有原子可能共
平面
【答案】C
【解析】电负性值越大,非金属性越强,则电负性:O>N>C,故A错误;根据氮原子的成键特点
形成3个σ键,还有一对孤对电子,故采用sp3杂化,碳原子形成的键中含有3个σ键,没有孤
对电子,故采用sp2杂化;故B错误;根据成键特点判断,单键是σ键,双键是1个σ键与1个
π键,故R分子中共含有11个σ键与1个π键,故之比为11:1,故C正确;氮原子采用sp3杂
化,空间构型是三角锥形,故R分子中的所有原子不可能共平面,故D错误。
故选C。
12.萜品油烯(D)可用作香料的原料,它可由A合成得到:下列说法正确的是( )
A. 有机物B的分子式为C H O B. 有机物D分子中所有碳原子一定共面
11 20 3
C. 1 mol有机物A中含有约1.204×1024个双键 D. 有机物C的同分异构体中不
可能有芳香族化合物
【答案】C
【解析】根据有机化合物B的结构简式可知,其分子式为C H O;有机物D分子中的环状结构并
11 18 3
不是苯环,故有机物D分子中所有碳原子一定不共面;由于有机物C的不饱和度为4,故其同分异
构体中可能有芳香族化合物。
13.氢键对生命物质的高级结构和生物活性具有重要意义。下列现象中不能用氢键解释的是( )
A. 磷酸、脱氧核糖和碱基形成DNA链状结构
B. 蛋白质的二级结构的形成
C. 棉织衣物具有很好的吸湿性和透气性
D. 水蒸气的相对分子质量测定值比按化学式HO计算出来的值明显大
2
【答案】C
【解析】DNA分子中的碱基靠氢键形成碱基对,从而将两条链连接在一起形成双螺旋结构,A正
确;蛋白质的二级结构通过骨架上的羰基与酰胺基团之间形成的氢键维持,B正确;布料吸湿性的
高低主要取决于纤维大分子上所含亲水基团的多少,透气性与面料的组织结构如厚度、平纹、斜
纹等有关,而与氢键无关,C错误;接近水的沸点的水蒸气中存在相当量的水分子因氢键而相互缔
合,形成所谓的缔合分子,因此水蒸气的相对分子质量测定值比按化学式计算出来的值明显大,D
正确。
14.a、b、c、d、e、f 为六种短周期元素, a、b、e 、f 位于同一周期,c、d 也是同一周期, 且
d、e 同一主族,原子半径 d<e,a、b、c、d、f原子最外层电子依次增多,则下列说法中正确的
是( )
A. e 的非金属性比 f 强 B. d 元素可能是第一周期元素
C. 六种元素中,a 元素最高价氧化物对应水化物碱性最强 D. a、b、c、d 的原子序数逐渐
增大
【答案】C【解析】a、b、c、d、e、f为六种短周期元素,a、b、c、d、f原子最外层电子依次增多,则d的
最外层电子数≥4;d、e同一主族,原子半径d<e,则d处于第二周期,e处于第三周期;a、b、
e、f位于同一周期,故a、b、e、f处于第三周期,c、d是同一周期,故c位于第二周期,原子序
数c<d<a<b<e<f。
a、b、c、d、f原子最外层电子依次增多,则d的最外层电子数≥4,e的最外层电子数大于等于
4,小于f的最外层电子数,且e 、f 位于同一周期,同周期从左到右非金属性逐渐增强,所以f的
非金属性比e强,故A错误;a、b、c、d、f原子最外层电子依次增多,则d的最外层电子数≥4,
d、e同一主族,原子半径d<e,则d处于第二周期,故B错误;c、d处于第二周期,a、b、e、f
处于第三周期,a、b、c、d、f原子最外层电子依次增多,所以金属性a最强,a元素最高价氧化物
对应水化物碱性最强,故C正确;由上述分析可知,c在d的左侧,a、b、e、f处于第三周期,所
以原子序数大小顺序是c<d<a<b,故D错误。
15.我们生活的衣食住行都离不开有机化合物,下列说法不正确的是( )
A. 甲烷是一种清洁能源,是天然气的主要成分
B. 用KMnO 溶液浸泡过的藻土可使水果保鲜,是利用了乙烯的还原性
4
C. 乙炔用于焊接或切割金属,是因为乙炔燃烧时放出大量的热
D. 聚氯乙烯(PVC)塑料,可用于制作食品包装袋
【答案】D
【解析】天然气的主要成分是甲烷,甲烷燃烧放出大量的热,且产物 CO 和HO不会污染环境,
2 2
故甲烷是一种清洁能源,故A正确;用高锰酸钾浸泡过的藻土可使水果保鲜,是用酸性高锰酸钾
溶液将乙烯氧化,即是利用了乙烯的还原性,故 B正确;因为乙炔燃烧时放出大量的热,所以乙
炔用于焊接或切割金属,故C正确;聚氯乙烯(PVC)含有氯元素,使用不当会产生有毒的氯化
物等,故聚氯乙烯(PVC)塑料不可用于制作食品包装袋,故D错误。故选D。
16.磁光存储的研究是Williams等在1957年使Mn和Bi形成的晶体薄膜磁化并用光读取之后开始
的。如图是Mn和Bi形成的某种晶体的结构示意图,则该晶体物质的化学式可表示为( )
A. MnBi B. MnBi C. MnBi D. MnBi
2 3 4 3
【答案】B
【解析】该晶胞中Mn原子的个数为12× +6× +2× +1=6,Bi原子的个数为6,则该晶体物
质的化学式为MnBi。二、非选择题(本大题共4小题,共55分)
17.D、E、F、X、Y、Z为前四周期元素,且原子序数依次增大。D的最高正价和最低负价的绝对
值相等;E有三个能级,且每个能级上的电子数相等;F原子未成对电子数在同周期元素中最多;
X与F同周期,第一电离能比F低;Y与E同主族,Z的最外层只有一个电子,其他电子层电子均
处于饱和状态。请回答下列问题:
(1)Y基态原子的核外电子排布式为 ;基态Z原子中电子占据的最高能
层符号为 。
(2)E、F、X的电负性由小到大的顺序为 (用元素符号表示)。
(3)D、E、F、X形成的有机化合物EX(FD ) 中E的杂化轨道类型为
,FX-
的空间结构是
2 2 3
。
(4)下列关于ED 分子和DX 分子的说法正确的是 (填字母)。
2 2 2 2
a.分子中都含σ键和π键
b.ED 分子的沸点明显低于DX 分子的沸点
2 2 2 2
c.都是含极性键和非极性键的非极性分子
【答案】(1)1s22s22p63s23p2 N
(2)C