文档内容
湖南省永州市2026年高考第一次模拟考试化学试卷
注意事项:
1.本试卷共18道小题,满分为100分,考试时量 75分钟。
2.考生务必将各题的答案填写在答题卡的相应位置,在本试卷上作答无效。考试结束后只交
答题卡。
3.可能用到的相对原子质量H-1 C-12 N-14 O-16 Na-23 Cu-64
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
1.2025年九三阅兵展示了我国多种高科技材料。下列材料属于金属材料的是
A.钛合金部件——新型战机发动机关键构件
B.氮化硅陶瓷轴承————地面装备传动系统核心部件
C.碳纤维复合材料————卫星通信车轻量化结构件
D.聚酰亚胺薄膜————电子对抗系统柔性电路基材
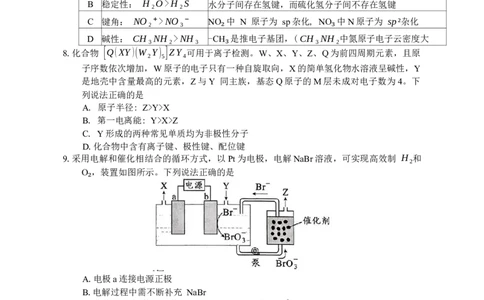
2.下列化学用语表述正确的是
22
A. 中子数为12的氖原子: Ne
12
B.基态 Be 原子的价电子排布图: 2S2P
C. PCl 分子的空间结构模型:
₃
D.反-1,2-二氟乙烯的结构式:
3.下列气体的提纯方法正确的是
A B C D
除去 CO 中的SO 除去 Cl 中的HCl 除去C H 中的 H₂S 干燥 NH₃
4.下列试剂保存与实验操作不规范的是
₂ ₂ ₂ ₂ ₂
A.四氯化碳保存在广口塑料瓶中
B.金属钠保存在石蜡油中
C.实验室中可以将未用完的白磷放回原试剂瓶
D.不慎将碱沾到皮肤上,应立即用大量水冲洗,然后涂上1%的硼酸
5.下列离子方程式与所给事实相符的是
A.过量铁粉与稀硝酸反应: Fe+NO−+4H+=Fe3++NO↑+2H O
3 2
B.用氯气氧化苦卤得到溴单质: 2Br−+Cl =Br +2Cl−
2 2
电解
2Cl−+2H O
C.用惰性电极电解MgCl 溶液: 2 _______ H ↑+2OH−+Cl ↑¿
¿ 2 2
D.用 Na CO 溶液处理水₂垢中的 CaSO :Ca2++CO2−=CaCO ↓
4 3 3
6. Na O 可 在 呼 吸 面 具 中 作 为 氧 气 的 来 源 , 其 原 理 为
₂ ₃
₂ ₂2Na O +2CO =2Na CO +O 。设 NA为阿伏加德罗常数的值。下列说法正
2 2 2 2 3 2
确的是
A.22.4LCO 中含σ键数目为2NA
2
B.7.8gNa O 固体中含有的离子数为0.4NA
2 2
C.1L1mol⋅L−1的 Na CO 溶液中 CO2−的数目小于 NA
2 3 3
D.等物质的量的Na O 分别与足量的水和CO 反应,转移电子数均为NA
7.下列有关物质性质的解释错误的是
₂ ₂ ₂
性质 解释
A 熔点: NaCl>CsCl 氯化钠中的离子键强于氯化铯中的离子键
B 稳定性: H₂O>H₂S 水分子间存在氢键,而硫化氢分子间不存在氢键
C 键角: NO₂⁺>NO₃⁻ NO 中 N 原子为 sp杂化, NO 中N原子为 sp²杂化
D 碱性: CH₃NH₂>NH₃ -CH 是推电子基团,( CH₃NH₂中氮原子电子云密度大
₂ ₃
8.化合物 [Q(XY)(W Y) ]ZY 可用于离子检测。W、X、Y、Z、Q为前四周期元素,且原
2 5 4 ₃
子序数依次增加,W原子的电子只有一种自旋取向,X的简单氢化物水溶液呈碱性,Y
是地壳中含量最高的元素,Z与Y 同主族,基态Q原子的M层未成对电子数为4。下
列说法正确的是
A. 原子半径: Z>Y>X
B. 第一电离能: Y>X>Z
C. Y形成的两种常见单质均为非极性分子
D.化合物中含有离子键、极性键、配位键
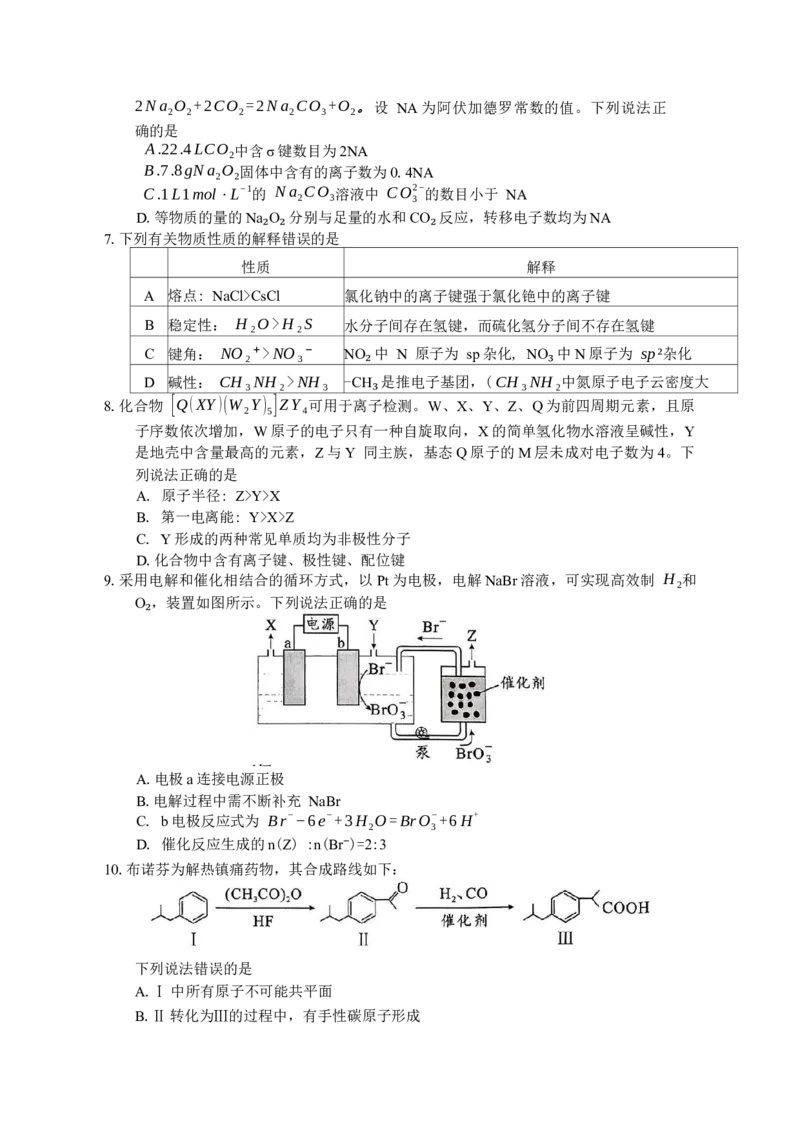
9.采用电解和催化相结合的循环方式,以Pt为电极,电解NaBr溶液,可实现高效制 H 和
2
O ,装置如图所示。下列说法正确的是
₂
A.电极a连接电源正极
B.电解过程中需不断补充 NaBr
C. b电极反应式为 Br−−6e−+3H O=BrO−+6H+
2 3
D. 催化反应生成的n(Z) :n(Br⁻)=2:3
10.布诺芬为解热镇痛药物,其合成路线如下:
下列说法错误的是
A.Ⅰ中所有原子不可能共平面
B.Ⅱ转化为Ⅲ的过程中,有手性碳原子形成C.Ⅱ转化为Ⅲ的反应,原子利用率为100%
D.1mol Ⅲ最多可与4mol H 反应
11.工业上可用低品位锰矿(主要成分MnO ,含 Fe、Al、Ni、Pb等元素的杂质)制备高纯二
₂
氧化锰,工艺流程如图所示。下列说法错误的是
₂
已知:常温下 K (PbS)=8.0×10−28、K (NiS)=1.0×10−21。
sp sp
A. “焙烧”前,需对低品位锰矿进行粉碎处理
B. “除铝”时, 可用足量的 NaOH溶液代替NH ·H O
C. “除镍铅”后的滤液中, c(Pb2+):c(Ni2+)=8.0×10−7
₃ ₂
D. “沉锰”时,反应的离子方程式为:
HCO−+N H ⋅H O+Mn2+=MnCO ↓+N H++H O
3 3 2 3 4 2
12.烟酸又称维生素B3,实验室可用3-甲基吡啶为原料来制备。
3-甲基吡啶(沸点: 144℃)
已知:烟酸微溶于冷水,易溶于热水。
实验步骤:①在3-甲基吡啶和水的混合液中分多次加入KMnO 固体,加热搅拌。
②将步骤①所得溶液转移至蒸馏烧瓶中,控制温度在144℃时蒸馏,趁热过滤。
₄
③用浓盐酸酸化滤液,并调节溶液的 pH为3.8~4.0,经一系列操作,获得粗产品。
下列说法错误的是
A.分多次加入高锰酸钾的目的是控制反应速率和提高产率
B.蒸馏的目的是为了除去未反应的3-甲基吡啶
C.步骤③中,可用广泛 pH 试纸测定溶液的pH
D.可采用重结晶的方法提纯粗产品
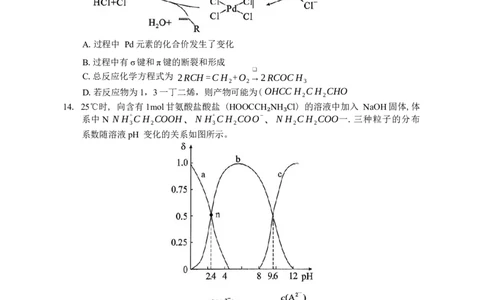
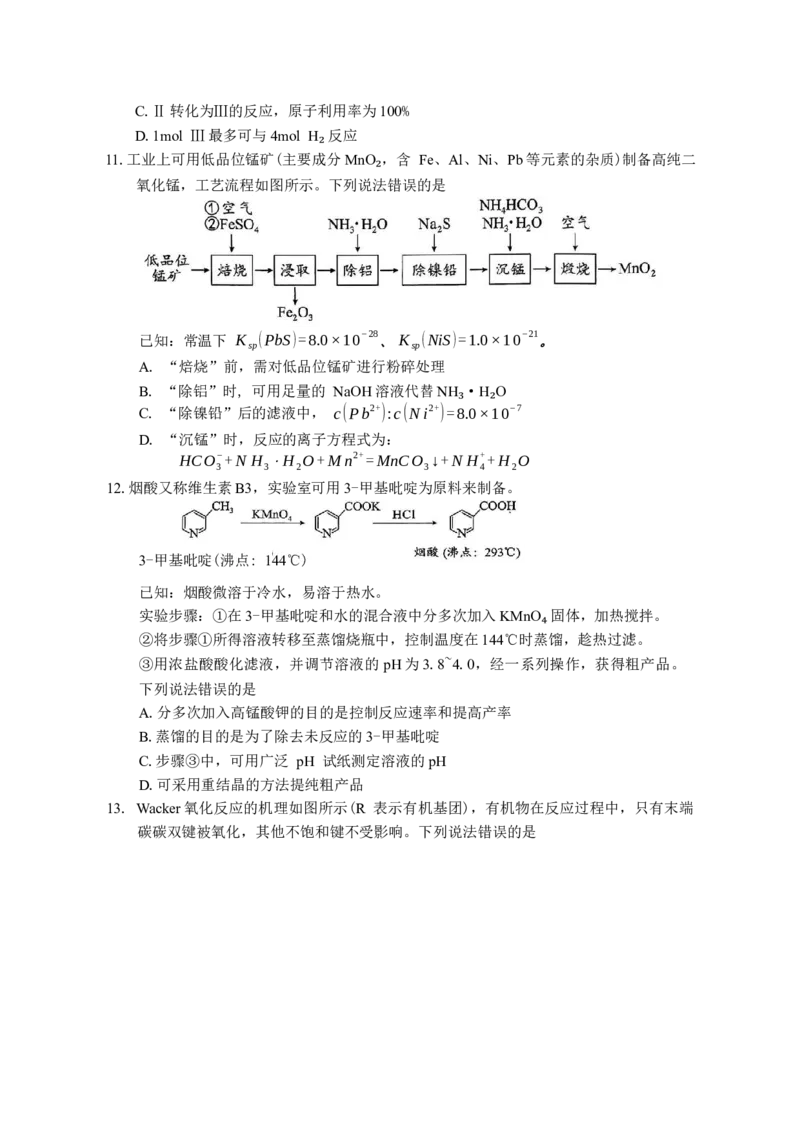
13. Wacker氧化反应的机理如图所示(R 表示有机基团),有机物在反应过程中,只有末端
碳碳双键被氧化,其他不饱和键不受影响。下列说法错误的是A.过程中 Pd元素的化合价发生了变化
B.过程中有σ键和π键的断裂和形成
❑
C.总反应化学方程式为 2RCH=CH +O →2RCOCH
2 2 3
D.若反应物为1,3一丁二烯,则产物可能为( OHCCH CH CHO
2 2
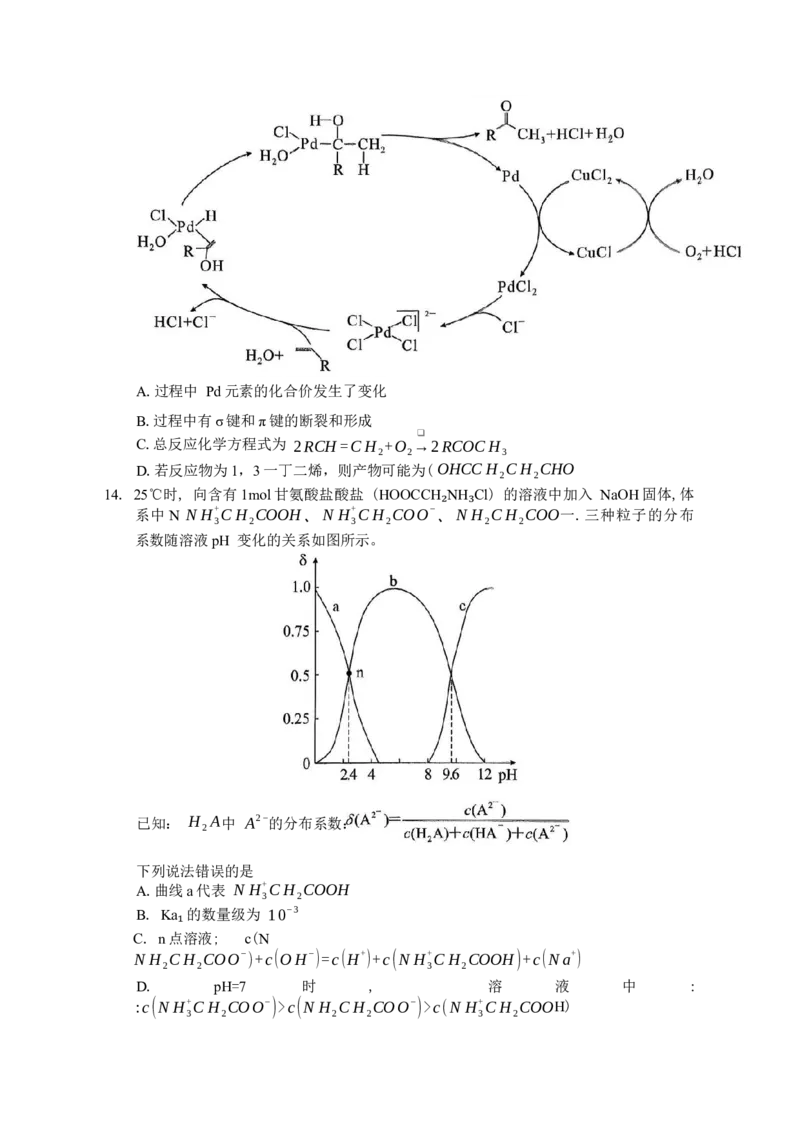
14. 25℃时, 向含有1mol甘氨酸盐酸盐 (HOOCCH NH Cl) 的溶液中加入 NaOH固体,体
系中 N N H+CH COOH、N H+CH COO−、N H CH COO一.三种粒子的分布
3 2 3 2 2 2
₂ ₃
系数随溶液pH 变化的关系如图所示。
已知: H A中 A2−的分布系数:
2
下列说法错误的是
A.曲线a代表 N H+CH COOH
3 2
B. Ka 的数量级为 10−3
C. n点溶液; c(N
₁
N H CH COO− )+c(OH−)=c(H+)+c(N H+CH COOH)+c(Na+)
2 2 3 2
D. pH=7 时 , 溶 液 中 :
:c(N H+CH COO−)>c(N H CH COO−)>c(N H+CH COOH)
3 2 2 2 3 2二、非选择题:本题共4小题,共58分。
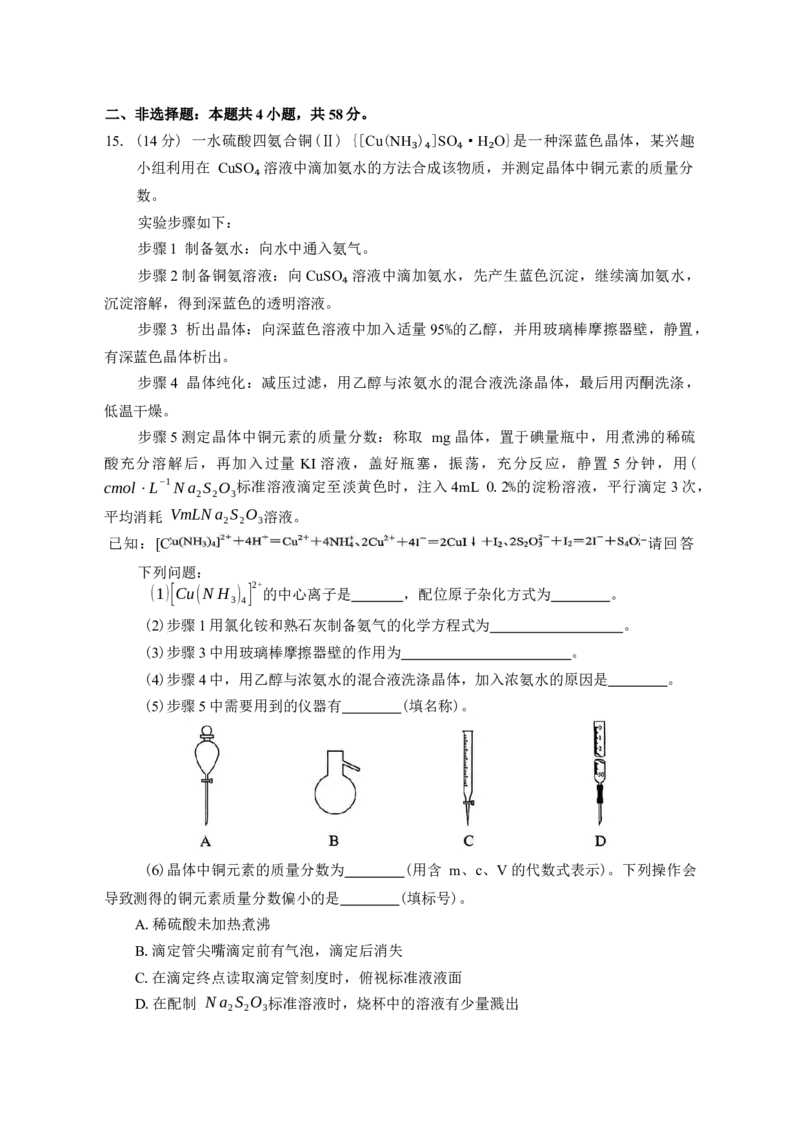
15. (14分) 一水硫酸四氨合铜(Ⅱ) {[Cu(NH ) ]SO ·H O}是一种深蓝色晶体,某兴趣
小组利用在 CuSO 溶液中滴加氨水的方法合成该物质,并测定晶体中铜元素的质量分
₃ ₄ ₄ ₂
数。
₄
实验步骤如下:
步骤1 制备氨水:向水中通入氨气。
步骤2制备铜氨溶液:向CuSO 溶液中滴加氨水,先产生蓝色沉淀,继续滴加氨水,
沉淀溶解,得到深蓝色的透明溶液。
₄
步骤3 析出晶体:向深蓝色溶液中加入适量95%的乙醇,并用玻璃棒摩擦器壁,静置,
有深蓝色晶体析出。
步骤4 晶体纯化:减压过滤,用乙醇与浓氨水的混合液洗涤晶体,最后用丙酮洗涤,
低温干燥。
步骤5测定晶体中铜元素的质量分数:称取 mg晶体,置于碘量瓶中,用煮沸的稀硫
酸充分溶解后,再加入过量 KI 溶液,盖好瓶塞,振荡,充分反应,静置 5 分钟,用(
cmol⋅L−1Na S O 标准溶液滴定至淡黄色时,注入4mL 0.2%的淀粉溶液,平行滴定3次,
2 2 3
平均消耗 VmLNa S O 溶液。
2 2 3
已知:[C ⁻请回答
下列问题:
2+
(1)[Cu(N H ) ] 的中心离子是 ,配位原子杂化方式为 。
3 4
(2)步骤1用氯化铵和熟石灰制备氨气的化学方程式为 。
(3)步骤3中用玻璃棒摩擦器壁的作用为 。
(4)步骤4中,用乙醇与浓氨水的混合液洗涤晶体,加入浓氨水的原因是 。
(5)步骤5中需要用到的仪器有 (填名称)。
(6)晶体中铜元素的质量分数为 (用含 m、c、V的代数式表示)。下列操作会
导致测得的铜元素质量分数偏小的是 (填标号)。
A.稀硫酸未加热煮沸
B.滴定管尖嘴滴定前有气泡,滴定后消失
C.在滴定终点读取滴定管刻度时,俯视标准液液面
D.在配制 Na S O 标准溶液时,烧杯中的溶液有少量溅出
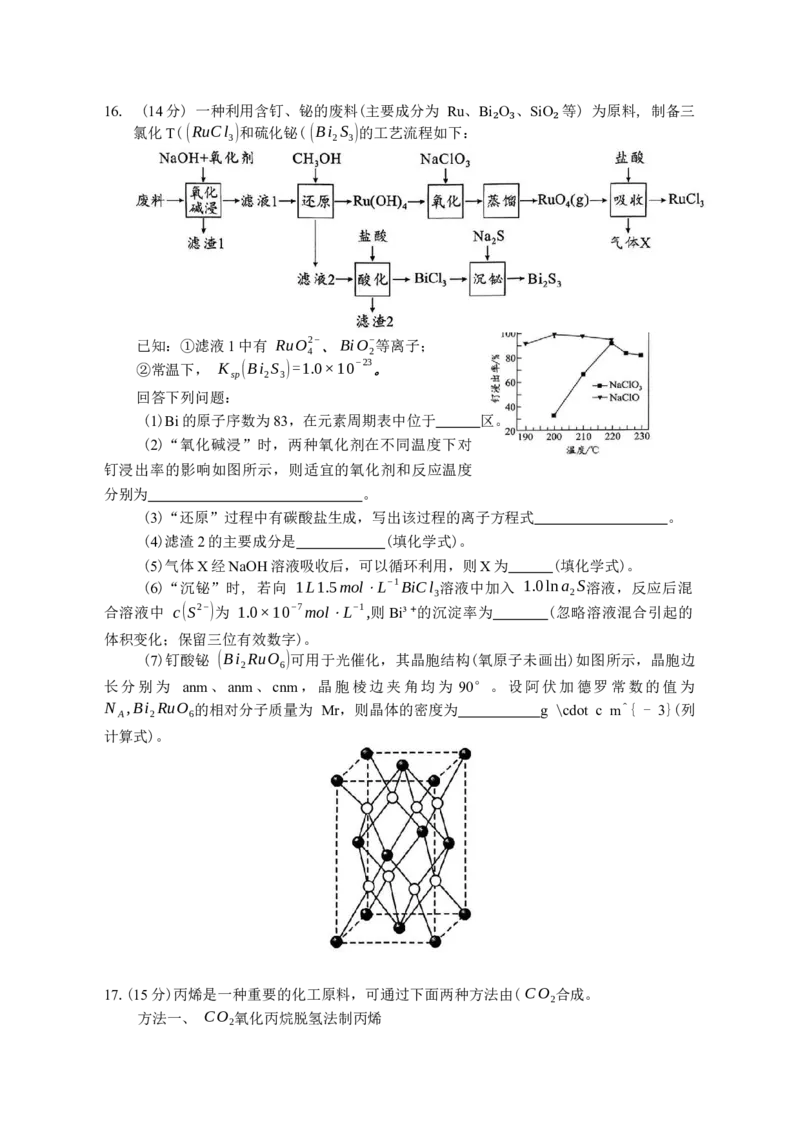
2 2 316. (14分) 一种利用含钉、铋的废料(主要成分为 Ru、Bi O 、SiO 等) 为原料, 制备三
氯化T( (RuCl )和硫化铋( (Bi S )的工艺流程如下:
3 2 3
₂ ₃ ₂
已知:①滤液1中有 RuO2−、BiO−等离子;
4 2
②常温下, K (Bi S )=1.0×10−23。
sp 2 3
回答下列问题:
(1)Bi的原子序数为83,在元素周期表中位于 区。
(2)“氧化碱浸”时,两种氧化剂在不同温度下对
钉浸出率的影响如图所示,则适宜的氧化剂和反应温度
分别为 。
(3)“还原”过程中有碳酸盐生成,写出该过程的离子方程式 。
(4)滤渣2的主要成分是 (填化学式)。
(5)气体X经NaOH溶液吸收后,可以循环利用,则X为 (填化学式)。
(6)“沉铋”时, 若向 1L1.5mol⋅L−1BiCl 溶液中加入 1.0lna S溶液,反应后混
3 2
合溶液中 c(S2−)为 1.0×10−7mol⋅L−1,则Bi³⁺的沉淀率为 (忽略溶液混合引起的
体积变化;保留三位有效数字)。
(7)钉酸铋 (Bi RuO )可用于光催化,其晶胞结构(氧原子未画出)如图所示,晶胞边
2 6
长分别为 anm、anm、cnm,晶胞棱边夹角均为 90°。设阿伏加德罗常数的值为
N ,Bi RuO 的相对分子质量为 Mr,则晶体的密度为 g \cdot c m^{ - 3}(列
A 2 6
计算式)。
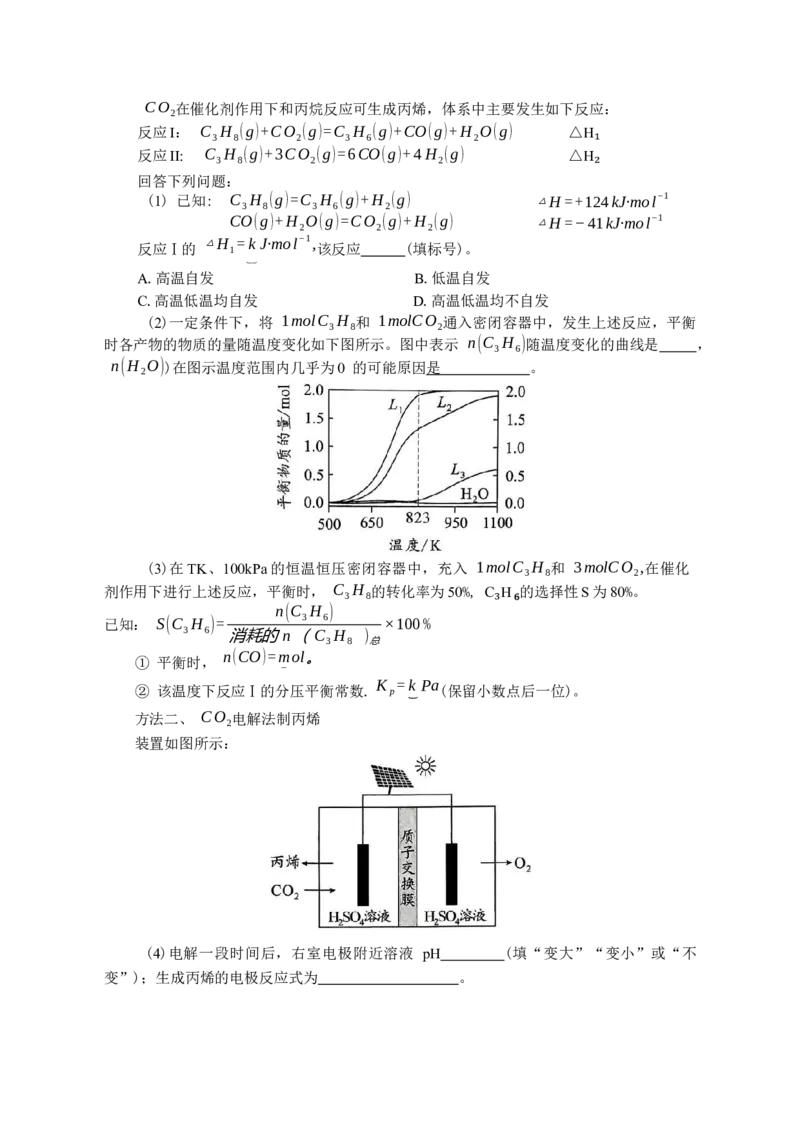
17.(15分)丙烯是一种重要的化工原料,可通过下面两种方法由( CO 合成。
2
方法一、 CO 氧化丙烷脱氢法制丙烯
2CO 在催化剂作用下和丙烷反应可生成丙烯,体系中主要发生如下反应:
2
反应I: C H (g)+CO (g)=C H (g)+CO(g)+H O(g) △H
3 8 2 3 6 2
反应II: C H (g)+3CO (g)=6CO(g)+4H (g) △H
3 8 2 2 ₁
回答下列问题:
₂
(1) 已知: C H (g)=C H (g)+H (g) △H=+124kJ·mol−1
3 8 3 6 2
CO(g)+H O(g)=CO (g)+H (g) △H=−41kJ·mol−1
2 2 2
△H =k J·mol−1,
反应Ⅰ的 1 该反应 (填标号)。
⏟
A.高温自发 B.低温自发
C.高温低温均自发 D.高温低温均不自发
(2)一定条件下,将 1molC H 和 1molCO 通入密闭容器中,发生上述反应,平衡
3 8 2
时各产物的物质的量随温度变化如下图所示。图中表示 n(C H )随温度变化的曲线是 ,
3 6
n(H O))在图示温度范围内几乎为0 的可能原因是 。
2
(3)在TK、100kPa的恒温恒压密闭容器中,充入 1molC H 和 3molCO ,在催化
3 8 2
剂作用下进行上述反应,平衡时, C H 的转化率为50%, C H₆的选择性S为80%。
3 8
n(C H )
已知: S(C H )= 3 6 ×100% ₃
3 6 消耗的n(C H )
3 8 总
n(CO)=mol。
① 平衡时,
¯
K =k Pa
② 该温度下反应Ⅰ的分压平衡常数. p (保留小数点后一位)。
︸
方法二、 CO 电解法制丙烯
2
装置如图所示:
(4)电解一段时间后,右室电极附近溶液 pH (填“变大”“变小”或“不
变”);生成丙烯的电极反应式为 。18.(15分)H是一种香料的主要成分,分子结构中含有三个六元环。其一种合成路线如下
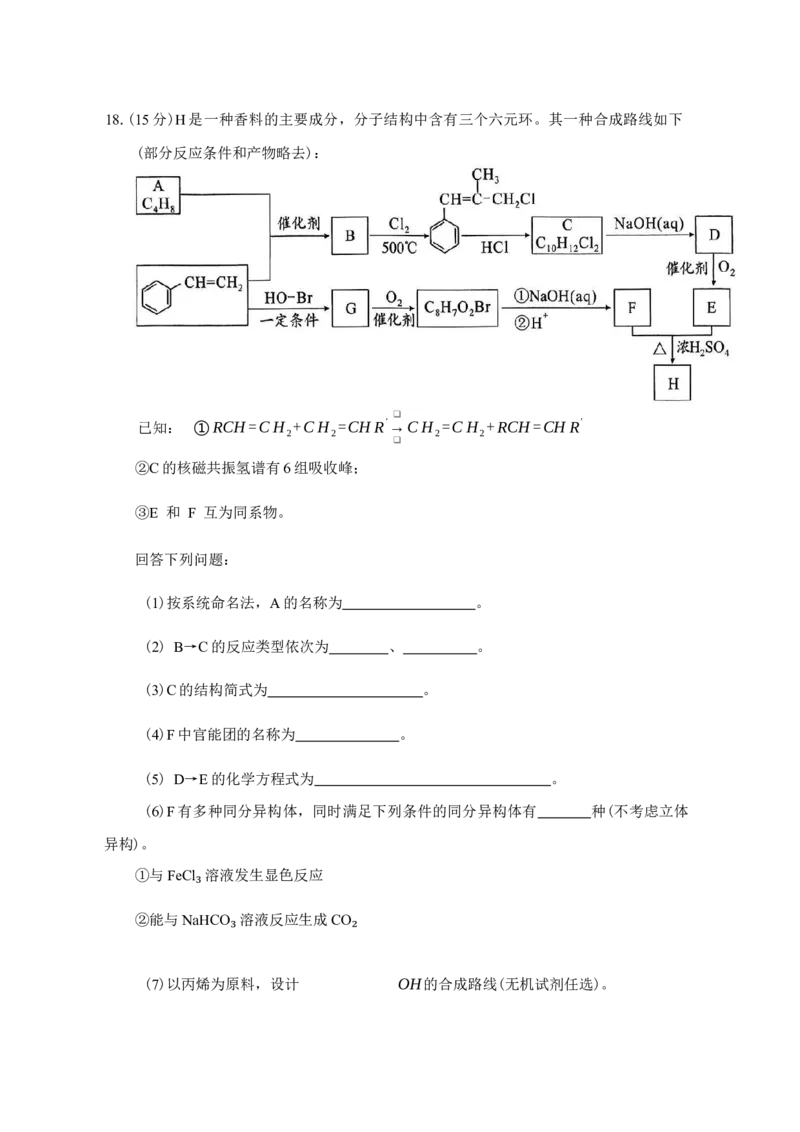
(部分反应条件和产物略去):
❑
已知: ①RCH=CH +CH =CH R'→CH =CH +RCH=CH R'
2 2 2 2
❑
②C的核磁共振氢谱有6组吸收峰;
③E 和 F 互为同系物。
回答下列问题:
(1)按系统命名法,A的名称为 。
(2) B→C的反应类型依次为 、 。
(3)C的结构简式为 。
(4)F中官能团的名称为 。
(5) D→E的化学方程式为 。
(6)F有多种同分异构体,同时满足下列条件的同分异构体有 种(不考虑立体
异构)。
①与FeCl 溶液发生显色反应
₃
②能与NaHCO 溶液反应生成CO
₃ ₂
(7)以丙烯为原料,设计 OH的合成路线(无机试剂任选)。永州市 2026 年高考第一次模拟考试
化学参考答案及评分标准
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 A D B A B C B D C D B C D C
二、非选择题:共58分。
15.(14 分)
(1) Cu²⁺(1分) sp³(1分)
(2)2N H Cl+Ca(OH) CaCl +2N H ↑+2H O(2分)
4 2 2 3 2
(3)以玻璃棒摩擦器壁产生的玻璃屑为晶核,促进晶体的析出(2分)
(4)提高氨的浓度,防止晶体在洗涤过程中分解失氨 (2分)
(5)碱式滴定管(2分)
6.4cV
(6) % (2分) C(2分)
m
16. (14分)
(1) p (2分)
(2) NaClO、200℃ (每个1分, 共2分)
( 3)3RuO2−+CH OH+6H O=3Ru(OH) ↓+CO2−+4OHI⁻(2分)
4 3 2 4 3
(4) H SiO 或H SiO (2分)
(5) Cl₂ (2分 ₃ ) ₄ ₄
(6) 86₂ .7%(2分)
4M
(7) r ×1021 (2分)
a2cN
A
17.(15分)
(1) +165(2分) A (2分)
(2) L (2分) 823K前, 反应Ⅱ占主导, 反应Ⅰ几乎不发生(1分); 823K后, 反应Ⅰ
生成的H O与CO继续反应被消耗(1分)。(其他合理答案也给分)
₃
(3) ①1(2分) ②2.8(2分)
₂
(4) 变小(1分) 3CO +18H++18e−=C H +6H O (2分)微信公众号“做事方法
2 3 6 2
很重要”
18.(15分)
(1) 2-甲基丙烯 (2分)(2)取代反应 (1分)加成反应 (1分)
(3) (2分)
(4) 羟基、羧基(2分)
(5)
(6) 13 (2分)
(7)
(3分)