文档内容
专题50 多池与膜在电化学中应用
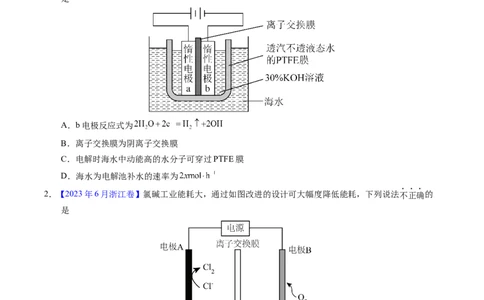
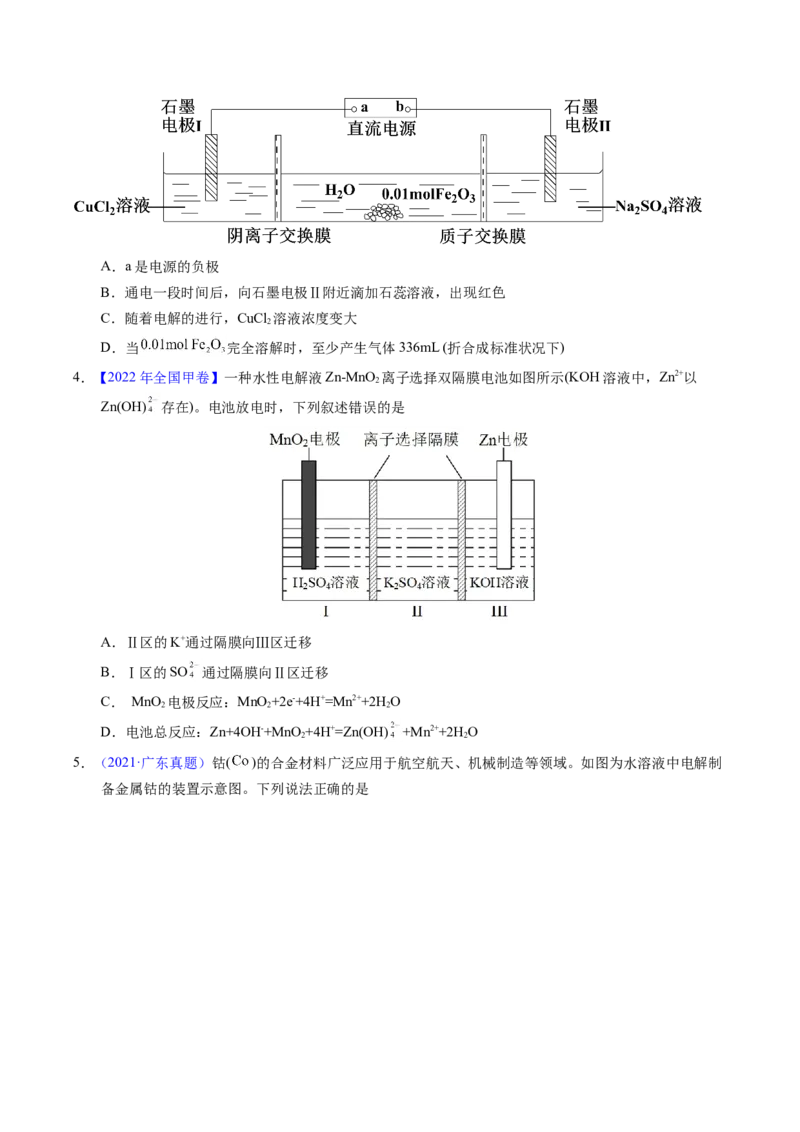
1.【2023年湖北卷】我国科学家设计如图所示的电解池,实现了海水直接制备氢气技术的绿色化。该装
置工作时阳极无 生成且KOH溶液的浓度不变,电解生成氢气的速率为 。下列说法错误的
是
A.b电极反应式为
B.离子交换膜为阴离子交换膜
C.电解时海水中动能高的水分子可穿过PTFE膜
D.海水为电解池补水的速率为
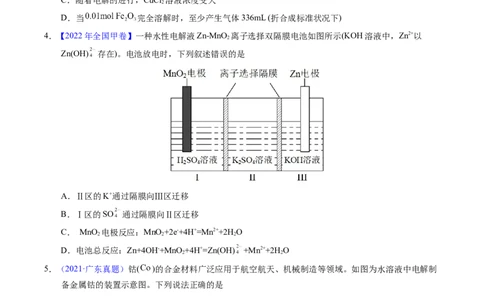
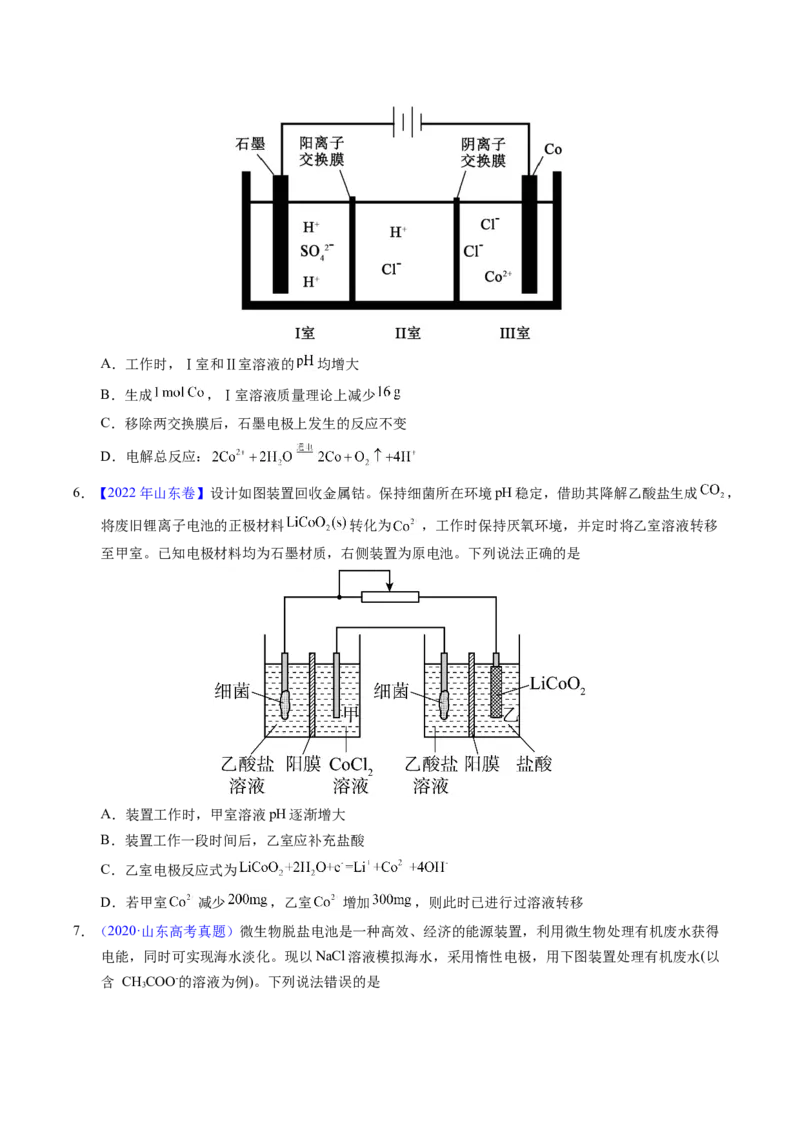
2.【2023年6月浙江卷】氯碱工业能耗大,通过如图改进的设计可大幅度降低能耗,下列说法不正确的
是
A.电极A接电源正极,发生氧化反应
B.电极B的电极反应式为:
C.应选用阳离子交换膜,在右室获得浓度较高的 溶液
D.改进设计中通过提高电极B上反应物的氧化性来降低电解电压,减少能耗
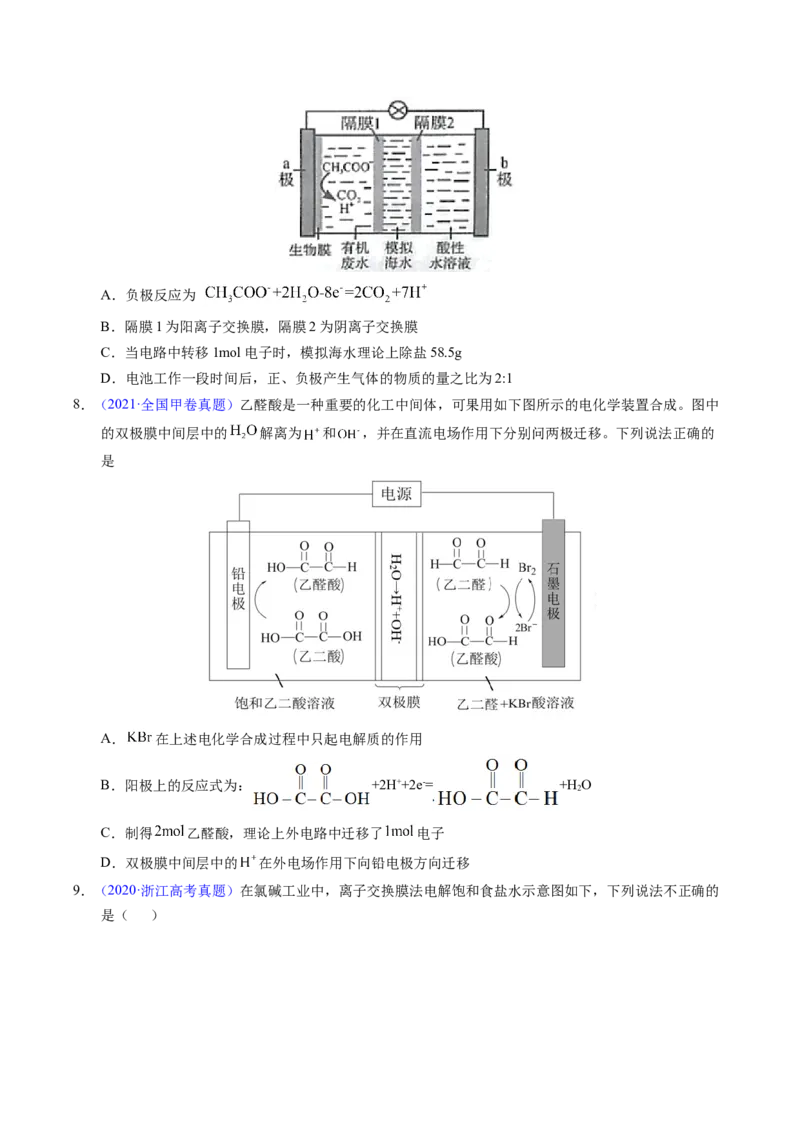
3.(2021·天津真题)如下所示电解装置中,通电后石墨电极Ⅱ上有O 生成,Fe O 逐渐溶解,下列判断
2 2 3
错误的是A.a是电源的负极
B.通电一段时间后,向石墨电极Ⅱ附近滴加石蕊溶液,出现红色
C.随着电解的进行,CuCl 溶液浓度变大
2
D.当 完全溶解时,至少产生气体336mL (折合成标准状况下)
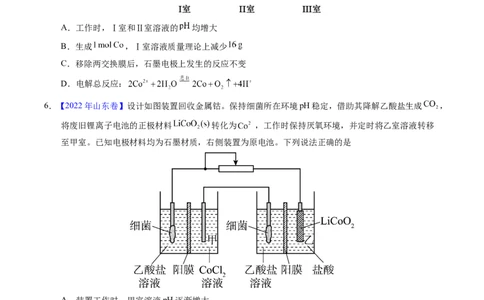
4.【2022年全国甲卷】一种水性电解液Zn-MnO 离子选择双隔膜电池如图所示(KOH溶液中,Zn2+以
2
Zn(OH) 存在)。电池放电时,下列叙述错误的是
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO 通过隔膜向Ⅱ区迁移
C. MnO 电极反应:MnO +2e-+4H+=Mn2++2H O
2 2 2
D.电池总反应:Zn+4OH-+MnO+4H+=Zn(OH) +Mn2++2H O
2 2
5.(2021·广东真题)钴( )的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶液中电解制
备金属钴的装置示意图。下列说法正确的是A.工作时,Ⅰ室和Ⅱ室溶液的 均增大
B.生成 ,Ⅰ室溶液质量理论上减少
C.移除两交换膜后,石墨电极上发生的反应不变
D.电解总反应:
6.【2022年山东卷】设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生成 ,
将废旧锂离子电池的正极材料 转化为 ,工作时保持厌氧环境,并定时将乙室溶液转移
至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是
A.装置工作时,甲室溶液pH逐渐增大
B.装置工作一段时间后,乙室应补充盐酸
C.乙室电极反应式为
D.若甲室 减少 ,乙室 增加 ,则此时已进行过溶液转移
7.(2020·山东高考真题)微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得
电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用下图装置处理有机废水(以
含 CHCOO-的溶液为例)。下列说法错误的是
3A.负极反应为
B.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜
C.当电路中转移1mol电子时,模拟海水理论上除盐58.5g
D.电池工作一段时间后,正、负极产生气体的物质的量之比为2:1
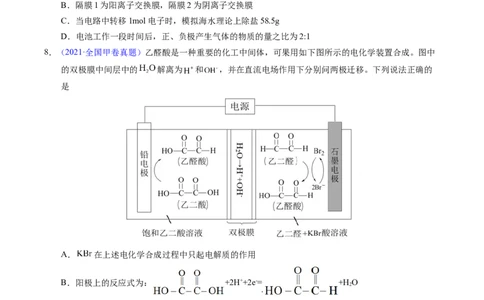
8.(2021·全国甲卷真题)乙醛酸是一种重要的化工中间体,可果用如下图所示的电化学装置合成。图中
的双极膜中间层中的 解离为 和 ,并在直流电场作用下分别问两极迁移。下列说法正确的
是
A. 在上述电化学合成过程中只起电解质的作用
B.阳极上的反应式为: +2H++2e-= +H O
2
C.制得 乙醛酸,理论上外电路中迁移了 电子
D.双极膜中间层中的 在外电场作用下向铅电极方向迁移
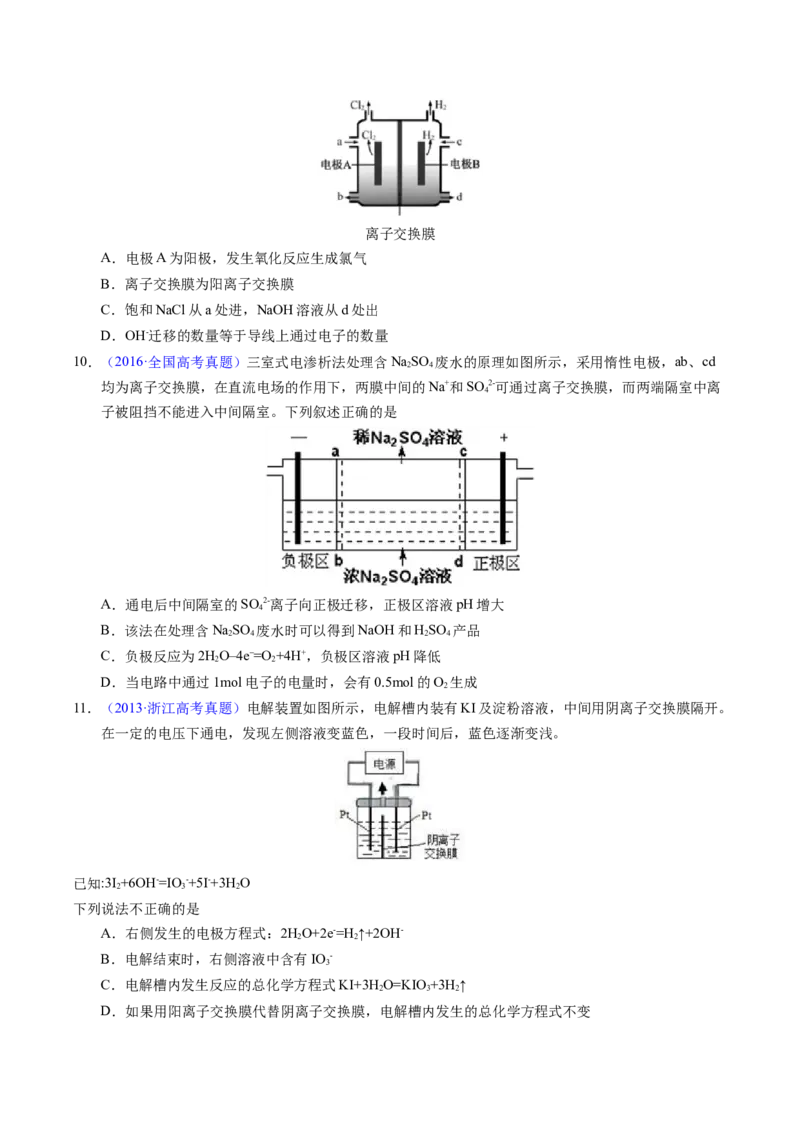
9.(2020·浙江高考真题)在氯碱工业中,离子交换膜法电解饱和食盐水示意图如下,下列说法不正确的
是( )离子交换膜
A.电极A为阳极,发生氧化反应生成氯气
B.离子交换膜为阳离子交换膜
C.饱和NaCl从a处进,NaOH溶液从d处出
D.OH-迁移的数量等于导线上通过电子的数量
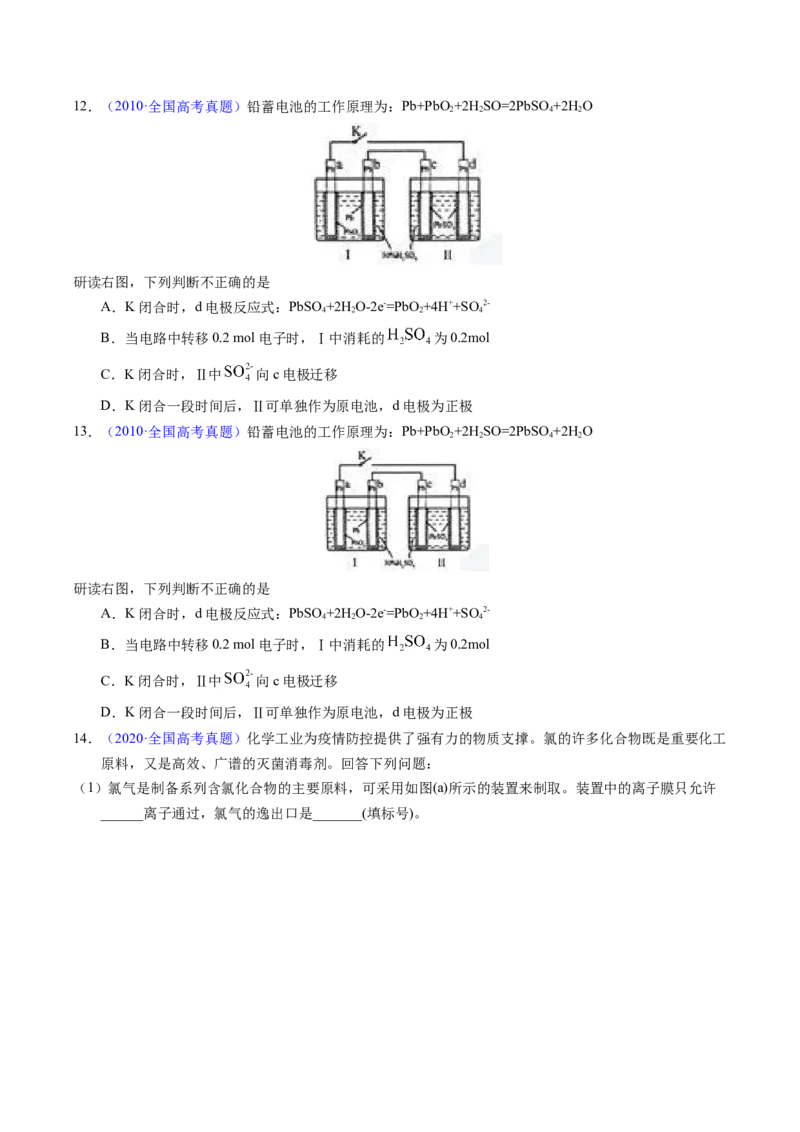
10.(2016·全国高考真题)三室式电渗析法处理含NaSO 废水的原理如图所示,采用惰性电极,ab、cd
2 4
均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO 2-可通过离子交换膜,而两端隔室中离
4
子被阻挡不能进入中间隔室。下列叙述正确的是
A.通电后中间隔室的SO 2-离子向正极迁移,正极区溶液pH增大
4
B.该法在处理含NaSO 废水时可以得到NaOH和HSO 产品
2 4 2 4
C.负极反应为2HO–4e–=O +4H+,负极区溶液pH降低
2 2
D.当电路中通过1mol电子的电量时,会有0.5mol的O 生成
2
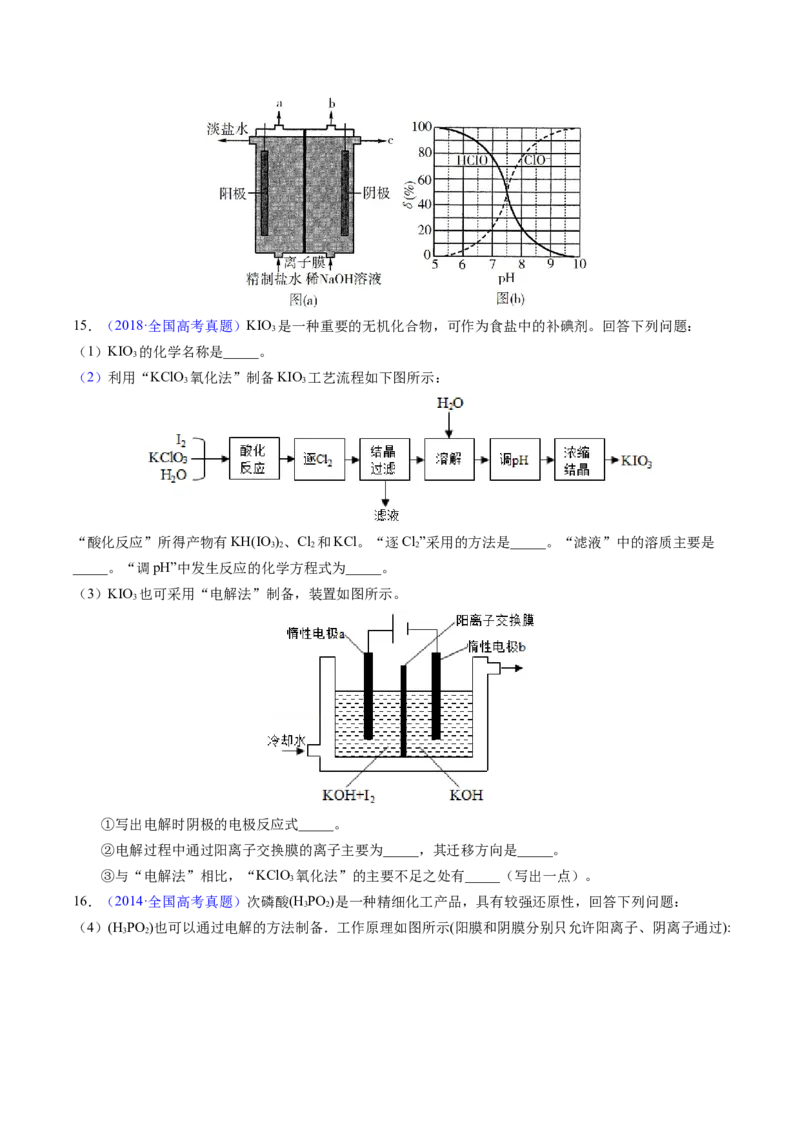
11.(2013·浙江高考真题)电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。
在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。
已知:3I +6OH-=IO -+5I-+3H O
2 3 2
下列说法不正确的是
A.右侧发生的电极方程式:2HO+2e-=H ↑+2OH-
2 2
B.电解结束时,右侧溶液中含有IO -
3
C.电解槽内发生反应的总化学方程式KI+3HO=KIO +3H ↑
2 3 2
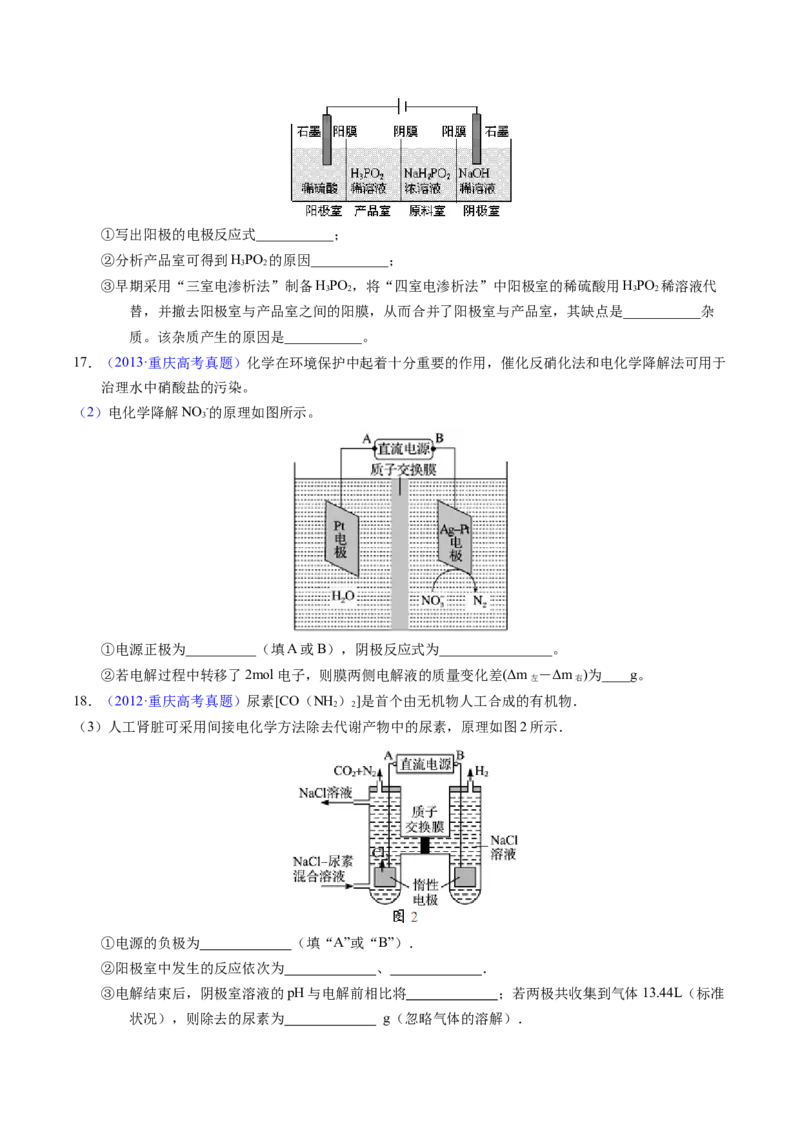
D.如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学方程式不变12.(2010·全国高考真题)铅蓄电池的工作原理为:Pb+PbO+2H SO=2PbSO +2H O
2 2 4 2
研读右图,下列判断不正确的是
A.K闭合时,d电极反应式:PbSO +2H O-2e-=PbO+4H++SO2-
4 2 2 4
B.当电路中转移0.2 mol电子时,Ⅰ中消耗的 为0.2mol
C.K闭合时,Ⅱ中 向c电极迁移
D.K闭合一段时间后,Ⅱ可单独作为原电池,d电极为正极
13.(2010·全国高考真题)铅蓄电池的工作原理为:Pb+PbO+2H SO=2PbSO +2H O
2 2 4 2
研读右图,下列判断不正确的是
A.K闭合时,d电极反应式:PbSO +2H O-2e-=PbO+4H++SO2-
4 2 2 4
B.当电路中转移0.2 mol电子时,Ⅰ中消耗的 为0.2mol
C.K闭合时,Ⅱ中 向c电极迁移
D.K闭合一段时间后,Ⅱ可单独作为原电池,d电极为正极
14.(2020·全国高考真题)化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工
原料,又是高效、广谱的灭菌消毒剂。回答下列问题:
(1)氯气是制备系列含氯化合物的主要原料,可采用如图(a)所示的装置来制取。装置中的离子膜只允许
______离子通过,氯气的逸出口是_______(填标号)。15.(2018·全国高考真题)KIO 是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:
3
(1)KIO 的化学名称是_____。
3
(2)利用“KClO 氧化法”制备KIO 工艺流程如下图所示:
3 3
“酸化反应”所得产物有KH(IO)、Cl 和KCl。“逐Cl”采用的方法是_____。“滤液”中的溶质主要是
3 2 2 2
_____。“调pH”中发生反应的化学方程式为_____。
(3)KIO 也可采用“电解法”制备,装置如图所示。
3
①写出电解时阴极的电极反应式_____。
②电解过程中通过阳离子交换膜的离子主要为_____,其迁移方向是_____。
③与“电解法”相比,“KClO 氧化法”的主要不足之处有_____(写出一点)。
3
16.(2014·全国高考真题)次磷酸(H PO )是一种精细化工产品,具有较强还原性,回答下列问题:
3 2
(4)(H PO )也可以通过电解的方法制备.工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):
3 2①写出阳极的电极反应式___________;
②分析产品室可得到HPO 的原因___________;
3 2
③早期采用“三室电渗析法”制备HPO ,将“四室电渗析法”中阳极室的稀硫酸用HPO 稀溶液代
3 2 3 2
替,并撤去阳极室与产品室之间的阳膜,从而合并了阳极室与产品室,其缺点是___________杂
质。该杂质产生的原因是___________。
17.(2013·重庆高考真题)化学在环境保护中起着十分重要的作用,催化反硝化法和电化学降解法可用于
治理水中硝酸盐的污染。
(2)电化学降解NO -的原理如图所示。
3
①电源正极为__________(填A或B),阴极反应式为________________。
②若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差(Δm -Δm )为____g。
左 右
18.(2012·重庆高考真题)尿素[CO(NH )]是首个由无机物人工合成的有机物.
2 2
(3)人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如图2所示.
①电源的负极为 (填“A”或“B”).
②阳极室中发生的反应依次为 、 .
③电解结束后,阴极室溶液的pH与电解前相比将 ;若两极共收集到气体13.44L(标准
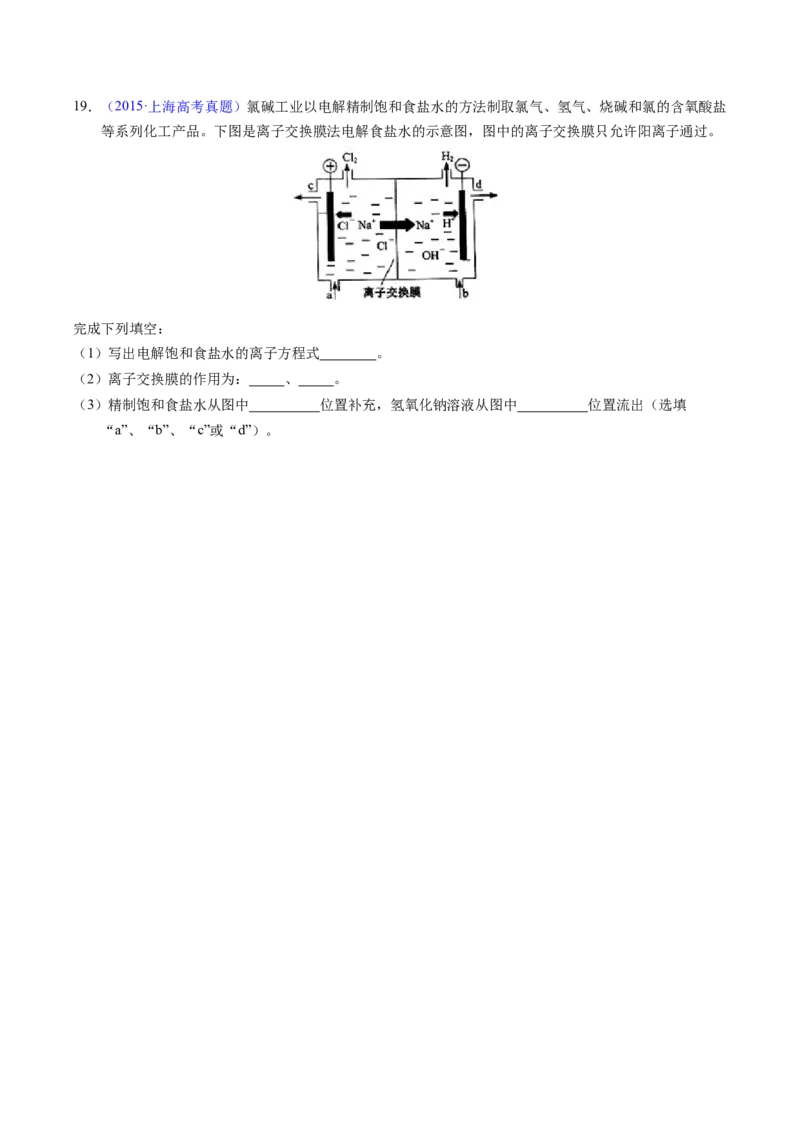
状况),则除去的尿素为 g(忽略气体的溶解).19.(2015·上海高考真题)氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐
等系列化工产品。下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。
完成下列填空:
(1)写出电解饱和食盐水的离子方程式 。
(2)离子交换膜的作用为: 、 。
(3)精制饱和食盐水从图中 位置补充,氢氧化钠溶液从图中 位置流出(选填
“a”、“b”、“c”或“d”)。