文档内容
专题94 工艺流程——结合理论综合
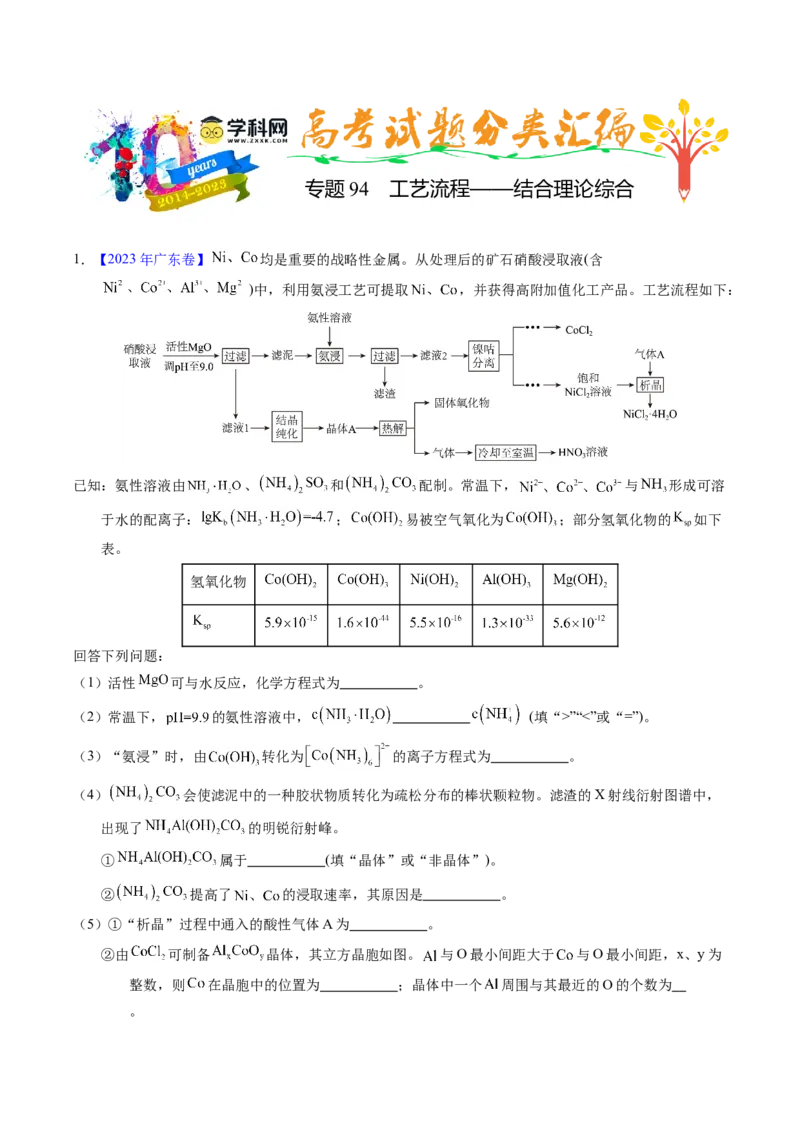
1.【2023年广东卷】 均是重要的战略性金属。从处理后的矿石硝酸浸取液(含
)中,利用氨浸工艺可提取 ,并获得高附加值化工产品。工艺流程如下:
已知:氨性溶液由 、 和 配制。常温下, 与 形成可溶
于水的配离子: ; 易被空气氧化为 ;部分氢氧化物的 如下
表。
氢氧化物
回答下列问题:
(1)活性 可与水反应,化学方程式为 。
(2)常温下, 的氨性溶液中, (填“>”“<”或“=”)。
(3)“氨浸”时,由 转化为 的离子方程式为 。
(4) 会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。滤渣的X射线衍射图谱中,
出现了 的明锐衍射峰。
① 属于 (填“晶体”或“非晶体”)。
② 提高了 的浸取速率,其原因是 。
(5)①“析晶”过程中通入的酸性气体A为 。
②由 可制备 晶体,其立方晶胞如图。 与O最小间距大于 与O最小间距,x、y为
整数,则 在晶胞中的位置为 ;晶体中一个 周围与其最近的O的个数为
。(6)①“结晶纯化”过程中,没有引入新物质。晶体A含6个结晶水,则所得 溶液中 与
的比值,理论上最高为 。
②“热解”对于从矿石提取 工艺的意义,在于可重复利用 和 (填化学式)。
【答案】(1)
(2)>
(3) 或
(4) 晶体 减少胶状物质对镍钴氢氧化物的包裹,增加了滤泥与氨性溶液的接触面积
(5) 体心 12
(6) 0.4或
【解析】硝酸浸取液(含 )中加入活性氧化镁调节溶液pH值,过滤,得到滤液主要
是硝酸镁,结晶纯化得到硝酸镁晶体,再热解得到氧化镁和硝酸。滤泥加入氨性溶液氨浸,过滤,向
滤液中进行镍钴分离,,经过一系列得到氯化铬和饱和氯化镍溶液,向饱和氯化镍溶液中加入氯化氢
气体得到氯化镍晶体。
(1)活性 可与水反应,化学方程式为 ;故答案为: 。
(2)常温下, 的氨性溶液中, , ,
,则 > ;故答案为:>。
(3)“氨浸”时, 与亚硫酸根发生氧化还原反应,再与氨水反应生成 ,则由
转化为 的离子方程式为
或
;故答案为:
或。
(4) 会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。滤渣的X射线衍射图谱中,
出现了 的明锐衍射峰。
①X射线衍射图谱中,出现了 的明锐衍射峰,则 属于晶体;故答案为:
晶体。
②根据题意 会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物,则 能提高
了 的浸取速率,其原因是减少胶状物质对镍钴氢氧化物的包裹,增加了滤泥与氨性溶液的接
触面积;故答案为:减少胶状物质对镍钴氢氧化物的包裹,增加了滤泥与氨性溶液的接触面积。
(5)①“析晶”过程中为了防止 水解,因此通入的酸性气体A为 ;故答案为: 。
②由 可制备 晶体,其立方晶胞如图。x、y为整数,根据图中信息Co、Al都只有一个原子,
而氧(白色)原子有3个, 与O最小间距大于 与O最小间距,则Al在顶点,因此 在晶胞中的
位置为体心;晶体中一个 周围与其最近的O原子,以顶点Al分析,面心的氧原子一个横截面有4
个,三个横截面共12个,因此晶体中一个 周围与其最近的O的个数为12;故答案为:体心;12。
(6)①“结晶纯化”过程中,没有引入新物质。晶体A含6个结晶水,则晶体A为 ,根
据 , ,还剩余5个水分子,因此所得
溶液中 与 的比值理论上最高为 ;故答案为:0.4或 。
②“热解”对于从矿石提取 工艺的意义,根据前面分析 ,
,在于可重复利用 和 ;故答案为: 。
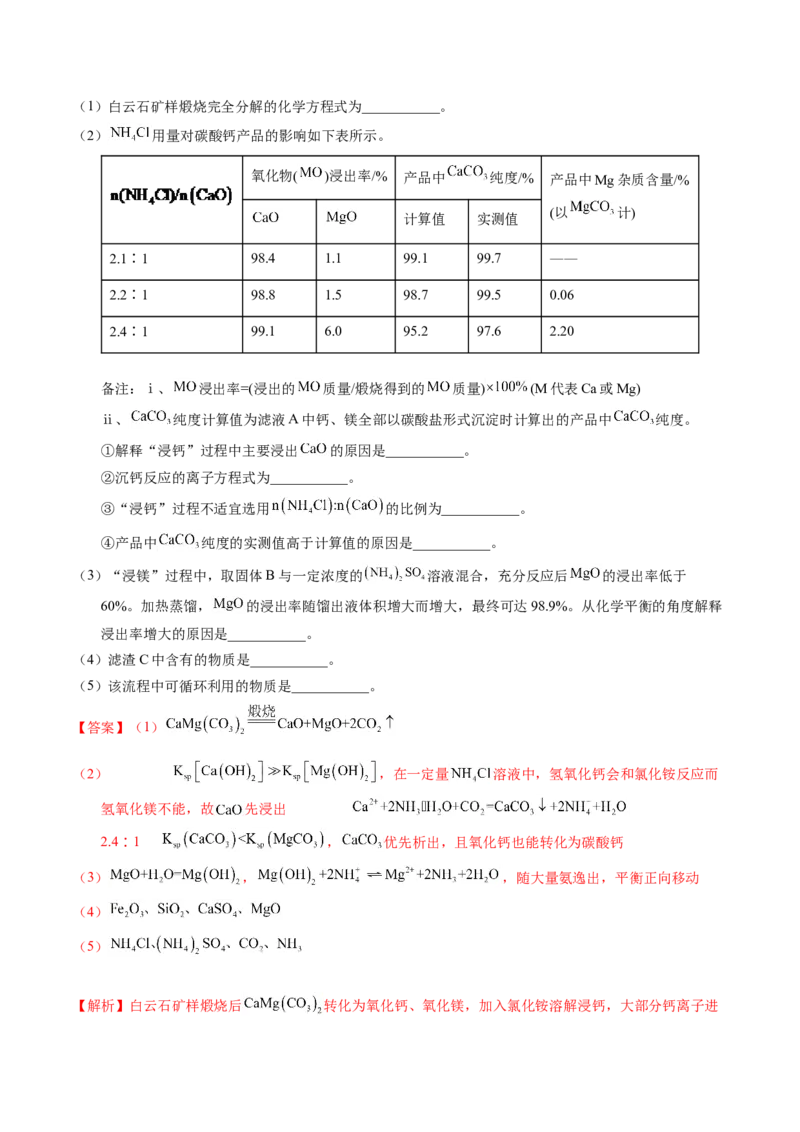
2.【2022年北京卷】白云石的主要化学成分为 ,还含有质量分数约为2.1%的Fe O 和1.0%
2 3
的SiO。利用白云石制备高纯度的碳酸钙和氧化镁,流程示意图如下。
2
已知:
物质(1)白云石矿样煅烧完全分解的化学方程式为___________。
(2) 用量对碳酸钙产品的影响如下表所示。
氧化物( )浸出率/% 产品中 纯度/% 产品中Mg杂质含量/%
(以 计)
计算值 实测值
2.1∶1 98.4 1.1 99.1 99.7 ——
2.2∶1 98.8 1.5 98.7 99.5 0.06
2.4∶1 99.1 6.0 95.2 97.6 2.20
备注:ⅰ、 浸出率=(浸出的 质量/煅烧得到的 质量) (M代表Ca或Mg)
ⅱ、 纯度计算值为滤液A中钙、镁全部以碳酸盐形式沉淀时计算出的产品中 纯度。
①解释“浸钙”过程中主要浸出 的原因是___________。
②沉钙反应的离子方程式为___________。
③“浸钙”过程不适宜选用 的比例为___________。
④产品中 纯度的实测值高于计算值的原因是___________。
(3)“浸镁”过程中,取固体B与一定浓度的 溶液混合,充分反应后 的浸出率低于
60%。加热蒸馏, 的浸出率随馏出液体积增大而增大,最终可达98.9%。从化学平衡的角度解释
浸出率增大的原因是___________。
(4)滤渣C中含有的物质是___________。
(5)该流程中可循环利用的物质是___________。
【答案】(1)
(2) ,在一定量 溶液中,氢氧化钙会和氯化铵反应而
氢氧化镁不能,故 先浸出
2.4∶1 , 优先析出,且氧化钙也能转化为碳酸钙
(3) , ,随大量氨逸出,平衡正向移动
(4)
(5)
【解析】白云石矿样煅烧后 转化为氧化钙、氧化镁,加入氯化铵溶解浸钙,大部分钙离子进入滤液A,通入二氧化碳生成碳酸钙;过滤分离出含有镁、铁、硅元素的固体B,加入硫酸铵将镁离
子转化为硫酸镁溶液,加入碳酸铵生成碳酸镁沉淀,煅烧得到氧化镁;
【解析】(1)白云石矿样煅烧完全分解生成氧化钙、氧化镁、二氧化碳气体,化学方程式为
;
(2)①氯化铵水解生成一水合氨与氢离子,可以调节溶液的pH,由图表可知,
,在一定量 溶液中,氢氧化钙会和氯化铵反应而氢氧化镁不
能,故 首先溶解被浸出;
②沉钙反应中通入二氧化碳和滤液中钙离子、氨气反应生成碳酸钙沉淀和铵根离子,离子方程式为
。
③由图表可知,“浸钙”过程 的比例为2.4∶1时,产品中镁元素杂质最多且碳酸钙纯度
最低,故不适宜选用 的比例为2.4∶1。
④ ,在反应中 会优先析出,但也有可能析出其他沉淀,且Mg2+部分以
Mg(OH) 形成沉淀,相比MgCO 质量更小,二者共同作用导致产品中 纯度的实测值高于计算值;
2 3
(3)“浸镁”过程中,发生反应: , ,加
热蒸馏随大量氨逸出,平衡正向移动,利于氢氧化镁转化为硫酸镁;
(4)白云石的主要化学成分为 ,还含有质量分数约为2.1%的Fe O 和1.0%的SiO;煅烧浸
2 3 2
钙后,绝大部分钙进入滤液中,部分钙进入B中加入硫酸铵后转化为微溶于的硫酸钙,氧化铁、二氧
化硅几乎不反应进入滤渣中;“浸镁”过程中, 的浸出率最终可达98.9% ,则还有部分氧化镁
进入滤渣中,故滤渣C中含有的物质是 ;
(5)沉钙反应中通入二氧化碳生成碳酸钙和氯化铵;“浸镁”过程中加热蒸馏会有大量氨逸出;滤液D
加入碳酸铵生成碳酸镁和硫酸铵,碳酸镁煅烧生成二氧化碳;白云石煅烧也会生成二氧化碳;在流程
中 既是反应物又是生成物,故该流程中可循环利用的物质是
。
3.(2021·福建真题)四钼酸铵是钼深加工的重要中间产品具有广泛的用途。一种以钼精矿(主要含 ,
还有 、 的化合物及 等)为原料制备四钼酸铵的工艺流程如下图所示。回答下列问题:
(1)“焙烧”产生的气体用_______吸收后可制取氮肥。
(2)“浸出”时, 转化为 。提高单位时间内钼浸出率的措施有_______(任写两种)。温度对
内钼浸出率的影响如图所示。当浸出温度超过 后,钼的浸出率反而降低,主要原因是温度
升高使水大量蒸发,导致_______。
(3)“净化”时,浸出液中残留的 、 转化为沉淀除去。研究表明,该溶液中 和pH的关系为:
。为了使溶液中的杂质离子浓度小于 ,应控制溶液的pH不小于
_______。(已知: ; 和 的 分别为35.2和17.2)
(4)“净化”后,溶液中若有低价钼(以 表示),可加入适量 将其氧化为 ,反应的离子方程
式为_______。
(5)“沉淀”时,加入 的目的是_______。
(6)高温下用 还原(NH )MoO 可制得金属钼,反应的化学方程式为_______。(已知:(NH )MoO
4 2 4 13 4 2 4 13
受热分解生成 )
【答案】
(1)氨水
(2) 适当升温、搅拌、增加 用量(增大 浓度)等 晶体析出,混入浸渣
(3)3.9
(4)
(5)提供 ,使 充分转化为沉淀析出
(6)
【解析】钼精矿(主要含 ,还有 、 的化合物及 等)通入氧气焙烧得到 、CuO、Fe O、
2 3
SiO 和SO ,焙烧产生的气体主要为SO ; 、CuO、Fe O、SiO 加NaCO、HO浸出,
2 2 2 2 3 2 2 3 2
转化为 ,铜、铁大多转化为氢氧化物,SiO 不反应,浸渣为SiO、氢氧化铁、氢氧化铜等,浸
2 2出液含 和少量Cu2+、Fe2+,加(NH )S净化,Cu2+、Fe2+转化CuS、FeS沉淀,滤渣为CuS、FeS,
4 2
滤液主要含 ,滤液中加NH NO 、HNO 进行沉淀得到(NH )MoO ·2H O。
4 3 3 4 2 4 13 2
(1)“焙烧”产生的气体为SO ,用氨水吸收后可制取氮肥硫酸铵;
2
(2)“浸出”时,提高单位时间内钼浸出率即提高反应速率,措施有适当升温、搅拌、增加 用量(增
大 浓度)(任写两种);当浸出温度超过 后,钼的浸出率反而降低,主要原因是温度升高使
水大量蒸发,导致 晶体析出,混入浸渣;
(3) 和 的 分别为35.2和17.2,则K (CuS)=10-35.2,K (FeS)=10-17.2,要使Cu2+浓度小于
sp sp
,则S2-浓度大于 mol/L=10-29.2mol/L,要使Fe2+浓度小于 ,则S2-
浓度大于 mol/L=10-11.2mol/L,综述:c(S2-)>10-11.2mol/L,c(S2-)=10-11.2mol/L时,lg(10-
11.2)=pH-15.1,pH=15.1-11.2=3.9,综上所述,为了使溶液中的杂质离子浓度小于 ,应
控制溶液的pH不小于3.9;
(4)溶液中若有低价钼(以 表示),可加入适量 将其氧化为 ,则氧化剂为 ,还原产
物为-2价的O,还原剂为 ,氧化产物为 ,则反应的离子方程式为
;
(5)由流程可知“沉淀”时,产生的沉淀为(NH )MoO ·2H O,因此加入 的目的是提供 ,使
4 2 4 13 2
充分转化为沉淀析出;
(6)高温下用 还原(NH )MoO 可制得金属钼,结合得失电子守恒、原子守恒可知反应的化学方程式
4 2 4 13
为 。
4.(2021·辽宁真题)从钒铬锰矿渣(主要成分为 、 、 )中提铬的一种工艺流程如下:
已知:pH较大时,二价锰[ ](在空气中易被氧化.回答下列问题:
(1)Cr元素位于元素周期表第_______周期_______族。(2)用 溶液制备 胶体的化学方程式为_______。
(3)常温下,各种形态五价钒粒子总浓度的对数[ ]与pH关系如图1。已知钒铬锰矿渣硫酸浸液
中 ,“沉钒”过程控制 ,则与胶体共沉降的五价钒粒子的存在形态为
_______(填化学式)。
(4)某温度下, 、 的沉淀率与pH关系如图2。“沉铬”过程最佳pH为_______;在该条件下
滤液B中 _______ ( 近似为 , 的 近似为 )。
(5)“转化”过程中生成 的离子方程式为_______。
(6)“提纯”过程中 的作用为_______。
【答案】
(1) 4 VIB
(2)FeCl +3H O Fe(OH) (胶体)+3HCl
3 2 3
(3)
(4) 6.0 1×10-6
(5)Mn2++H O+2OH-=MnO+2H O
2 2 2 2
(6)防止pH较大时,二价锰[ ]被空气中氧气氧化,转化为MnO 附在Cr(OH) 的表面,使产物不纯
2 3
【解析】分析本工艺流程图可知,“沉钒”步骤中使用氢氧化铁胶体吸附含有钒的杂质,滤液中主要含有
Mn2+和Cr3+,加热NaOH“沉铬”后,Cr3+转化为固体A为Cr(OH) 沉淀,滤液B中主要含有MnSO ,
3 4
加入NaSO 主要时防止pH较大时,二价锰[ ]被空气中氧气氧化,Cr(OH) 煅烧后生成
2 2 3 3
Cr O,“转化”步骤中的反应离子方程式为:Mn2++H O+2OH-=MnO+2H O,据此分析解题。
2 3 2 2 2 2
(1)Cr是24号元素,价层电子对排布式为:3d54s1,根据最高能层数等于周期序数,价电子数等于族序
数,故Cr元素位于元素周期表第4周期VIB族,故答案为:4;VIB;
(2)用 溶液制备 胶体的化学方程式为FeCl +3H O Fe(OH) (胶体)+3HCl,故答案为:
3 2 3
FeCl +3H O Fe(OH) (胶体)+3HCl;
3 2 3(3)常温下,各种形态五价钒粒子总浓度的对数[ ]与pH关系如图1。已知钒铬锰矿渣硫酸浸液
中 , =-2,从图中可知, “沉钒”过程控制 , =-2时,与胶
体共沉降的五价钒粒子的存在形态为 ,故答案为: ;
(4)某温度下, 、 的沉淀率与pH关系如图2,由图中信息可知“沉铬”过程最佳pH为
6.0;则此时溶液中OH-的浓度为:c(OH-)=10-8mol/L,在该条件下滤液B中 =
=1×10-6 ,故答案为:6.0;1×10-6;
(5)由分析可知,“转化”过程中生成 的离子方程式为Mn2++H O+2OH-=MnO+2H O,故答案为:
2 2 2 2
Mn2++H O+2OH-=MnO+2H O;
2 2 2 2
(6)由分析可知,“提纯”过程中 的作用为防止pH较大时,二价锰[ ]被空气中氧气氧化,
转化为MnO 附在Cr(OH) 的表面,使产物不纯,故答案为:防止pH较大时,二价锰[ ]被空气
2 3
中氧气氧化,转化为MnO 附在Cr(OH) 的表面,使产物不纯。
2 3
5.(2021·全国乙卷真题)磁选后的炼铁高钛炉渣,主要成分有 、 、 、 、 以及
少量的 。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
该工艺条件下,有关金属离子开始沉淀和沉淀完全的 见下表
金属离子
开始沉淀的 2.2 3.5 9.5 12.4
沉淀完全 的 3.2 4.7 11.1 13.8
回答下列问题:
(1)“焙烧”中, 、 几乎不发生反应, 、 、 、 转化为相应的硫酸盐,写出
转化为 的化学方程式_______。(2)“水浸”后“滤液”的 约为2.0,在“分步沉淀”时用氨水逐步调节 至11.6,依次析出的金属离子是
_______。
(3)“母液①"中 浓度为_______ 。
(4)“水浸渣”在160℃“酸溶”最适合的酸是_______。“酸溶渣”的成分是_______、_______。
(5)“酸溶”后,将溶液适当稀释并加热, 水解析出 沉淀,该反应的离子方程式是
_______。
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得_______,循环利用。
【答案】
(1)
(2)
(3)
(4)硫酸
(5)
(6)
【解析】由题给流程可知,高钛炉渣与硫酸铵混合后焙烧时,二氧化钛和二氧化硅不反应,氧化铝、氧化
镁、氧化钙、氧化铁转化为相应的硫酸盐,尾气为氨气;将焙烧后物质加入热水水浸,二氧化钛、二
氧化硅不溶于水,微溶的硫酸钙部分溶于水,硫酸铁、硫酸镁和硫酸铝铵溶于水,过滤得到含有二氧
化钛、二氧化硅、硫酸钙的水浸渣和含有硫酸铁、硫酸镁、硫酸铝铵和硫酸钙的滤液;向pH约为2.0
的滤液中加入氨水至11.6,溶液中铁离子、铝离子和镁离子依次沉淀,过滤得到含有硫酸铵、硫酸钙
的母液①和氢氧化物沉淀;向水浸渣中加入浓硫酸加热到160℃酸溶,二氧化硅和硫酸钙与浓硫酸不
反应,二氧化钛与稀硫酸反应得到TiOSO ,过滤得到含有二氧化硅、硫酸钙的酸溶渣和TiOSO 溶液;
4 4
将TiOSO 溶液加入热水稀释并适当加热,使TiOSO 完全水解生成TiO·x H O沉淀和硫酸,过滤得到
4 4 2 2
含有硫酸的母液②和TiO·x H O。
2 2
(1)氧化铝转化为硫酸铝铵发生的反应为氧化铝、硫酸铵在高温条件下反应生成硫酸铝铵、氨气和水,
反应的化学方程式为Al O+4(NH )SO NH Al(SO )+4NH↑+3H O,故答案为:Al O+4(NH )SO
2 3 4 2 4 4 4 2 3 2 2 3 4 2 4
NH Al(SO )+4NH↑+3H O;
4 4 2 3 2
(2)由题给开始沉淀和完全沉淀的pH可知,将pH约为2.0的滤液加入氨水调节溶液pH为11.6时,铁离
子首先沉淀、然后是铝离子、镁离子,钙离子没有沉淀,故答案为:Fe3+、Al3+、Mg2+;
(3)由镁离子完全沉淀时,溶液pH为11.1可知,氢氧化镁的溶度积为1×10—5×(1×10—2.9)2=1×10—10.8,当
溶液pH为11.6时,溶液中镁离子的浓度为 =1×10—6mol/L,故答案为:1×10—6;
(4)增大溶液中硫酸根离子浓度,有利于使微溶的硫酸钙转化为沉淀,为了使微溶的硫酸钙完全沉淀,
减少TiOSO 溶液中含有硫酸钙的量,应加入浓硫酸加热到160℃酸溶;由分析可知,二氧化硅和硫酸
4钙与浓硫酸不反应,则酸溶渣的主要成分为二氧化硅和硫酸钙,故答案为:硫酸;SiO、CaSO;
2 4
(5)酸溶后将TiOSO 溶液加入热水稀释并适当加热,能使TiOSO 完全水解生成TiO·x H O沉淀和硫酸,
4 4 2 2
反应的离子方程式为TiO2++(x+1)HO TiO·xHO+2H+,故答案为:TiO2++(x+1)HO
2 2 2 2
TiO·xHO+2H+;
2 2
(6)由分析可知,尾气为氨气,母液①为硫酸铵、母液②为硫酸,将母液①和母液②混合后吸收氨气得
到硫酸铵溶液,可以循环使用,故答案为:(NH )SO 。
4 2 4
6.【2022年山东卷】工业上以氟磷灰石[ ,含 等杂质]为原料生产磷酸和石膏,工艺流程
如下:
回答下列问题:
(1)酸解时有 产生。氢氟酸与 反应生成二元强酸 ,离子方程式为_______。
(2)部分盐的溶度积常数见下表。精制Ⅰ中,按物质的量之比 加入 脱氟,
充分反应后, _______ ;再分批加入一定量的 ,首先转化为沉淀的离子是
_______。
(3) 浓度(以 计)在一定范围时,石膏存在形式与温度、 浓度(以 计)的关系如图甲
所示。酸解后,在所得 、 为45的混合体系中,石膏存在形式为_______(填化学式);洗涤
时使用一定浓度的硫酸溶液而不使用水,原因是_______,回收利用洗涤液X的操作单元是_______;
一定温度下,石膏存在形式与溶液中 和 的关系如图乙所示,下列条件能实现酸解所得石
膏结晶转化的是_______(填标号)。A. 、 、 B. 、 、
C. 、 、 D. 、 、
【答案】(1)6HF+SiO =2H++ +2H O
2 2
(2)
(3) CaSO•0.5HO 抑制CaSO 的溶解,提高产品石膏的产率 酸解 AD
4 2 4
【解析】
氟磷灰石用硫酸溶解后过滤,得到粗磷酸和滤渣,滤渣经洗涤后结晶转化为石膏;粗磷酸以精制I脱氟、
除硫酸根离子和 ,过滤,滤液经精制II等一系列操作得到磷酸。
(1)氢氟酸与SiO 反应生成二元强酸HSiF,该反应的离子方程式为6HF+SiO =2H++ +2H O。
2 2 6 2 2
(2)精制1中,按物质的量之比n(Na CO):n( )= 1:1加入NaCO 脱氟,该反应的化学方程式为
2 3 2 3
HSiF+ Na CO= Na SiF↓+CO ↑+ H O,充分反应后得到沉淀NaSiF,溶液中有饱和的NaSiF,且
2 6 2 3 2 6 2 2 2 6 2 6
c(Na+)=2c( ),根据NaSiF 的溶度积可知Ksp= c2(Na+)• c( )=4c3( ),c( ) =
2 6
mol•L-1,因此c(Na+)=2c( )= mol•L-1;同时,粗磷酸中还有硫酸钙的
饱和溶液,c(Ca2+)=c( )= mol•L-1;分批加入一定量的BaCO ,当BaSiF 沉淀
3 6
开始生成时,c(Ba2+)= mol•L-1,当BaSO 沉淀开始生成时,c(Ba2+)=
4
mol•L-1,因此,首先转化为沉淀的离子是 ,然后才是 。
(3)根据图中的坐标信息,酸解后,在所得100℃、PO%为45的混合体系中,石膏存在形式为
2 5
CaSO•0.5HO;CaSO 在硫酸中的溶解度小于在水中的,因此,洗涤时使用一定浓度的硫酸溶液而不
4 2 4
使用水的原因是:减少CaSO 的溶解损失,提高产品石膏的产率;洗涤液X中含有硫酸,其具有回收
4
利用的价值,由于酸解时使用的也是硫酸,因此,回收利用洗涤液X的操作单元是:酸解。由图甲信
息可知,温度越低,越有利于实现酸解所得石膏结晶的转化,由图乙信息可知,体系温度为65℃时,
位于65℃线上方的晶体全部以CaSO•0.5HO形式存在,位于65℃线下方的晶体全部以CaSO•2H O。
4 2 4 2体系温度为80℃时,位于80℃线下方的晶体全部以CaSO•2H O形式存在,位于80℃线上方的晶体全
4 2
部以CaSO•0.5HO形式存在,据此分析:
4 2
A. PO%= l5、SO %= 15,由图乙信息可知,该点坐标位于65℃线以下,晶体以CaSO•2H O形式存在,
2 5 3 4 2
可以实现石膏晶体的转化,A符合题意;
B. PO%= 10、SO %= 20,由图乙信息可知,该点坐标位于80℃线的上方,晶体全部以CaSO•0.5HO
2 5 3 4 2
形式存在,故不能实现晶体的转化, B不符合题意;
C.PO%= 10、SO %= 30,由图乙信息可知,该点坐标位于65℃线上方,晶体全部以CaSO•0.5HO形式
2 5 3 4 2
存在,故不能实现晶体转化, C不符合题意;
D. PO%=10、SO %= 10,由图乙信息可知,该点坐标位于80℃线下方,晶体全部以CaSO•2H O形式
2 5 3 4 2
存在,故能实现晶体的完全转化,D符合题意;
综上所述,能实现酸解所得石膏结晶转化的是AD。
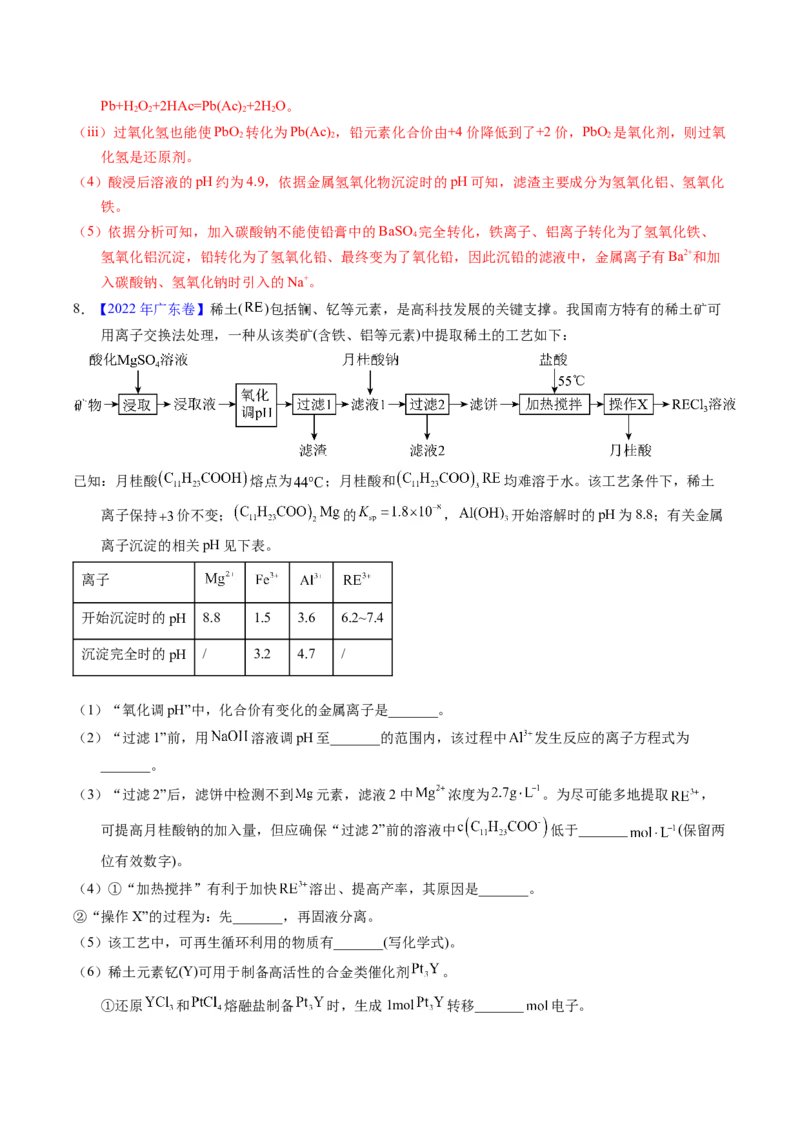
7.【2022年全国乙卷】废旧铅蓄电池的铅膏中主要含有 、 、 和Pb。还有少量BA.Fe、
Al的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实现铅的回收。
一些难溶电解质的溶度积常数如下表:
难溶电解质
一定条件下,一些金属氢氧化物沉淀时的 如下表:
金属氢氧化物
开始沉淀的pH 2.3 6.8 3.5 7.2
完全沉淀的pH 3.2 8.3 4.6 9.1
回答下列问题:
(1)在“脱硫”中 转化反应的离子方程式为________,用沉淀溶解平衡原理解释选择 的原
因________。
(2)在“脱硫”中,加入 不能使铅膏中 完全转化,原因是________。
(3)在“酸浸”中,除加入醋酸( ),还要加入 。(ⅰ)能被 氧化的离子是________;
(ⅱ) 促进了金属Pb在醋酸中转化为 ,其化学方程式为________;
(ⅲ) 也能使 转化为 , 的作用是________。
(4)“酸浸”后溶液的pH约为4.9,滤渣的主要成分是________。
(5)“沉铅”的滤液中,金属离子有________。
【答案】(1) PbSO (s)+CO (aq)= PbCO (s)+SO (aq) 反应PbSO (s)+CO (aq)= PbCO (s)+SO
4 3 4 3
(aq)的平衡常数K= =3.4 105>105,PbSO 可以比较彻底的转化为PbCO
4 3
(2)反应BaSO(s)+CO (aq)= BaCO (s)+SO (aq)的平衡常数K= =0.04<<105,反应正向进行的程
4 3
度有限
(3) Fe2+ Pb+HO+2HAc=Pb(Ac) +2H O 作还原剂
2 2 2 2
(4)Fe(OH) 、Al(OH)
3 3
(5)Ba2+、Na+
【解析】铅膏中主要含有PbSO 、PbO 、PbO和Pb,还有少量BA.Fe、Al的盐或氧化物等,向铅膏中加
4 2
入碳酸钠溶液进行脱硫,硫酸铅转化为碳酸铅,过滤,向所得固体中加入醋酸、过氧化氢进行酸浸,
过氧化氢可将溶液中的亚铁离子氧化为铁离子,酸浸后溶液的pH约为4.9,依据金属氢氧化物沉淀时
的pH可知,滤渣主要成分为氢氧化铝、氢氧化铁,过滤后,向滤液中加入氢氧化钠溶液进行沉铅,
得到氢氧化铅沉淀,滤液中的金属阳离子主要为钠离子和钡离子,氢氧化铅再进行处理得到PbO。
(1)“脱硫”中,碳酸钠溶液与硫酸铅反应生成碳酸铅和硫酸钠,反应的离子方程式为:PbSO (s)+CO
4
(aq)= PbCO (s)+SO (aq),由一些难溶电解质的溶度积常数的数据可知,K (PbCO )=7.4 10-14,
3 sp 3
K (PbSO )=2.5 10-8,反应PbSO (s)+CO (aq)= PbCO (s)+SO (aq)的平衡常数K= =
sp 4 4 3
= = ≈3.4 105>105,说明可以转化的比较彻底,且转化后生成的
碳酸铅可由酸浸进入溶液中,减少铅的损失。
(2)反应BaSO(s)+CO (aq)= BaCO (s)+SO (aq)的平衡常数K= = = =
4 3
≈0.04<<105,说明该反应正向进行的程度有限,因此加入碳酸钠不能使铅膏中的BaSO 完全
4
转化。
(3)(i)过氧化氢有氧化性,亚铁离子有还原性,会被过氧化氢氧化为铁离子。
(ii)过氧化氢促进金属Pb在醋酸溶液中转化为Pb(Ac) ,过氧化氢与PB.HAc发生氧还原反应生成
2
Pb(Ac) 和HO,依据得失电子守恒和原子守恒可知,反应的化学方程式为:
2 2Pb+HO+2HAc=Pb(Ac) +2H O。
2 2 2 2
(iii)过氧化氢也能使PbO 转化为Pb(Ac) ,铅元素化合价由+4价降低到了+2价,PbO 是氧化剂,则过氧
2 2 2
化氢是还原剂。
(4)酸浸后溶液的pH约为4.9,依据金属氢氧化物沉淀时的pH可知,滤渣主要成分为氢氧化铝、氢氧化
铁。
(5)依据分析可知,加入碳酸钠不能使铅膏中的BaSO 完全转化,铁离子、铝离子转化为了氢氧化铁、
4
氢氧化铝沉淀,铅转化为了氢氧化铅、最终变为了氧化铅,因此沉铅的滤液中,金属离子有Ba2+和加
入碳酸钠、氢氧化钠时引入的Na+。
8.【2022年广东卷】稀土( )包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿可
用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下:
已知:月桂酸 熔点为 ;月桂酸和 均难溶于水。该工艺条件下,稀土
离子保持 价不变; 的 , 开始溶解时的pH为8.8;有关金属
离子沉淀的相关pH见下表。
离子
开始沉淀时的pH 8.8 1.5 3.6 6.2~7.4
沉淀完全时的pH / 3.2 4.7 /
(1)“氧化调pH”中,化合价有变化的金属离子是_______。
(2)“过滤1”前,用 溶液调pH至_______的范围内,该过程中 发生反应的离子方程式为
_______。
(3)“过滤2”后,滤饼中检测不到 元素,滤液2中 浓度为 。为尽可能多地提取 ,
可提高月桂酸钠的加入量,但应确保“过滤2”前的溶液中 低于_______ (保留两
位有效数字)。
(4)①“加热搅拌”有利于加快 溶出、提高产率,其原因是_______。
②“操作X”的过程为:先_______,再固液分离。
(5)该工艺中,可再生循环利用的物质有_______(写化学式)。
(6)稀土元素钇(Y)可用于制备高活性的合金类催化剂 。
①还原 和 熔融盐制备 时,生成1mol 转移_______ 电子。② 用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化 的还原,发生的电极反应为
_______。
【答案】(1)Fe2+
(2) 4.7 pH<6.2
(3)4.0 10-4
(4) 加热搅拌可加快反应速率 冷却结晶
(5)MgSO
4
(6) 15 O+4e-+2H O=4OH-
2 2
【解析】由流程可知,该类矿(含铁、铝等元素)加入酸化MgSO 溶液浸取,得到浸取液中含有 、
4
、 、 、 、 等离子,经氧化调pH使 、 形成沉淀,经过滤除去,滤液1
中含有 、 、 等离子,加入月桂酸钠,使 形成 沉淀,滤液2主要
含有MgSO 溶液,可循环利用,滤饼加盐酸,经加热搅拌溶解后,再冷却结晶,析出月桂酸,再固液
4
分离得到RECl 溶液。
3
(1)由分析可知,“氧化调pH”目的是除去含铁、铝等元素的离子,需要将Fe2+氧化为Fe3+,以便后续除
杂,所以化合价有变化的金属离子是Fe2+,故答案为:Fe2+;
(2)由表中数据可知, 沉淀完全的pH为4.7,而 开始沉淀的pH为6.2~7.4,所以为保证 、
沉淀完全,且 不沉淀,要用 溶液调pH至4.7 pH<6.2的范围内,该过程中 发生反
应的离子方程式为 ,故答案为:4.7 pH<6.2; ;
(3)滤液2中 浓度为 ,即0.1125mol/L,根据
,若要加入月桂酸钠后只生成 ,而
不产生 ,则 = =4.0 10-4
,故答案为:4.0 10-4;
(4)①“加热搅拌”有利于加快 溶出、提高产率,其原因是加热搅拌可加快反应速率,故答案为:
加热搅拌可加快反应速率;
② “操作X”的结果是分离出月桂酸,由信息可知,月桂酸 熔点为 ,故“操作X”的过
程为:先冷却结晶,再固液分离,故答案为:冷却结晶;
(5)由分析可知,该工艺中,可再生循环利用的物质有MgSO ,故答案为:MgSO ;
4 4
(6)① 中Y为+3价, 中Pt为+4价,而 中金属均为0价,所以还原 和 熔融盐制
备 时,生成1mol 转移15 电子,故答案为:15;
②碱性溶液中,氢氧燃料电池正极发生还原反应,发生的电极反应为O+4e-+2H O=4OH,故答案为:
2 2
O+4e-+2H O=4OH-。
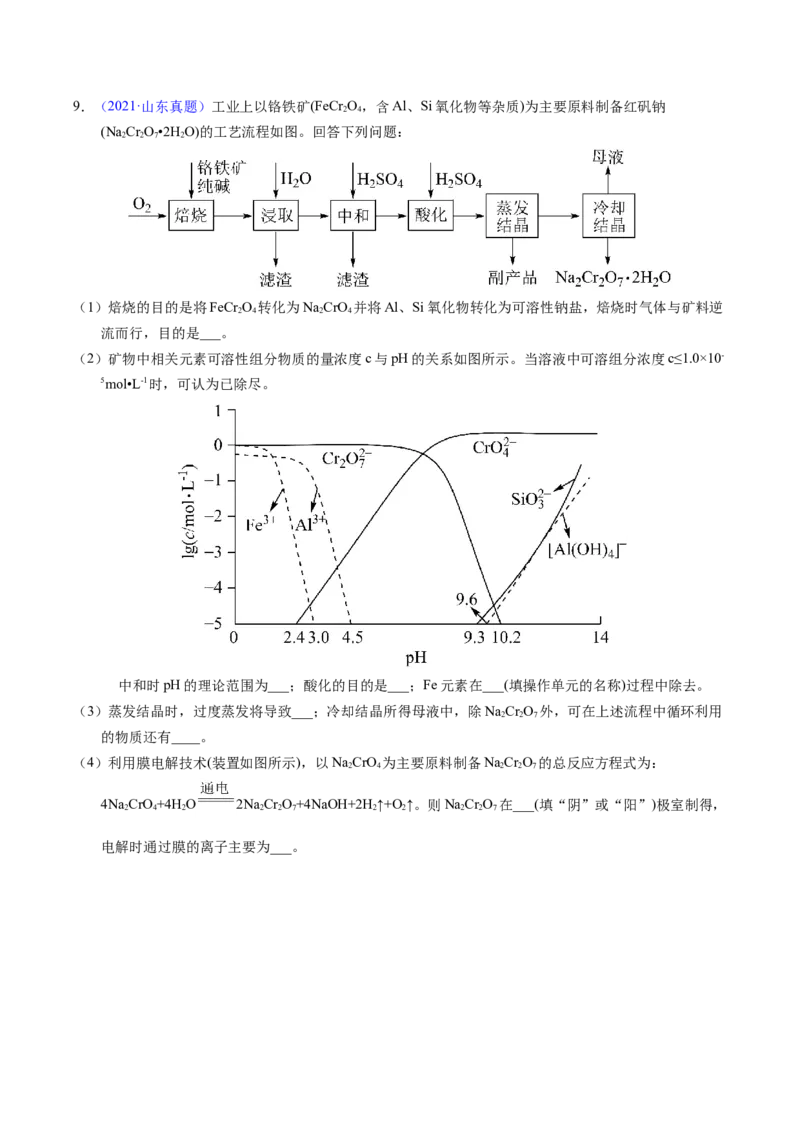
2 29.(2021·山东真题)工业上以铬铁矿(FeCr O,含Al、Si氧化物等杂质)为主要原料制备红矾钠
2 4
(NaCr O•2HO)的工艺流程如图。回答下列问题:
2 2 7 2
(1)焙烧的目的是将FeCr O 转化为NaCrO 并将Al、Si氧化物转化为可溶性钠盐,焙烧时气体与矿料逆
2 4 2 4
流而行,目的是___。
(2)矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图所示。当溶液中可溶组分浓度c≤1.0×10-
5mol•L-1时,可认为已除尽。
中和时pH的理论范围为___;酸化的目的是___;Fe元素在___(填操作单元的名称)过程中除去。
(3)蒸发结晶时,过度蒸发将导致___;冷却结晶所得母液中,除NaCr O 外,可在上述流程中循环利用
2 2 7
的物质还有____。
(4)利用膜电解技术(装置如图所示),以NaCrO 为主要原料制备NaCr O 的总反应方程式为:
2 4 2 2 7
4NaCrO+4HO 2NaCr O+4NaOH+2H↑+O↑。则NaCr O 在___(填“阴”或“阳”)极室制得,
2 4 2 2 2 7 2 2 2 2 7
电解时通过膜的离子主要为___。【答案】
(1)增大反应物接触面积,提高化学反应速率
(2) 使 平衡正向移动,提高NaCr O 的产率 浸取
2 2 7
(3)所得溶液中含有大量NaSO •10HO HSO
2 4 2 2 4
(4)阳 Na+
【解析】以铬铁矿(FeCr O,含Al、Si氧化物等杂质)为主要原料制备红矾钠(NaCr O•2HO)过程中,向铬
2 4 2 2 7 2
铁矿中加入纯碱和O 进行焙烧,FeCr O 转化为NaCrO,Fe(II)被O 氧化成Fe O,Al、Si氧化物转
2 2 4 2 4 2 2 3
化为NaAlO 、NaSiO,加入水进行“浸取”,Fe O 不溶于水,过滤后向溶液中加入HSO 调节溶液
2 2 3 2 3 2 4
pH使 、 转化为沉淀过滤除去,再向滤液中加入HSO ,将NaCrO 转化为NaCr O,将溶
2 4 2 4 2 2 7
液蒸发结晶将NaSO 除去,所得溶液冷却结晶得到NaCr O•2HO晶体,母液中还含有大量HSO 。
2 4 2 2 7 2 2 4
据此解答。
(1)焙烧时气体与矿料逆流而行,目的是利用热量使O 向上流动,增大固体与气体的接触面积,提高化
2
学反应速率,故答案为:增大反应物接触面积,提高化学反应速率。
(2)中和时调节溶液pH目的是将 、 转化为沉淀过滤除去,由图可知,当溶液pH≥4.5时,
Al3+除尽,当溶液pH>9.3时,HSiO 会再溶解生成 ,因此中和时pH的理论范围为
2 3
;将Al元素和Si元素除去后,溶液中Cr元素主要以 和 存在,溶液中存在平
衡: ,降低溶液pH,平衡正向移动,可提高NaCr O 的产率;由上
2 2 7
述分析可知,Fe元素在“浸取”操作中除去,故答案为: ;使
平衡正向移动,提高NaCr O 的产率;浸取。
2 2 7
(3)蒸发结晶时,NaSO 主要以NaSO •10HO存在,NaSO •10HO的溶解度随温度升高先增大后减小,
2 4 2 4 2 2 4 2
若蒸发结晶时,过度蒸发将导致所得溶液中含有大量NaSO •10HO;由上述分析可知,流程中循环利
2 4 2
用的物质除NaCr O 外,还有HSO ,故答案为:所得溶液中含有大量NaSO •10HO;HSO 。
2 2 7 2 4 2 4 2 2 4
(4)由4NaCrO+4HO 2NaCr O+4NaOH+2H↑+O↑可知,电解过程中实质是电解水,阳极上
2 4 2 2 2 7 2 2
水失去电子生成H+和O,阴极上H+得到电子生成H,由 可知,
2 2在氢离子浓度较大的电极室中制得,即NaCr O 在阳极室产生;电解过程中,阴极产生氢氧根
2 2 7
离子,氢氧化钠在阴极生成,所以为提高制备NaCr O 的效率,Na+通过离子交换膜移向阴极,故答
2 2 7
案为:阳;Na+。
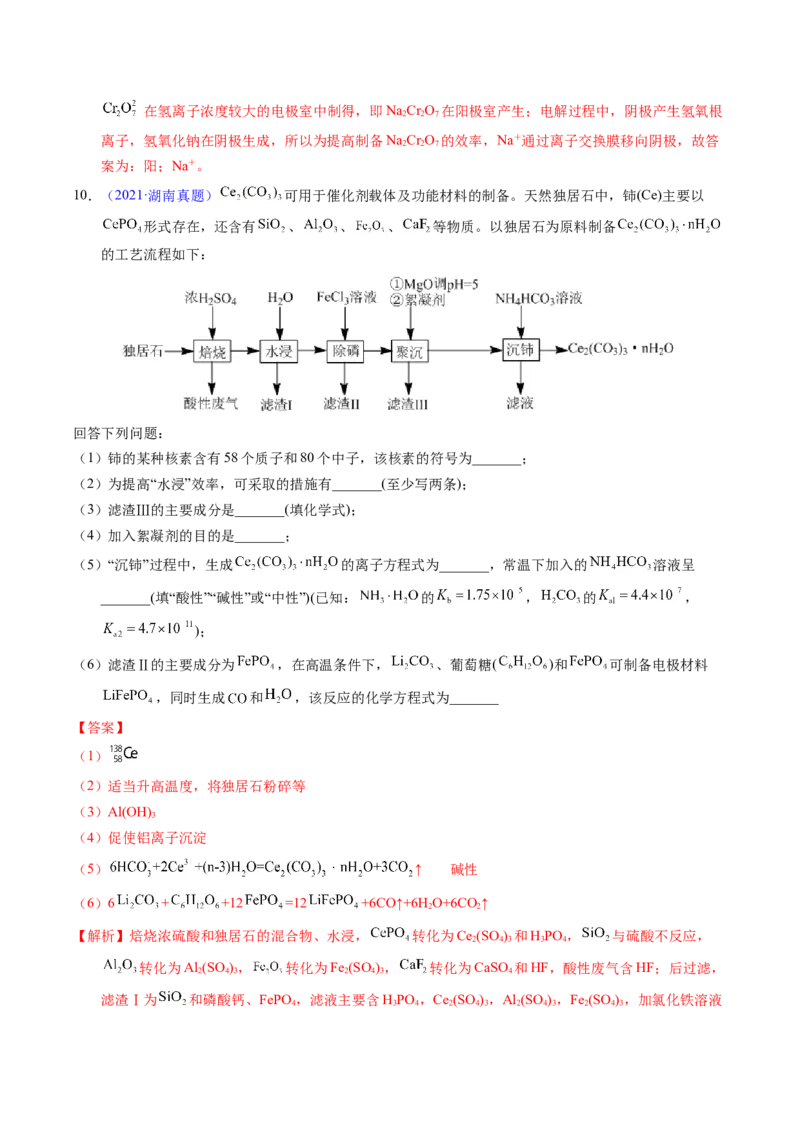
10.(2021·湖南真题) 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以
形式存在,还含有 、 、 、 等物质。以独居石为原料制备
的工艺流程如下:
回答下列问题:
(1)铈的某种核素含有58个质子和80个中子,该核素的符号为_______;
(2)为提高“水浸”效率,可采取的措施有_______(至少写两条);
(3)滤渣Ⅲ的主要成分是_______(填化学式);
(4)加入絮凝剂的目的是_______;
(5)“沉铈”过程中,生成 的离子方程式为_______,常温下加入的 溶液呈
_______(填“酸性”“碱性”或“中性”)(已知: 的 , 的 ,
);
(6)滤渣Ⅱ的主要成分为 ,在高温条件下, 、葡萄糖( )和 可制备电极材料
,同时生成 和 ,该反应的化学方程式为_______
【答案】
(1)
(2)适当升高温度,将独居石粉碎等
(3)Al(OH)
3
(4)促使铝离子沉淀
(5) ↑ 碱性
(6)6 + +12 =12 +6CO↑+6H O+6CO↑
2 2
【解析】焙烧浓硫酸和独居石的混合物、水浸, 转化为Ce (SO ) 和HPO , 与硫酸不反应,
2 4 3 3 4
转化为Al (SO ), 转化为Fe (SO ), 转化为CaSO 和HF,酸性废气含HF;后过滤,
2 4 3 2 4 3 4
滤渣Ⅰ为 和磷酸钙、FePO ,滤液主要含HPO ,Ce (SO ),Al (SO ),Fe (SO ),加氯化铁溶液
4 3 4 2 4 3 2 4 3 2 4 3除磷,滤渣Ⅱ为FePO ;聚沉将铁离子、铝离子转化为沉淀,过滤除去,滤渣Ⅲ主要为氢氧化铝,还
4
含氢氧化铁;加碳酸氢铵沉铈得Ce (CO)·nH O。
2 3 3 2
(1)铈的某种核素含有58个质子和80个中子,则质量数为58+80=138,该核素的符号为 ;
(2)为提高“水浸”效率,可采取的措施有适当升高温度,将独居石粉碎等;
(3)结合流程可知,滤渣Ⅲ的主要成分是Al(OH) ;
3
(4)加入絮凝剂的目的是促使铝离子沉淀;
(5)用碳酸氢铵“沉铈”,则结合原子守恒、电荷守恒可知生成 的离子方程式为
↑;铵根离子的水解常数K( )=
h
≈5.7×10-10,碳酸氢根的水解常数K( )== ≈2.3×10-8,则K( )