文档内容
山大附中高三年级开学摸底测试
化学试题
8.21
注意事项:
1.答题前,考生先将自己的姓名、考生号、座号填写在相应位置,认真核对条形码
上的姓名、考生号和座号,并将条形码粘贴在指定位置上。
2.选择题答案必须使用2B铅笔(按填涂样例)正确填涂;非选择题答案必须使用
0.5毫米黑色签字笔书写,字体工整、笔迹清楚。
3.请按照题号在各题目的答题区域内作答,超出答题区域书写的答案无效;在草
稿纸、试题卷上答题无效.保持卡面清洁,不折叠、不破损。
可能用到的相对原子质量:
H 1 C 12 N 14 O 16 Na 23 Ag108 S 32 Cl35.5 Cr 52 Zn 65
一、选择题:每小题 2 分,共 30分。每小题只有一个选项符合题意。
1.化学与生活密切相关,下列说法正确的是( )
A.苯甲酸钠可作为食品防腐剂是由于其具有酸性
B.豆浆能产生丁达尔效应是由于胶体粒子对光线的散射
C.SO 可用于丝织品漂白是由于其能氧化丝织品中有色成分
2
D.维生素C可用作水果罐头的抗氧化剂是由于其难以被氧化
2. 下列说法错误的是
A. 容量瓶使用前需用蒸馏水洗净并烘干
B. 蒸馏开始时应先通冷凝水再加热
C. 滴瓶中的滴管用后不必清洗,直接放到滴瓶中
D. 酸式滴定管查漏时发现轻微漏水,可涂抹少量凡士林
3.N 为阿伏加德罗常数的值。下列叙述正确的是( )
A
A.0.50mol异丁烷分子中共价键的数目为6.5N
A
B.标准状况下,2.24LSO 中电子的数目为4.00N
3 A
C.1.0LpH 2的H SO 溶液中H的数目为0.02N
2 4 A
D. 1.0L1.0molL1 的 Na CO 溶液中 CO2 的数目为 1.0N
2 3 3 A
化学试题第 1页 共8页
{#{QQABYYSUggCgQBBAABgCQQWiCgOQkBAACKgGAAAIIAAACBNABAA=}#}4. 光学性能优良的高分子材料聚碳酸异山梨醇酯可由如下反应制备。
下列说法错误的是
A. 该高分子材料可降解 B. 异山梨醇分子中有3个手性碳
C. 反应式中化合物X为甲醇 D. 该聚合反应为缩聚反应
5.X、Y为第二周期相邻的两种元素,X的最高正价与最低负价代数和为 2,二者形
成的固态化合物以
XY
+
XY
-的形式存在,下列说法错误的是
2 3
A. 原子半径:X>Y B. X、Y 均属于p区元素
C. X、Y的第一电离能:XSi—Si、C—H>Si—H,因此 C H 稳定性大于 Si H
2 6 2 6
B.立方型SiC是与金刚石成键、结构均相似的共价晶体,因此具有很高的硬度
C.SiH 中Si的化合价为+4,CH 中C的化合价为-4,因此SiH 还原性小于CH
4 4 4 4
D.Si 原子间难形成双键而 C 原子间可以,是因为 Si 的原子半径大于 C,难形成
p-p π键
化学试题第 2页 共8页
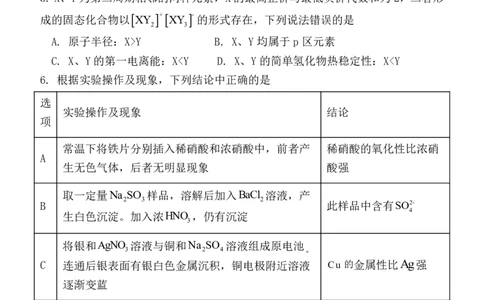
{#{QQABYYSUggCgQBBAABgCQQWiCgOQkBAACKgGAAAIIAAACBNABAA=}#}8. 从中草药中提取的calebinA(结构简式如下)可用于治疗阿尔茨海默症。下列关
于calebin A的说法错误的是( )
A.可与FeCl 溶液发生显色反应
3
B.其酸性水解的产物均可与NaCO 溶液反应
2 3
C.苯环上氢原子发生氯代时,一氯代物有 6 种
D.1 mol该分子最多与8 mol H 发生加成反应
2
9. 某工业食盐样品中混有NaBr杂质,现对其进行提纯,并获取液态溴,可设计实
验流程如图所示:下列说法错误的是
A. 依据实验流程可知,操作Ⅰ为萃取、分液,可选取CCl 作为萃取剂
4
B. 由液体D中获取液溴时采用蒸馏操作,所用温度计的水银球应插入液面以下
C. 在进行操作Ⅱ时,需要的主要仪器有铁架台(带铁圈)、酒精灯、蒸发皿、玻璃
棒、坩埚钳
D. 若样品为44.0g,最终获得42.1g氯化钠固体,则原固体混合物中氯化钠的质量
分数约为90%
10. 三氟化氮(NF)和六氟化硫(SF)都是微电子工业中的优良蚀刻剂,随着纳米技
3 6
术及电子工业的发展,它们的需求量日益增加。下列说法正确的是
A. NF 和SF 都是含有极性键的非极性分子
3 6
B. 六氟化硫分子的空间构型为平面正六边形
C. 三氟化氮的沸点高于三氟化磷
D. 三氟化氮和甲烷中的N、C杂化方式相同
二、选择题:本题共5 小题,每小题 4 分,共 20 分。在每小题给出的四个选项中,
有一个或两个选项符合题目要求,全部选对的得 4分,选对但不全的得 2 分,有选
错的得 0分。
11. 利用热再生氨电池可实现CuSO 电镀废液的浓
4
缩再生。电池装置如图所示,甲、乙两室均预加相同
的CuSO 电镀废液,向甲室加入足量氨水后电池开始
4
工作。下列说法正确的是( )
A. 甲室Cu电极为正极
化学试题第 3页 共8页
{#{QQABYYSUggCgQBBAABgCQQWiCgOQkBAACKgGAAAIIAAACBNABAA=}#}B. 隔膜为阳离子膜
C. 电池总反应为:Cu2 4NH Cu NH 2
3 3 4
D. NH 扩散到乙室将对电池电动势产生影响
3
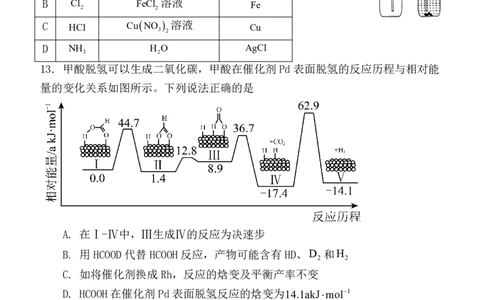
12、某同学按图示装置进行实验,欲使瓶中少量固体粉末最终消失并得到澄清溶液。
下列物质组合不符合要求的是( )
气体 液体 固体粉末
A CO 饱和 Na CO 溶液 CaCO
2 2 3 3
B Cl FeCl 溶液 Fe
2 2
C
HCl
CuNO 溶液
Cu
3 2
D NH H O AgCl
3 2
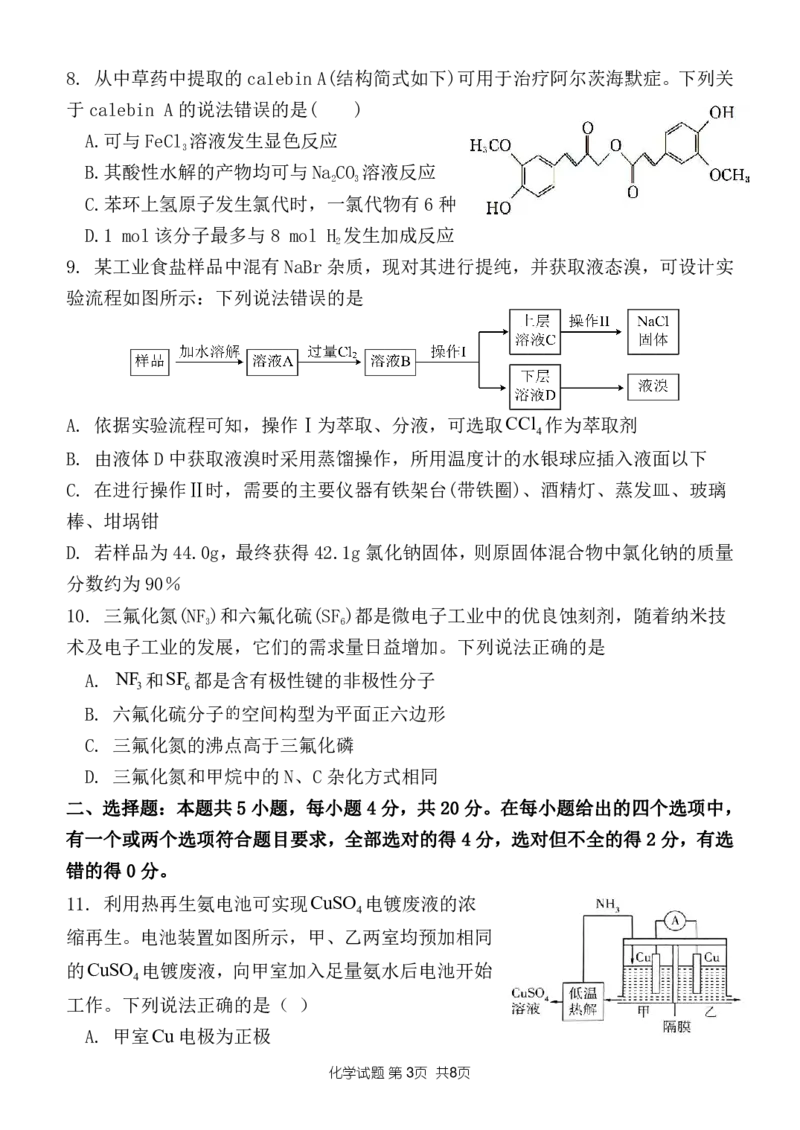
13. 甲酸脱氢可以生成二氧化碳,甲酸在催化剂Pd表面脱氢的反应历程与相对能
量的变化关系如图所示。下列说法正确的是
A. 在Ⅰ-Ⅳ中,Ⅲ生成Ⅳ的反应为决速步
B. 用HCOOD代替HCOOH反应,产物可能含有HD、D 和H
2 2
C. 如将催化剂换成Rh,反应的焓变及平衡产率不变
D. HCOOH在催化剂Pd表面脱氢反应的焓变为14.1akJmol1
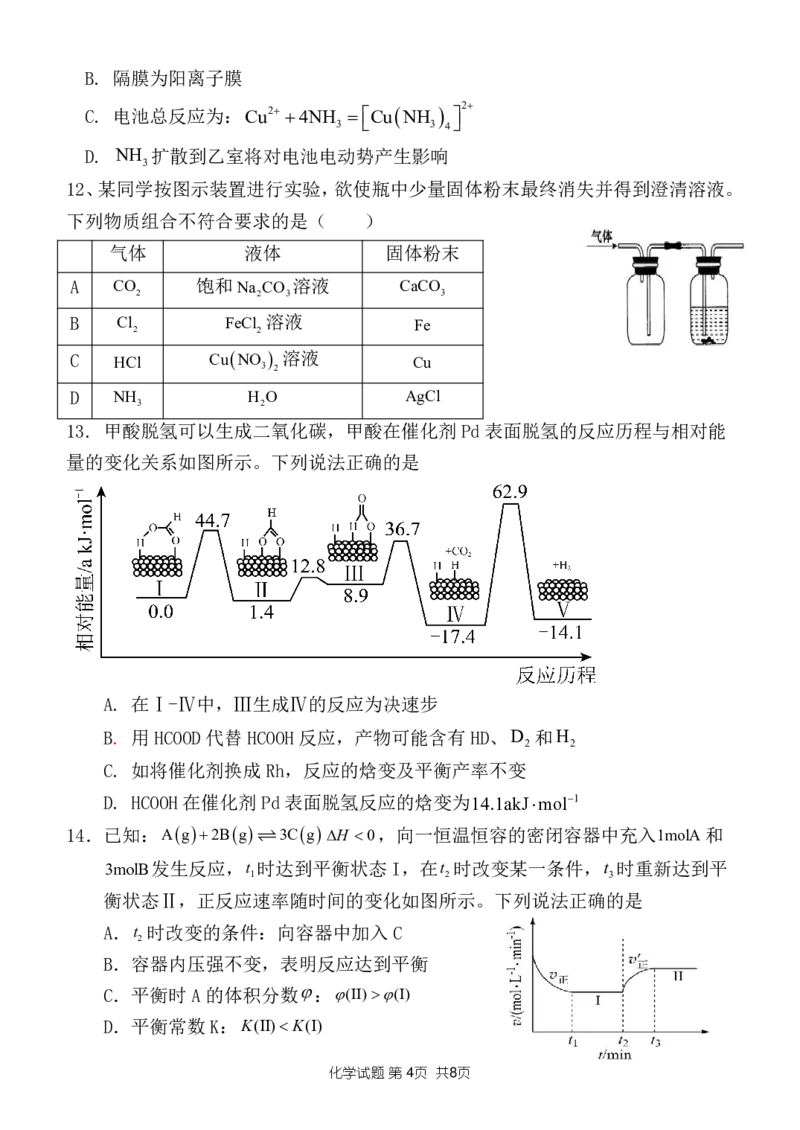
14.已知:Ag2Bg 3Cg H 0,向一恒温恒容的密闭容器中充入1molA和
3molB发生反应,t 时达到平衡状态I,在t 时改变某一条件,t 时重新达到平
1 2 3
衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
A.t 时改变的条件:向容器中加入C
2
B.容器内压强不变,表明反应达到平衡
C.平衡时A的体积分数:(II)(I)
D.平衡常数K:K(II)K(I)
化学试题第 4页 共8页
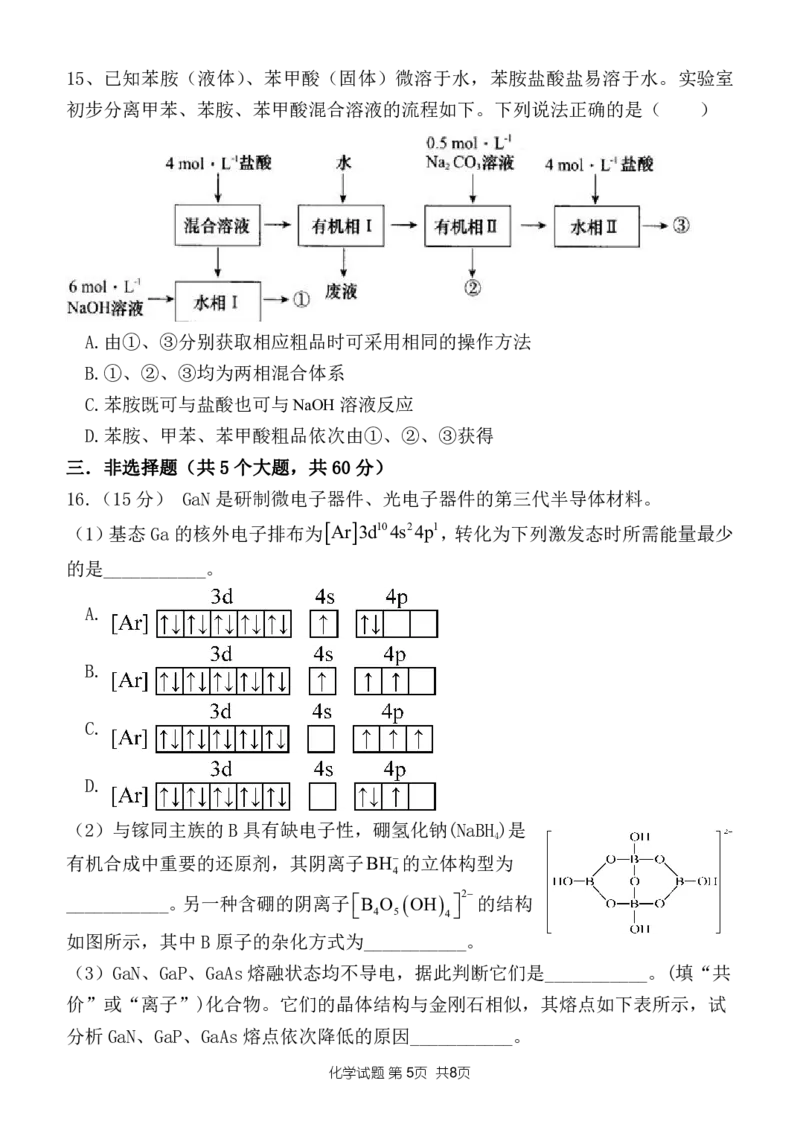
{#{QQABYYSUggCgQBBAABgCQQWiCgOQkBAACKgGAAAIIAAACBNABAA=}#}15、已知苯胺(液体)、苯甲酸(固体)微溶于水,苯胺盐酸盐易溶于水。实验室
初步分离甲苯、苯胺、苯甲酸混合溶液的流程如下。下列说法正确的是( )
A.由①、③分别获取相应粗品时可采用相同的操作方法
B.①、②、③均为两相混合体系
C.苯胺既可与盐酸也可与NaOH溶液反应
D.苯胺、甲苯、苯甲酸粗品依次由①、②、③获得
三.非选择题(共 5 个大题,共 60分)
16.(15分) GaN是研制微电子器件、光电子器件的第三代半导体材料。
(1)基态Ga的核外电子排布为 Ar 3d104s24p1,转化为下列激发态时所需能量最少
的是___________。
A.
B.
C.
D.
(2)与镓同主族的B具有缺电子性,硼氢化钠(NaBH)是
4
有机合成中重要的还原剂,其阴离子BH的立体构型为
4
___________。另一种含硼的阴离子B O OH 2 的结构
4 5 4
如图所示,其中B原子的杂化方式为___________。
(3)GaN、GaP、GaAs熔融状态均不导电,据此判断它们是___________。(填“共
价”或“离子”)化合物。它们的晶体结构与金刚石相似,其熔点如下表所示,试
分析 GaN、GaP、GaAs熔点依次降低的原因___________。
化学试题第 5页 共8页
{#{QQABYYSUggCgQBBAABgCQQWiCgOQkBAACKgGAAAIIAAACBNABAA=}#}物质 GaN GaP GaAs
熔点/℃ 1700 1480 1238
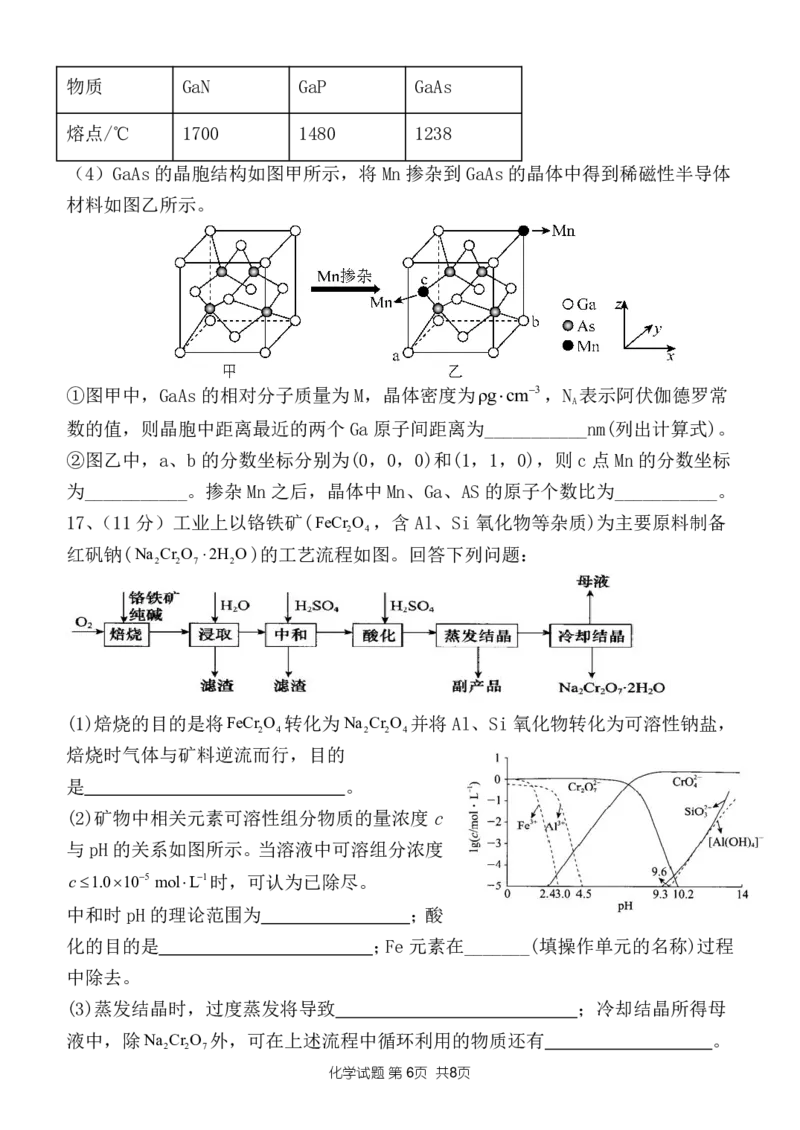
(4)GaAs的晶胞结构如图甲所示,将Mn 掺杂到GaAs的晶体中得到稀磁性半导体
材料如图乙所示。
①图甲中,GaAs的相对分子质量为M,晶体密度为ρgcm3,N 表示阿伏伽德罗常
A
数的值,则晶胞中距离最近的两个Ga原子间距离为___________nm(列出计算式)。
②图乙中,a、b的分数坐标分别为(0,0,0)和(1,1,0),则c点Mn的分数坐标
为___________。掺杂Mn之后,晶体中Mn、Ga、AS的原子个数比为___________。
17、(11分)工业上以铬铁矿(FeCrO ,含 Al、Si氧化物等杂质)为主要原料制备
2 4
红矾钠(Na CrO 2H O)的工艺流程如图。回答下列问题:
2 2 7 2
(1)焙烧的目的是将FeCrO 转化为Na CrO 并将 Al、Si氧化物转化为可溶性钠盐,
2 4 2 2 4
焙烧时气体与矿料逆流而行,目的
是 。
(2)矿物中相关元素可溶性组分物质的量浓度c
与pH 的关系如图所示。当溶液中可溶组分浓度
c1.0105 molL1时,可认为已除尽。
中和时pH的理论范围为 ;酸
化的目的是 ;Fe元素在_______(填操作单元的名称)过程
中除去。
(3)蒸发结晶时,过度蒸发将导致 ;冷却结晶所得母
液中,除Na CrO 外,可在上述流程中循环利用的物质还有 。
2 2 7
化学试题第 6页 共8页
{#{QQABYYSUggCgQBBAABgCQQWiCgOQkBAACKgGAAAIIAAACBNABAA=}#}(4)利用膜电解技术(装置如图所示),以Na CrO 为主要原料制备Na CrO 的总反应
2 4 2 2 7
通电
方程式为4Na CrO +4H O 2Na CrO +4NaOH+2H +O ,
2 4 2 2 2 7 2 2
则Na CrO 在 (填“阴”或“阳”)极室制得,
2 2 7
电解时通过膜的离子主要为 。
18.(14分)无水三氯化铬(CrCl)为紫色单斜晶体,熔点为
3
83℃,易潮解,易升华,高温下易被氧气氧化,在工业上主
要用作媒染剂和催化剂,某化学小组在氮气的氛围下用CrO 和CCl (沸点:76.8℃)
2 3 4
在高温下制备无水三氯化铬,并测定某样品中三氯化铬的质量分数,回答下列问题:
(1)仪器a的名称为___________,制备 CrCl 时有
3
光气(COCl)生成,写出管式炉内发生反应的 化学
2
方程式___ ________。
(2)实验过程中需持续通入N ,写出
2
通入N 的两个作用___________、
2
___________。
(3)为保证产生稳定的CCl 气流,需对a加热,适宜的加热方式为___________,实
4
验结束时,C中的现象为__ _________。
(4)测定某样品中三氯化铬的含量。
称取 0.7000g样品溶于水配制成500mL溶液,取50.00mL所得溶液于锥形瓶中,加
入 20.00mL0.0200molL1的EDTA(NaHY)溶液,充分反应后,加入指示剂,用
2 2
0.0100molL1的ZnCl 标准溶液滴定至终点时,消耗标准溶液的体积为 5.00mL(已知:
2
Cr3++H Y2-=CrY-+2H+、Zn2++H Y2-=ZnH Y)。该样品中CrCl 的质量分数为
2 2 2 3
___________(计算结果精确到1%),如果滴定管用蒸馏水洗涤后未用待装溶液润洗,
则测定结果___________(填“偏高”“偏低”或“无影响”)。
19.(8分)汽车尾气中的CO、NO 、碳氮化合物是大气污染物。科研工作者经过研
x
究,可以用不同方法处理氮的氧化物﹐防止空气污染。回答下列问题:
(1)已知:
N gO g2NOg ΔH180.4kJmol1
2 2
4NH g5O g4NO g 6H O l ΔH905.8kJmol1
3 2 2
NH 能将NO转化成无毒物质。写出在 298K 时该反应的热化学方程式:___________。
3
(2)我国科研人员研究出了用活性炭对汽车尾气中NO处理的方法:
化学试题第 7页 共8页
{#{QQABYYSUggCgQBBAABgCQQWiCgOQkBAACKgGAAAIIAAACBNABAA=}#}Cs2NOg N gCO g H0。在恒压密闭容器中加入足量的活性炭和
2 2
一定量的NO气体,反应相同时间时,测得 NO 的转化率α(NO)随温度的变化关系如
图所示:
由图可知,温度低于1050K时,NO的转化率随温度升高
而增大,原因是___________。用某物质的平衡分压代替
其物质的量浓度也可以表示化学平衡常数(记作K )。在
p
1050K、 1.1106Pa 时,该反应的化学平衡常数K =
p
___________[已知:气体分压P =气体总压P 体积分数]。
分 总
(3)氮氧化物也可以用尿素NH CO水溶液吸收。用尿素水溶液吸收体积比为
2 2
1∶1 的NO和NO 混合气,可将N元素转变为对环境无害的气体。该反应的化学方
2
程式为______ _____。
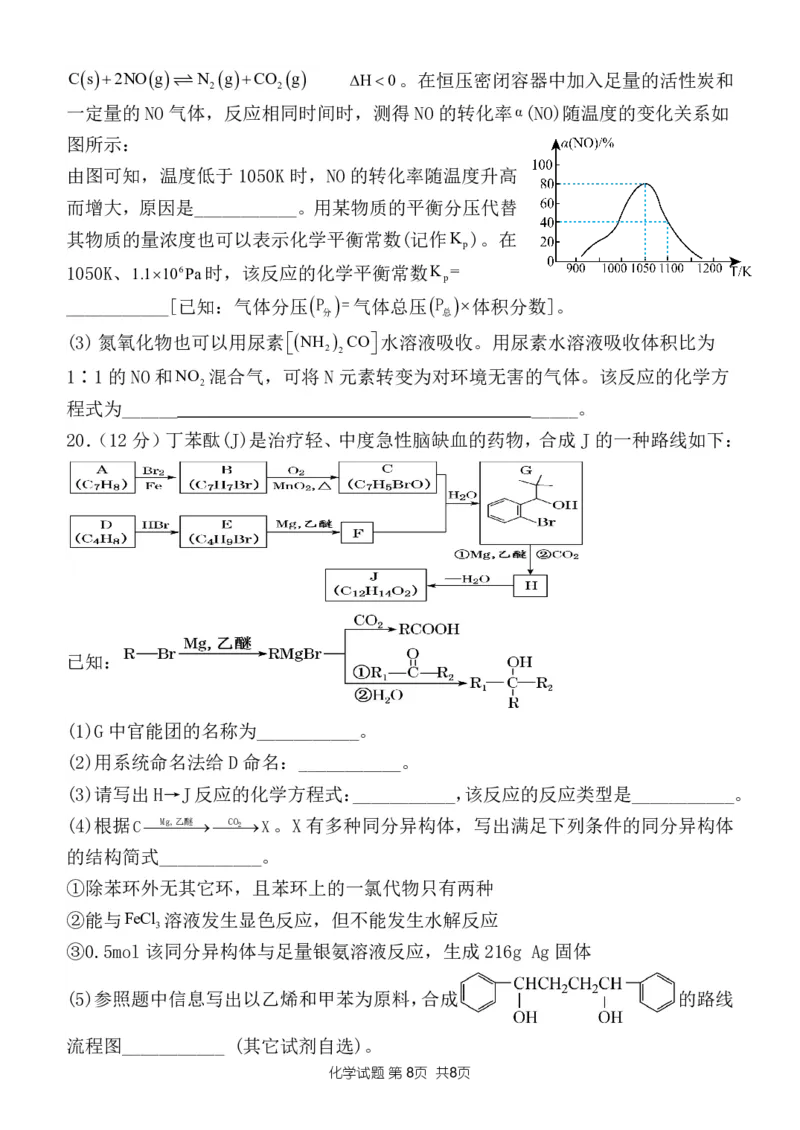
20.(12分)丁苯酞(J)是治疗轻、中度急性脑缺血的药物,合成 J 的一种路线如下:
已知:
(1)G 中官能团的名称为___________。
(2)用系统命名法给D命名:___________。
(3)请写出H→J反应的化学方程式:___________,该反应的反应类型是___________。
(4)根据CMg,乙醚CO2X。X有多种同分异构体,写出满足下列条件的同分异构体
的结构简式___________。
①除苯环外无其它环,且苯环上的一氯代物只有两种
②能与FeCl 溶液发生显色反应,但不能发生水解反应
3
③0.5mol该同分异构体与足量银氨溶液反应,生成216g Ag固体
(5)参照题中信息写出以乙烯和甲苯为原料,合成 的路线
流程图___________ (其它试剂自选)。
化学试题第 8页 共8页
{#{QQABYYSUggCgQBBAABgCQQWiCgOQkBAACKgGAAAIIAAACBNABAA=}#}(化学答案)
一、选择题:本题共10 小题,每小题2分,共20 分,每小题只有一个选项符合题
目要求。
1--5.BAABC 6--10.CCDBD
二、选择题:本题共5个小题,每小 题 4分,共2 0分。每小题有一个或两个选项
符合题意,全部选对得4分,选对但不全的得 2分,有选错的得 0分。
11--15. CD 、A、BC、AC、D
三.非选择题(共5个大题,共 60分)
16.(15 分)
(1)B (2) ①. 正四面体 ②. sp3
(3) ①. 共价 ②. 它们均为原子(共价)晶体,由于N、P、As的原子半径
依次增大,故Ga-N、Ga-P、Ga-As的键长依次增大,共价键越长键能越小,故导致
GaN、GaP、GaAs熔点依次降低
2 4M 1 1
(4) ①. 107 ②. (0, , ) ③. 5:27:32
3
2 ρN 2 2
A
17、(11分)
(1)增大反应物接触面积,提高化学反应速率
(2)4.5pH9.3 ;使2CrO2-+2H+ ⇌ CrO2-+HO平衡正向移动,提高Na CrO 的产率;
4 2 7 2 2 2 7
浸取
(3)有Na CrO 析出;H SO
2 2 7 2 4
(4)阳 ; Na
18.(14分)
高温
(1) 三颈烧瓶 CrO+3CCl 2CrCl+3COCl
=
2 3 4 3 2
(2) 排净装置中空气 吹出CCl(或吹出CrCl)
4 3
(3) 水浴加热 长导管和容器内壁有紫色固体附着
(4) 79% 偏低
19. (8分)
(1)4NH g6NOg5N g 6H O l ΔH1807.8kJmol1
3 2 2
(2)温度低于1050K时,反应未达到平衡状态,随温度升高,反应速率加快,NO
转化率增大
1
{#{QQABYYSUggCgQBBAABgCQQWiCgOQkBAACKgGAAAIIAAACBNABAA=}#}4 (3) NH CONONO 2N CO 2H O
2 2 2 2 2 2
20. (12分) (1) 羟基、溴原子 (2) 2-甲基-1-丙烯(或2-甲基丙烯)
(3) 酯化反应或取代反应
(4) 、
【详细解析】
18.【解析】用氮气将装置中的空气排净,从装置A中出来的四氯化碳与CrO 反应
2 3
生成无水三氯化铬,无水三氯化铬易升华,用装置C收集,制备CrCl 时有光气(COCl)
3 2
生成,装置 D处理尾气并防止倒吸。
(1)仪器 a的名称为三颈烧瓶;依据题意,管式炉内四氯化碳与CrO 反应生成三
2 3
高温
氯化铬和 COCl,反应化学方程式为:CrO+3CCl 2CrCl+3COCl。
=
2 2 3 4 3 2
(2)实验过程中需持续通入氮气,其目的是排净装置中的空气,防止无水三氯化
铬被氧化、吹出CCl,使四氯化碳与CrO 反应、将CrCl 从管式炉中吹出。
4 2 3 3
(3)四氯化碳的沸点为:76.8℃,为保证产生稳定的四氯化碳气流,应对a采取
水浴加热;装置C为收集装置,无水三氯化铬(CrCl)为紫色单斜晶体,因此当实验
3
结束时,装置 C中的现象为:长导管和容器内壁有紫色固体附着。
(4)由题意可知,50.00mLCrCl 溶液中CrCl 的物质的量为:
3 3
20.0010-3L0.0200mol/L-0.0100mol/L5.0010-3L=3.510-4mol,则该样品中
500mL
CrCl 的质量为:3.510-4mol 158.5g/mol=0.55475g,CrCl 的质量分数为:
3 3
50mL
0.55475g
100%≈79%;如果滴定管用蒸馏水洗涤后未用待装溶液润洗,会造成消耗
0.7000g
标准液体积偏大,氯化锌消耗EDTA的量偏高,所测CrCl 含量偏低,测定结果偏低。
3
19.【解析】(1)根据题干信息,NH 能将NO转化成无毒物质,该无毒物质为N,又
3 2
已知:
N gO g2NOg ΔH180.4kJmol1
2 2
4NH g5O g4NO g 6H O l ΔH905.8kJmol1
3 2 2
2
{#{QQABYYSUggCgQBBAABgCQQWiCgOQkBAACKgGAAAIIAAACBNABAA=}#}则反应的热化学方程式为
4NH g6NOg5N g 6H O l
3 2 2
ΔH905.8kJmol15 180.4kJmol11807.8kJ mo l1 ;
(2)温度低于 1050K时,反应未达到平衡状态,因此随温度升高,反应速率加快,
NO转化率增大,1050K、 1.1106Pa 时,NO的转化率为80%,假设起始投入NO的物质
的量为 1mol,则列三段式有:
Cs +2NO g N g +CO g
2 2
起始mol 1 0 0
转化mol 0.8 0.4 0.4
平衡mol 0.2 0.4 0.4
0.4 0.4
1.1106Pa 1.1106Pa
1.0 1.0
因此反应的平衡常数K 4;
p 2
0.2
1.1106Pa
1.0
(3)由题可知,用尿素水溶液吸收体积比为1∶1的NO和NO 混合气,可将N元素转
2
变为对环境无害的气体N,则反应的化学方程式为
2
NH CONONO 2N CO 2H O ;
2 2 2 2 2 2
20.【解析】C、F发生信息中第二步中RMgBr与RCOR 的反应生成G,结合C的分子
1 2
式、G的结构,可推知C为 、F为(CH)CMgBr,结合条件、分子式逆推可知E
3 3
为(CH )CBr、D为 、B为 、A为 ,结合信息中
3 3
R-BrMg,乙醚 RMgBrCO2RCOOH,由G可推知H为 ,结合J的分子
式,可知 G分子内脱去1分子水形成J,则J为 。
【详解】(1)据分析可知,G中官能团的名称为:羟基、溴原子,故答案为:羟基、
溴原子;
(2)D 为 ,D的名称是:2-甲基-1-丙烯(或2-甲基丙烯),故答案为:2-
甲基-1-丙烯(或2-甲基丙烯);
3
{#{QQABYYSUggCgQBBAABgCQQWiCgOQkBAACKgGAAAIIAAACBNABAA=}#}(3)H 为 ,J为 ,则H→J发生酯化反应,反应的化学方程式为:
,故答案为: ;酯
化反应或取代反应;
(4) Mg,乙醚CO2 , 的同分异构体中,能与FeCl 溶
3
液发生显色反应,说明有酚羟基;0.5mol该同分异构体与足量银氨溶液反应,生成
216
Ag物质的量: =2mol,说明该物质有两个醛基;苯环上的一氯代物只有两
108g/mol
种,则满足条件的同分异构体有: 、 ,故答案为:
; ;
(5)由 和两种原料(乙烯、甲苯)的分子结构并且结合题中信
息(R-BrMg,乙醚 RMgBr )可知,要合成
需要先合成苯甲醛和1,2-二溴乙烷;乙烯与溴发生加成反应可以合成1,2-二溴
乙烷;根据题中B到C的变化可知,甲苯可以被氧气、二氧化锰氧化为苯甲醛。因
此,合成 的路线流程图可以表示为:
。
4
{#{QQABYYSUggCgQBBAABgCQQWiCgOQkBAACKgGAAAIIAAACBNABAA=}#}