文档内容
绝密★启用前
2023~2024 学年度高三年级 9 月质量检测
化学
全卷满分100分,考试时间90分钟。
注意事项:
1.答题前,先将自己的姓名、准考证号填写在试卷和答题卡上,并将条形码粘贴在答题卡上的
指定位置。
2.请按题号顺序在答题卡上各题目的答题区域内作答,写在试卷、草稿纸和答题卡上的非答题
区域均无效。
3.选择题用2B铅笔在答题卡上把所选答案的标号涂黑;非选择题用黑色签字笔在答题卡上作答;
字体工整,笔迹清楚。
4.考试结束后,请将试卷和答题卡一并上交。
可能用到的相对原子质量:H1 C12 O16 Mn55 Fe56 Cu64
Br80
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.天宫、天和、天问、神舟体现了中国强大的航天科技实力。下列成果所涉及的材料为复合材料的是
A.“天宫二号”航天器使用的材料——钛合金
B.“天和号”使用的柔性太阳电池阵的材料——砷化镓
C.“天间一号”火星车使用的热控材料——纳米气凝胶
D.“神州十六号”飞船返回舱使用的耐高温材料——酚醛树脂基低密度材料
2.M、Z均为第三周期元素,Z元素的单质及化合物常用于自来水的消毒,二者形成的一种化合物能以
【MZ 】+【MZ 】ˉ的形式存在。下列说法错误的是
4 6
A.原子半径:M>Z
B.简单氢化物的热稳定性:MLi B.6Li的中子数为6
3
C.2H是3H的同素异形体 D.2H、3H的化学性质基本不相同
1 1 1 1
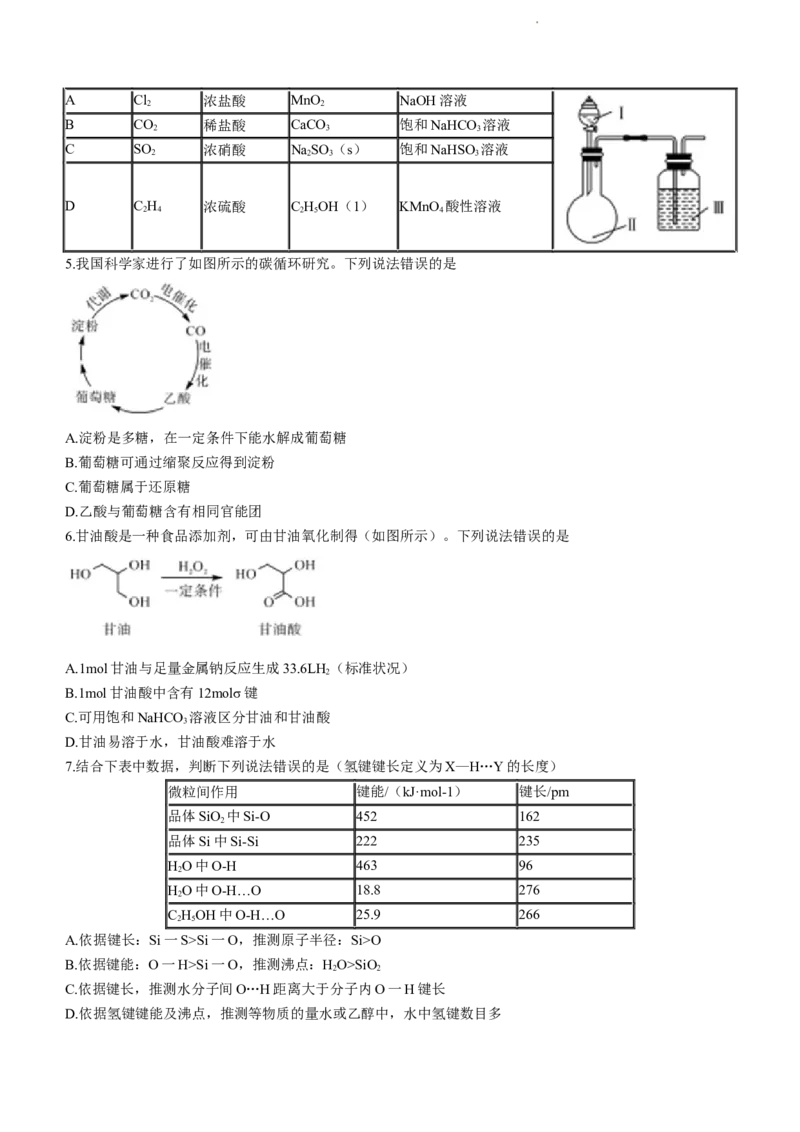
4.利用下列试剂和如图所示装置制备气体并除去其中的非水杂质,能达到目的的是(必要时可加热,加热及
夹持装置已略去)
选项 气体 试剂I 试剂II 试剂Ⅲ
学科网(北京)股份有限公司A Cl 浓盐酸 MnO NaOH溶液
2 2
B CO 稀盐酸 CaCO 饱和NaHCO 溶液
2 3 3
C SO 浓硝酸 NaSO (s) 饱和NaHSO 溶液
2 2 3 3
D C H 浓硫酸 C HOH(1) KMnO 酸性溶液
2 4 2 5 4
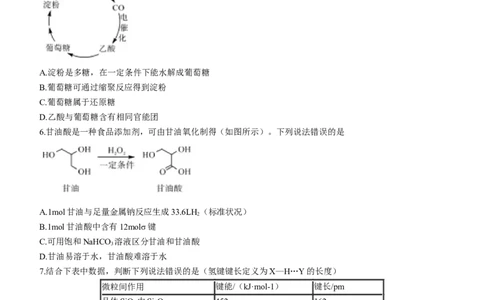
5.我国科学家进行了如图所示的碳循环研究。下列说法错误的是
A.淀粉是多糖,在一定条件下能水解成葡萄糖
B.葡萄糖可通过缩聚反应得到淀粉
C.葡萄糖属于还原糖
D.乙酸与葡萄糖含有相同官能团
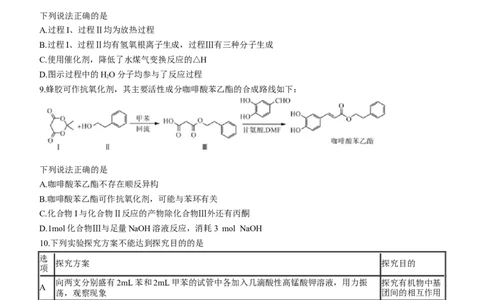
6.甘油酸是一种食品添加剂,可由甘油氧化制得(如图所示)。下列说法错误的是
A.1mol甘油与足量金属钠反应生成33.6LH (标准状况)
2
B.1mol甘油酸中含有12molσ键
C.可用饱和NaHCO 溶液区分甘油和甘油酸
3
D.甘油易溶于水,甘油酸难溶于水
7.结合下表中数据,判断下列说法错误的是(氢键键长定义为X—H…Y的长度)
微粒间作用 键能/(kJ·mol-1) 键长/pm
品体SiO 中Si-O 452 162
2
品体Si中Si-Si 222 235
HO中O-H 463 96
2
HO中O-H…O 18.8 276
2
C HOH中O-H…O 25.9 266
2 5
A.依据键长:Si一S>Si一O,推测原子半径:Si>O
B.依据键能:O一H>Si一O,推测沸点:HO>SiO
2 2
C.依据键长,推测水分子间O…H距离大于分子内O一H键长
D.依据氢键键能及沸点,推测等物质的量水或乙醇中,水中氢键数目多
学科网(北京)股份有限公司8.科学家在水煤气变换【 】中突破了低温下高转化率
与高反应速率不能兼得的难题,该过程是基于双功能催化剂(能吸附不同粒子)催化实现的。
反应过程示意图如下(图中 代表 ):
下列说法正确的是
A.过程I、过程Ⅱ均为放热过程
B.过程I、过程Ⅱ均有氢氧根离子生成,过程Ⅲ有三种分子生成
C.使用催化剂,降低了水煤气变换反应的△H
D.图示过程中的HO分子均参与了反应过程
2
9.蜂胶可作抗氧化剂,其主要活性成分咖啡酸苯乙酯的合成路线如下:
下列说法正确的是
A.咖啡酸苯乙酯不存在顺反异构
B.咖啡酸苯乙酯可作抗氧化剂,可能与苯环有关
C.化合物I与化合物Ⅱ反应的产物除化合物Ⅲ外还有丙酮
D.1mol化合物Ⅲ与足量NaOH溶液反应,消耗3 mol NaOH
10.下列实验探究方案不能达到探究目的的是
选
探究方案 探究目的
项
向两支分别盛有2mL苯和2mL甲苯的试管中各加入几滴酸性高锰酸钾溶液,用力振 探究有机物中基
A
荡,观察现象 团间的相互作用
向两支试管中各加入2mL0.1mol·L-1NaSO 溶液,分别放入盛有冷水和热水的两个烧杯 探究温度对化学
B 2 2 3
中,再同时分别向两支试管中加入2mL0.1mol·L-1HSO 溶液,振荡,观察现象 反应速率的影响
2 4
以Zn、Fe为电极,以酸化的3%NaCl溶液作电解质溶液,连接成原电池装置,过一段
探究金属的电化
C 时间,用胶头滴管从Fe电极区域取少量溶液于试管中,再向试管中滴入2滴K【Fe
3 学保护法
(CN)】溶液,观察现象
6
探究乙酸、碳酸
用分液漏斗向盛有NaCO 固体的锥形瓶中滴加适量浓乙酸,将产生的气体通入盛有苯
D 2 3 和苯酚的酸性强
酚钠溶液的试管中,观察现象
弱
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,
全部选对得4分,选对但不全的得2分,有选错的得0分。
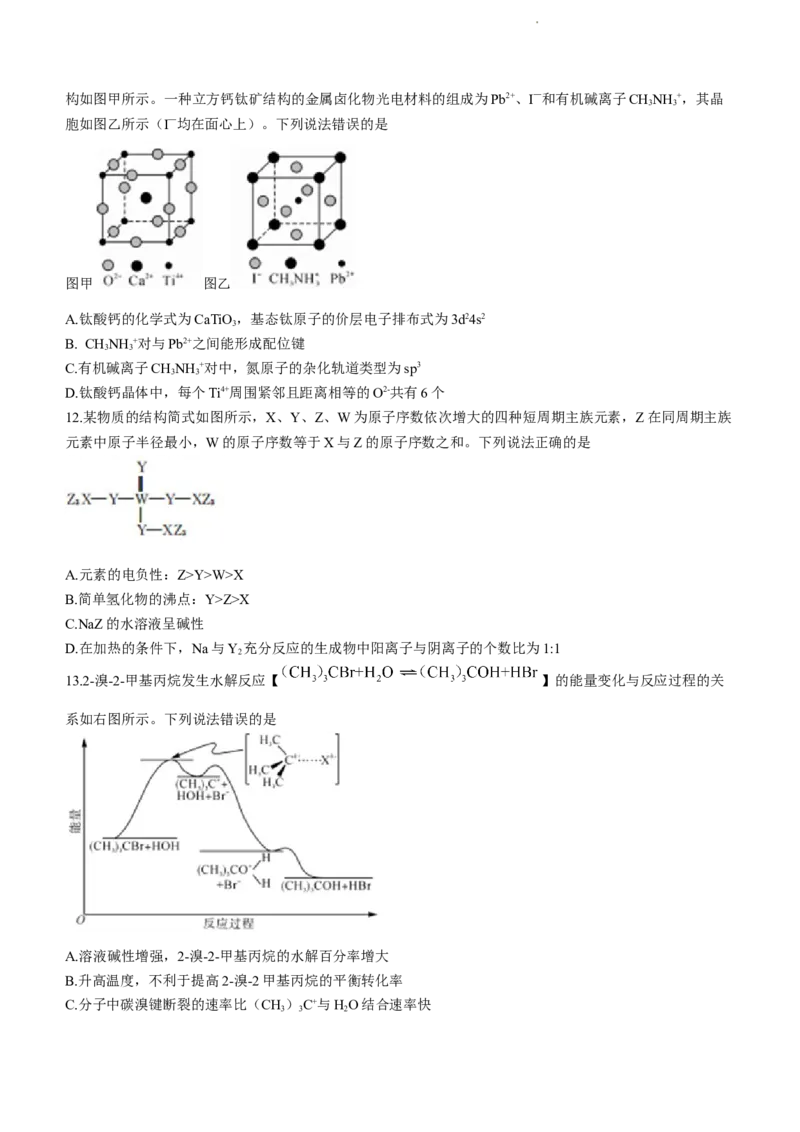
11.钛酸钙是一种具有优异介电特性、温度特性、机械特性以及光学特性的基础无机介电材料,钛酸钙晶胞结
学科网(北京)股份有限公司构如图甲所示。一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I—和有机碱离子CHNH +,其晶
3 3
胞如图乙所示(I—均在面心上)。下列说法错误的是
图甲 图乙
A.钛酸钙的化学式为CaTiO ,基态钛原子的价层电子排布式为3d24s2
3
B. CHNH +对与Pb2+之间能形成配位键
3 3
C.有机碱离子CHNH +对中,氮原子的杂化轨道类型为sp3
3 3
D.钛酸钙晶体中,每个Ti4+周围紧邻且距离相等的O2-共有6个
12.某物质的结构简式如图所示,X、Y、Z、W为原子序数依次增大的四种短周期主族元素,Z在同周期主族
元素中原子半径最小,W的原子序数等于X与Z的原子序数之和。下列说法正确的是
A.元素的电负性:Z>Y>W>X
B.简单氢化物的沸点:Y>Z>X
C.NaZ的水溶液呈碱性
D.在加热的条件下,Na与Y 充分反应的生成物中阳离子与阴离子的个数比为1:1
2
13.2-溴-2-甲基丙烷发生水解反应【 】的能量变化与反应过程的关
系如右图所示。下列说法错误的是
A.溶液碱性增强,2-溴-2-甲基丙烷的水解百分率增大
B.升高温度,不利于提高2-溴-2甲基丙烷的平衡转化率
C.分子中碳溴键断裂的速率比(CH)C+与HO结合速率快
3 3 2
学科网(北京)股份有限公司D.推测(CH)C一X水解生成(CH)C一OH的速率为
3 3 3 3
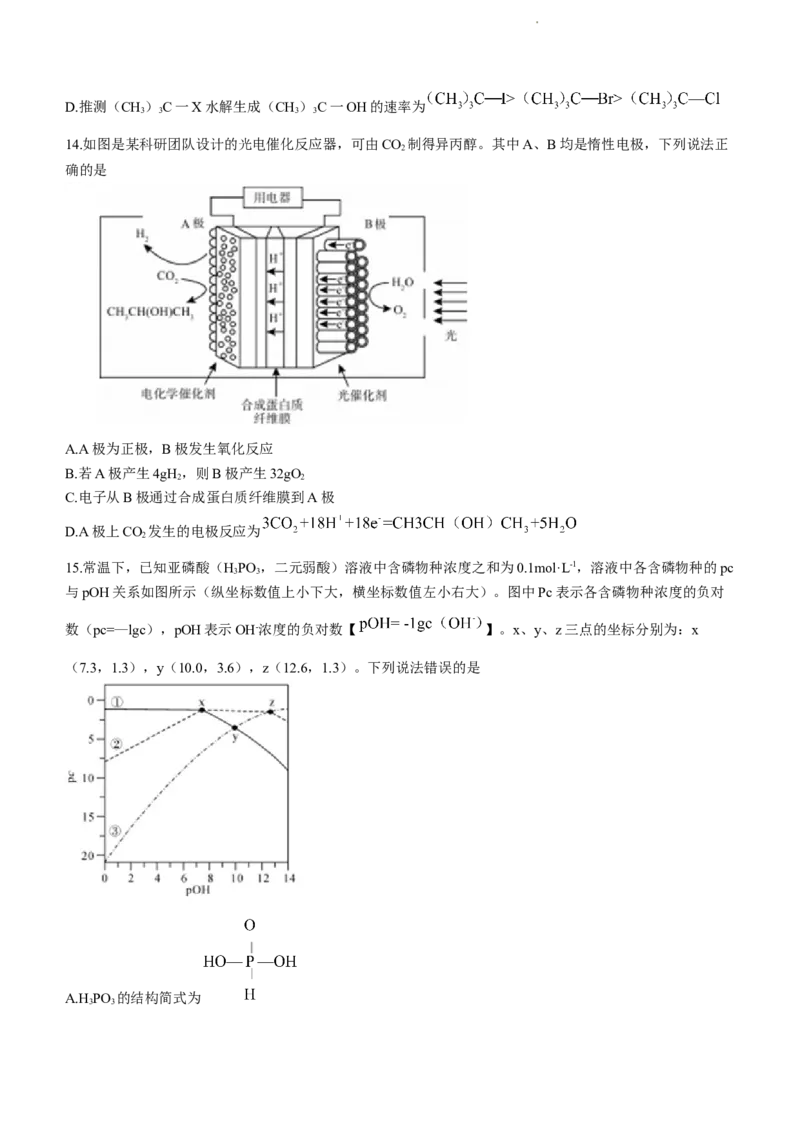
14.如图是某科研团队设计的光电催化反应器,可由CO 制得异丙醇。其中A、B均是惰性电极,下列说法正
2
确的是
A.A极为正极,B极发生氧化反应
B.若A极产生4gH,则B极产生32gO
2 2
C.电子从B极通过合成蛋白质纤维膜到A极
D.A极上CO 发生的电极反应为
2
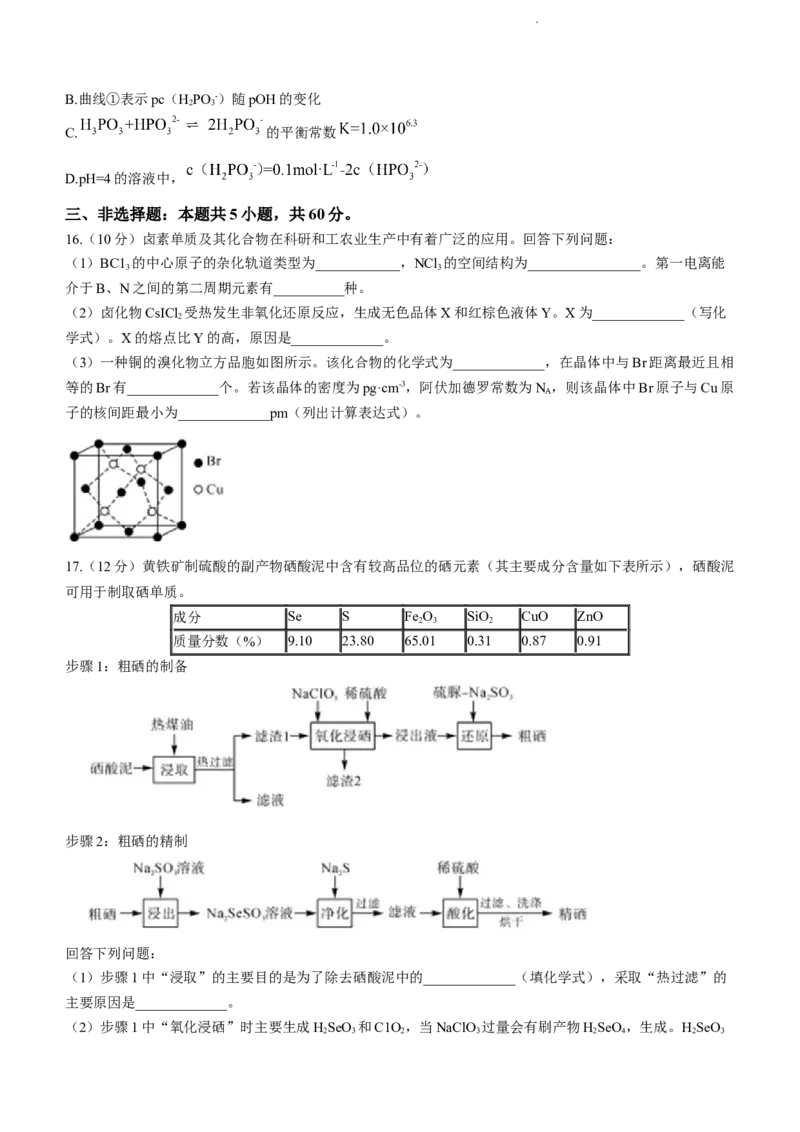
15.常温下,已知亚磷酸(HPO ,二元弱酸)溶液中含磷物种浓度之和为0.1mol·L-1,溶液中各含磷物种的pc
3 3
与pOH关系如图所示(纵坐标数值上小下大,横坐标数值左小右大)。图中Pc表示各含磷物种浓度的负对
数(pc=—lgc),pOH表示OH-浓度的负对数【 】。x、y、z三点的坐标分别为:x
(7.3,1.3),y(10.0,3.6),z(12.6,1.3)。下列说法错误的是
A.HPO 的结构简式为
3 3
学科网(北京)股份有限公司B.曲线①表示pc(HPO -)随pOH的变化
2 3
C. 的平衡常数
D.pH=4的溶液中,
三、非选择题:本题共5小题,共60分。
16.(10分)卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
(1)BC1 的中心原子的杂化轨道类型为____________,NCl 的空间结构为________________。第一电离能
3 3
介于B、N之间的第二周期元素有__________种。
(2)卤化物CsICl 受热发生非氧化还原反应,生成无色品体X和红棕色液体Y。X为_____________(写化
2
学式)。X的熔点比Y的高,原因是_____________。
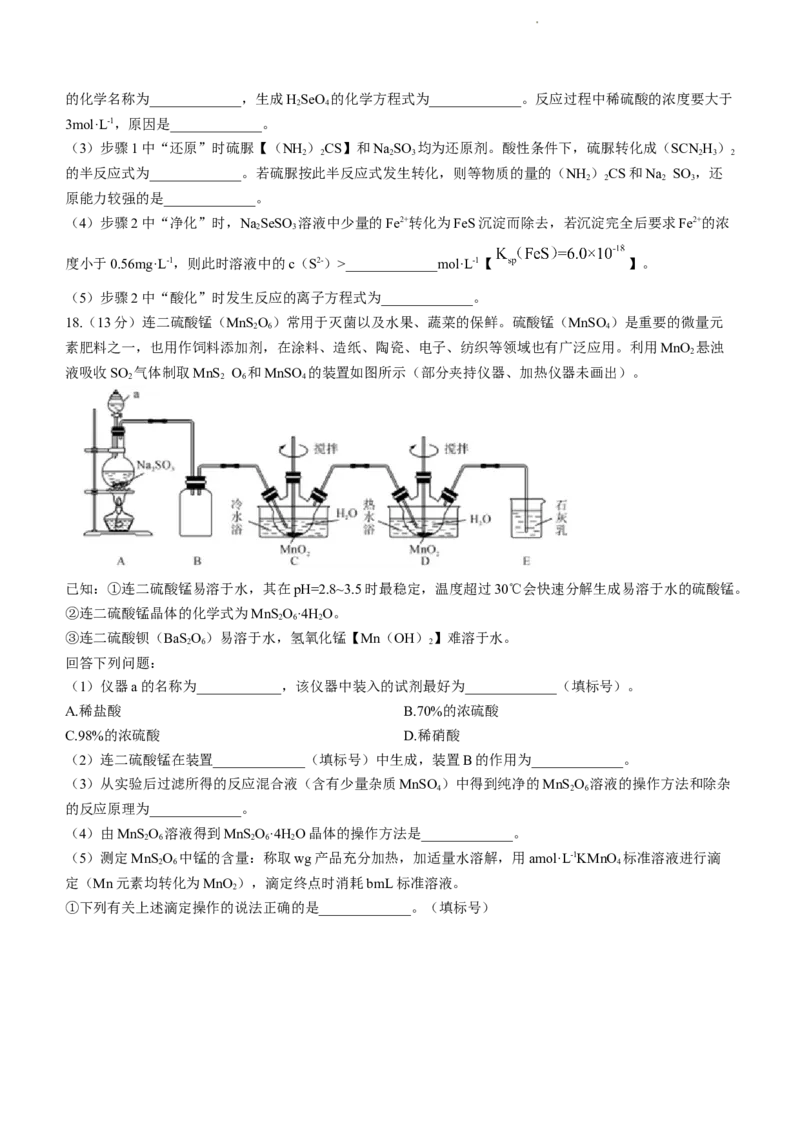
(3)一种铜的溴化物立方品胞如图所示。该化合物的化学式为_____________,在晶体中与Br距离最近且相
等的Br有_____________个。若该晶体的密度为pg·cm-3,阿伏加德罗常数为N ,则该晶体中Br原子与Cu原
A
子的核间距最小为_____________pm(列出计算表达式)。
17.(12分)黄铁矿制硫酸的副产物硒酸泥中含有较高品位的硒元素(其主要成分含量如下表所示),硒酸泥
可用于制取硒单质。
成分 Se S Fe O SiO CuO ZnO
2 3 2
质量分数(%) 9.10 23.80 65.01 0.31 0.87 0.91
步骤1:粗硒的制备
步骤2:粗硒的精制
回答下列问题:
(1)步骤1中“浸取”的主要目的是为了除去硒酸泥中的_____________(填化学式),采取“热过滤”的
主要原因是_____________。
(2)步骤1中“氧化浸硒”时主要生成HSeO 和C1O,当NaClO 过量会有刷产物HSeO,生成。HSeO
2 3 2 3 2 4 2 3
学科网(北京)股份有限公司的化学名称为_____________,生成HSeO 的化学方程式为_____________。反应过程中稀硫酸的浓度要大于
2 4
3mol·L-1,原因是_____________。
(3)步骤1中“还原”时硫脲【(NH )CS】和NaSO 均为还原剂。酸性条件下,硫脲转化成(SCN H)
2 2 2 3 2 3 2
的半反应式为_____________。若硫脲按此半反应式发生转化,则等物质的量的(NH )CS和Na SO ,还
2 2 2 3
原能力较强的是_____________。
(4)步骤2中“净化”时,NaSeSO 溶液中少量的Fe2+转化为FeS沉淀而除去,若沉淀完全后要求Fe2+的浓
2 3
度小于0.56mg·L-1,则此时溶液中的c(S2-)>_____________mol·L-1【 】。
(5)步骤2中“酸化”时发生反应的离子方程式为_____________。
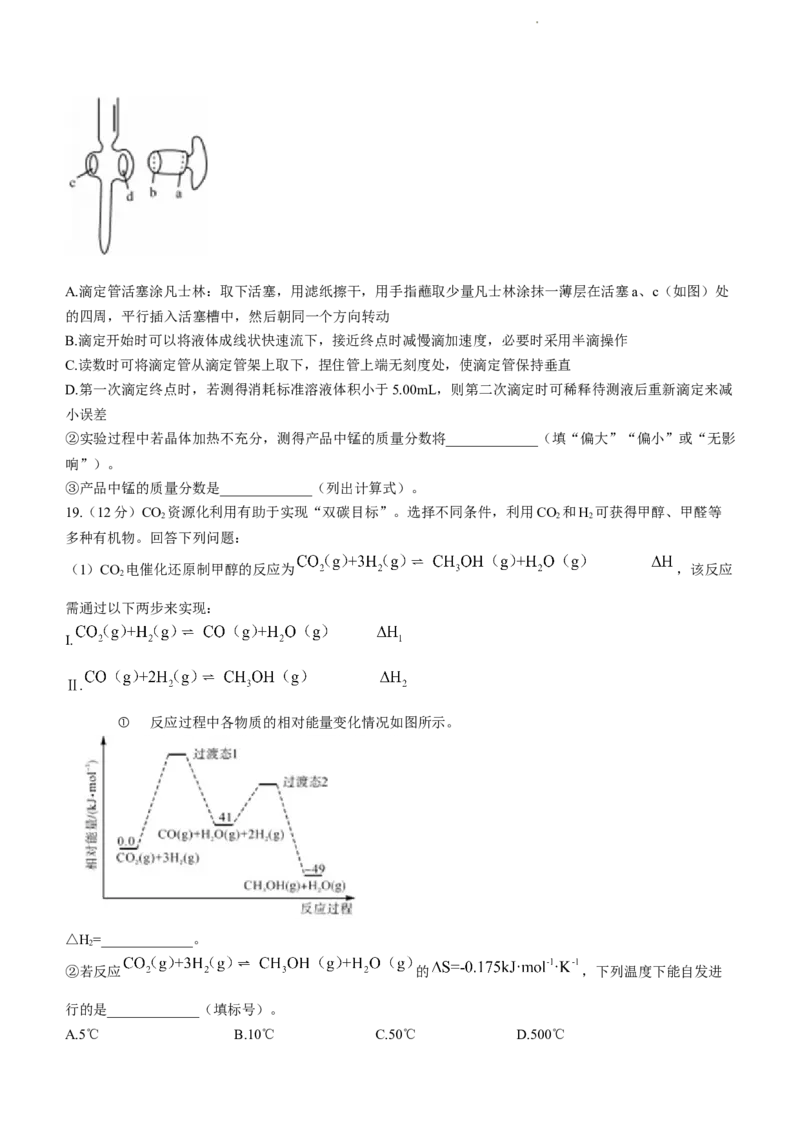
18.(13分)连二硫酸锰(MnSO)常用于灭菌以及水果、蔬菜的保鲜。硫酸锰(MnSO )是重要的微量元
2 6 4
素肥料之一,也用作饲料添加剂,在涂料、造纸、陶瓷、电子、纺织等领域也有广泛应用。利用MnO 悬浊
2
液吸收SO 气体制取MnS O 和MnSO 的装置如图所示(部分夹持仪器、加热仪器未画出)。
2 2 6 4
已知:①连二硫酸锰易溶于水,其在pH=2.8~3.5时最稳定,温度超过30℃会快速分解生成易溶于水的硫酸锰。
②连二硫酸锰晶体的化学式为MnS O·4H O。
2 6 2
③连二硫酸钡(BaS O)易溶于水,氢氧化锰【Mn(OH)】难溶于水。
2 6 2
回答下列问题:
(1)仪器a的名称为____________,该仪器中装入的试剂最好为_____________(填标号)。
A.稀盐酸 B.70%的浓硫酸
C.98%的浓硫酸 D.稀硝酸
(2)连二硫酸锰在装置_____________(填标号)中生成,装置B的作用为_____________。
(3)从实验后过滤所得的反应混合液(含有少量杂质MnSO )中得到纯净的MnS O 溶液的操作方法和除杂
4 2 6
的反应原理为_____________。
(4)由MnS O 溶液得到MnS O·4H O晶体的操作方法是_____________。
2 6 2 6 2
(5)测定MnS O 中锰的含量:称取wg产品充分加热,加适量水溶解,用amol·L-1KMnO 标准溶液进行滴
2 6 4
定(Mn元素均转化为MnO ),滴定终点时消耗bmL标准溶液。
2
①下列有关上述滴定操作的说法正确的是_____________。(填标号)
学科网(北京)股份有限公司A.滴定管活塞涂凡士林:取下活塞,用滤纸擦干,用手指蘸取少量凡士林涂抹一薄层在活塞a、c(如图)处
的四周,平行插入活塞槽中,然后朝同一个方向转动
B.滴定开始时可以将液体成线状快速流下,接近终点时减慢滴加速度,必要时采用半滴操作
C.读数时可将滴定管从滴定管架上取下,捏住管上端无刻度处,使滴定管保持垂直
D.第一次滴定终点时,若测得消耗标准溶液体积小于5.00mL,则第二次滴定时可稀释待测液后重新滴定来减
小误差
②实验过程中若晶体加热不充分,测得产品中锰的质量分数将_____________(填“偏大”“偏小”或“无影
响”)。
③产品中锰的质量分数是_____________(列出计算式)。
19.(12分)CO 资源化利用有助于实现“双碳目标”。选择不同条件,利用CO 和H 可获得甲醇、甲醛等
2 2 2
多种有机物。回答下列问题:
(1)CO 电催化还原制甲醇的反应为 ,该反应
2
需通过以下两步来实现:
I.
Ⅱ.
① 反应过程中各物质的相对能量变化情况如图所示。
△H=_____________。
2
②若反应 的 ,下列温度下能自发进
行的是_____________(填标号)。
A.5℃ B.10℃ C.50℃ D.500℃
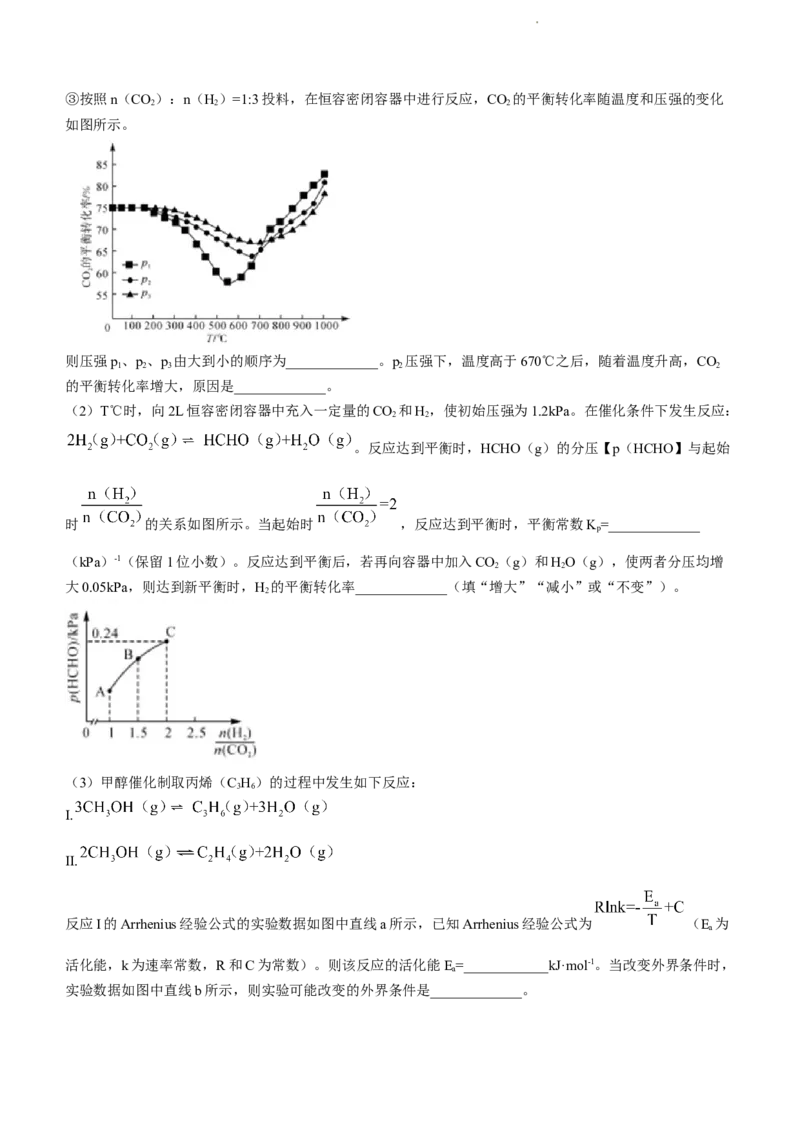
学科网(北京)股份有限公司③按照n(CO):n(H)=1:3投料,在恒容密闭容器中进行反应,CO 的平衡转化率随温度和压强的变化
2 2 2
如图所示。
则压强p、p、p 由大到小的顺序为_____________。p 压强下,温度高于670℃之后,随着温度升高,CO
1 2 3 2 2
的平衡转化率增大,原因是_____________。
(2)T℃时,向2L恒容密闭容器中充入一定量的CO 和H,使初始压强为1.2kPa。在催化条件下发生反应:
2 2
。反应达到平衡时,HCHO(g)的分压【p(HCHO】与起始
时 的关系如图所示。当起始时 ,反应达到平衡时,平衡常数K=_____________
p
(kPa)-1(保留1位小数)。反应达到平衡后,若再向容器中加入CO(g)和HO(g),使两者分压均增
2 2
大0.05kPa,则达到新平衡时,H 的平衡转化率_____________(填“增大”“减小”或“不变”)。
2
(3)甲醇催化制取丙烯(C H)的过程中发生如下反应:
3 6
I.
II.
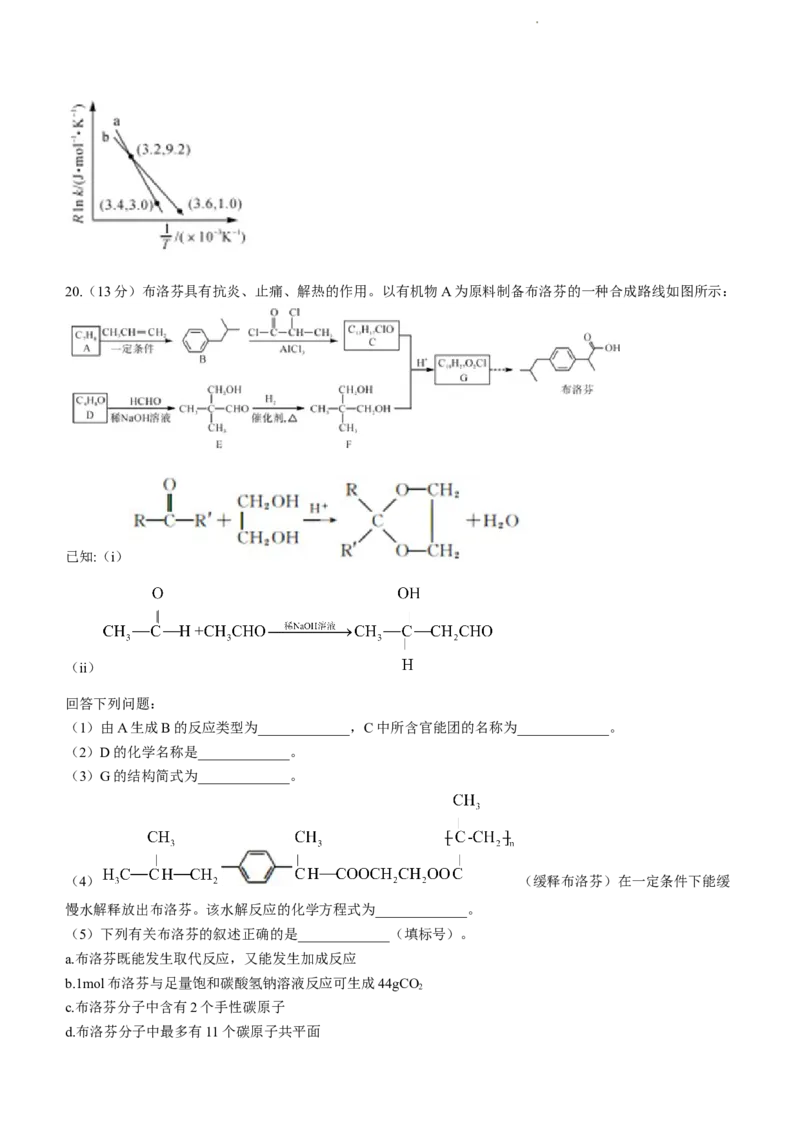
反应I的Arrhenius经验公式的实验数据如图中直线a所示,已知Arrhenius经验公式为 (E 为
a
活化能,k为速率常数,R和C为常数)。则该反应的活化能E=____________kJ·mol-1。当改变外界条件时,
a
实验数据如图中直线b所示,则实验可能改变的外界条件是_____________。
学科网(北京)股份有限公司20.(13分)布洛芬具有抗炎、止痛、解热的作用。以有机物A为原料制备布洛芬的一种合成路线如图所示:
已知:(i)
(ii)
回答下列问题:
(1)由A生成B的反应类型为_____________,C中所含官能团的名称为_____________。
(2)D的化学名称是_____________。
(3)G的结构简式为_____________。
(4) (缓释布洛芬)在一定条件下能缓
慢水解释放出布洛芬。该水解反应的化学方程式为_____________。
(5)下列有关布洛芬的叙述正确的是_____________(填标号)。
a.布洛芬既能发生取代反应,又能发生加成反应
b.1mol布洛芬与足量饱和碳酸氢钠溶液反应可生成44gCO
2
c.布洛芬分子中含有2个手性碳原子
d.布洛芬分子中最多有11个碳原子共平面
学科网(北京)股份有限公司(6)满足下列条件的布洛芬的同分异构体共有_____________种(不考虑立体异构),其中能发生银镜反应
且核磁共振氢谱的峰面积比为12:2:2:1:1的结构简式为_____________(任写一种)。
①苯环上有三个取代基,苯环上的一氯代物有两种
②能发生水解反应,且水解产物之一能与FeC1 溶液发生显色反应
3
(7)季戊四醇( )是一种重要的化工原料。设计由甲醇和乙醛为起始原料制备季
戊四醇的合成路线_____________(无机试剂任选)。
学科网(北京)股份有限公司