文档内容
惠州市 2024 届高三第一次调研考试试题
化 学
1.本卷共20个题目,卷面分100分。考试时间75分钟。
2. 可能用到的相对原子质量:H-1 C-12 O-16 Na-23 A1-27 S-32 Fe-56 Cu-64
一、单项选择题:本题共 16 小题,共 44 分。第 1-10 小题,每小题 2 分;第
11~16小题, 每小题4分。每小题只有一个选项符合题意。
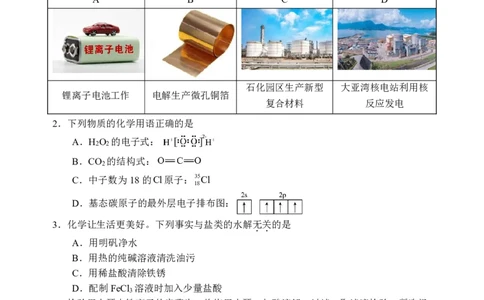
1.惠州的特色产业发展离不开化学。下列过程中不涉及化学变化的是
A B C D
石化园区生产新型 大亚湾核电站利用核
锂离子电池工作 电解生产微孔铜箔
复合材料 反应发电
2.下列物质的化学用语正确的是
A.H O 的电子式:
2 2
B.CO 的结构式:
2
C.中子数为18的Cl原子:35Cl
18
D.基态碳原子的最外层电子排布图:
3.化学让生活更美好。下列事实与盐类的水解无
.
关
.
的是
A.用明矾净水
B.用热的纯碱溶液清洗油污
C.用稀盐酸清除铁锈
D.配制FeCl 溶液时加入少量盐酸
3
4.检验黑木耳中铁离子的步骤为:灼烧黑木耳→加酸溶解→过滤→取滤液检验,所选择
的装置(夹持装置已略去)或操作不正确的是
A.灼烧黑木耳 B.加酸后搅拌溶解 C.过滤得滤液 D.检验铁离子
{#{QQABJY6QoggAAgAAAABCAwXgCAIQkhAACIgGBFAcoEIBCAFABAA=}#}5.下列措施中,不能增大反应速率的是
A.铁和稀盐酸反应制氢气时,用铁粉代替铁片
B.常温下用浓硫酸代替稀硫酸与铝反应制氢气
C.乙酸和乙醇进行酯化反应时采取加热措施
D.H O 分解制O 时加入少量MnO
2 2 2 2
6.反应NH ClNaNO NaClN 2H O放热且产生气体,可用于冬天石油开采。设
4 2 2 2
N 为阿伏伽德罗常数的值。下列说法不正确的是
A
A.0.1molN 中含有π键数目为0.2N
2 A
B.18gH O中所含电子数目为10N
2 A
C.常温时,pH=8的NaNO 溶液中所含OH- 的数目为10-6N
2 A
D.上述反应中,每生成0.1molN 转移的电子数目为0.3N
2 A
7.常温下,下列各组离子在指定溶液中一定能大量共存的是
A.使淀粉-KI溶液变蓝的溶液:H+、NH+、S2-、Br-
4
B.滴入酚酞呈红色的溶液:Na+、K+、CH COO-、Cl-
3
C.滴入苯酚显紫色的溶液:Mg2+、NH+、Cl-、SCN-
4
D.滴入甲基橙呈红色的溶液:K+、Na+、HCO-、NO-
3 3
8.下列现象与电化学腐蚀无关的是
A.铜锌合金(黄铜)不易被腐蚀
B.银质物品久置表面变黑
C.附有银制配件的铁制品其接触处易生锈
D.铁锅炒菜后未洗净擦干容易生锈
9.化学创造美好生活。下列生产活动与对应化学原理有关联的是
选项 生产活动 化学原理
A 家务劳动:用白醋清洗水壶中的水垢 白醋可用来消毒
B 实践活动:红酒中加入适量SO SO 具有漂白性
2 2
C 自主探究:以油脂为原料制肥皂 油脂在碱性条件下可发生水解反应
D 社区服务:用酒精对图书馆桌椅消毒 乙醇具有还原性
{#{QQABJY6QoggAAgAAAABCAwXgCAIQkhAACIgGBFAcoEIBCAFABAA=}#}10.合成布洛芬的方法如图所示(其他物质省略)。下列说法错误的是
A.X分子中所有原子可能共平面 B.Y的分子式为C H O
13 16 2
C.X、Y都能发生加成反应 D.布洛芬能与碳酸钠溶液反应
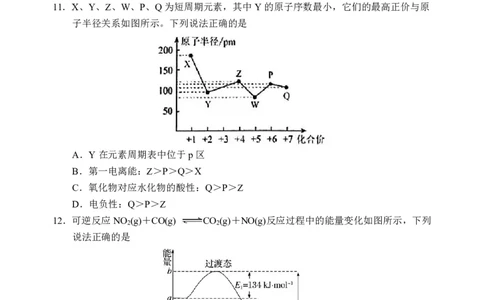
11.X、Y、Z、W、P、Q为短周期元素,其中Y的原子序数最小,它们的最高正价与原
子半径关系如图所示。下列说法正确的是
A.Y在元素周期表中位于p区
B.第一电离能:Z>P>Q>X
C.氧化物对应水化物的酸性:Q>P>Z
D.电负性:Q>P>Z
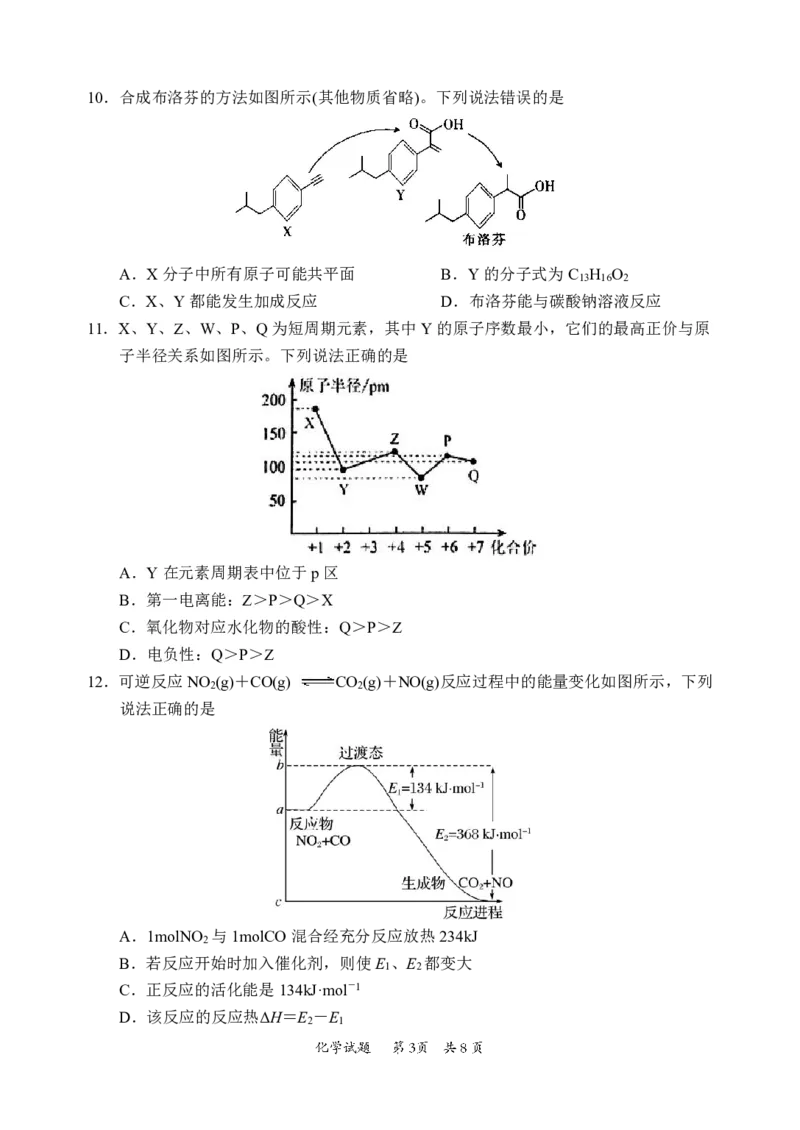
12.可逆反应NO (g)+CO(g) CO (g)+NO(g)反应过程中的能量变化如图所示,下列
2 2
说法正确的是
A.1molNO 与1molCO混合经充分反应放热234kJ
2
B.若反应开始时加入催化剂,则使E 、E 都变大
1 2
C.正反应的活化能是134kJ·mol-1
D.该反应的反应热ΔH=E -E
2 1
{#{QQABJY6QoggAAgAAAABCAwXgCAIQkhAACIgGBFAcoEIBCAFABAA=}#}13.MnO 催化除去HCHO的机理如右图所示,
2
下列说法不正确的是
A.反应①~④均是氧化还原反应
B.反应②中碳氧双键未断裂
C.HCHO中碳原子采取sp2杂化
D.上述机理总反应为HCHOO MnO2CO H O
2 2 2
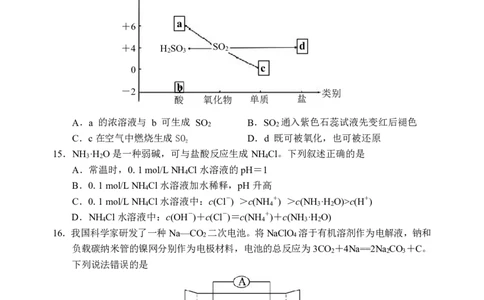
14.部分含硫物质的分类与相应化合价关系如图所示。下列推断不合理的是
化合价
+6 a
+4 H 2 SO 3 SO 2 d
0 c
b
-2 类别
酸 氧化物 单质 盐
A.a 的浓溶液与 b 可生成 SO B.SO 通入紫色石蕊试液先变红后褪色
2 2
C.c在空气中燃烧生成SO D.d 既可被氧化,也可被还原
2
15.NH ·H O是一种弱碱,可与盐酸反应生成NH Cl。下列叙述正确的是
3 2 4
A.常温时,0.1mol/LNH Cl水溶液的pH=1
4
B.0.1mol/LNH Cl水溶液加水稀释,pH升高
4
C.0.1mol/LNH Cl水溶液中:c(Cl-) >c(NH +) >c(NH ·H O)>c(H+)
4 4 3 2
D.NH Cl水溶液中:c(OH-)+c(Cl-)=c(NH +)+c(NH ·H O)
4 4 3 2
16.我国科学家研发了一种Na—CO 二次电池。将NaClO 溶于有机溶剂作为电解液,钠和
2 4
负载碳纳米管的镍网分别作为电极材料,电池的总反应为3CO +4Na==2Na CO +C。
2 2 3
下列说法错误的是
A.放电时,ClO-向负极移动
4
B.充电时释放CO ,放电时吸收CO
2 2
C.放电时,正极反应为3CO +4e-===2CO2-+C
2 3
D.充电时,阳极反应为Na++e-===Na
{#{QQABJY6QoggAAgAAAABCAwXgCAIQkhAACIgGBFAcoEIBCAFABAA=}#}二、非选择题:共56分。
17.(14分)某小组在做铜与浓硫酸(装置如下图)的反应实验时,发现有如下的反应现象:
序号 操作 现象
① 加热 铜丝表面变黑
有大量气泡产生,溶液变为墨绿色浊液,试管底部开
② 继续加热
始有灰白色沉淀生成。品红溶液褪色。
试管中出现“白雾”,浊液逐渐变为澄清,溶液颜色
③ 再加热
慢慢变为浅蓝色,试管底部灰白色沉淀增多
冷却,将灰白色固体
④ 形成蓝色溶液
倒入水中
【查阅资料】聚氯乙烯受热分解产生氯化氢,[CuCl ]2-呈黄色,[Cu(H O) ]2+呈蓝色,两者
4 2 4
混合则成绿色,铜的化合物中CuO、CuS、Cu S都为黑色,其中CuO溶于盐酸;CuS、
2
Cu S不溶于稀盐酸,但溶于浓盐酸。
2
(1)铜丝与浓硫酸反应的化学方程式为_______________________________
(2)试管中品红溶液褪色,体现SO 的___________性,浸NaOH溶液的棉团作用是_____
2
(3)甲组同学对实验中形成的墨绿色溶液进行探究,特进行下列实验:
操作 现象
Ⅰ组 直接取其铜丝(表面有聚氯乙烯薄膜)做实验 溶液变成墨绿色
Ⅱ组 实验前,先将铜丝进行灼烧处理 溶液变蓝
请解释形成墨绿色的原因:_____________________
(4)乙组同学对白雾的成分经检验为H SO ,请设计实验证明该白雾为硫酸:______
2 4
(5)丙组同学进一步对灰白色沉淀通过加水溶解、过滤,最后沉淀为黑色,取其黑色沉
淀,进行成分探究:滴加适量稀盐酸,则发现黑色沉淀几乎不溶解,溶液也不变蓝,
则说明黑色沉淀中不含有____________。滴加适量浓盐酸,振荡,加热,观察到黑
色沉淀几乎完全溶解,生成呈略黄色的 [CuCl ]2-n(n=1~4)。写出CuS与浓盐酸反应
n
的离子方程式:___________
(6)某工厂将热空气通入稀硫酸中来溶解废铜屑制备CuSO ·5H O,消耗含铜元素80%的
4 2
废铜屑240kg固体时,得到500kg产品,产率为_______(结果保留两位小数)。
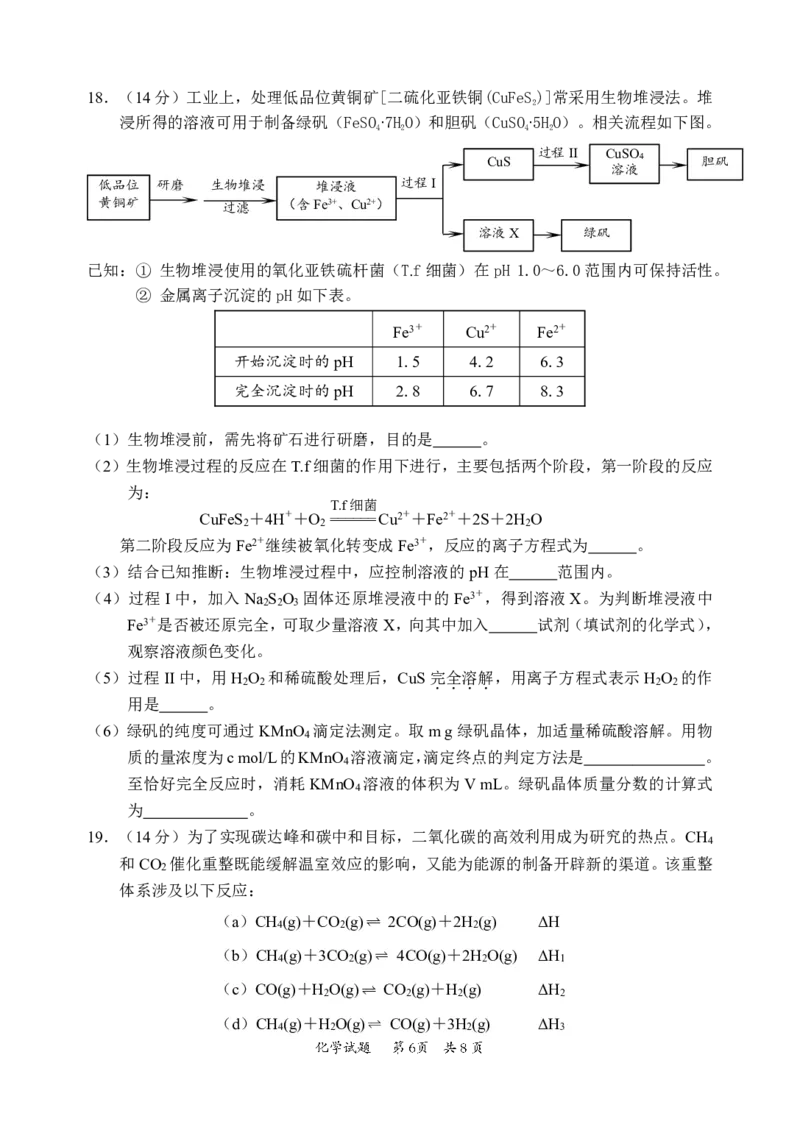
{#{QQABJY6QoggAAgAAAABCAwXgCAIQkhAACIgGBFAcoEIBCAFABAA=}#}18.(14分)工业上,处理低品位黄铜矿[二硫化亚铁铜(CuFeS)]常采用生物堆浸法。堆
2
浸所得的溶液可用于制备绿矾(FeSO∙7HO)和胆矾(CuSO∙5HO)。相关流程如下图。
4 2 4 2
CuS
过程II CuSO4
胆矾
溶液
低品位 研磨 生物堆浸 堆浸液 过程I
黄铜矿 过滤 (含Fe3+、Cu2+)
溶液X 绿矾
已知:① 生物堆浸使用的氧化亚铁硫杆菌(T.f细菌)在pH 1.0~6.0范围内可保持活性。
② 金属离子沉淀的pH如下表。
Fe3+ Cu2+ Fe2+
开始沉淀时的pH 1.5 4.2 6.3
完全沉淀时的pH 2.8 6.7 8.3
(1)生物堆浸前,需先将矿石进行研磨,目的是 。
(2)生物堆浸过程的反应在T.f细菌的作用下进行,主要包括两个阶段,第一阶段的反应
为:
T.f细菌
CuFeS +4H++O ======Cu2++Fe2++2S+2H O
2 2 2
第二阶段反应为Fe2+继续被氧化转变成Fe3+,反应的离子方程式为 。
(3)结合已知推断:生物堆浸过程中,应控制溶液的pH在 范围内。
(4)过程I中,加入Na S O 固体还原堆浸液中的Fe3+,得到溶液X。为判断堆浸液中
2 2 3
Fe3+是否被还原完全,可取少量溶液X,向其中加入 试剂(填试剂的化学式),
观察溶液颜色变化。
(5)过程II中,用H 2 O 2 和稀硫酸处理后,CuS完 . 全 . 溶 . 解 . ,用离子方程式表示H 2 O 2 的作
用是 。
(6)绿矾的纯度可通过KMnO 滴定法测定。取mg绿矾晶体,加适量稀硫酸溶解。用物
4
质的量浓度为cmol/L的KMnO 溶液滴定,滴定终点的判定方法是 。
4
至恰好完全反应时,消耗KMnO 溶液的体积为VmL。绿矾晶体质量分数的计算式
4
为 。
19.(14分)为了实现碳达峰和碳中和目标,二氧化碳的高效利用成为研究的热点。CH
4
和CO 催化重整既能缓解温室效应的影响,又能为能源的制备开辟新的渠道。该重整
2
体系涉及以下反应:
(a)CH
4
(g)+CO
2
(g) 2CO(g)+2H
2
(g) ΔH
(b)CH
4
(g)+3CO
2
(g) 4CO(g)+2H
2
O(g) ΔH
1
(c)CO(g)+H
2
O(g) CO
2
(g)+H
2
(g) ΔH
2
(d)CH
4
(g)+H
2
O(g) CO(g)+3H
2
(g) ΔH
3
{#{QQABJY6QoggAAgAAAABCAwXgCAIQkhAACIgGBFAcoEIBCAFABAA=}#}(1)根据盖斯定律,反应a的 ΔH=______________(写出一个代数式即可)
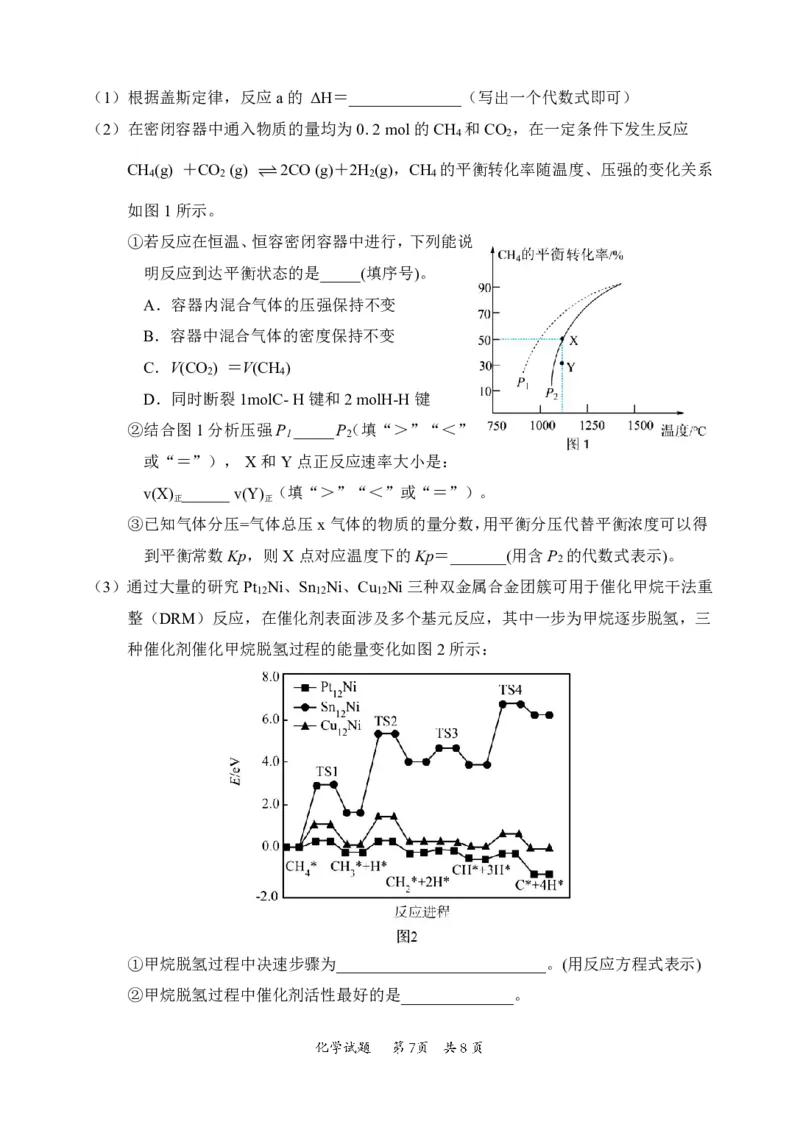
(2)在密闭容器中通入物质的量均为0.2mol的CH 和CO ,在一定条件下发生反应
4 2
CH
4
(g) +CO
2
(g) 2CO(g)+2H
2
(g),CH
4
的平衡转化率随温度、压强的变化关系
如图1所示。
①若反应在恒温、恒容密闭容器中进行,下列能说
明反应到达平衡状态的是_____(填序号)。
A.容器内混合气体的压强保持不变
B.容器中混合气体的密度保持不变
C.V(CO ) =V(CH )
2 4
D.同时断裂1molC-H键和2molH-H键
②结合图1分析压强P _____P(填“>”“<”
1 2
或“=”), X和Y点正反应速率大小是:
v(X) ______v(Y) (填“>”“<”或“=”)。
正 正
③已知气体分压=气体总压x气体的物质的量分数,用平衡分压代替平衡浓度可以得
到平衡常数Kp,则X点对应温度下的Kp=_______(用含P 的代数式表示)。
2
(3)通过大量的研究Pt Ni、Sn Ni、Cu Ni三种双金属合金团簇可用于催化甲烷干法重
12 12 12
整(DRM)反应,在催化剂表面涉及多个基元反应,其中一步为甲烷逐步脱氢,三
种催化剂催化甲烷脱氢过程的能量变化如图2所示:
①甲烷脱氢过程中决速步骤为__________________________。(用反应方程式表示)
②甲烷脱氢过程中催化剂活性最好的是______________。
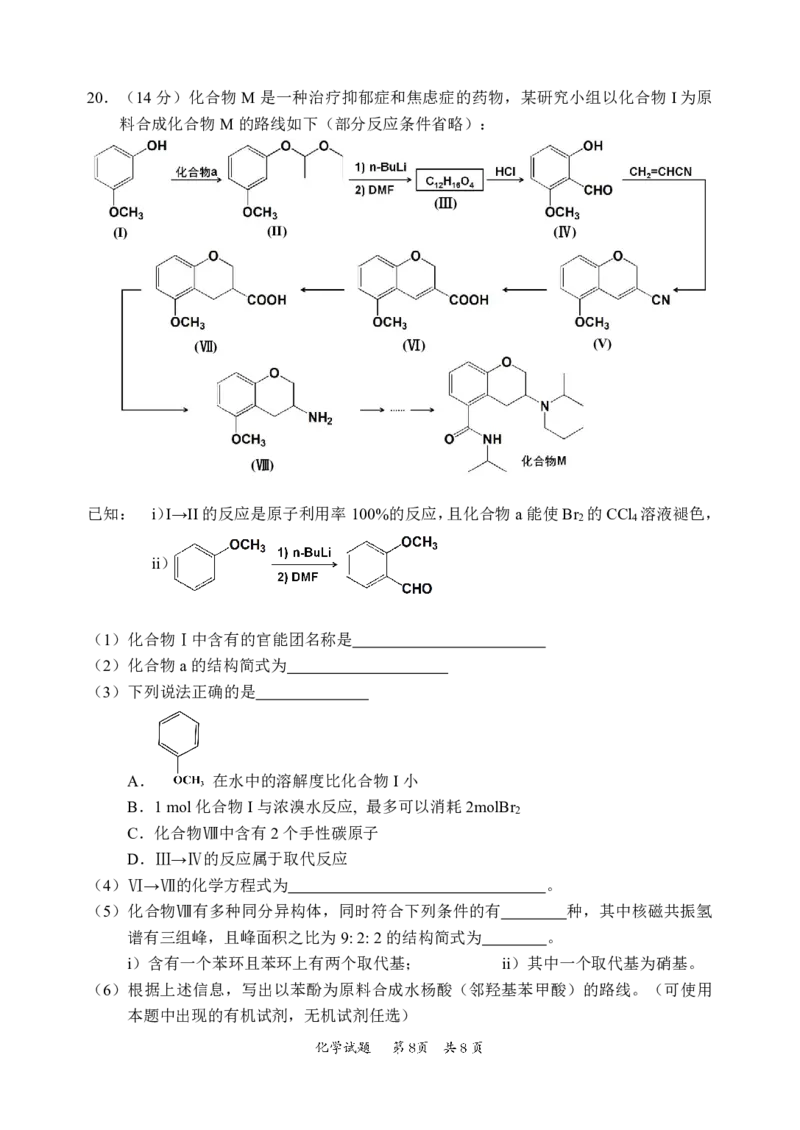
{#{QQABJY6QoggAAgAAAABCAwXgCAIQkhAACIgGBFAcoEIBCAFABAA=}#}20.(14分)化合物M是一种治疗抑郁症和焦虑症的药物,某研究小组以化合物I为原
料合成化合物M的路线如下(部分反应条件省略):
(Ⅲ)
(I) (II) (Ⅳ)
(Ⅶ) (Ⅵ) (V)
(Ⅷ)
已知: i)I→II的反应是原子利用率100%的反应,且化合物a能使Br 的CCl 溶液褪色,
2 4
ii)
(1)化合物Ⅰ中含有的官能团名称是
(2)化合物a的结构简式为
(3)下列说法正确的是
A. 在水中的溶解度比化合物I小
B.1mol化合物I与浓溴水反应, 最多可以消耗2molBr
2
C.化合物Ⅷ中含有2个手性碳原子
D.Ⅲ→Ⅳ的反应属于取代反应
(4)Ⅵ→Ⅶ的化学方程式为 。
(5)化合物Ⅷ有多种同分异构体,同时符合下列条件的有 种,其中核磁共振氢
谱有三组峰,且峰面积之比为9:2:2的结构简式为 。
i)含有一个苯环且苯环上有两个取代基; ii)其中一个取代基为硝基。
(6)根据上述信息,写出以苯酚为原料合成水杨酸(邻羟基苯甲酸)的路线。(可使用
本题中出现的有机试剂,无机试剂任选)
{#{QQABJY6QoggAAgAAAABCAwXgCAIQkhAACIgGBFAcoEIBCAFABAA=}#}