文档内容
浙江省强基联盟 2023 学年第一学期高三年级 塞,C错误;可利用碘单质在四氯化碳中的溶解度大于在水中的溶解度,萃取碘水中的碘单质,D
正确。
10 月联考化学学科参考答案
6.C
题号 1 2 3 4 5 6 7 8 过程Ⅰ的化学方程式为4NH 3 +COCl 2 =CO(NH 2 ) 2 +2NH 4 Cl,A正确;根据CO(NH 2 ) 2 氮价态为-3价,
答案 C B A A D C D D N 2 H 4 氮元素价态为-2价,试剂A具有氧化性,若试剂A是NaClO,其还原产物为NaCl,B正确;
题号 9 10 11 12 13 14 15 16 N 2 H 4 +HNO 2 =HN 3 +2H 2 O,每生成3molHN 3 ,则转移10mol电子,C错误;根据NH 2 OH氮价态为
答案 A C B C B C D B -1价,NH 氮元素价态为-3价,试剂B具有氧化性,D正确。
3
7.D
1.C
根据n= ,0.1molNaHSO 中含有0.1N 个阳离子,A错误;N=c×V×N ,
4 A A
小苏打是NaHCO ,属于钠盐,A错误;食盐是NaCl,属于钠盐, B错误;维生素C的结构 12
3
已知信息 中=缺12少0 · V , −1B =错0误.1; 缺 少标准状况信息,且丁烷分解可能生成C和氢气, C错误;n=
,含有σ键数目为1.2N ,D正确。 =
简式为 ,为有机物,C正确;二氧化硫氧化物,D错误。 A
7.8
788.D · −1=0.1
甲烷与氯气取代反应得到的液态混合物含有二氯甲烷(沸点40℃)、三氯甲烷(沸点62℃)和四氯
2.B
化碳(沸点77℃),可利用其沸点不同分离,A正确;纤维素分子中存在葡萄糖单元醇羟基,能与
碳原子半径大于氧原子,二氧化碳的空间填充模型为 ,A错误;根据VSEPR模型,P
硝酸发生酯化反应,生成的硝酸纤维极易燃烧,可用于生产火药,B正确;1,3-丁二烯含有双键,
能发生加聚反应生成以顺式为主的顺丁橡胶,C正确;饱和碳酸钠溶液与乙醇、乙醛、乙酸、乙酸
的孤电子对数为1,价层电子对数为3,价层电子对互斥模型为 ,B正确;羟基的电子式
乙酯混合后的现象分别是互溶、互溶、生成气泡、分层,不能鉴别乙醇与乙醛,D错误。
9.A
为 ,C错误;1,1-二溴乙烷的结构简式:CHBr CH ,D错误。
2 3
高铁酸钾溶液与浓盐酸反应:2FeO 2−+16H++6Cl−===△2Fe3++3Cl ↑+8H O,A错误;铝与氢氧化钠
4 2 2
3.A 反 应 生 成 四 氢 氧 化 铝 酸 钠 和 氢 气 , 根 据 得 失 电 子 守 恒 , 离 子 方 程 式 为
次氯酸钠是盐类,属于强电解质,A错误;根据次氯酸分解生成氧气与氯化氢,次氯酸钠分解生
2Al+2OH-+6H O=2Al(OH) -+3H ↑,B正确;根据酸性:HCl>H CO >HClO>HCO -,碳酸钠与少
2 4 2 2 3 3
成氯化钠与氧气,B正确;氢氧化钠与氯气反应生成氯化钠与次氯酸钠,C正确;次氯酸钠具有氧
量新制氯水(1mol)的反应可看成 2 步,①Cl +H O H++Cl-+HClO,②H++CO 2-=HCO -,
2 2 3 3
化性,可用于游泳池的消毒,D正确。
HClO+CO 2-=HCO -+HClO,①+②得到离子方程式2CO 2-+Cl +H O=2HCO -+Cl-+ClO-,C正确;
3 3 3 2 2 3
4.A 向次氯酸钙溶液中通入少量二氧化硫(1mol)看成 2 步,①ClO-+SO +H O=SO 2-+Cl-+2H+;
2 2 4
氨具有碱性,可吸收烟气中的二氧化硫,A错误;根据铁的价态为+3价,具有氧化性,能与铜单
②Ca2++SO 2 =CaSO , H++ClO- ===HClO①+② 得 到 离 子 方 程 式
4 4
质反应,用于印刷电路板,2FeCl +Cu=2FeCl +CuCl ,B正确;碳酸钠因水解,溶液呈碱性,可用
3 2 2 Ca2++3ClO-+SO +H O=CaSO ↓+Cl-+2HClO,D正确。
2 2 4
作食用碱,C正确;钠、钾的熔点低,合金在常温下为液态,可用于核反应堆的热交换剂,D正确。
10.C
5.D 形成碳碳双键的两个H原子及羧基中的碳原子一定共平面,羧基中两个氧原子与碳碳双键中的碳
氯化铵受热易分解,所以用蒸发结晶的操作分离方法最终不能得到NH Cl晶体,A错误;二氧化
4 原子一定共平面,旋转单键,富马酸12个原子可全部共平面,A正确;富马酸含有碳碳双键,与
锰和浓盐酸加热条件下生成氯气,B错误;图③操作中,酸式滴定管使用的正确操作为左手空握旋
化学 第1页(共5页) 24-63C
{#{QQABYQSAggioAAJAAAhCQwWQCgMQkBGCAKoGgBAAMAAAwQFABAA=}#}别为弱碱性,弱酸性,选用双指示剂指示终点,依次为酚酞、甲基红,A正确;无论HCl量为多
水发生加成反应,X的结构简式为 ,B正确;X含有羟基,Y属于钠盐,溶
少,Na与C的元素质量守恒一定为2c(Na+)=3[c(CO 2-)+c(HCO -)+c(H CO )], B正确;NaHCO
3 3 2 3 3
解 度 大 于 富 马 酸 , C 错 误 ; 富 马 酸 与 乙 二 醇 发 生 缩 聚 反 应 , 链 节 为 过量,实验Ⅱ中发生反应:Ca2++2HCO 3 -=CaCO 3 ↓+H 2 CO 3 ,C正确;V(CaCl 2 )=40mL说明CO 3 2-
已沉淀完全,c(Ca2+)= =0.05mol/L,c(CO 2-)=Ksp/c(Ca2+)=6.6×10-8,D错
3
,D正确。 0.1mol/L×0.04L-0.1mol/L×0.02L×0.5
误。 (0.02+0.04)L
11.B 16.B
N、O、F为同周期元素,随原子序数递增,第一电离能呈增大趋势,但氮原子最外层为半满稳定 往Na
2
S溶液中滴加Na
2
SO
3
溶液,无明显现象,是因为S2-在酸性环境中与SO
3
2-反应生成S,A错
结构,其第一电离能大于O,则第一电离能:OSi,非金属性越强,最高价氧化物对应水化物的酸性越强,则酸性: 由于溶液中水较少,看到白色固体,稀释时,需要将其加入水中,C错误;现象是先无明显现象,
HNO 3 >H 2 SiO 3 ,D正确。 后产生沉淀,原因是H 2 SO 3 被空气中的O 2 氧化,与BaCl 2 生成BaSO 4 沉淀, D错误。
12.C
研碎的目的是为了加快溶解,A正确;操作Ⅱ紫色石蕊在酸性溶液中显红色,操作Ⅴ可观察到溶液 17. (10分)
显紫色,B正确;操作Ⅲ稀硫酸为了促进酯的水解,如果用NaOH替代,需要中和过量的NaOH (1)3s23p2(1分)
溶液,否则FeCl 与NaOH反应,无法形成紫色溶液,C错误;Fe3++6C H OH [Fe(C H O) ]3- (2)abd(2分,选对1个不给分,选对2个给1分,全对2分,有错选不给分)
3 6 5 6 5 6
(紫色)+3H+,过量H+使平衡逆向移动,D正确。 a.Si-Cl键极性更大,则 Si-Cl键更易断裂,因此,SiCl
4
比CCl
4
易水解,a有关; b.Si的
13.B 原子半径更大,因此,SiCl 4 中的共用电子对更加偏向于Cl,从而导致Si-Cl键极性更大,且
根据甲室隔膜两侧溶液的浓度,Cu(2) 失去电子,故电极为负极,电极反应式为Cu-2e-=Cu2+,Cu(1) Si原子更易受到水电离的OH-的进攻,因此,SiCl 比CCl 易水解,b有关;c.通常键能越大
4 4
电极为正极,电极上发生得电子的还原反应,电极反应为Cu2++2e-=Cu,则电解槽中石墨(1)极为阴 化学键越稳定且不易断裂,因此,Si-Cl键键能更大不能说明Si-Cl更易断裂,故不能说明SiCl
4
极、石墨(2)极为阳极,A正确;当甲室两电极质量差为6.4g时,转移电子的物质的量为0.1mol, 比CCl 易水解,c无关;d.Si有更多的价层轨道,因此更易与水电离的OH-形成化学键,从
4
由2CH
2
=CHCN+2H++2e-=NC(CH
2
)
4
CN可知,制备0.05mol己二腈,B错误;根据乙室阳极、阴极 而导致SiCl
4
比CCl
4
易水解,d有关;
的反应,乙室选用阳离子交换膜,H+移向阴极,C 正确;石墨电极(1)的电极反应式为 (3)洪特规则(1分)
2CH
2
=CHCN+2H++2e-=NC(CH
2
)
4
CN,D正确。 (4)b(1分)
14.C (5)S O 2-中的中心原子S 的价层电子对数为4,无孤电子对,不能做配位原子;端基S原子含
2 3
根据能量-反应进程图,反应I△H
1
>反应Ⅱ△H
2
,A正确;平衡时,产物II能量低,为平衡时主要
有孤电子对,能做配位原子。(2分)
产物,B正确;平衡时,改变温度,对吸收、放出热量多的反应影响大,产物Ⅱ减小的幅度大于产
4M
(6)4(1分); ╳1021(2分)
物Ⅰ减小的程度,增大平衡n(产物Ⅰ)/n(产物Ⅱ)的比值,C错误;根据能量-反应进程图,第二 N
A
abc
步反应I的活化能较小,较短时间,产物I较多,D正确。 【解析】
15.D (1)基态硅原子的价层电子排布式为3s23p2
Na 2 CO 3 、NaHCO 3 混合溶液中滴加0.1mol/LHCl溶液,滴定终点分别为NaHCO 3 、H 2 CO 3 溶液,分 (2)a.Si-Cl键极性更大,则 Si-Cl键更易断裂,因此,SiCl 比CCl 易水解,a有关; b.Si
4 4
化学 第2页(共5页) 24-63C
{#{QQABYQSAggioAAJAAAhCQwWQCgMQkBGCAKoGgBAAMAAAwQFABAA=}#}的原子半径更大,因此,SiCl 中的共用电子对更加偏向于Cl,从而导致Si-Cl键极性更大, (4)根据题干信息,平衡[Cu(NH ) ]2+ Cu2++4NH 不易发生,加入浓盐酸,导致NH 与H+反
4 3 4 3 3
且Si原子更易受到水电离的OH-的进攻,因此,SiCl 比CCl 易水解,b有关;c.通常键能越 应,平衡正向移动,Cu2+与Cl-反应生成[CuCl ]2-(黄色)。
4 4 4
大化学键越稳定且不易断裂,因此,Si-Cl键键能更大不能说明Si-Cl更易断裂,故不能说明 (5)I 的CCl 层呈紫红色。根据题干信息,将CCl 层溶液转移入分液漏斗中,加入足量浓氢氧化
2 4 4
SiCl 比CCl 易水解,c无关;d.Si有更多的价层轨道,因此更易与水电离的OH-形成化学键, 钠溶液,充分振荡静置分液,I 因发生歧化反应进入水层,取上层溶液于烧杯中,滴加足量浓盐酸,
4 4 2
从而导致SiCl 比CCl 易水解,d有关; 发生归中反应,生成I 固体,过滤、洗涤、干燥可得单质碘 ;5I-+IO -+6H+=3I +3H O。
4 4 2 3 2 2
(3)洪特规则指出:基态原子中,填入简并轨道的电子总是先单独分占,且自旋平行。因此,违 19.(10分)
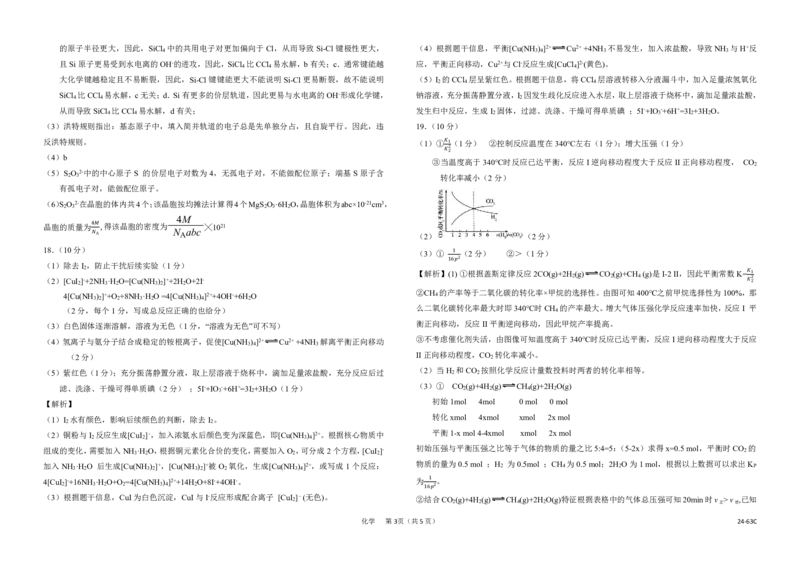
反洪特规则。 (1)① (1分) ②控制反应温度在340℃左右(1分);增大压强(1分)
1
(4)b 2
③当 2温度高于340℃时反应已达平衡,反应I逆向移动程度大于反应II正向移动程度, CO
2
(5)S O 2-中的中心原子S 的价层电子对数为4,无孤电子对,不能做配位原子;端基S原子含
2 3 转化率减小(2分)
有孤电子对,能做配位原子。
(6)S O 2-在晶胞的体内共4个;该晶胞按均摊法计算得4个MgS O ·6H O,晶胞体积为abc×10-21cm3,
2 3 2 3 2
4M
晶胞的质量为 得该晶胞的密度为 ╳1021
N abc
4 A (2) (2分)
A,
18.(10分)
(3)① (2分) ②>(1分)
(1)除去I
2
,防止干扰后续实验(1分) 1
2
【解析】1(16 )①根据盖斯定律反应2CO(g)+2H (g) CO (g)+CH (g)是I-2II,因此平衡常数K=
2 2 4
(2)[CuI 2 ]-+2NH 3 ·H 2 O=[Cu(NH 3 ) 2 ]++2H 2 O+2I- 1
2
②CH 的产率等于二氧化碳的转化率×甲烷的选择性。由图可知400℃之前甲烷选择性为100%, 那2
4[Cu(NH ) ]++O +8NH ·H O=4[Cu(NH ) ]2++4OH-+6H O 4
3 2 2 3 2 3 4 2
(2分,每个1分,写成总反应正确的也给分)
么二氧化碳转化率最大时即340℃时CH
4
的产率最大。增大气体压强化学反应速率加快,反应I 平
(3)白色固体逐渐溶解,溶液为无色(1分,“溶液为无色”可不写)
衡正向移动,反应II平衡逆向移动,因此甲烷产率提高。
(4)氢离子与氨分子结合成稳定的铵根离子,促使[Cu(NH ) ]2+ Cu2++4NH 解离平衡正向移动
③不考虑催化剂失活,由图像可知温度高于340℃时反应已达平衡,反应I逆向移动程度大于反应
3 4 3
(2分)
II正向移动程度,CO
2
转化率减小。
(5)紫红色(1分);充分振荡静置分液,取上层溶液于烧杯中,滴加足量浓盐酸,充分反应后过
(2)当H
2
和CO
2
按照化学反应计量数投料时两者的转化率相等。
滤、洗涤、干燥可得单质碘(2分) ;5I-+IO -+6H+=3I +3H O(1分) (3)① CO 2 (g)+4H 2 (g) CH 4 (g)+2H 2 O(g)
3 2 2
【解析】 初始1mol 4mol 0mol 0mol
(1)I 水有颜色,影响后续颜色的判断,除去I 。 转化xmol 4xmol xmol 2xmol
2 2
(2)铜粉与I 反应生成[CuI ]-,加入浓氨水后颜色变为深蓝色,即[Cu(NH ) ]2+。根据核心物质中 平衡1-xmol4-4xmol xmol 2xmol
2 2 3 4
组成的变化,需要加入NH ·H O,根据铜元素化合价的变化,需要加入O ,可分成2个方程,[CuI ]-
初始压强与平衡压强之比等于气体的物质的量之比5:4=5:(5-2x)求得x=0.5mol,平衡时CO
2
的
3 2 2 2
加入NH ·H O 后生成[Cu(NH ) ]+,[Cu(NH ) ]+被O 氧化,生成[Cu(NH ) ]2+,或写成1个反应:
物质的量为0.5mol ;H
2
为0.5mol ;CH
4
为0.5mol;2H
2
O为1mol,根据以上数据可以求出K
P
3 2 3 2 3 2 2 3 4
4[CuI ]-+16NH ·H O+O =4[Cu(NH ) ]2++14H O+8I-+4OH-。 为 。
2 3 2 2 3 4 2
1
(3)根据题干信息,CuI为白色沉淀,CuI与I-反应形成配合离子 [CuI 2 ]-(无色)。 ②1结6 合 2 CO 2 (g)+4H 2 (g) CH 4 (g)+2H 2 O(g)特征根据表格中的气体总压强可知20min时v 正 >v 逆 ,已知
化学 第3页(共5页) 24-63C
{#{QQABYQSAggioAAJAAAhCQwWQCgMQkBGCAKoGgBAAMAAAwQFABAA=}#}COOH
v
20
正
.
=
(
k 正
1
·
0
c(
分
CO
)
2 )·c4(H 2 ),v 逆 =k 逆 ·c(CH 4 )·c2(H 2 O),即
正 逆
>
C
C
H
O
4
2
·
·
2 4 (
(
H
H
2
2
O
)
) (5)
浓
浓
硫
HN
酸
O
Δ
3 NO 2
F
C
e
l 2
Cl
NO K 2 MnO
4
NO 2 Fe/HCl COO N H H 2
3
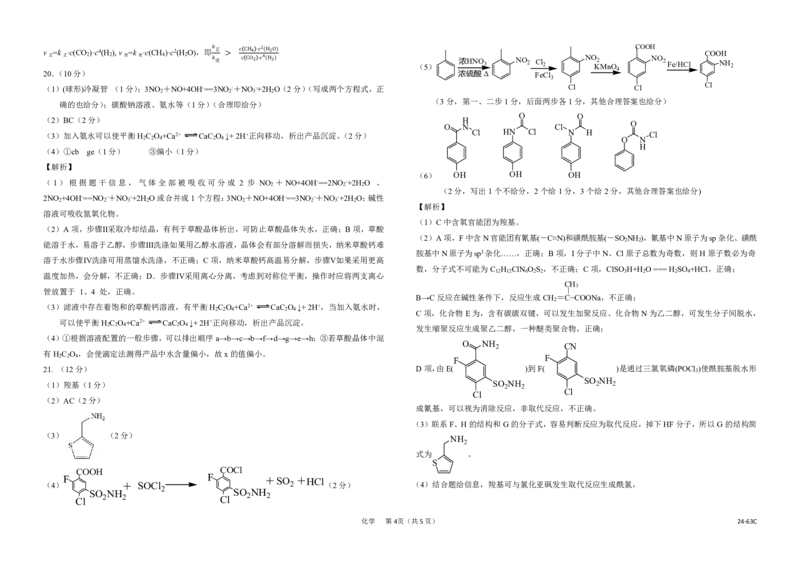
(1)(球形)冷凝管 (1分);3NO +NO+4OH-==3NO -+NO -+2H O(2分)(写成两个方程式,正 Cl Cl Cl
2 2 3 2
确的也给分);碳酸钠溶液、氨水等(1分)(合理即给分)
(3分,第一、二步1分,后面两步各1分,其他合理答案也给分)
O O
(2)BC(2分) H
O
O N Cl
(3)加入氨水可以使平衡H C O +Ca2+ CaC O ↓+2H+正向移动,析出产品沉淀。(2分) Cl HN Cl N H Cl
2 2 4 2 4 O N
H
(4)①cb ge(1分) ③偏小(1分)
【解析】
(6) OH OH OH
(1)根据题干信息,气体全部被吸收可分成 2 步 NO +NO+4OH-==2NO -+2H O 、
2 2 2
(2分,写出1个不给分,2个给1分,3个给2分,其他合理答案也给分)
2NO +4OH-==NO -+NO -+2H O或合并成1个方程:3NO +NO+4OH-==3NO -+NO -+2H O;碱性
2 2 3 2 2 2 3 2
【解析】
溶液可吸收氮氧化物。
(1)C中含氧官能团为羧基。
(2)A项,步骤Ⅱ采取冷却结晶,有利于草酸晶体析出,可防止草酸晶体失水,正确;B项,草酸
(2)A项,F中含N官能团有氰基(-C≡N)和磺酰胺基(-SO NH ),氰基中N原子为sp杂化、磺酰
2 2
能溶于水,易溶于乙醇,步骤Ⅲ洗涤如果用乙醇水溶液,晶体会有部分溶解而损失,纳米草酸钙难
胺基中N原子为sp3杂化……,正确;B项,I分子中N、Cl原子总数为奇数,则H原子数必为奇
溶于水步骤Ⅳ洗涤可用蒸馏水洗涤,不正确;C项,纳米草酸钙高温易分解,步骤Ⅴ如果采用更高
数,分子式不可能为C H ClN O S ,不正确;C项,ClSO H+H O===H SO +HCl,正确;
12 12 6 2 2 3 2 2 4
温度加热,会分解,不正确;D.步骤Ⅳ采用离心分离,考虑到对称位平衡,操作时应将两支离心
CH
3
管放置于 1、4 处,正确。 |
B→C反应在碱性条件下,反应生成CH =C−COONa,不正确;
2
(3)滤液中存在着饱和的草酸钙溶液,有平衡H C O +Ca2+ CaC O ↓+2H+,当加入氨水时,
2 2 4 2 4 C项,化合物E为,含有碳碳双键,可以发生加聚反应。化合物N为乙二醇,可发生分子间脱水,
可以使平衡H C O +Ca2+ CaC O ↓+2H+正向移动,析出产品沉淀。
2 2 4 2 4 发生缩聚反应生成聚乙二醇,一种醚类聚合物,正确;
(4)①根据溶液配置的一般步骤,可以排出顺序a→b→c→b→f→d→g→e→h;③若草酸晶体中混
O NH
2 CN
有H C O ,会使滴定法测得产品中水含量偏小,故x的值偏小。
2 2 4 F
F
21. (12分) D项,由E( )到F( )是通过三氯氧磷(POCl 3 )使酰胺基脱水形
SO NH
(1)羧基(1分) SO
2
NH
2
2 2
Cl
Cl
(2)AC(2分)
成氰基,可以视为消除反应,非取代反应,不正确。
(3)联系F、H的结构和G的分子式,容易判断反应为取代反应,掉下HF分子,所以G的结构简
(3) (2分)
NH
2
式为 。
S
COOH COCl
F F + SO +HCl
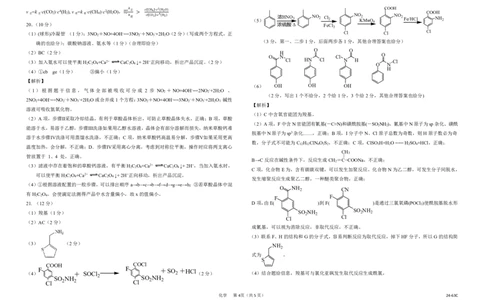
(4) + SOCl 2 (2分) (4)结合题给信息,羧基可与氯化亚砜发生取代反应生成酰氯,
2
SO NH SO NH
Cl 2 2 Cl 2 2
化学 第4页(共5页) 24-63C
{#{QQABYQSAggioAAJAAAhCQwWQCgMQkBGCAKoGgBAAMAAAwQFABAA=}#}COOH COCl
F F + SO +HCl
+ SOCl 2 。
2
Cl SO 2 NH 2 Cl SO 2 NH 2
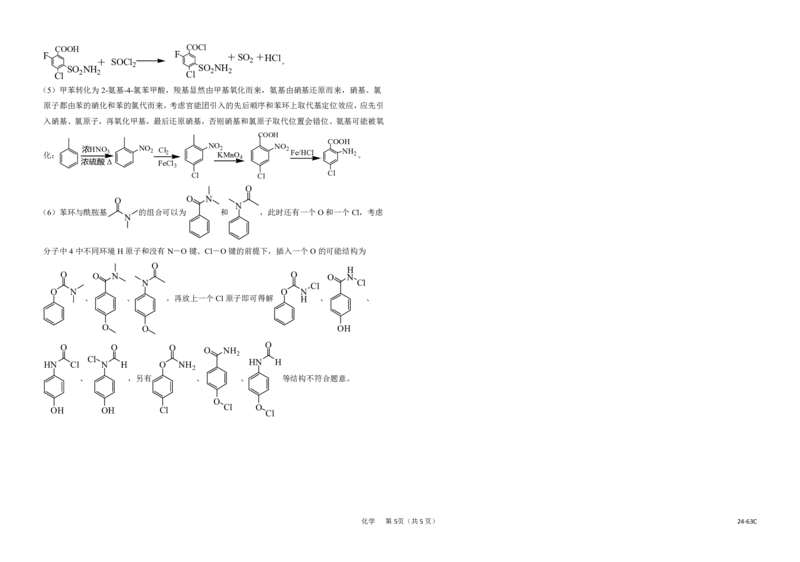
(5)甲苯转化为2-氨基-4-氯苯甲酸,羧基显然由甲基氧化而来,氨基由硝基还原而来,硝基、氯
原子都由苯的硝化和苯的氯代而来,考虑官能团引入的先后顺序和苯环上取代基定位效应,应先引
入硝基、氯原子,再氧化甲基,最后还原硝基,否则硝基和氯原子取代位置会错位、氨基可能被氧
COOH
COOH
化: 浓HNO 3 NO 2 Cl 2 NO K 2 MnO NO 2 Fe/HCl NH 2。
4
浓硫酸 Δ FeCl
3
Cl Cl Cl
O
O O N
N
(6)苯环与酰胺基 的组合可以为 和 ,此时还有一个O和一个Cl,考虑
N
分子中4中不同环境H原子和没有N-O键、Cl-O键的前提下,插入一个O的可能结构为
O
H
O O N O O N
N Cl
Cl
O N O N
、 、 。再放上一个Cl原子即可得解 H 、 、
O O OH
O
O O O
O NH
2
Cl
HN H
HN Cl N H O NH
2
、 ,另有 、 、 等结构不符合题意。
O
Cl O
OH OH Cl
Cl
化学 第5页(共5页) 24-63C
{#{QQABYQSAggioAAJAAAhCQwWQCgMQkBGCAKoGgBAAMAAAwQFABAA=}#}