文档内容
第二章 烃
第一节 烷烃
第1课时
1.关于CH 和 的叙述正确的是( )
4
A.均能用通式C H 来表示
n 2n+2
B.与所有烷烃互为同素异形体
C.通常情况下它们都是气态烷烃
D.因为它们结构相似,所以它们的化学性质相似,物理性质相同
【答案】A
【详解】
A. 的分子式是C H ,与甲烷均属于烷烃,均能用通式C H 表示,故A正确;
5 12 n 2n+2
B.同素异形体是指同种元素组成的不同单质,CH 和 都是化合物,不属于同素
4
异形体,故B错误;
C.碳原子数为1-4的烷烃常温下是气体, 为5个碳原子的烷烃,呈液态,故C
错误;
D.CH 和 二者C原子成键处于饱和,结构相似,化学性质相似,分子式不同,
4
物理性质不同,故D错误;
答案为A。
2.下列关于甲烷的说法正确的是
A.实验室可以用排水法收集甲烷
B.只有纯净甲烷才能在空气中安静燃烧
C.甲烷与溴水发生取代反应
D.甲烷在空气中燃烧只生成二氧化碳和水【答案】A
【详解】
甲烷难溶于水,可以用排水法收集,A项正确;甲烷与空气的混合物中甲烷的体积分数只要在爆炸极限之
外,甲烷就能安静燃烧,B项错误;甲烷与卤素单质发生取代反应的条件是光照,甲烷不能与溴水反应,
C项错误;在氧气不足条件下,甲烷燃烧会生成一氧化碳和水,D项错误。故选A。
3.(2020·紫金县第二中学高二期中)下列有机物中,不属于烃类的是( )
A.CHCH B.C H C.CHCl D.CH=CH
3 3 6 6 3 2 2
【答案】C
【详解】
A.CHCH 是乙烷,属于烃类,故A不符合题意;
3 3
B.C H 是苯,属于烃类,故B不符合题意;
6 6
C.CHCl是一氯甲烷,是卤代烃,故C符合题意;
3
D.CH=CH 是乙烯,属于烃类,故D不符合题意。
2 2
综上所述,答案为C。
4.(2020·紫金县第二中学高二期中)关于CH 和 的叙述错误的是( )
4
A.均能用组成通式C H 来表示
n 2n+2
B.互为同系物
C.它们都不能跟酸性高锰酸钾、强酸、强碱溶液发生反应
D.通常情况下它们都是气态烷烃
【答案】D
【详解】
A.两种物质分子中C原子的价电子全部形成化学键,二者都是烷烃,分子式符合烷烃分子式通式
C H ,A正确;
n 2n+2
B.它们都是属于烷烃,因此二者属于同系物,B正确;
C.它们都是属于烷烃,分子具有稳定性,不能使酸性高锰酸钾溶液褪色,也不能跟强酸、强碱溶液发生
反应,C正确;
D.CH 在常温下为气态, 分子中含有5个C原子,在常温下为液态,不是呈气态,D
4
错误;
故合理选项是D。
5.下列说法正确的是( )A.分子式符合C H 的不同物质一定互为同系物
n 2n+2
B.分子式符合C H 的烃不一定是烯烃
n 2n
C.烷烃、烯烃和炔烃都属于链状烃
D.芳香族化合物均具有香味
【答案】B
【详解】
A.分子式符合C H ,说明物质中碳原子均达到饱和状态,属于烷烃,如果碳原子数不同,则一定互为
n 2n+2
同系物,如碳原子数目相同,则为同分异构体,A不正确;
B.分子式符合C H 的烃可能是烯烃也可能是环烷烃,B正确;
n 2n
C.烷烃、烯烃和炔烃若分子中无环状结构,则属于链状烃,但分子中有环式结构,也可能是烯烃,如环
戊烯等,C不正确;
C.芳香族化合物指分子中含有苯环的有机物,它们并不一定具有香味,D不正确。
答案选B。
6.丁烷催化裂化时碳链按两种方式断裂,生成两种烷烃和两种烯烃。如果丁烷的裂化率为60%,且裂化
生成的两种烯烃物质的量相等,则裂化后得到的含氢质量分数最高的气体占混合气体的体积分数为
A.18.75% B.30% C.15% D.22.5%
【答案】A
【解析】分析:由题中信息可知,丁烷发生催化裂化时,碳链按两种方式断裂,生成两种烷烃和两种烯烃,
则两种烷烃是甲烷和乙烷,两种烯烃为乙烯和丙烯。裂化后得到的含氢质量分数最高的气体为甲烷。
详解:由题中信息可知,丁烷发生催化裂化时,碳链按两种方式断裂,生成两种烷烃和两种烯烃,则两种
烷烃是甲烷和乙烷,两种烯烃为乙烯和丙烯。如果丁烷的裂化率为60%,设丁烷的物质的量为1mol,,则
已裂化的丁烷有0.6mol、未裂化的丁烷有0.4mol。裂化生成的两种烯烃物质的量相等,则乙烯、乙烷、丙
烯和甲烷的物质的量均为0.6mol×0.5=0.3mol,故裂化后得到的含氢质量分数最高的甲烷占混合气体的体
0.3mol
积分数为 ×100%=18.75%。A正确,本题选A。
0.4mol+0.3mol×4
7.在20 ℃时,某气态烃与氧气混合,装入密闭容器中,点燃爆炸后,又恢复到20 ℃,此时容器内气体
的压强为反应前的一半,经NaOH溶液吸收后,容器内几乎成真空,此烃的分子式可能是( )
A.CH B.C H C.C H D.C H
4 2 6 3 8 7 16
【答案】C
【解析】
根据烃题意可知烃和氧气完全反应生成CO 气体,没有气体剩余,设烃的分子式为C H,发生的反应为:
2 x yC H+(x+y/4)O→xCO+(y/2)H O, 根据同温同容下,气体的压强比等于气体的物质的量之比可得
x y 2 2 2
1+x+y/4=2x,解得x=1+y/4,只有C中的C H 中的C和H个数符合此关系,故答案选C。
3 8
点睛:烃或烃的含氧衍生物燃烧的计算是一个难点,不管是单一烃还是混合烃,均可设其化学式为C H,
x y
然后根据燃烧的化学方程式和题中所给的有关数据列式,找到x和y之间的某种关系,若是混合烃,所求
的分子式为平均值,再根据平均值的概念判断烃的组成情况,解答此类题目时一是需要注意水的状态,二
是要熟练运用阿伏伽德罗定律的两个重要推论:同温同压下,气体的体积比等于气体的物质的量之比;同
温同容下,气体的压强比等于气体的物质的量之比。
8.有机物M、N的结构简式如图所示。下列说法错误的是()
A.M、N都不能使酸性高锰酸钾溶液退色
B.M有两种同分异构体
C.M、N分子中每个碳原子都形成4个共价键
D.等质量的M、N在足量氧气中燃烧,完全燃烧时生成 的质量相同
【答案】D
【详解】
A. M和N都是烷烃,不能与酸性高锰酸钾溶液反应,A项正确;
B. M是新戊烷,有两种同分异构体: 、 ,B项正确;
C. 观察M、N分子,每个碳原子形成4个共价键,C项正确;
D. M的分子式是 的分子式是 ,M、N的最简式不同,等质量的M、N在足量氧气中燃烧,
生成 的物质的量不同,D项错误;
答案选D。
9.(2020·四川省南充高级中学高二期中)液化石油气的主要成分是丙烷和丁烷,下列有关的叙述中正确
的是
A.丙烷分子中碳原子在一条直线上
B.光照下,丙烷和丁烷均可以和溴水发生取代反应
C.丙烷比丁烷更易液化D.丙烷的二氯代物有4种同分异构体
【答案】D
【详解】
A.烷烃分子中有多个碳原子应呈锯齿形,丙烷呈角形,碳原子不在一条直线上,A错误;
B.丙烷等烷烃在光照的条件下可以和气态卤单质发生取代反应,跟卤水(像氯水,溴水等)不反应,B错误;
C.烷烃中碳个数越多沸点越高,丙烷分子中碳原子数小于丁烷,故丁烷沸点高,更易液化,C错误;
D.丙烷的碳链结构为C—C—C,2个Cl可以分别在两端的碳原子上,或者在中间和一端的碳原子上,也
可以同时在中间的碳原子上或者同时在一端的碳原子上,一共4种,D正确。故选D。
10.(2020·兴安县第三中学高二月考)下列说法正确的是
A.分子组成相差一个或几个“-CH-”原子团的物质互为同系物.
2
B.不带支链的烃其分子都是直线型的
C.甲烷是烷烃中碳的含量最低的,也是最简单的烃
D.常温时烷烃的同系物只有四种呈气态
【答案】C
【详解】
A.分子组成相差一个或几个“-CH-”原子团的物质,不一定是同系物,结构不一定相似,如甲烷与乙醇,
2
故A错误;
B.不带支链的含有多个碳原子的烷烃,其碳链是锯齿状,不是直线形;苯属于烃类,不带支链但分子构
型为平面形等,故B错误;
C.甲烷是最简单的烃,分子中1个碳原子结合4个氢原子,氢原子含量最高,故碳的含量最低,故C正
确;
D.常温时,甲烷、乙烷、丙烷、丁烷都是气体,戊烷的同分异构体新戊烷支链多,沸点较低,在常温下
也是气体,故D错误;
答案选C。
11.(2020·云南省玉溪第一中学高二月考)正己烷是优良的有机溶剂,其球棍模型如图所示。下列有关说
法正确的是
A.正己烷的分子式为C H ,其沸点比丙烷低
6 12
B.己烷有5种同分异构体C.正己烷能与溴水发生取代反应而使溴水褪色
D.正己烷所有碳原子可在一条直线上
【答案】B
【详解】
A.正己烷的分子式为C H ,故A错误;
6 14
B.己烷有5种同分异构体,分别是:
1、正己烷 :CH CH CH CH CH CH ;
2、2,2-二甲基丁烷₃ :C₂H C₂(CH₂ ) C₂H C₃H ;
3、2-甲基戊烷: CH CH₃CH C₃H₂(CH₂) ;₃
4、2,3-二甲基丁烷:₃CH₂CH(₂CH )CH₃(C₂H )CH ;
5、3-甲基戊烷:CH CH₃CH(CH₃)CH CH₃; ₃
故B正确; ₃ ₂ ₃ ₂ ₃
C.正己烷不能与溴水发生反应,故C错误;
D.由球棍模型可以看出,正己烷所有碳原子不在一条直线上,故D错误;
故选B。
12.关于烷烃的叙述不正确的是 ( )
A.分子式符合C H 的烃一定是烷烃
n 2n+2
B.烷烃均能与氯水发生取代反应
C.正戊烷的熔沸点比异戊烷的高
D.烷烃不能被酸性高锰酸钾等强氧化剂氧化
【答案】B
【分析】
对烷烃的概念应从“单键、饱和、链状”三方面理解。
【详解】
A. 分子式符合C H 的烃中碳原子均已饱和,A项正确;
n 2n+2
B. 烷烃的化学性质与甲烷相似,取代反应必须与纯卤素单质反应,B项错误;
C. 同分异构体中,支链越多,沸点越低,则正戊烷的熔、沸点比异戊烷的高,C项正确;
D. 烷烃均由单键组成,性质相对稳定,不能被酸性高锰酸钾溶液等强氧化剂氧化,D项正确;
答案选B。
13.(2020·辽宁高一期末)下列关于有机化合物M(如图)的说法中,不正确的是( )A.与甲烷互为同系物
B.M有同分异构体
C.不能使酸性高锰酸钾溶液褪色
D.光照时,能与Cl 发生取代反应
2
【答案】B
【详解】
A.该物质分子中碳原子之间以单键结合形成链状,其余价电子全部与H原子结合,达到结合H原子的最
大数目,因此属于烷烃,其为丙烷,与甲烷属于同系物,A说法正确;
B.根据图示可知该物质分子式是C H,没有同分异构体,B说法错误;
3 8
C.该物质属于烷烃,不能被酸性高锰酸钾溶液氧化,因此不能使酸性高锰酸钾溶液褪色,C说法正确;
D.该物质属于烷烃,在光照时,能与Cl 发生取代反应,D说法正确;
2
故合理选项是B。
14.(2020·长葛市第一高级中学高三月考)如图表示4个碳原子相互结合的方式。小球表示碳原子,小棍
表示化学键,假如碳原子上其余的化学键都是与氢结合。
(1)图中属于烷烃的是________(填编号)
(2)图中属于甲烷同系物的是________(填编号)
(3)图中与B互为同分异构体的是________(填编号)
【答案】AC AC EFH
【分析】
由球棍模型得出A、B、C、D、E、F、G、H的结构简式分别为CHCHCHCH、CHCH=CHCH 、
3 2 2 3 3 3
(CH)CCH、CHC≡CCH、CHCHCH=CH、(CH)C=CH 、CHCHC≡CH、 。
3 3 3 3 3 3 2 2 3 2 2 3 2【详解】
(1)图中属于烷烃的是分子中不含有不饱和键的链状烃,故选AC。答案为:AC;
(2)图中属于甲烷同系物的是分子中只含有单键的链状烃(甲烷除外),故选AC。答案为:AC;
(3)图中B的分子式为C H,与B互为同分异构体的是EFH。答案为:EFH。
4 8
15.某烷烃和单烯烃的混合气体2.24L,将其完全燃烧,产生的气体缓缓通过浓硫酸,浓硫酸增重4.05克,将剩
余气体通入碱石灰,碱石灰质量增加了6.60克,另取该混合气体2.24L通过过量溴水,溴水质量增加了1.05克。
(1)混合气体由哪两种烃组成____?
(2)两种烃的体积分数各是多少______?
【答案】CH 和C H CH:75%,C H:25%
4 3 6 4 3 6
【分析】
根据有机物燃烧时,有机物中的碳全部转化为二氧化碳,其质量可以根据澄清石灰水质量增加量来确定,
有机物中的氢全部转化为水,其质量可以根据浓硫酸质量增加来确定,烯烃和溴单质能发生加成反应,溴
水质量增加量就是烯烃的质量,根据水以及二氧化碳的量可以确定碳和氢原子的个数之比。
【详解】
(1)混合气体的物质的量为 =0.1mol;燃烧后通过浓HSO ,增重的质量即水的质量为4.05g,
2 4
即 =0.225mol,再通过碱石灰,增重的质量即生成CO 的质量为6.60g,即 =0.15mol;
2
取0.1mol混合物通入溴水,增重的质量即烯烃的质量为1.05g.所以设烷烃、烯烃分别为C H 、C H ,
x 2x+2 y 2y
且两种烃的物质的量分别为a,b,则有:1.05g=14yg/mol×b;a+b=0.1mol;(2x+2)a+2yb=0.225mol×2((H守
恒);ax+by=0.15mol(C守恒);解得x=1,y=3,a=0.075mol,b=0.025mol,所以烷烃为CH;
4
(2)烯烃为C H,CH 的体积分数为 ×100%=75%;C H 的体积分数为
3 6 4 3 6
×100%=25%。
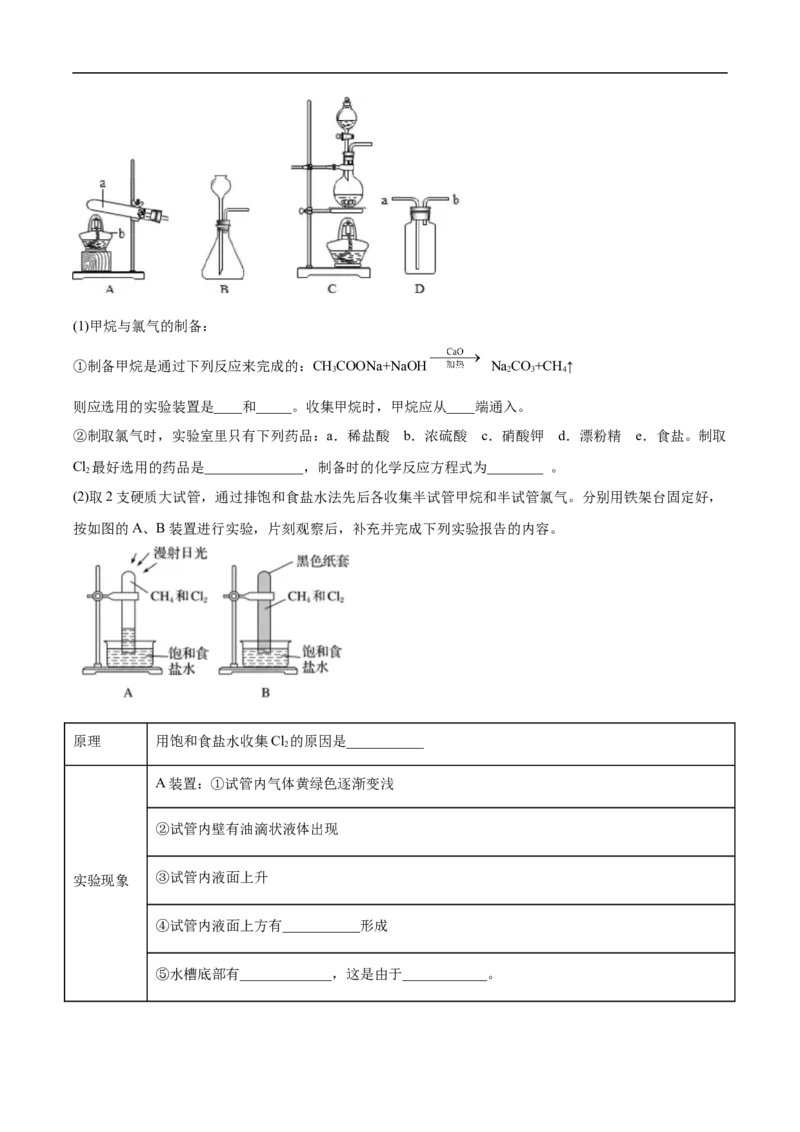
16.(2020·四川省广汉中学高三月考)甲烷是天然气、沼气、油田气和煤矿坑道气的主要成分。某兴趣小
组利用下列装置来制取甲烷,并探究其与氯气反应的条件。(1)甲烷与氯气的制备:
①制备甲烷是通过下列反应来完成的:CHCOONa+NaOH Na CO+CH ↑
3 2 3 4
则应选用的实验装置是____和_____。收集甲烷时,甲烷应从____端通入。
②制取氯气时,实验室里只有下列药品:a.稀盐酸 b.浓硫酸 c.硝酸钾 d.漂粉精 e.食盐。制取
Cl 最好选用的药品是______________,制备时的化学反应方程式为________ 。
2
(2)取2支硬质大试管,通过排饱和食盐水法先后各收集半试管甲烷和半试管氯气。分别用铁架台固定好,
按如图的A、B装置进行实验,片刻观察后,补充并完成下列实验报告的内容。
原理 用饱和食盐水收集Cl 的原因是___________
2
A装置:①试管内气体黄绿色逐渐变浅
②试管内壁有油滴状液体出现
实验现象 ③试管内液面上升
④试管内液面上方有___________形成
⑤水槽底部有_____________,这是由于____________。B装置:___________
结论 CH 与Cl 在_________条件下才能发生化学反应
4 2
【答案】A D b b、d、e Ca(ClO) +2NaCl+2HSO =CaSO +Na SO +2Cl↑+2H O 用饱和食
2 2 4 4 2 4 2 2
盐水收集Cl 的原因是增大c(Cl-),能使化学平衡Cl+H O H++ Cl-+HClO向左移动;使溶解平衡Cl(g)
2 2 2 2
Cl(aq)向气体方向移动,从而抑制Cl 的溶解 试管内液面上方有少量白雾形成 水槽底部有白
2 2
色晶体析出 这是由于饱和食盐水中存在结晶溶解平衡:Cl- (aq)+Na+(aq) NaCl(s)。生成的HCl
溶于饱和食盐水中,c(Cl-)增大,结晶溶解平衡向结晶方向移动,析出了NaCl晶体。 无明显现象
CH 与Cl 在光照条件下才能发生化学反应
4 2
【分析】
(1)①根据制取物质的存在状态和反应条件判断使用的装置,根据气体密度大小判断收集方法;
②从节能、环保角度分析制取氯气的方法;
(2)根据氯气与水反应的可逆性,结合平衡移动原理及物质的颜色、状态、溶解性等分析解答。
【详解】
(1)①根据反应原理可知:用固体混合物在加热条件下反应制取气体,则应该选择装置A来制取甲烷;由于
甲烷的密度比空气小,因此应该选择向下排空气的方法收集甲烷气体,选择D装置进行收集,收集气体时
要短管进长管出,甲烷气体由b端进入集气瓶中;
②根据题目已知物质,从节能、环保角度分析可知:最好选用浓硫酸、漂粉精 、食盐混合,在常温下制
取Cl。在酸性条件下,这三种物质产生的Cl-、ClO-、H+在溶液中发生氧化还原反应产生Cl,浓硫酸具有
2 2
酸性、吸水性,浓硫酸溶于水会放出大量热,降低Cl 在溶液中的溶解而逸出,故合理选项是bde。用这种
2
方法制备Cl 时的化学反应方程式为:Ca(ClO) +2NaCl+2HSO =CaSO +Na SO +2Cl↑+2H O;
2 2 2 4 4 2 4 2 2
(2)用饱和食盐水收集Cl,可以除去Cl 中杂质HCl,同时也可以减少Cl 的消耗,这是由于Cl 在水中存在
2 2 2 2
化学平衡:Cl+H O H++Cl-+HClO,水中溶解食盐,增大了c(Cl-),使化学平衡逆向移动,溶解平衡
2 2
Cl(g) Cl(aq)逆向移动,从而抑制Cl 的溶解,有利于Cl 的收集;
2 2 2 2
在A装置中,Cl 与CH 在光照条件下发生取代反应产生HCl及CHCl、CHCl、CHCl 、CCl ,反应消耗
2 4 3 2 2 3 4
Cl,使试管内气体黄绿色逐渐变浅,同时由于气体消耗,水槽中的水在大气压强作用下进入试管,试管内
2
的液面不断上升。在产生的有机物中,只有CHCl是气体,CHCl、CHCl 、CCl 都呈液态,这些物质不
3 2 2 3 4
溶于水,使试管内壁有油滴状液体出现;HCl气体遇水蒸气形成盐酸小液滴,使试管内液面上方有少量白雾形成;
由于饱和食盐水中存在结晶溶解平衡:Cl- (aq)+Na+(aq) NaCl(s)。当生成的HCl溶于饱和食盐水中
时,使溶液中c(Cl-)增大,导致溶解结晶平衡向结晶方向移动,因此在水槽底部会析出NaCl晶体,所以水
槽底部有白色晶体析出;
通过上述实验现象证明CH 与Cl 在光照条件下能发生取代反应,
4 2
【点睛】
本题考查了氯气的实验室制取方法及Cl 与甲烷在光照条件下发生取代反应的现象分析。掌握物质的性质、
2
反应条件,根据平衡移动原理分析解答。