文档内容
第二课时 影响化学反应速率的因素基础练习题
1.下列事实能说明影响化学反应速率的决定性因素是反应物本身性质的是 ( )
A.Cu能与浓硝酸反应,而不与浓盐酸反应
B.Cu与浓硝酸反应比与稀硝酸反应快
C.N 与O 在常温、常压下不反应,放电时可反应
2 2
D.Cu与浓HSO 能反应,而不与稀HSO 反应
2 4 2 4
2.反应2A(g) 2B(g)+C(g)△H>0,达平衡时,要使A的浓度增大、v 增大,应采取的措施是 ( )
正
A.降温 B.加催化剂 C.升温 D.加压
3.对于反应:C(s)+2NO(g) N(g)+CO (g),下列说法正确的是 ( )
2 2
A.降低温度能加快反应速率
B.增加NO的浓度能减慢反应速率
C.使用恰当的催化剂能加快反应速率
D.加入足量的活性炭可以实现NO的100%转化
4.把镁条投入盛有盐酸的敞口容器里,产生氢气的速率变化如图所示。下列影响反应的因素有 ( )
①盐酸的浓度 ②镁条的表面积 ③溶液的温度 ④Cl-的浓度
A.①④ B.③④ C.①②③ D.②③④
5.(双选)将盐酸滴到NaCO 粉末上,能使反应的最初速率加快的是( )
2 3
A.盐酸浓度不变,使用量增大一倍帕
B.盐酸浓度增加一倍,用量减至原来的一半
C.增大NaCO 粉末的量
2 3
D.使反应在较高温度下进行
6.硫代硫酸钠溶液与稀硫酸反应的化学方程式为:NaSO+H SO =Na SO +SO+S↓+H O,下列各组实验中最先出现浑
2 2 3 2 4 2 4 2 2
浊的是( )
NaSO 溶液 稀HSO HO
实验 反应温度/℃ 2 2 3 2 4 2
V/mL c/(mol·L-1) V/mL c/(mol·L-1) V/mL
A 25 5 0.1 10 0.1 5
B 25 5 0.2 5 0.2 10
C 35 5 0.15 5 0.15 5
D 35 5 0.2 5 0.2 20
7.在恒温恒容的密闭容器中发生可逆反应:2NO(g)+O (g) 2NO (g)。其他条件相同时,按下列各组投料进行反应,
2 2
平衡时反应速率最快的是( )
A.2 mol NO 和1molO B.1 mol NO和1molO C.1 mol NO和2molO D.2 mol NO和1molO
2 2 2 2 2
8.反应C(s)+CO(g)=2CO(g)为吸热反应,反应速率为v,反应N(g)+3H(g)=2NH (g)为放热反应,反应速率为v 。对于
2 1 2 2 3 2
上述反应,当温度升高时,v 和v 的变化情况为( )
1 2
A.均增大 B.均减小 C.v 增大,v 减小 D.v 减小,v 增大
1 2 1 2
9.反应C(s)+HO(g) CO(g)+H(g)在一容积可变的密闭容器中进行,下列条件的改变能够引起反应速率增大的是(
2 2
)
A.增加C(s)的量
B.将容器的容积缩小一半
C.保持容器容积不变,充入Ar使体系压强增大
D.保持压强不变,充入Ar使容器容积增大
10.下列关于化学反应速率的说法中不正确的是( )
A.同时改变两个变量来研究反应速率的变化,能更快得出有关规律
B.反应速率的大小与吸、放热无关
C.一定条件下,使用催化剂能加快反应速率
D.相同温度下,H(g)+CO (g) CO(g)+HO(g)中,密闭容器中两种反应物浓度为0.020mol·L-1的反应速率大于两种
2 2 2
反应物浓度为0.010mol·L-1的反应速率
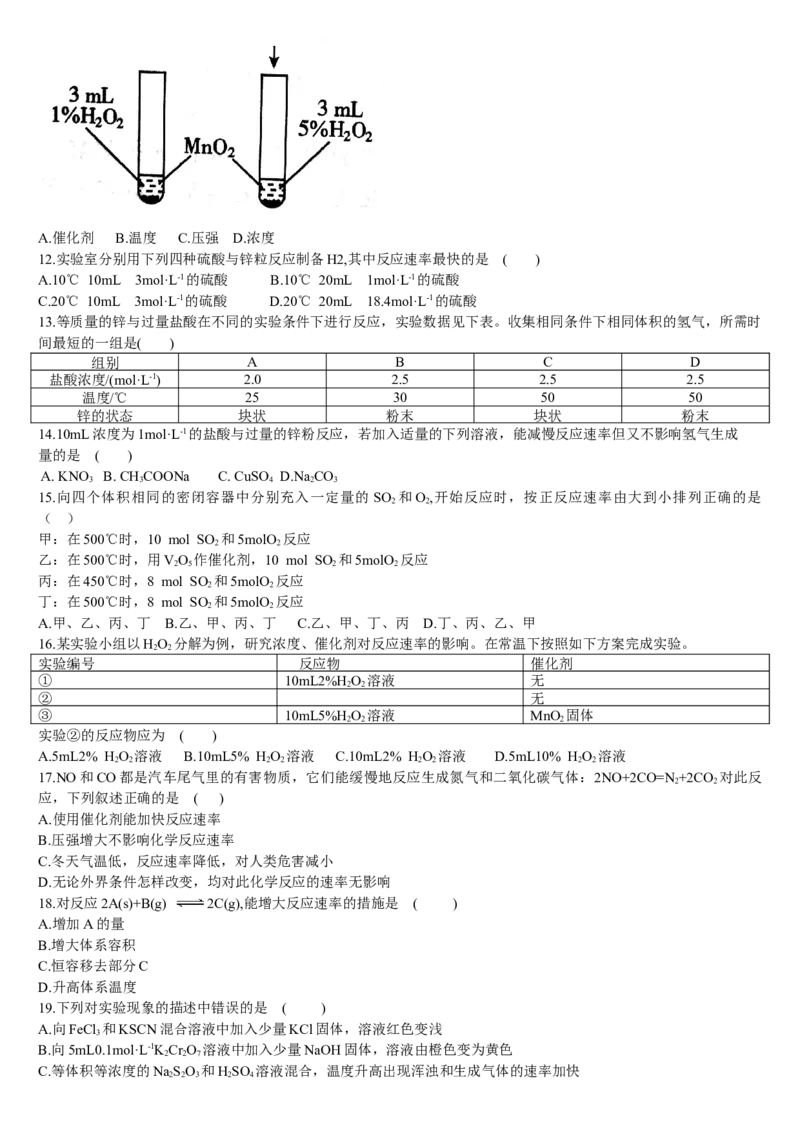
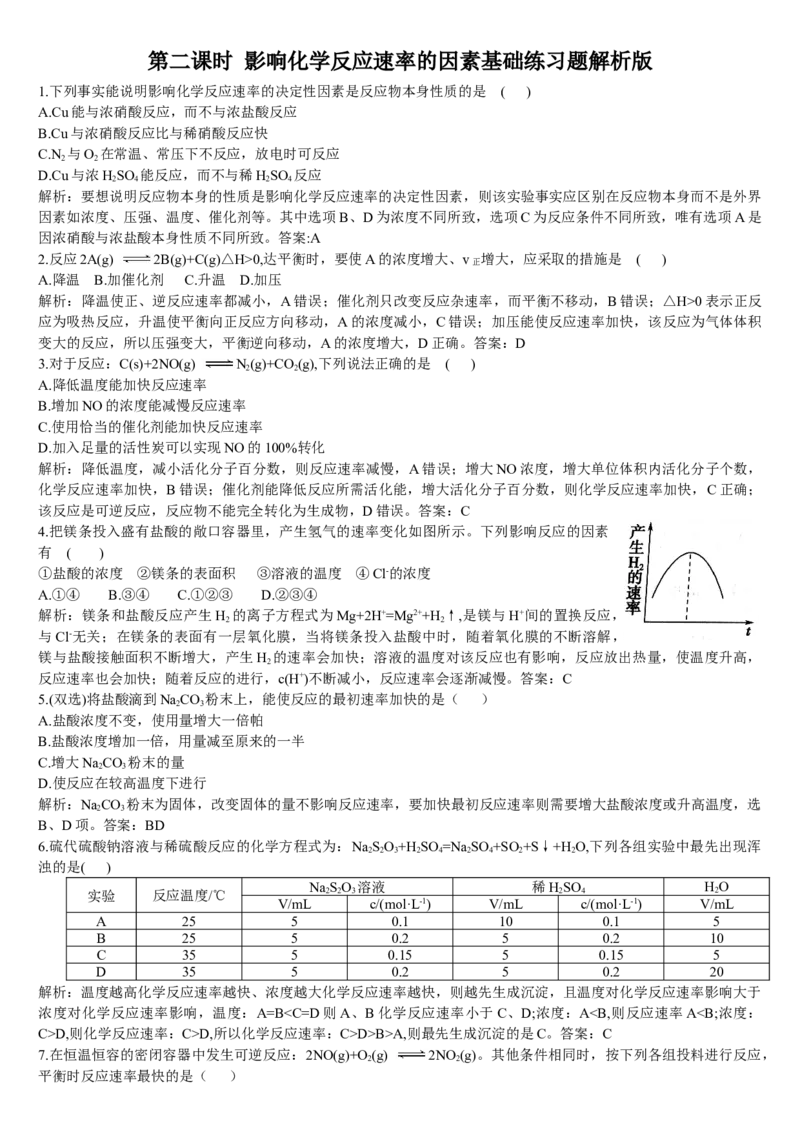
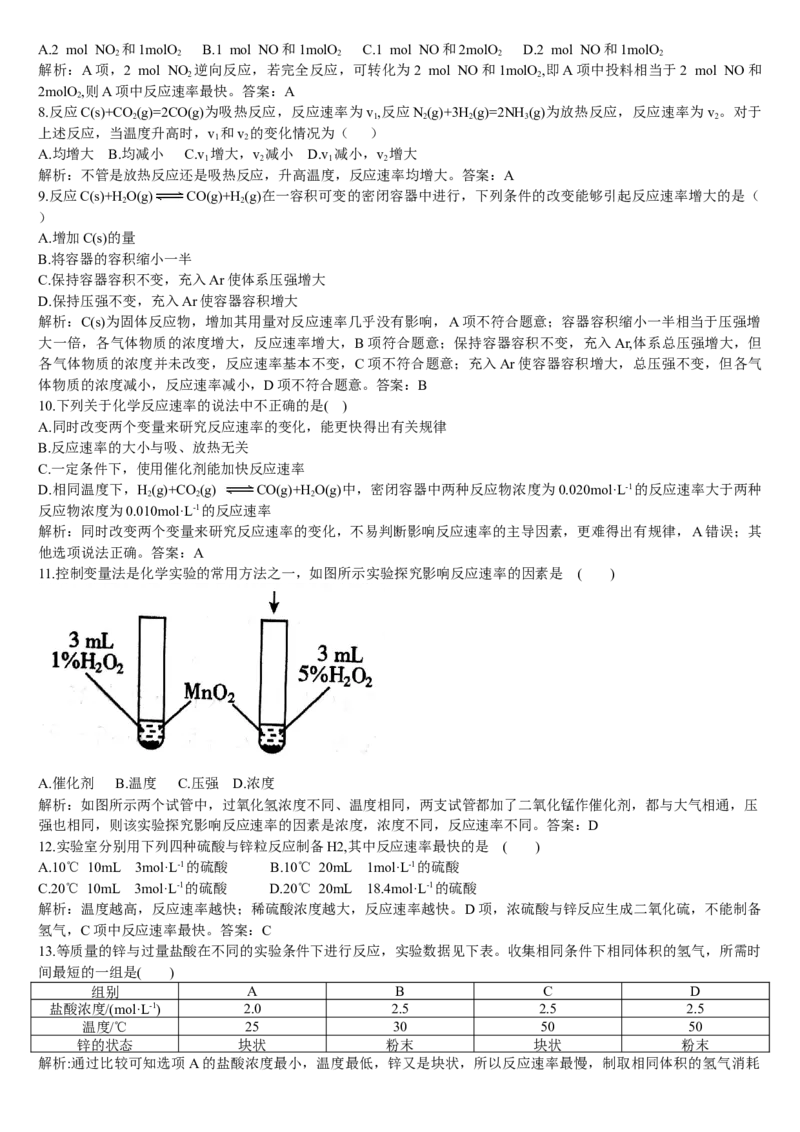
11.控制变量法是化学实验的常用方法之一,如图所示实验探究影响反应速率的因素是 ( )A.催化剂 B.温度 C.压强 D.浓度
12.实验室分别用下列四种硫酸与锌粒反应制备H2,其中反应速率最快的是 ( )
A.10℃ 10mL 3mol·L-1的硫酸 B.10℃ 20mL 1mol·L-1的硫酸
C.20℃ 10mL 3mol·L-1的硫酸 D.20℃ 20mL 18.4mol·L-1的硫酸
13.等质量的锌与过量盐酸在不同的实验条件下进行反应,实验数据见下表。收集相同条件下相同体积的氢气,所需时
间最短的一组是( )
组别 A B C D
盐酸浓度/(mol·L-1) 2.0 2.5 2.5 2.5
温度/℃ 25 30 50 50
锌的状态 块状 粉末 块状 粉末
14.10mL浓度为1mol·L-1的盐酸与过量的锌粉反应,若加入适量的下列溶液,能减慢反应速率但又不影响氢气生成
量的是 ( )
A. KNO B. CH COONa C. CuSO D.NaCO
3 3 4 2 3
15.向四个体积相同的密闭容器中分别充入一定量的 SO 和O,开始反应时,按正反应速率由大到小排列正确的是
2 2
( )
甲:在500℃时,10 mol SO 和5molO 反应
2 2
乙:在500℃时,用VO 作催化剂,10 mol SO 和5molO 反应
2 5 2 2
丙:在450℃时,8 mol SO 和5molO 反应
2 2
丁:在500℃时,8 mol SO 和5molO 反应
2 2
A.甲、乙、丙、丁 B.乙、甲、丙、丁 C.乙、甲、丁、丙 D.丁、丙、乙、甲
16.某实验小组以HO 分解为例,研究浓度、催化剂对反应速率的影响。在常温下按照如下方案完成实验。
2 2
实验编号 反应物 催化剂
① 10mL2%H O 溶液 无
2 2
② 无
③ 10mL5%H O 溶液 MnO 固体
2 2 2
实验②的反应物应为 ( )
A.5mL2% HO 溶液 B.10mL5% HO 溶液 C.10mL2% HO 溶液 D.5mL10% HO 溶液
2 2 2 2 2 2 2 2
17.NO和CO都是汽车尾气里的有害物质,它们能缓慢地反应生成氮气和二氧化碳气体:2NO+2CO=N +2CO 对此反
2 2
应,下列叙述正确的是 ( )
A.使用催化剂能加快反应速率
B.压强增大不影响化学反应速率
C.冬天气温低,反应速率降低,对人类危害减小
D.无论外界条件怎样改变,均对此化学反应的速率无影响
18.对反应2A(s)+B(g) 2C(g),能增大反应速率的措施是 ( )
A.增加A的量
B.增大体系容积
C.恒容移去部分C
D.升高体系温度
19.下列对实验现象的描述中错误的是 ( )
A.向FeCl 和KSCN混合溶液中加入少量KCl固体,溶液红色变浅
3
B.向5mL0.1mol·L-1KCr O 溶液中加入少量NaOH固体,溶液由橙色变为黄色
2 2 7
C.等体积等浓度的NaSO 和HSO 溶液混合,温度升高出现浑浊和生成气体的速率加快
2 2 3 2 4D.酸性KMnO 溶液中滴加HC O,H C O 浓度越大,褪色和生成气体的速率越快
4 2 2 4 2 2 4
20. 2SO +O 2SO 是接触法制硫酸工艺中的重要反应,下列关于该反应的说法中错误的是 ( )
2 2 3
A.增加SO 的浓度能加快该反应的速率
2
B.通常使用铁作催化剂
C.降低体系温度会减慢该反应的速率
D.使用催化剂能改变该反应的速率
21.在一密闭容器中,充入1molN 和3molH ,并在一定温度和压强下,使其发生反应:N(g)+3H(g) 2NH (g)
2 2 2 2 3
△H=-92.4kJ·mol-1。回答下列问题:
(1)若保持容器容积不变,再向其中充入1molN ,反应速率会 (填“加快”“减慢”或“不变”,下同),理
2
由是
(2)若保持容器容积不变,再向其中充入1 mol He,反应速率会 ,理由是 。
(3)若保持容器内气体压强不变,再向其中充入1 mol He,反应速率会 ,理由是 。
(4)加入催化剂,反应速率会 。
22.某研究性学习小组利用HC O 溶液和酸性KMnO 溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,
2 2 4 4
实验如下:
KMnO 溶液 HC O 溶液 HO 溶液褪色时间
实验序号 实验温度 4 2 2 4 2
V(mL) c (mol·L-1) V(mL) c (mol·L-1) V(mL) t(s)
A 293K 2 0.02 4 0.1 0 t
1
B T 2 0.02 3 0.1 V 8
1 1
C 313K 2 0.02 V 0.1 1 t
2 2
(1)通过实验A、B,可探究出 的改变对反应速率的影响,其中V= ,T= ,通过实验 可
1 1
探究出温度变化对化学反应速率的影响。
(2)若t<8,则由实验A、B可以得出的结论是 ;
1
利用实验B中数据计算,从反应开始到结束,用KMnO 的浓度变化表示的反应速率为 。
4
(3)该反应中有无色无味气体产生,且锰被还原为Mn2+写出相应反应的离子方程式:
(4)该小组的一位同学通过查阅资料发现:反应一段时间后该反应速率会加快,造成此种变化的原因是反应体系中的某
种粒子对KMnO 与HC O 之间的反应有某种特殊的作用,则该作用是 ,相应的粒子最有可能是
4 2 2 4
(填符号)第二课时 影响化学反应速率的因素基础练习题解析版
1.下列事实能说明影响化学反应速率的决定性因素是反应物本身性质的是 ( )
A.Cu能与浓硝酸反应,而不与浓盐酸反应
B.Cu与浓硝酸反应比与稀硝酸反应快
C.N 与O 在常温、常压下不反应,放电时可反应
2 2
D.Cu与浓HSO 能反应,而不与稀HSO 反应
2 4 2 4
解析:要想说明反应物本身的性质是影响化学反应速率的决定性因素,则该实验事实应区别在反应物本身而不是外界
因素如浓度、压强、温度、催化剂等。其中选项B、D为浓度不同所致,选项C为反应条件不同所致,唯有选项A是
因浓硝酸与浓盐酸本身性质不同所致。答案:A
2.反应2A(g) 2B(g)+C(g)△H>0,达平衡时,要使A的浓度增大、v 增大,应采取的措施是 ( )
正
A.降温 B.加催化剂 C.升温 D.加压
解析:降温使正、逆反应速率都减小,A错误;催化剂只改变反应杂速率,而平衡不移动,B错误;△H>0表示正反
应为吸热反应,升温使平衡向正反应方向移动,A的浓度减小,C错误;加压能使反应速率加快,该反应为气体体积
变大的反应,所以压强变大,平衡逆向移动,A的浓度增大,D正确。答案:D
3.对于反应:C(s)+2NO(g) N(g)+CO (g),下列说法正确的是 ( )
2 2
A.降低温度能加快反应速率
B.增加NO的浓度能减慢反应速率
C.使用恰当的催化剂能加快反应速率
D.加入足量的活性炭可以实现NO的100%转化
解析:降低温度,减小活化分子百分数,则反应速率减慢,A错误;增大NO浓度,增大单位体积内活化分子个数,
化学反应速率加快,B错误;催化剂能降低反应所需活化能,增大活化分子百分数,则化学反应速率加快,C正确;
该反应是可逆反应,反应物不能完全转化为生成物,D错误。答案:C
4.把镁条投入盛有盐酸的敞口容器里,产生氢气的速率变化如图所示。下列影响反应的因素
有 ( )
①盐酸的浓度 ②镁条的表面积 ③溶液的温度 ④Cl-的浓度
A.①④ B.③④ C.①②③ D.②③④
解析:镁条和盐酸反应产生H 的离子方程式为Mg+2H+=Mg2++H ↑,是镁与H+间的置换反应,
2 2
与Cl-无关;在镁条的表面有一层氧化膜,当将镁条投入盐酸中时,随着氧化膜的不断溶解,
镁与盐酸接触面积不断增大,产生H 的速率会加快;溶液的温度对该反应也有影响,反应放出热量,使温度升高,
2
反应速率也会加快;随着反应的进行,c(H+)不断减小,反应速率会逐渐减慢。答案:C
5.(双选)将盐酸滴到NaCO 粉末上,能使反应的最初速率加快的是( )
2 3
A.盐酸浓度不变,使用量增大一倍帕
B.盐酸浓度增加一倍,用量减至原来的一半
C.增大NaCO 粉末的量
2 3
D.使反应在较高温度下进行
解析:NaCO 粉末为固体,改变固体的量不影响反应速率,要加快最初反应速率则需要增大盐酸浓度或升高温度,选
2 3
B、D项。答案:BD
6.硫代硫酸钠溶液与稀硫酸反应的化学方程式为:NaSO+H SO =Na SO +SO+S↓+H O,下列各组实验中最先出现浑
2 2 3 2 4 2 4 2 2
浊的是( )
NaSO 溶液 稀HSO HO
实验 反应温度/℃ 2 2 3 2 4 2
V/mL c/(mol·L-1) V/mL c/(mol·L-1) V/mL
A 25 5 0.1 10 0.1 5
B 25 5 0.2 5 0.2 10
C 35 5 0.15 5 0.15 5
D 35 5 0.2 5 0.2 20
解析:温度越高化学反应速率越快、浓度越大化学反应速率越快,则越先生成沉淀,且温度对化学反应速率影响大于
浓度对化学反应速率影响,温度:A=BD,则化学反应速率:C>D,所以化学反应速率:C>D>B>A,则最先生成沉淀的是C。答案:C
7.在恒温恒容的密闭容器中发生可逆反应:2NO(g)+O (g) 2NO (g)。其他条件相同时,按下列各组投料进行反应,
2 2
平衡时反应速率最快的是( )A.2 mol NO 和1molO B.1 mol NO和1molO C.1 mol NO和2molO D.2 mol NO和1molO
2 2 2 2 2
解析:A项,2 mol NO 逆向反应,若完全反应,可转化为2 mol NO和1molO ,即A项中投料相当于2 mol NO和
2 2
2molO ,则A项中反应速率最快。答案:A
2
8.反应C(s)+CO(g)=2CO(g)为吸热反应,反应速率为v,反应N(g)+3H(g)=2NH (g)为放热反应,反应速率为v 。对于
2 1 2 2 3 2
上述反应,当温度升高时,v 和v 的变化情况为( )
1 2
A.均增大 B.均减小 C.v 增大,v 减小 D.v 减小,v 增大
1 2 1 2
解析:不管是放热反应还是吸热反应,升高温度,反应速率均增大。答案:A
9.反应C(s)+HO(g) CO(g)+H(g)在一容积可变的密闭容器中进行,下列条件的改变能够引起反应速率增大的是(
2 2
)
A.增加C(s)的量
B.将容器的容积缩小一半
C.保持容器容积不变,充入Ar使体系压强增大
D.保持压强不变,充入Ar使容器容积增大
解析:C(s)为固体反应物,增加其用量对反应速率几乎没有影响,A项不符合题意;容器容积缩小一半相当于压强增
大一倍,各气体物质的浓度增大,反应速率增大,B项符合题意;保持容器容积不变,充入Ar,体系总压强增大,但
各气体物质的浓度并未改变,反应速率基本不变,C项不符合题意;充入Ar使容器容积增大,总压强不变,但各气
体物质的浓度减小,反应速率减小,D项不符合题意。答案:B
10.下列关于化学反应速率的说法中不正确的是( )
A.同时改变两个变量来研究反应速率的变化,能更快得出有关规律
B.反应速率的大小与吸、放热无关
C.一定条件下,使用催化剂能加快反应速率
D.相同温度下,H(g)+CO (g) CO(g)+HO(g)中,密闭容器中两种反应物浓度为0.020mol·L-1的反应速率大于两种
2 2 2
反应物浓度为0.010mol·L-1的反应速率
解析:同时改变两个变量来研究反应速率的变化,不易判断影响反应速率的主导因素,更难得出有规律,A错误;其
他选项说法正确。答案:A
11.控制变量法是化学实验的常用方法之一,如图所示实验探究影响反应速率的因素是 ( )
A.催化剂 B.温度 C.压强 D.浓度
解析:如图所示两个试管中,过氧化氢浓度不同、温度相同,两支试管都加了二氧化锰作催化剂,都与大气相通,压
强也相同,则该实验探究影响反应速率的因素是浓度,浓度不同,反应速率不同。答案:D
12.实验室分别用下列四种硫酸与锌粒反应制备H2,其中反应速率最快的是 ( )
A.10℃ 10mL 3mol·L-1的硫酸 B.10℃ 20mL 1mol·L-1的硫酸
C.20℃ 10mL 3mol·L-1的硫酸 D.20℃ 20mL 18.4mol·L-1的硫酸
解析:温度越高,反应速率越快;稀硫酸浓度越大,反应速率越快。D项,浓硫酸与锌反应生成二氧化硫,不能制备
氢气,C项中反应速率最快。答案:C
13.等质量的锌与过量盐酸在不同的实验条件下进行反应,实验数据见下表。收集相同条件下相同体积的氢气,所需时
间最短的一组是( )
组别 A B C D
盐酸浓度/(mol·L-1) 2.0 2.5 2.5 2.5
温度/℃ 25 30 50 50
锌的状态 块状 粉末 块状 粉末
解析:通过比较可知选项A的盐酸浓度最小,温度最低,锌又是块状,所以反应速率最慢,制取相同体积的氢气消耗时间最长,A错误;而选项B、C、D的盐酸浓度相同,则在锌均为粉末状态的情况下,B的温度比D低,因此B的
反应速率较慢,制取相同体积氢气消耗时间较长,B错误;而C与D温度也相同,但C的锌为块状固体,接触面积比
相同质量的粉末状固体小,反应速率较慢,因此制取相同体积氢气消耗时间较长,C错误;D反应速率最快,消耗时
间最短,D正确。答案:D
14.10mL浓度为1mol·L-1的盐酸与过量的锌粉反应,若加入适量的下列溶液,能减慢反应速率但又不影响氢气生成
量的是 ( )
A. KNO B. CH COONa C. CuSO D.NaCO
3 3 4 2 3
解析:与稀盐酸反应过程中,若加入物质使反应速率降低,则溶液中的H+浓度减小,但由于不影响氢气的生成量,故
H+的总物质的量不变。加入KNO,则可看成溶液中有硝酸,硝酸与锌反应不产生氢气,A错误;加入醋酸钠,则与盐
3
酸反应生成醋酸,使溶液中H+浓度减小,随着反应的进行,CHCOOH最终又完全电离,故H+物质的量不变,B正确;
3
加入硫酸钢溶液,Cu2+会与锌反应生成铜,构成原电池,会加快反应速率,C错误;加入碳酸钠溶液,会与盐酸反应,
使溶液中的H+的物质的量减少,反应速率减小,生成氢气的量减少,D错误。答案:B
15.向四个体积相同的密闭容器中分别充入一定量的 SO 和O,开始反应时,按正反应速率由大到小排列正确的是
2 2
( )
甲:在500℃时,10 mol SO 和5molO 反应
2 2
乙:在500℃时,用VO 作催化剂,10 mol SO 和5molO 反应
2 5 2 2
丙:在450℃时,8 mol SO 和5molO 反应
2 2
丁:在500℃时,8 mol SO 和5molO 反应
2 2
A.甲、乙、丙、丁 B.乙、甲、丙、丁 C.乙、甲、丁、丙 D.丁、丙、乙、甲
解析:温度越高,有催化剂,浓度越大,速率越快。答案:C
16.某实验小组以HO 分解为例,研究浓度、催化剂对反应速率的影响。在常温下按照如下方案完成实验。
2 2
实验编号 反应物 催化剂
① 10mL2%H O 溶液 无
2 2
② 无
③ 10mL5%H O 溶液 MnO 固体
2 2 2
实验②的反应物应为 ( )
A.5mL2% HO 溶液 B.10mL5% HO 溶液 C.10mL2% HO 溶液 D.5mL10% HO 溶液
2 2 2 2 2 2 2 2
解析:据单一变量原则可知,实验①②中没有使用催化剂,因此改变的条件应是HO 的浓度;③中使用了催化剂,
2 2
所以实验②③中改变的条件是催化剂,说明②③中反应物的体积和浓度完全相同。答案:B
17.NO和CO都是汽车尾气里的有害物质,它们能缓慢地反应生成氮气和二氧化碳气体:2NO+2CO=N +2CO 对此反
2 2
应,下列叙述正确的是 ( )
A.使用催化剂能加快反应速率
B.压强增大不影响化学反应速率
C.冬天气温低,反应速率降低,对人类危害减小
D.无论外界条件怎样改变,均对此化学反应的速率无影响
解析:使用(正)催化剂能加快反应速率,A正确;增大压强,反应速率增大,B错;冬天气温低,反应速率降低,对人
体危害较大,因为NO、CO都有毒,C错;改变温度、压强等外界条件,该化学反应的速率会改变,D错。答案:A
18.对反应2A(s)+B(g) 2C(g),能增大反应速率的措施是 ( )
A.增加A的量
B.增大体系容积
C.恒容移去部分C
D.升高体系温度
解析:A是固体,增加A的用量对反应速率无影响,A项错误;增大体系容积,相当于减小气体的浓度,反应速率减
慢,B项错误;恒容移去部分C,C的浓度减小,反应速率减慢,C项错误;升温能加快反应速率,D项正确。答案:
D
19.下列对实验现象的描述中错误的是 ( )
A.向FeCl 和KSCN混合溶液中加入少量KCl固体,溶液红色变浅
3
B.向5mL0.1mol·L-1KCr O 溶液中加入少量NaOH固体,溶液由橙色变为黄色
2 2 7
C.等体积等浓度的NaSO 和HSO 溶液混合,温度升高出现浑浊和生成气体的速率加快
2 2 3 2 4
D.酸性KMnO 溶液中滴加HC O,H C O 浓度越大,褪色和生成气体的速率越快
4 2 2 4 2 2 4解析:KCl不参与反应,故加入氯化钾固体,不会对反应产生影响。答案:A
20. 2SO +O 2SO 是接触法制硫酸工艺中的重要反应,下列关于该反应的说法中错误的是 ( )
2 2 3
A.增加SO 的浓度能加快该反应的速率
2
B.通常使用铁作催化剂
C.降低体系温度会减慢该反应的速率
D.使用催化剂能改变该反应的速率
解析:通常使用五氧化二钒作催化剂。答案:B
21.在一密闭容器中,充入1molN 和3molH ,并在一定温度和压强下,使其发生反应:N(g)+3H(g) 2NH (g)
2 2 2 2 3
△H=-92.4kJ·mol-1。回答下列问题:
(1)若保持容器容积不变,再向其中充入1molN ,反应速率会 (填“加快”“减慢”或“不变”,下同),理
2
由是
(2)若保持容器容积不变,再向其中充入1 mol He,反应速率会 ,理由是 。
(3)若保持容器内气体压强不变,再向其中充入1 mol He,反应速率会 ,理由是 。
(4)加入催化剂,反应速率会 。
参考答案:加快 反应物浓度变大 不变 反应物浓度不变 减慢 体积变大导致反应物浓度减小 加快
解析:(1)若保持容器体积不变,再向其中充入1molN ,氮气的浓度增大,反应速率加快;(2)若保持容器体积不变,再
2
向其中充入1 mol He,反应物的浓度不变,反应速率不变;(3)若保持容器气体压强不变,再向其中充入1 mol He,气
体体积和气体的物质的量成正比,容器的体积增大,反应物和生成物的浓度均减小,反应速率减慢;(4)使用催化剂,
反应速率会加快。
22.某研究性学习小组利用HC O 溶液和酸性KMnO 溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,
2 2 4 4
实验如下:
KMnO 溶液 HC O 溶液 HO 溶液褪色时间
实验序号 实验温度 4 2 2 4 2
V(mL) c (mol·L-1) V(mL) c (mol·L-1) V(mL) t(s)
A 293K 2 0.02 4 0.1 0 t
1
B T 2 0.02 3 0.1 V 8
1 1
C 313K 2 0.02 V 0.1 1 t
2 2
(1)通过实验A、B,可探究出 的改变对反应速率的影响,其中V= ,T= ,通过实验 可
1 1
探究出温度变化对化学反应速率的影响。
(2)若t<8,则由实验A、B可以得出的结论是 ;
1
利用实验B中数据计算,从反应开始到结束,用KMnO 的浓度变化表示的反应速率为 。
4
(3)该反应中有无色无味气体产生,且锰被还原为Mn2+写出相应反应的离子方程式:
(4)该小组的一位同学通过查阅资料发现:反应一段时间后该反应速率会加快,造成此种变化的原因是反应体系中的某
种粒子对KMnO 与HC O 之间的反应有某种特殊的作用,则该作用是 ,相应的粒子最有可能是
4 2 2 4
(填符号)
参考答案:浓度 1 293K BC 其他条件相同时,增大反应物浓度,反应速率增大 8.3×10-4mol·L-1·s-1
MnO -+5H C O+6H+=2Mn2++10CO↑+8HO 作催化剂 Mn2+
4 2 2 4 2 2
解析:(1)实验A、B中,高锰酸钾溶液的浓度是相同的,而HC O 溶液的浓度是不同的,故通过实验A、B可探究出
2 2 4
浓度的改变对反应速率的影响,根据控制变量的原理,要控制两实验的温度相同、溶液的总体积相同,故其中
V=1,T =293K。同理,B、C两实验除温度不同外,其余条件相同,故通过实验B、C可探究出温度变化对化学反应速
1 1
率的影响。(2)若t<8,则实验A的反应速率较大,实验A中草酸的浓度大于实验B,则由实验A、B可以得出的结论是
1
其他条件相同时,增大反应物浓度,反应速率增大;利用实验 B 中数据计算,混合后起始浓度 c(KMnO )=
4
, 溶 液 褪 色 用 时 8s 、 c(KMnO )=0, 故 用 KMnO 的 浓 度 变 化 表 示 的 反 应 速 率 为
4 4
。(3)该反应中有无色无味气体产生,该气体为CO,锰被还原为Mn2+,该
2
反应的离子方程式为MnO -+5H C O+6H+=2Mn2++10CO↑+8HO (4)该小组的一位同学通过查阅资料发现:反应一段
4 2 2 4 2 2
时间后该反应速率会加快,造成此种变化的原因是反应体系中的某种粒子对 KMnO 与HC O 之间的反应有某种特殊
4 2 2 4的作用,由于反应是在一定的温度下进行的,故反应体系中的某种粒子的作用是作催化剂,分析反应的各种产物,相
应的粒子最有可能是Mn2+