文档内容
第三课时 活化能基础练习题
1.有效碰撞是指 ( )
A.反应物分子间的碰撞
B.反应物活化分子间的碰撞
C.反应物分子发生合适取向的碰撞
D.活化分子之间发生合适取向的碰撞
2.改变外界条件可以影响化学反应速率,针对H(g)+I (g) 2HI(g),其中能使活化分子百分数增加的是( )
2 2
①增加反应物浓度 ②增大气体的压强 ③升高体系的温度 ④使用催化剂
A.①② B.②③ C.①④ D.③④
3.在气体反应中,改变条件:①增大反应物的浓度,②升高温度,③增大压强,④移去生成物,⑤加入催化剂。能使
反应物中活化分子数和活化分子的百分数同时增大的方法是 ( )
A.①⑤ B.①③ C.②⑤ D.③⑤
4.(双选)下列反应属于基元反应的是( )
A. 2H+O 2HO B.H•+O →•OH+O• C.H++OH-= H O D.2O =3O
2 2 2 2 2 3 2
5.下列说法正确的是( )
A.反应物分子相互碰撞即能发生化学反应
B.活化分子之间的碰撞,一定可以发生化学反应
C.活化分子所具有的能量称为活化能
D.活化分子百分数越大,反应速率越大
6.下列有关温度对化学反应速率影响的说法正确的是( )
①升高温度,活化分子数增加,反应速率加快
②升高温度,活化分子百分数增大,反应速率加快
③升高温度,单位时间内有效碰撞次数增加,反应速率加快
④升高温度,分子运动速率加快,有效碰撞次数增加,反应速率加快
A.②③ B.②④ C.①②③ D.全部
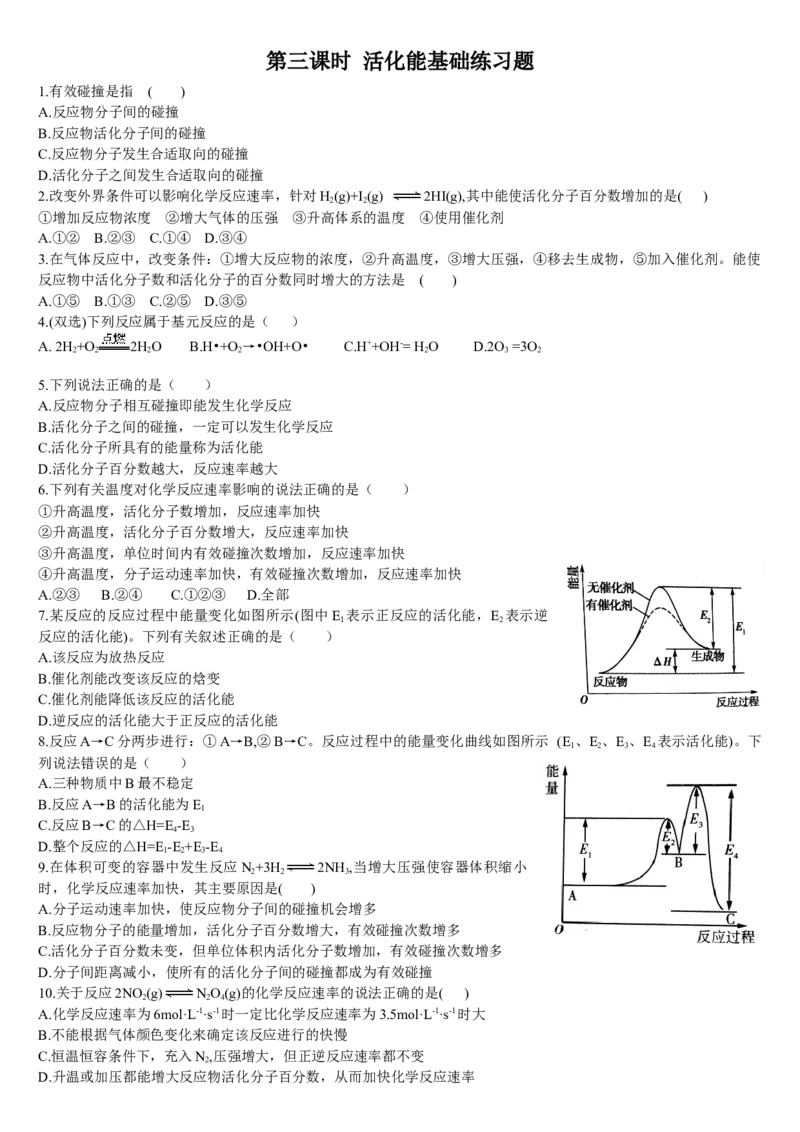
7.某反应的反应过程中能量变化如图所示(图中E 表示正反应的活化能,E 表示逆
1 2
反应的活化能)。下列有关叙述正确的是( )
A.该反应为放热反应
B.催化剂能改变该反应的焓变
C.催化剂能降低该反应的活化能
D.逆反应的活化能大于正反应的活化能
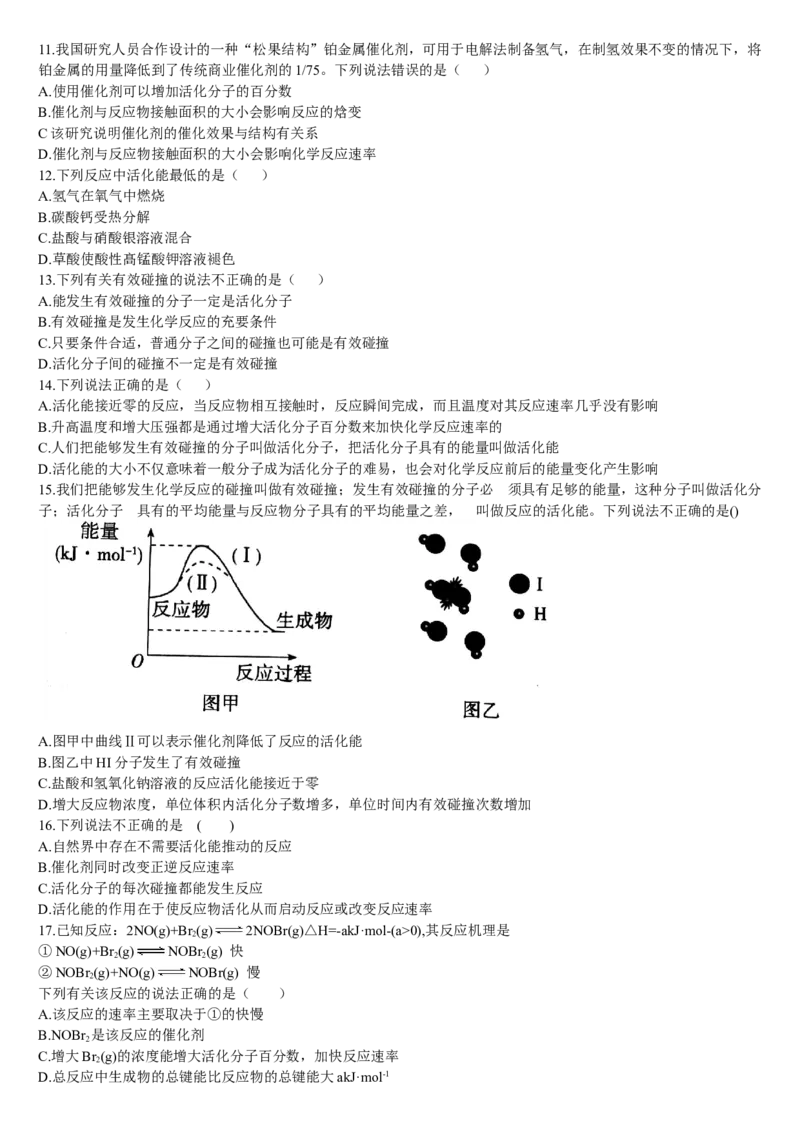
8.反应A→C分两步进行:①A→B,②B→C。反应过程中的能量变化曲线如图所示 (E 、E 、E 、E 表示活化能)。下
1 2 3 4
列说法错误的是( )
A.三种物质中B最不稳定
B.反应A→B的活化能为E
1
C.反应B→C的△H=E -E
4 3
D.整个反应的△H=E -E +E-E
1 2 3 4
9.在体积可变的容器中发生反应N+3H 2NH ,当增大压强使容器体积缩小
2 2 3
时,化学反应速率加快,其主要原因是( )
A.分子运动速率加快,使反应物分子间的碰撞机会增多
B.反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多
C.活化分子百分数未变,但单位体积内活化分子数增加,有效碰撞次数增多
D.分子间距离减小,使所有的活化分子间的碰撞都成为有效碰撞
10.关于反应2NO (g) NO(g)的化学反应速率的说法正确的是( )
2 2 4
A.化学反应速率为6mol·L-1·s-1时一定比化学反应速率为3.5mol·L-1·s-1时大
B.不能根据气体颜色变化来确定该反应进行的快慢
C.恒温恒容条件下,充入N,压强增大,但正逆反应速率都不变
2
D.升温或加压都能增大反应物活化分子百分数,从而加快化学反应速率11.我国研究人员合作设计的一种“松果结构”铂金属催化剂,可用于电解法制备氢气,在制氢效果不变的情况下,将
铂金属的用量降低到了传统商业催化剂的1/75。下列说法错误的是( )
A.使用催化剂可以增加活化分子的百分数
B.催化剂与反应物接触面积的大小会影响反应的焓变
C该研究说明催化剂的催化效果与结构有关系
D.催化剂与反应物接触面积的大小会影响化学反应速率
12.下列反应中活化能最低的是( )
A.氢气在氧气中燃烧
B.碳酸钙受热分解
C.盐酸与硝酸银溶液混合
D.草酸使酸性髙锰酸钾溶液褪色
13.下列有关有效碰撞的说法不正确的是( )
A.能发生有效碰撞的分子一定是活化分子
B.有效碰撞是发生化学反应的充要条件
C.只要条件合适,普通分子之间的碰撞也可能是有效碰撞
D.活化分子间的碰撞不一定是有效碰撞
14.下列说法正确的是( )
A.活化能接近零的反应,当反应物相互接触时,反应瞬间完成,而且温度对其反应速率几乎没有影响
B.升高温度和增大压强都是通过增大活化分子百分数来加快化学反应速率的
C.人们把能够发生有效碰撞的分子叫做活化分子,把活化分子具有的能量叫做活化能
D.活化能的大小不仅意味着一般分子成为活化分子的难易,也会对化学反应前后的能量变化产生影响
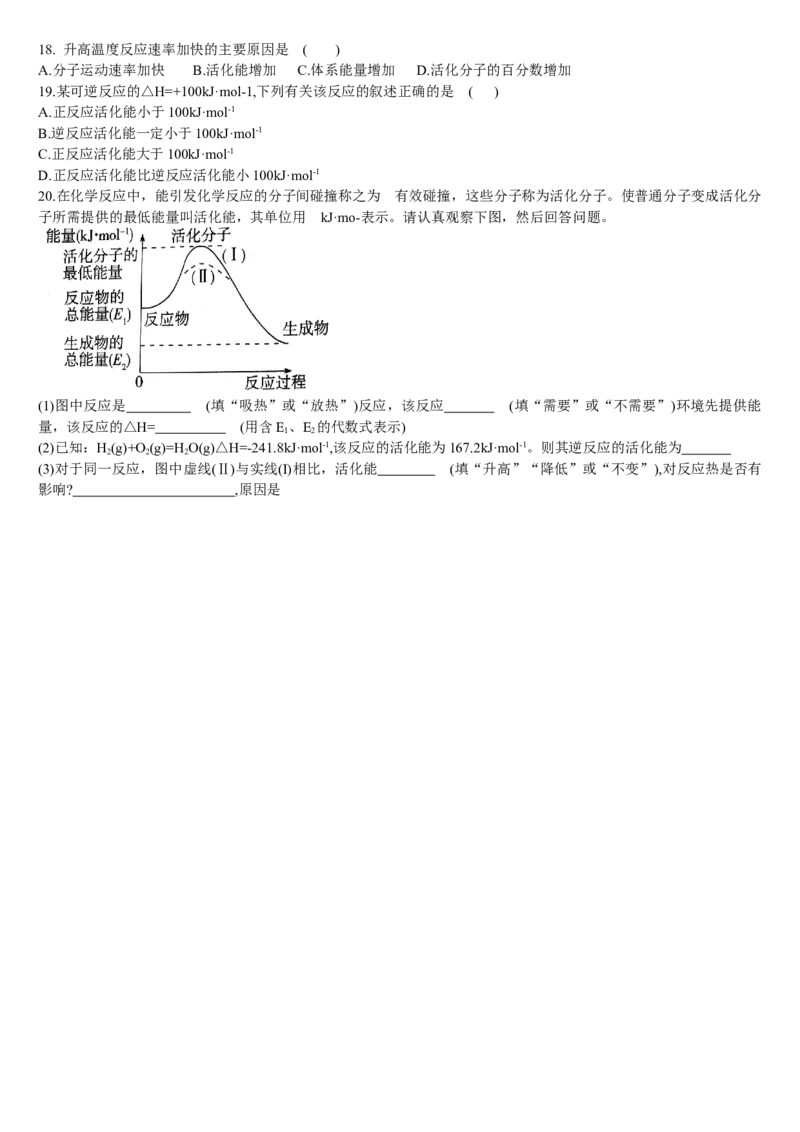
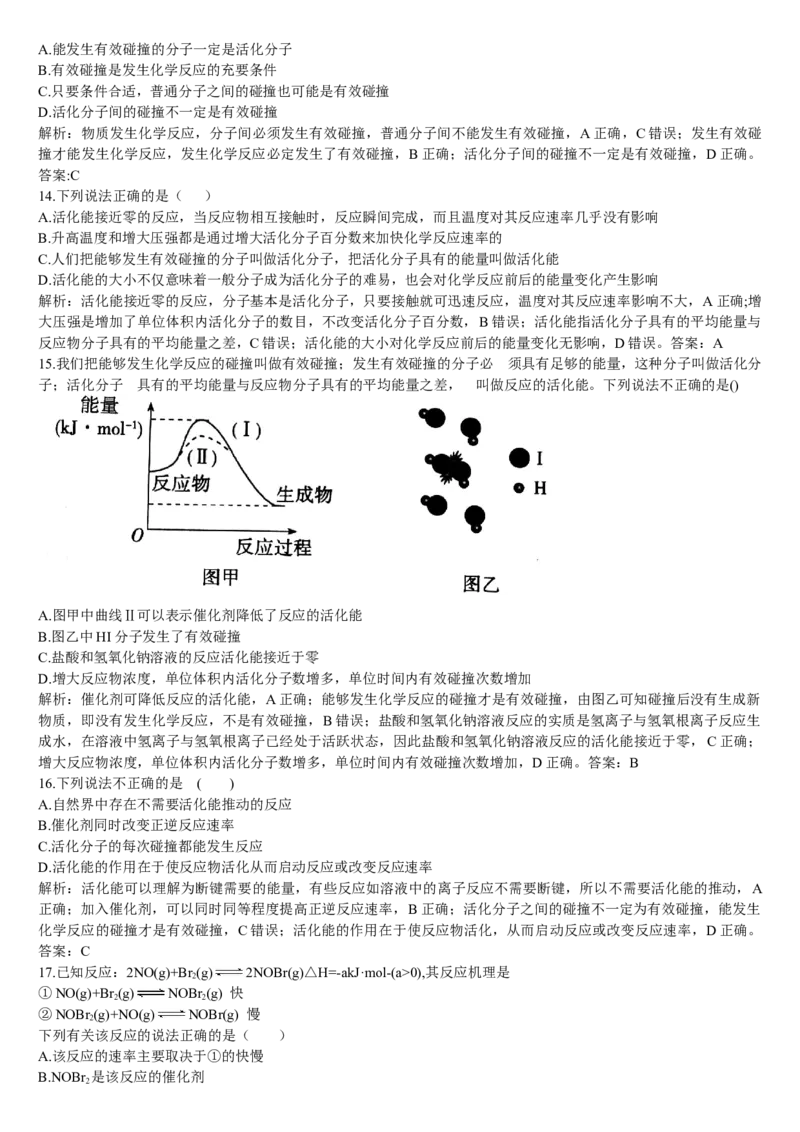
15.我们把能够发生化学反应的碰撞叫做有效碰撞;发生有效碰撞的分子必 须具有足够的能量,这种分子叫做活化分
子;活化分子 具有的平均能量与反应物分子具有的平均能量之差, 叫做反应的活化能。下列说法不正确的是()
A.图甲中曲线Ⅱ可以表示催化剂降低了反应的活化能
B.图乙中HI分子发生了有效碰撞
C.盐酸和氢氧化钠溶液的反应活化能接近于零
D.增大反应物浓度,单位体积内活化分子数增多,单位时间内有效碰撞次数增加
16.下列说法不正确的是 ( )
A.自然界中存在不需要活化能推动的反应
B.催化剂同时改变正逆反应速率
C.活化分子的每次碰撞都能发生反应
D.活化能的作用在于使反应物活化从而启动反应或改变反应速率
17.已知反应:2NO(g)+Br (g) 2NOBr(g)△H=-akJ·mol-(a>0),其反应机理是
2
①NO(g)+Br (g) NOBr (g) 快
2 2
②NOBr (g)+NO(g) NOBr(g) 慢
2
下列有关该反应的说法正确的是( )
A.该反应的速率主要取决于①的快慢
B.NOBr 是该反应的催化剂
2
C.增大Br (g)的浓度能增大活化分子百分数,加快反应速率
2
D.总反应中生成物的总键能比反应物的总键能大akJ·mol-118. 升高温度反应速率加快的主要原因是 ( )
A.分子运动速率加快 B.活化能增加 C.体系能量增加 D.活化分子的百分数增加
19.某可逆反应的△H=+100kJ·mol-1,下列有关该反应的叙述正确的是 ( )
A.正反应活化能小于100kJ·mol-1
B.逆反应活化能一定小于100kJ·mol-1
C.正反应活化能大于100kJ·mol-1
D.正反应活化能比逆反应活化能小100kJ·mol-1
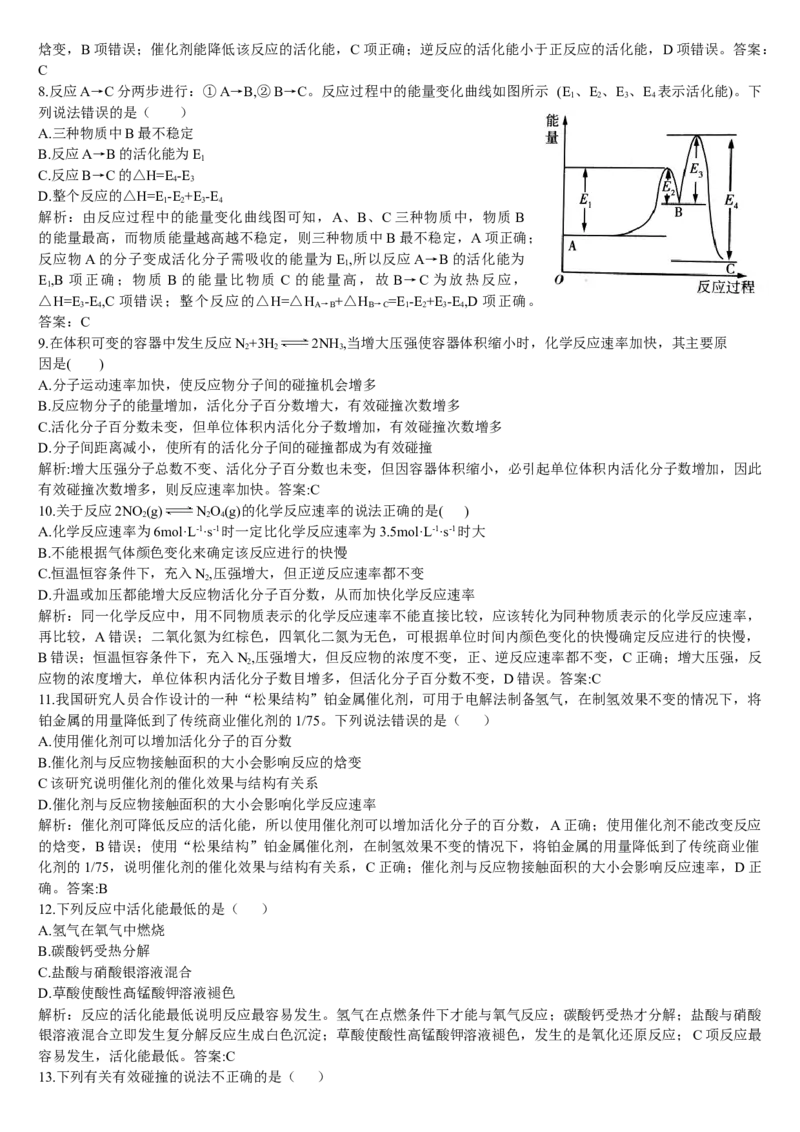
20.在化学反应中,能引发化学反应的分子间碰撞称之为 有效碰撞,这些分子称为活化分子。使普通分子变成活化分
子所需提供的最低能量叫活化能,其单位用 kJ·mo-表示。请认真观察下图,然后回答问题。
(1)图中反应是 (填“吸热”或“放热”)反应,该反应 (填“需要”或“不需要”)环境先提供能
量,该反应的△H= (用含E、E 的代数式表示)
1 2
(2)已知:H(g)+O(g)=HO(g)△H=-241.8kJ·mol-1,该反应的活化能为167.2kJ·mol-1。则其逆反应的活化能为
2 2 2
(3)对于同一反应,图中虚线(Ⅱ)与实线(I)相比,活化能 (填“升高”“降低”或“不变”),对反应热是否有
影响? ,原因是第三课时 活化能基础练习题解析版
1.有效碰撞是指 ( )
A.反应物分子间的碰撞
B.反应物活化分子间的碰撞
C.反应物分子发生合适取向的碰撞
D.活化分子之间发生合适取向的碰撞
解析:有效碰撞指活化分子之间发生合适取向的碰撞。答案:D
2.改变外界条件可以影响化学反应速率,针对H(g)+I (g) 2HI(g),其中能使活化分子百分数增加的是( )
2 2
①增加反应物浓度 ②增大气体的压强 ③升高体系的温度 ④使用催化剂
A.①② B.②③ C.①④ D.③④
解析:①增加反应物浓度能增加活化分子个数,只能增加单位体积的活化分子的数目,活化分子百分数是不变的,①
错误;②对于有气体参与的化学反应,其他条件不变时(除体积),增大压强,即体积减小,反应物浓度增大,单位体积
内活化分子数增多,但活化分子百分数是不变的,②错误③升高温度,活化分子百分数增多,③正确;④催化剂改变
化学反应速率是降低了反应的活化能,活化分子百分数增多,④正确。答案:D
3.在气体反应中,改变条件:①增大反应物的浓度,②升高温度,③增大压强,④移去生成物,⑤加入催化剂。能使
反应物中活化分子数和活化分子的百分数同时增大的方法是 ( )
A.①⑤ B.①③ C.②⑤ D.③⑤
解析:①增大反应物的浓度,只能增大单位体积内活化分子数;③增大压强实际为增大反应物浓度,同①相同;④移
去生成物不影响反应物的活化分子数及活化分子的百分数。答案:C
4.(双选)下列反应属于基元反应的是( )
A. 2H+O 2HO B.H•+O →•OH+O• C.H++OH-= H O D.2O =3O
2 2 2 2 2 3 2
解析:氢气和氧气的反应要经过多步反应才能完成,不属于基元反应,A项错误;B项中反应是氢气和氧气反应过程中
的一个基元反应,B项正确;H+和OH-的中和反应是基元反应,C项正确;O 转化为O 的反应是总反应,要经过几步
3 2
反应才能完成,不属于基元反应,D项错误。答案:BC
5.下列说法正确的是( )
A.反应物分子相互碰撞即能发生化学反应
B.活化分子之间的碰撞,一定可以发生化学反应
C.活化分子所具有的能量称为活化能
D.活化分子百分数越大,反应速率越大
解析:活化分子之间的有效碰撞才能发生化学反应,A、B项错误;活化能是活化分子具有的平均能量与反应物分子
具有的平均能量之差,C项错误;活化分子百分数越大,则单位体积内活化分子数越多,单位时间内有效碰撞的次数
越多,反应速率越大,D项正确。答案:D
6.下列有关温度对化学反应速率影响的说法正确的是( )
①升高温度,活化分子数增加,反应速率加快
②升高温度,活化分子百分数增大,反应速率加快
③升高温度,单位时间内有效碰撞次数增加,反应速率加快
④升高温度,分子运动速率加快,有效碰撞次数增加,反应速率加快
A.②③ B.②④ C.①②③ D.全部
解析:升高温度,反应物分子的能量升高,使一部分原来能量较低的分子变成活化分子,①正确;反应物总分子数不
变,活化分子数增加,则活化分子百分数增大,②正确;活化分子百分数增大,则单位时间内有效碰撞次数增加,③
正确;升高温度,分子运动速率加快,有效碰撞次数增加,④正确。答案:D
7.某反应的反应过程中能量变化如图所示(图中E 表示正反应的活化能,E 表示
1 2
逆反应的活化能)。下列有关叙述正确的是( )
A.该反应为放热反应
B.催化剂能改变该反应的焓变
C.催化剂能降低该反应的活化能
D.逆反应的活化能大于正反应的活化能
解析:由题图可知,反应物的总能量比生成物的总能量低,故该反应为吸热反应,A项错误;催化剂不能改变反应的焓变,B项错误;催化剂能降低该反应的活化能,C项正确;逆反应的活化能小于正反应的活化能,D项错误。答案:
C
8.反应A→C分两步进行:①A→B,②B→C。反应过程中的能量变化曲线如图所示 (E 、E 、E 、E 表示活化能)。下
1 2 3 4
列说法错误的是( )
A.三种物质中B最不稳定
B.反应A→B的活化能为E
1
C.反应B→C的△H=E -E
4 3
D.整个反应的△H=E -E +E-E
1 2 3 4
解析:由反应过程中的能量变化曲线图可知,A、B、C三种物质中,物质B
的能量最高,而物质能量越高越不稳定,则三种物质中B最不稳定,A项正确;
反应物A的分子变成活化分子需吸收的能量为E,所以反应A→B的活化能为
1
E,B 项正确;物质 B 的能量比物质 C 的能量高,故 B→C 为放热反应,
1
△H=E -E ,C项错误;整个反应的△H=△H +△H =E-E +E-E ,D项正确。
3 4 A→B B→C 1 2 3 4
答案:C
9.在体积可变的容器中发生反应N+3H 2NH ,当增大压强使容器体积缩小时,化学反应速率加快,其主要原
2 2 3
因是( )
A.分子运动速率加快,使反应物分子间的碰撞机会增多
B.反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多
C.活化分子百分数未变,但单位体积内活化分子数增加,有效碰撞次数增多
D.分子间距离减小,使所有的活化分子间的碰撞都成为有效碰撞
解析:增大压强分子总数不变、活化分子百分数也未变,但因容器体积缩小,必引起单位体积内活化分子数增加,因此
有效碰撞次数增多,则反应速率加快。答案:C
10.关于反应2NO (g) NO(g)的化学反应速率的说法正确的是( )
2 2 4
A.化学反应速率为6mol·L-1·s-1时一定比化学反应速率为3.5mol·L-1·s-1时大
B.不能根据气体颜色变化来确定该反应进行的快慢
C.恒温恒容条件下,充入N,压强增大,但正逆反应速率都不变
2
D.升温或加压都能增大反应物活化分子百分数,从而加快化学反应速率
解析:同一化学反应中,用不同物质表示的化学反应速率不能直接比较,应该转化为同种物质表示的化学反应速率,
再比较,A错误;二氧化氮为红棕色,四氧化二氮为无色,可根据单位时间内颜色变化的快慢确定反应进行的快慢,
B错误;恒温恒容条件下,充入N,压强增大,但反应物的浓度不变,正、逆反应速率都不变,C正确;增大压强,反
2
应物的浓度增大,单位体积内活化分子数目增多,但活化分子百分数不变,D错误。答案:C
11.我国研究人员合作设计的一种“松果结构”铂金属催化剂,可用于电解法制备氢气,在制氢效果不变的情况下,将
铂金属的用量降低到了传统商业催化剂的1/75。下列说法错误的是( )
A.使用催化剂可以增加活化分子的百分数
B.催化剂与反应物接触面积的大小会影响反应的焓变
C该研究说明催化剂的催化效果与结构有关系
D.催化剂与反应物接触面积的大小会影响化学反应速率
解析:催化剂可降低反应的活化能,所以使用催化剂可以增加活化分子的百分数,A正确;使用催化剂不能改变反应
的焓变,B错误;使用“松果结构”铂金属催化剂,在制氢效果不变的情况下,将铂金属的用量降低到了传统商业催
化剂的1/75,说明催化剂的催化效果与结构有关系,C正确;催化剂与反应物接触面积的大小会影响反应速率,D正
确。答案:B
12.下列反应中活化能最低的是( )
A.氢气在氧气中燃烧
B.碳酸钙受热分解
C.盐酸与硝酸银溶液混合
D.草酸使酸性髙锰酸钾溶液褪色
解析:反应的活化能最低说明反应最容易发生。氢气在点燃条件下才能与氧气反应;碳酸钙受热才分解;盐酸与硝酸
银溶液混合立即发生复分解反应生成白色沉淀;草酸使酸性高锰酸钾溶液褪色,发生的是氧化还原反应;C项反应最
容易发生,活化能最低。答案:C
13.下列有关有效碰撞的说法不正确的是( )A.能发生有效碰撞的分子一定是活化分子
B.有效碰撞是发生化学反应的充要条件
C.只要条件合适,普通分子之间的碰撞也可能是有效碰撞
D.活化分子间的碰撞不一定是有效碰撞
解析:物质发生化学反应,分子间必须发生有效碰撞,普通分子间不能发生有效碰撞,A正确,C错误;发生有效碰
撞才能发生化学反应,发生化学反应必定发生了有效碰撞,B正确;活化分子间的碰撞不一定是有效碰撞,D正确。
答案:C
14.下列说法正确的是( )
A.活化能接近零的反应,当反应物相互接触时,反应瞬间完成,而且温度对其反应速率几乎没有影响
B.升高温度和增大压强都是通过增大活化分子百分数来加快化学反应速率的
C.人们把能够发生有效碰撞的分子叫做活化分子,把活化分子具有的能量叫做活化能
D.活化能的大小不仅意味着一般分子成为活化分子的难易,也会对化学反应前后的能量变化产生影响
解析:活化能接近零的反应,分子基本是活化分子,只要接触就可迅速反应,温度对其反应速率影响不大,A正确;增
大压强是增加了单位体积内活化分子的数目,不改变活化分子百分数,B错误;活化能指活化分子具有的平均能量与
反应物分子具有的平均能量之差,C错误;活化能的大小对化学反应前后的能量变化无影响,D错误。答案:A
15.我们把能够发生化学反应的碰撞叫做有效碰撞;发生有效碰撞的分子必 须具有足够的能量,这种分子叫做活化分
子;活化分子 具有的平均能量与反应物分子具有的平均能量之差, 叫做反应的活化能。下列说法不正确的是()
A.图甲中曲线Ⅱ可以表示催化剂降低了反应的活化能
B.图乙中HI分子发生了有效碰撞
C.盐酸和氢氧化钠溶液的反应活化能接近于零
D.增大反应物浓度,单位体积内活化分子数增多,单位时间内有效碰撞次数增加
解析:催化剂可降低反应的活化能,A正确;能够发生化学反应的碰撞才是有效碰撞,由图乙可知碰撞后没有生成新
物质,即没有发生化学反应,不是有效碰撞,B错误;盐酸和氢氧化钠溶液反应的实质是氢离子与氢氧根离子反应生
成水,在溶液中氢离子与氢氧根离子已经处于活跃状态,因此盐酸和氢氧化钠溶液反应的活化能接近于零,C正确;
增大反应物浓度,单位体积内活化分子数增多,单位时间内有效碰撞次数增加,D正确。答案:B
16.下列说法不正确的是 ( )
A.自然界中存在不需要活化能推动的反应
B.催化剂同时改变正逆反应速率
C.活化分子的每次碰撞都能发生反应
D.活化能的作用在于使反应物活化从而启动反应或改变反应速率
解析:活化能可以理解为断键需要的能量,有些反应如溶液中的离子反应不需要断键,所以不需要活化能的推动,A
正确;加入催化剂,可以同时同等程度提高正逆反应速率,B正确;活化分子之间的碰撞不一定为有效碰撞,能发生
化学反应的碰撞才是有效碰撞,C错误;活化能的作用在于使反应物活化,从而启动反应或改变反应速率,D正确。
答案:C
17.已知反应:2NO(g)+Br (g) 2NOBr(g)△H=-akJ·mol-(a>0),其反应机理是
2
①NO(g)+Br (g) NOBr (g) 快
2 2
②NOBr (g)+NO(g) NOBr(g) 慢
2
下列有关该反应的说法正确的是( )
A.该反应的速率主要取决于①的快慢
B.NOBr 是该反应的催化剂
2C.增大Br (g)的浓度能增大活化分子百分数,加快反应速率
2
D.总反应中生成物的总键能比反应物的总键能大akJ·mol-1
解析:反应速率主要取决于慢的一步,所以反应速率主要取决于②的快慢,A项错误;NOBr 是中间产物,不是催化剂,
2
B项错误;增大Br (g)的浓度,活化分子百分数不变,C项错误;a>0,正反应为放热反应,则生成物的总键能比反应物
2
的总键能大akJ·mol-1,D项正确。 答案:D
18. 升高温度反应速率加快的主要原因是 ( )
A.分子运动速率加快 B.活化能增加 C.体系能量增加 D.活化分子的百分数增加
解析:升高温度增大活化分子百分数,活化分子数目增大,分子之间的有效碰撞次数增加,化学反应速率加快,D正确。
答案:D
19.某可逆反应的△H=+100kJ·mol-1,下列有关该反应的叙述正确的是 ( )
A.正反应活化能小于100kJ·mol-1
B.逆反应活化能一定小于100kJ·mol-1
C.正反应活化能大于100kJ·mol-1
D.正反应活化能比逆反应活化能小100kJ·mol-1
解析:某反应的△H=+100kJ·mol-1,反应为吸热反应,说明反应物总能量小于生成物总能量,则正反应的活化能一逆反应
的活化能=+100kJ·mol-1,说明正反应的活化能比逆反应的活化能大 100kJ·mol-1,无法确定正反应活化能的大小,C正确。
答案:C
20.在化学反应中,能引发化学反应的分子间碰撞称之为 有效碰撞,这些分子称为活化分子。使普通分子变成活化分
子所需提供的最低能量叫活化能,其单位用 kJ·mo-表示。请认真观察下图,然后回答问题。
(1)图中反应是 (填“吸热”或“放热”)反应,该反应 (填“需要”或“不需要”)环境先提供能
量,该反应的△H= (用含E、E 的代数式表示)
1 2
(2)已知:H(g)+O(g)=HO(g)△H=-241.8kJ·mol-1,该反应的活化能为167.2kJ·mol-1。则其逆反应的活化能为
2 2 2
(3)对于同一反应,图中虚线(Ⅱ)与实线(I)相比,活化能 (填“升高”“降低”或“不变”),对反应热是否有
影响? ,原因是
参考答案:(1)放热 需要 E-E
2 1
(2)409.0kJ·mol-1
(3)降低 无影响 催化剂只能降低反应的活化能,不能改变反应物的总能量和生成物的总能量之差,即反
应热不改变
解析:(2)由图示可知△H=正反应活化能-逆反应活化能,故逆反应活化能=正反应活化能-△H=167.2kJ·mol-1-
(-241.8kJ·mol-1)=409.0k·mol-1