文档内容
第一课时 化学反应速率基础练习题
1、反应4NH (g)+3O=2N (g)+6HO(g)在2L的密闭容器中进行,半分钟后N 的物质的量增加了0.6mol。下列各物质表
3 2 2 2 2
示的反应速率正确的是( )
A.v(NH )=0.04mol·L-1·s-1 B.v(O )=0.015mol·L-1·s-1 C.v(N )=0.02mol·L-1·s-1 D.v(HO)=0.02mol·L-1·s-1
3 2 2 2
2、在反应3A(g)+B(g)=3C(g)+5D(g)中,各物质表示的反应速率最快的是( )
A.v(A)=0.5mol· L-1·s-1 B.v(B)=3mol·L-1·min-1 C.v(C)=0.3mol·L-1·s-1 D.v(D)=1mol·L-1·s-1
3、已知反应3A(g)+B(g)==2C(g)+2D(g),在不同条件下,用不同物质表示其反应速率,分别为①v(A)=0.6mol·L-1·min-1
,②v(B)=0.45mol· L-1·min-1,③v(C)=0.015mol·L-1·s-1,④v(D)=0.45mol·L-1·min-1。则此反应在不同条件下进行最快的是(
)
A.②③ B.①③ C.②④ D.①②
4、向2L的恒容密闭容器中通入4molA和5molB,发生反应:4A(g)+5B(g)=3C(g)+3D(s)。5min后,容器内压强变为原
来的80%,则该反应在0~5min内的平均反应速率可表示为( )
A.v(A)=0.24mol L-1·min-1 B.v(B)=0.15mol·L-1·min-1 C.v(C)=0.18mol·L-1·min-1 D.v(D)=0.36mol·L-1·min-1
5.下列关于化学反应速率的说法中,正确的是( )
A.化学反应速率是指某一时刻,某种反应物的瞬时反应速率
B.化学反应速率为0.8mol·L-1·s-1是指反应1s时某物质的浓度为0.8mol·L-1
C.根据化学反应速率的大小可以知道化学反应进行的快慢
D.化学反应速率可用反应体系中任何一种物质浓度的变化来表示
6.在2L密闭容器内,某气体反应物在2s内由8mol变为7.2mol,则该反应的平均反应速率为 ( )
A.0.4mol·L-1·s-1 B.0.3mol·L-1·s-1 C.0.2mol·L-1·s-1 D.0.1mol·L-1·s-1
7.5.6g铁粉投入到盛有100mL2mol·L-1稀硫酸的烧杯中,2min时铁粉刚好溶解(溶解前后溶液体积变化忽略不计),下列
表示这个反应的速率正确的是( )
A.v(HSO )=0.5 mol·L-1·min-1 B.v(H SO )=1 mol·L-1·min-1 C.v(Fe)=0.5 mol·L-1·min-1 D.v(FeSO )=1 mol·L-1·min-1
2 4 2 4 4
8.反应4A(s)+3B(g) 2C(g)+D(g),经2min后,B的浓度减少了0.6mol·L-1。下列反应速率的表示正确的是( )
A.用A表示的反应速率是0.4mol·L-1·min-1
B.2min末时的反应速率,用B表示为0.3mol·L-1·min-1
C.用B表示的平均反应速率是0.3mol·L-1·min-1
D.在这2min内,用B表示的反应速率的值是减小的,用C表示的反应速率逐渐增大
9.在铝与稀硫酸的反应中,已知10s末硫酸的浓度减少了0.9mol·L-1,若不考虑反应过程中溶液体积的变化,则10s内生
成硫酸铝的平均反应速率是 ( )
A.0.03mol·L-1·min-1 B.1.8 mol·L-1·min-1 C.1.2 mol·L-1·min-1 D.0.18 mol·L-1·min-1
10.已知 2SO +O =2SO 经一段时间反应后,SO 的浓度增加了 0.4mol·L-1,在这段时间内用 O 表示的反应速率为
2 2 3 3 2
0.04mol·L-1·s-1,则这段时间为( )
A.0.1s B.5s C.2.5s D.10s11、反应A(g)+3B(g)=2C(g)+2D(g)在四种不同情况下的反应速率分别为
①v(A)=0.15mol·L-1·s-1
②v(B)=0.6 mol·L-1·s-1
③v(C)=0.4 mol·L-1·s-1
④v(D)=0.45mol·L-1·min-1
该反应进行的快慢顺序为 ( )
A.②>④>③>① B.④>②=③>① C.②=③>①>④ D.②>③=④>①
12.已知某条件下,合成氨反应的数据如下:N(g)+3H(g) 2NH (g)
2 2 3
N H NH
2 2 3
起始浓度(mol·L-1) 1.0 3.0 0.2
2s末浓度(mol·L-1) 0.6 1.8 1.0
4s末浓度(mol·L-1) 0.4 1.2 1.4
当用NH 浓度的增加来表示该反应的化学反应速率时,下列说法错误的是( )
3
A.2~4s内的平均反应速率为0.2 mol·L-1·s-1
B.前4s内的平均反应速率为0.3 mol·L-1·s-1
C.前2s内的平均反应速率为0.4 mol·L-1·s-1
D.2s末的反应速率为0.4 mol·L-1·s-1
13. 把 0.6molX 气体和 0.4molY 气体混合于 2L 密闭容器中,使它们发生如下反应:3X(g)+Y(g) nZ(g)
+2W(g);5min末已生成0.2molW,若测知以Z浓度来表示的反应速率为0.01mol·L-1·min-1,则上述反应中Z气体的化学计
量数n的值是( )
A.1 B.2 C.3 D.4
14.在密闭容器中发生反应mA(g)+nB(g)=wC(g),同一时间段内测得:A的浓度每分钟减少0.15mol·L-1,B的浓度每分钟
减少0.05mol·L-1,C的浓度每分钟增加0.1mol·L-1。则下列叙述正确的是 ( )
A.在容器容积和温度不变的条件下,随着反应的进行,体系的压强逐渐增大
B.化学计量数之比是m:n:w=3:1:2
C.单位时间内反应物浓度的减少等于生成物浓度的增加
D.若在前10s内A减少了xmol,则在前20s内A减少了2xmol
15.在一定条件下,将 3molA 和 1molB 两种气体混合于固定容积为 2L 的密闭容器中,发生如下反应:3A(g)+
B(g)=xC(g)+2D(g)。2min时测得生成0.8molD、0.4molC。下列判断不正确的是 ( )
A.x=1
B.2min时,A的浓度为0.9mol·L-1
C.2min内A的反应速率为0.3 mol·L-1·min-1
D.B的转化率为60%
16.将气体 A 、B 各1mol充入 1L的密闭容器中反应,生成气体 C,一段时间后,测得 c(A)为0.58mol·L-1,c(B )为
2 2 2 2
0.16mol·L-1,c(C)为0.84mol·L-1,则C的化学式为 ( )
A. AB B. A B C. AB D. AB
2 2 2 217.一定温度下,向一个容积为3L的真空密闭容器中通入1molN 和3molH ,2min后,测得容器内的压强是开始时的
2 2
0.8倍,则这段时间内v(H )为 ( )
2
A.0.2 mol·L-1·min-1 B.0.6 mol·L-1·min-1 C.0.1 mol·L-1·min-1 D.0.3 mol·L-1·min-1
18.把4molX气体和6molY气体混合于2L密闭容器中,使它们发生如下反应:X(g)+2Y(g)=3Z(g)+nW(g),5min末已生
成3molZ,若测知以W的浓度变化来表示的反应速率为0.2mol·L-1·min-1,下列选项正确的是 ( )
A.前5min内用X的浓度变化表示的平均反应速率为0.5 mol·L-1·min-1
B.5min末时Y的浓度为2mol·L-1
C.化学方程式中n=3
D.5min末时W的物质的量为1mol
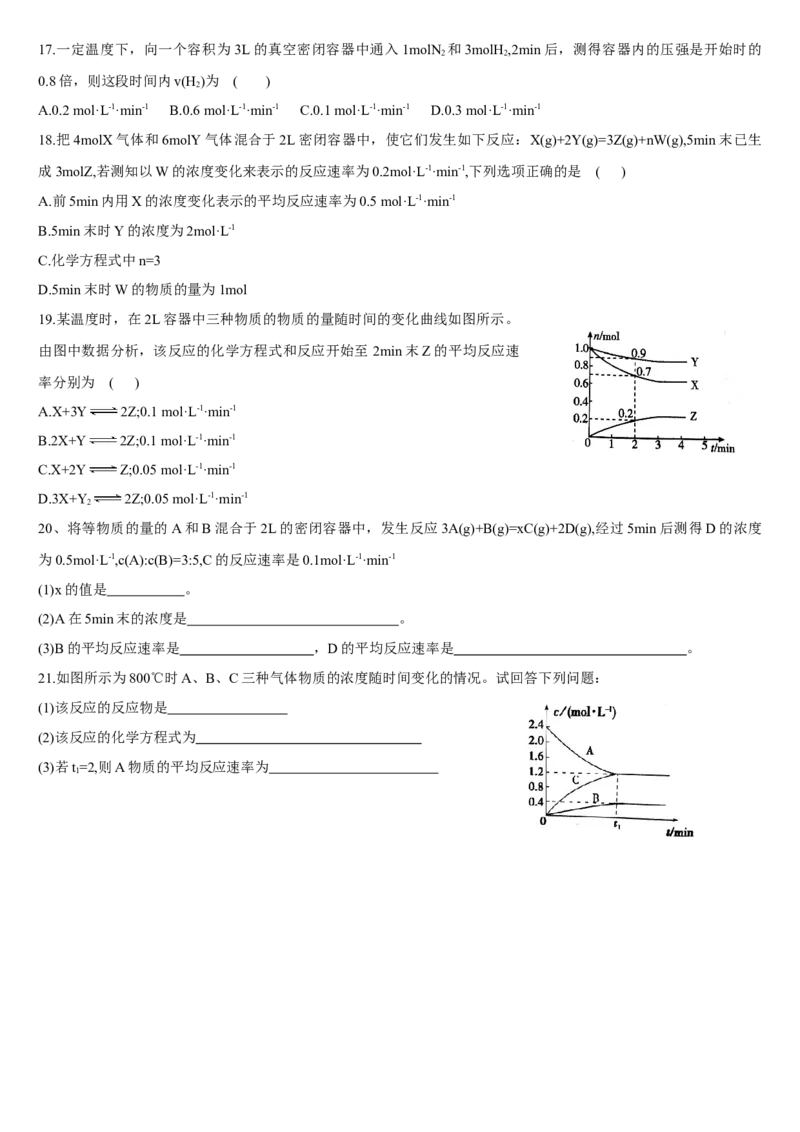
19.某温度时,在2L容器中三种物质的物质的量随时间的变化曲线如图所示。
由图中数据分析,该反应的化学方程式和反应开始至 2min末Z的平均反应速
率分别为 ( )
A.X+3Y 2Z;0.1 mol·L-1·min-1
B.2X+Y 2Z;0.1 mol·L-1·min-1
C.X+2Y Z;0.05 mol·L-1·min-1
D.3X+Y 2Z;0.05 mol·L-1·min-1
2
20、将等物质的量的A和B混合于2L的密闭容器中,发生反应3A(g)+B(g)=xC(g)+2D(g),经过5min后测得D的浓度
为0.5mol·L-1,c(A):c(B)=3:5,C的反应速率是0.1mol·L-1·min-1
(1)x的值是 。
(2)A在5min末的浓度是 。
(3)B的平均反应速率是 ,D的平均反应速率是 。
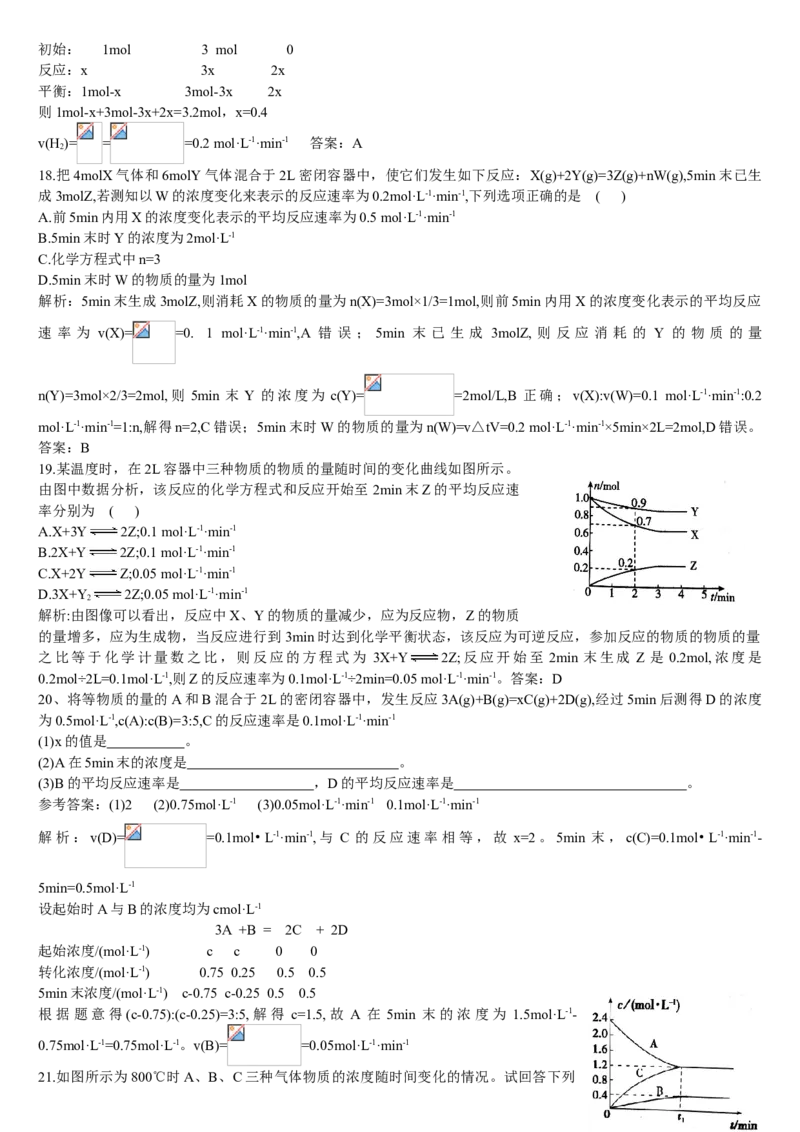
21.如图所示为800℃时A、B、C三种气体物质的浓度随时间变化的情况。试回答下列问题:
(1)该反应的反应物是
(2)该反应的化学方程式为
(3)若t=2,则A物质的平均反应速率为
1第一课时 化学反应速率基础练习题解析版
1、反应4NH (g)+3O=2N (g)+6HO(g)在2L的密闭容器中进行,半分钟后N 的物质的量增加了0.6mol。下列各物质表
3 2 2 2 2
示的反应速率正确的是( )
A.v(NH )=0.04mol·L-1·s-1 B.v(O )=0.015mol·L-1·s-1 C.v(N )=0.02mol·L-1·s-1 D.v(HO)=0.02mol·L-1·s-1
3 2 2 2
解析:v(N )= =0.01mol·L-1·s-1,C项错误;由各物质的反应速率之比等于化学方程式中各物质的化学计量数之
2
比可知,v(NH )=2v(N)=0.02mol·L-1·s-1,A 项错误;v(O )=3/2v(N )=0.015mol·L-1·s-1,B项正确v(H O)=3v(N )
3 2 2 2 2 2
=0.03mol·L-1·s-1,D项错误。答案:B
2、在反应3A(g)+B(g)=3C(g)+5D(g)中,各物质表示的反应速率最快的是( )
A.v(A)=0.5mol· L-1·s-1 B.v(B)=3mol·L-1·min-1 C.v(C)=0.3mol·L-1·s-1 D.v(D)=1mol·L-1·s-1
解 析 : A 项 , v(B)=1/3v(A)≈ 0.17mol·L-1·s-1;B 项 , v(B)=3mol·L-1·min-1=0.05mol·L-1·s-1;C 项 , v(B)=1/3v(C)
=0.1mol·L-1·s-1
;D项,v(B)=1/5v(D)=0.2mol·L-1·s-1。由此可知,D项表示的反应速率最快。答案:D
3、已知反应3A(g)+B(g)==2C(g)+2D(g),在不同条件下,用不同物质表示其反应速率,分别为①v(A)=0.6mol·L-1·min-1
,②v(B)=0.45mol· L-1·min-1,③v(C)=0.015mol·L-1·s-1,④v(D)=0.45mol·L-1·min-1。则此反应在不同条件下进行最快的是(
)
A.②③ B.①③ C.②④ D.①②
解析:同一化学反应中,在单位统一的条件下,各物质表示的化学反应速率与其化学计量数之比越大,该反应速率越
大。① v(A)/3=0.2mol·L-1·min-1;v(b)/1=0.45mol·L-1·min-1;v(C)/2=0.45mol·L-1·min-1;④ v(D)/2=0.225mol·L-1·min-1综上所述,
②③进行最快。答案:A
4、向2L的恒容密闭容器中通入4molA和5molB,发生反应:4A(g)+5B(g)=3C(g)+3D(s)。5min后,容器内压强变为原
来的80%,则该反应在0~5min内的平均反应速率可表示为( )
A.v(A)=0.24mol L-1·min-1 B.v(B)=0.15mol·L-1·min-1 C.v(C)=0.18mol·L-1·min-1 D.v(D)=0.36mol·L-1·min-1
解析:设0~5min内参加反应的A的物质的量为xmol。应用“三段式”法进行计算:
4A(g)+5B(g)=3C(g)+3D(s)
起始的量/mol 4 5 0
转化的量/mol x
5min时的量/mol 4-x 5-
由 压 强 与 体 系 中 气 体 的 物 质 的 量 成 正 比 可 知 , 4-x+ 5- + = 9×80%, 则 x=1.2,v(A)=
=0.12mol·L-1·min-1,A项误;v(B)=5/4v(A)=0.15mol·L-1·min-1,B项正确;v(C)=3/4v(A)=0.09mol·L-1·min-1 C项错误;生成
物D为固体,不能用来表示反应速率,D项错误。答案:B
5.下列关于化学反应速率的说法中,正确的是( )
A.化学反应速率是指某一时刻,某种反应物的瞬时反应速率
B.化学反应速率为0.8mol·L-1·s-1是指反应1s时某物质的浓度为0.8mol·L-1
C.根据化学反应速率的大小可以知道化学反应进行的快慢
D.化学反应速率可用反应体系中任何一种物质浓度的变化来表示
答案:C
6.在2L密闭容器内,某气体反应物在2s内由8mol变为7.2mol,则该反应的平均反应速率为 ( )
A.0.4mol·L-1·s-1 B.0.3mol·L-1·s-1 C.0.2mol·L-1·s-1 D.0.1mol·L-1·s-1
解析:在2L密闭容器内,某气体反应物在2s内由8mol变为7.2mol,2s内该物质表示的平均反应速率为
=0. 2 mol·L-1·s-1
7.5.6g铁粉投入到盛有100mL2mol·L-1稀硫酸的烧杯中,2min时铁粉刚好溶解(溶解前后溶液体积变化忽略不计),下列
表示这个反应的速率正确的是( )
A.v(HSO )=0.5 mol·L-1·min-1 B.v(H SO )=1 mol·L-1·min-1 C.v(Fe)=0.5 mol·L-1·min-1 D.v(FeSO )=1 mol·L-1·min-1
2 4 2 4 4解析:Fe的物质的量为 =0.1mol,由Fe+H SO =FeSO+H ↑可知,参加反应的硫酸也是0.1mol,硫酸的浓度变
2 4 4 2
化量为0.1mol =1mol·L-1,故v(H SO )= =0.5mol·L-1·min-1,A正确,B错误;Fe为纯固体,不能用浓度
2 4
变化量表示反应速率,C错误;化学反应速率之比等于化学计量数之比,则 v(FeSO )=v(HSO )=0.5mol·L-1·min-1,D错
4 2 4
误。答案:A
8.反应4A(s)+3B(g) 2C(g)+D(g),经2min后,B的浓度减少了0.6mol·L-1。下列反应速率的表示正确的是( )
A.用A表示的反应速率是0.4mol·L-1·min-1
B.2min末时的反应速率,用B表示为0.3mol·L-1·min-1
C.用B表示的平均反应速率是0.3mol·L-1·min-1
D.在这2min内,用B表示的反应速率的值是减小的,用C表示的反应速率逐渐增大
解析:A物质是固体,浓度不变,不能用来表示反应速率,A错误;2min末时的反应速率为即时速率,2min内用B物
质表示的化学反应速率v(B)= = =0.3mol·L-1·min-1是平均速率,B错误;C正确;用不同物质表示的反应
速率,速率之比等于化学方程式的化学计量数之比,由于反应物的浓度逐渐降低,所以在这 2min内,用B表示的反
应速率的值是减小的,用C表示的反应速率也是逐渐减小的,D错误。答案:C
9.在铝与稀硫酸的反应中,已知10s末硫酸的浓度减少了0.9mol·L-1,若不考虑反应过程中溶液体积的变化,则10s内生
成硫酸铝的平均反应速率是 ( )
A.0.03mol·L-1·min-1 B.1.8 mol·L-1·min-1 C.1.2 mol·L-1·min-1 D.0.18 mol·L-1·min-1
解析:10s 末,硫酸的浓度减少了 0.9mol·L-1,则 v(H SO )= =0.09mol·L-1•s-1=0.09mol·L-1·s-1,发生反应为
2 4
2A1+3HSO =Al(SO )+3H ↑,速率之比等于化学计量数之比,故v[Al(SO )]=1/3v(H SO )= 0.09mol·L-1·s-1=
2 4 2 4 3 2 2 4 3 2 4
0.03mol·L-1·s-1=1.8mol·L-1· min -1。答案:B
10.已知 2SO +O =2SO 经一段时间反应后,SO 的浓度增加了 0.4mol·L-1,在这段时间内用 O 表示的反应速率为
2 2 3 3 2
0.04mol·L-1·s-1,则这段时间为( )
A.0.1s B.5s C.2.5s D.10s
解析:用 O 表示的反应速率为 0.04mol·L-1·s-1,则 v(SO )=2v(O)=2×0.04mol·L-1·s-1=0.08 mol·L-1·s-1 ,故反应时间=
2 3 2
=5s 答案:B
11、反应A(g)+3B(g)=2C(g)+2D(g)在四种不同情况下的反应速率分别为
①v(A)=0.15mol·L-1·s-1
②v(B)=0.6 mol·L-1·s-1
③v(C)=0.4 mol·L-1·s-1
④v(D)=0.45mol·L-1·min-1
该反应进行的快慢顺序为 ( )
A.②>④>③>① B.④>②=③>① C.②=③>①>④ D.②>③=④>①
解析:根据反应速率之比等于化学计量数之比可知:① v(A)=0.15 mol·L-1·s-1;② v(B)=0.6 mol·L-1·s-1,则 v(A)=0.2
mol·L-1·s-1;③v(C)=0.4 mol·L-1·s-1,则v(A)=0.2 mol·L-1·s-1;④v(D)=0.45 mol·L-1·min-1,则v(A)=0.00375 mol·L-1·s-1,所以快慢
顺序为②=③>①>④ 答案:C
12.已知某条件下,合成氨反应的数据如下:N(g)+3H(g) 2NH (g)
2 2 3
N H NH
2 2 3
起始浓度(mol·L-1) 1.0 3.0 0.2
2s末浓度(mol·L-1) 0.6 1.8 1.0
4s末浓度(mol·L-1) 0.4 1.2 1.4
当用NH 浓度的增加来表示该反应的化学反应速率时,下列说法错误的是( )
3
A.2~4s内的平均反应速率为0.2 mol·L-1·s-1
B.前4s内的平均反应速率为0.3 mol·L-1·s-1
C.前2s内的平均反应速率为0.4 mol·L-1·s-1D.2s末的反应速率为0.4 mol·L-1·s-1
解析:2~4s时间内NH 的浓度变化为(1.4一1.0)mol·L-1=0.4mol·L-1,平均反应速率为 =0.2 mol·L-1·s-1,,A正确;
3
前4s时间内NH 的浓度变化为(1.4-0.2)mol·L-1=1.2 mol·L-1,平均反应速率为 =0.3 mol·L-1·s-1,B正确;前2s时
3
间内NH3的浓度变化为(1.0-0.2)mol·L-1=0.8mol·L-1,NH 的平均反应速率为 =0.4 mol·L-1·s-1,C正确;2s内NH
3 3
的平均速率为0.4 mol·L-1·s-1,不是即时速率,D错误。答案:D
13. 把 0.6molX 气体和 0.4molY 气体混合于 2L 密闭容器中,使它们发生如下反应:3X(g)+Y(g) nZ(g)
+2W(g);5min末已生成0.2molW,若测知以Z浓度来表示的反应速率为0.01mol·L-1·min-1,则上述反应中Z气体的化学计
量数n的值是( )
A.1 B.2 C.3 D.4
解析:5min内,v(W)=0.2mol÷(2L×5min)= 0.02mol·L-1·min-1,利用化学反应速率之比等于化学计量数之比可知n=1。答案:
A
14.在密闭容器中发生反应mA(g)+nB(g)=wC(g),同一时间段内测得:A的浓度每分钟减少0.15mol·L-1,B的浓度每分钟
减少0.05mol·L-1,C的浓度每分钟增加0.1mol·L-1。则下列叙述正确的是 ( )
A.在容器容积和温度不变的条件下,随着反应的进行,体系的压强逐渐增大
B.化学计量数之比是m:n:w=3:1:2
C.单位时间内反应物浓度的减少等于生成物浓度的增加
D.若在前10s内A减少了xmol,则在前20s内A减少了2xmol
解析:由题意知,v(A):v(B):v(C)=3:1:2。根据化学反应中各物质的反应速率之比等于化学方程式中相应应物质的化学
计量数之比可知,m:n:w=3:1:2,A、C项均错误,B项正确。反应过程中,反应都不是等速率进行的,前10s与前20s
内反应速率不同,D项错误。答案:B
15.在一定条件下,将 3molA 和 1molB 两种气体混合于固定容积为 2L 的密闭容器中,发生如下反应:3A(g)+
B(g)=xC(g)+2D(g)。2min时测得生成0.8molD、0.4molC。下列判断不正确的是 ( )
A.x=1
B.2min时,A的浓度为0.9mol·L-1
C.2min内A的反应速率为0.3 mol·L-1·min-1
D.B的转化率为60%
解析:相同时间内生成C、D的物质的量之比等于其化学计量数之比,所以x:2=0.4mol:0.8mol=1:2,x=1,A正确;在相
同时间内,各反应物和生成物物质的量的变化之比等于化学计量数之比,△n(A):△n(D)=3:2=△n(A):0.8mol,则求得
△n(A)=1.2mol,未反应的A物质的量为3mol-1.2mol=1.8mol,所以此时A的物质的量浓度为c(A)= =0.9mol·L-1,B
正确;由选项 B 可知,在 2min 时△n(A)= 1.2mol, 则用 A 物质表示的反应速率为 v(A)= =0.3
mol·L-1·min-1,C正确;生成0.8molD的同时消耗n(B)=0.8mo÷2=0.4mol,则B物质的转化率为 ×100%=40%,D错
误。答案:D
16.将气体 A 、B 各1mol充入 1L的密闭容器中反应,生成气体 C,一段时间后,测得 c(A)为0.58mol·L-1,c(B )为
2 2 2 2
0.16mol·L-1,c(C)为0.84mol·L-1,则C的化学式为 ( )
A. AB B. A B C. AB D. AB
2 2 2 2
解析:该段时间内,A 、B 两种物质按照化学方程式中的化学计量数之比进行反应。由题意可得 A 、B 、C三种物质
2 2 2 2
的量浓度的变化值,求出A 、B 、C三种物质的化学计量数之比为1:2:2,结合质量守恒定律可知C的化学式为AB 。
2 2 2
答案:C
17.一定温度下,向一个容积为3L的真空密闭容器中通入1molN 和3molH ,2min后,测得容器内的压强是开始时的
2 2
0.8倍,则这段时间内v(H )为 ( )
2
A.0.2 mol·L-1·min-1 B.0.6 mol·L-1·min-1 C.0.1 mol·L-1·min-1 D.0.3 mol·L-1·min-1
解析:恒温恒容的密闭容器中,压强之比等于物质的量之比,则1:0.8=4mol:n,n=3.2mol
N(g) + 3H(g) 2NH (g)
2 2 3初始: 1mol 3 mol 0
反应:x 3x 2x
平衡:1mol-x 3mol-3x 2x
则1mol-x+3mol-3x+2x=3.2mol,x=0.4
v(H )= = =0.2 mol·L-1·min-1 答案:A
2
18.把4molX气体和6molY气体混合于2L密闭容器中,使它们发生如下反应:X(g)+2Y(g)=3Z(g)+nW(g),5min末已生
成3molZ,若测知以W的浓度变化来表示的反应速率为0.2mol·L-1·min-1,下列选项正确的是 ( )
A.前5min内用X的浓度变化表示的平均反应速率为0.5 mol·L-1·min-1
B.5min末时Y的浓度为2mol·L-1
C.化学方程式中n=3
D.5min末时W的物质的量为1mol
解析:5min末生成3molZ,则消耗X的物质的量为n(X)=3mol×1/3=1mol,则前5min内用X的浓度变化表示的平均反应
速 率 为 v(X)= =0. 1 mol·L-1·min-1,A 错 误 ; 5min 末 已 生 成 3molZ, 则 反 应 消 耗 的 Y 的 物 质 的 量
n(Y)=3mol×2/3=2mol,则 5min 末 Y 的浓度为 c(Y)= =2mol/L,B 正确;v(X):v(W)=0.1 mol·L-1·min-1:0.2
mol·L-1·min-1=1:n,解得n=2,C错误;5min末时W的物质的量为n(W)=v△tV=0.2 mol·L-1·min-1×5min×2L=2mol,D错误。
答案:B
19.某温度时,在2L容器中三种物质的物质的量随时间的变化曲线如图所示。
由图中数据分析,该反应的化学方程式和反应开始至 2min末Z的平均反应速
率分别为 ( )
A.X+3Y 2Z;0.1 mol·L-1·min-1
B.2X+Y 2Z;0.1 mol·L-1·min-1
C.X+2Y Z;0.05 mol·L-1·min-1
D.3X+Y 2Z;0.05 mol·L-1·min-1
2
解析:由图像可以看出,反应中X、Y的物质的量减少,应为反应物,Z的物质
的量增多,应为生成物,当反应进行到 3min时达到化学平衡状态,该反应为可逆反应,参加反应的物质的物质的量
之比等于化学计量数之比,则反应的方程式为 3X+Y 2Z;反应开始至 2min 末生成 Z 是 0.2mol,浓度是
0.2mol÷2L=0.1mol·L-1,则Z的反应速率为0.1mol·L-1÷2min=0.05 mol·L-1·min-1。答案:D
20、将等物质的量的A和B混合于2L的密闭容器中,发生反应3A(g)+B(g)=xC(g)+2D(g),经过5min后测得D的浓度
为0.5mol·L-1,c(A):c(B)=3:5,C的反应速率是0.1mol·L-1·min-1
(1)x的值是 。
(2)A在5min末的浓度是 。
(3)B的平均反应速率是 ,D的平均反应速率是 。
参考答案:(1)2 (2)0.75mol·L-1 (3)0.05mol·L-1·min-1 0.1mol·L-1·min-1
解析:v(D)= =0.1mol•L-1·min-1,与 C 的反应速率相等,故 x=2。5min 末,c(C)=0.1mol•L-1·min-1-
5min=0.5mol·L-1
设起始时A与B的浓度均为cmol·L-1
3A +B = 2C + 2D
起始浓度/(mol·L-1) c c 0 0
转化浓度/(mol·L-1) 0.75 0.25 0.5 0.5
5min末浓度/(mol·L-1) c-0.75 c-0.25 0.5 0.5
根据题意得(c-0.75):(c-0.25)=3:5,解得 c=1.5,故 A 在 5min 末的浓度为 1.5mol·L-1-
0.75mol·L-1=0.75mol·L-1。v(B)= =0.05mol·L-1·min-1
21.如图所示为800℃时A、B、C三种气体物质的浓度随时间变化的情况。试回答下列问题:
(1)该反应的反应物是
(2)该反应的化学方程式为
(3)若t=2,则A物质的平均反应速率为
1
参考答案:(1)A (2)3A B+3C (3)0.6mol·L-1·min-1
解析:(1)由题图可知,随着反应的进行,A的浓度减小,B、C的浓度增大,说明A是反应物,B、C是生成物。
(2)0~tmin,A的浓度变化量△c(A)=-1.2mol·L-1,B的浓度变化量△c(B)=0.4mol·L-1,C的浓度变化量△c(C)=1.2mol·L-1A、
1
B、C三种物质的浓度变化量绝对值之比为3:1:3,最终各物质的浓度不变且均不为零,故该反应为可逆反应,化学方程
式为3A B+3C。(3)v(A)= =0.6mol·L-1·min-1