文档内容
2.2.1 化学平衡状态 化学平衡常数 练习(原卷版)
1.在一个恒容密闭容器中发生反应:2SO (g)+O (g) 2SO (g),反应过程中某一时刻测得
2 2 3
SO 、O 、SO 的浓度分别为1.0mo1•L﹣1、1.0mo1•L﹣1⇌、0.5mo1•L﹣1,当反应达到最大限度时,
2 2 3
可能出现的数据是( )
A.c(SO )═1.5mo1•L﹣1 B.c(O )=c(SO )═0.75mo1•L﹣1
3 2 3
C.c(O )═1.25mo1•L﹣1 D.c(SO )+c(SO )═1.5mo1•L﹣1
2 2 3
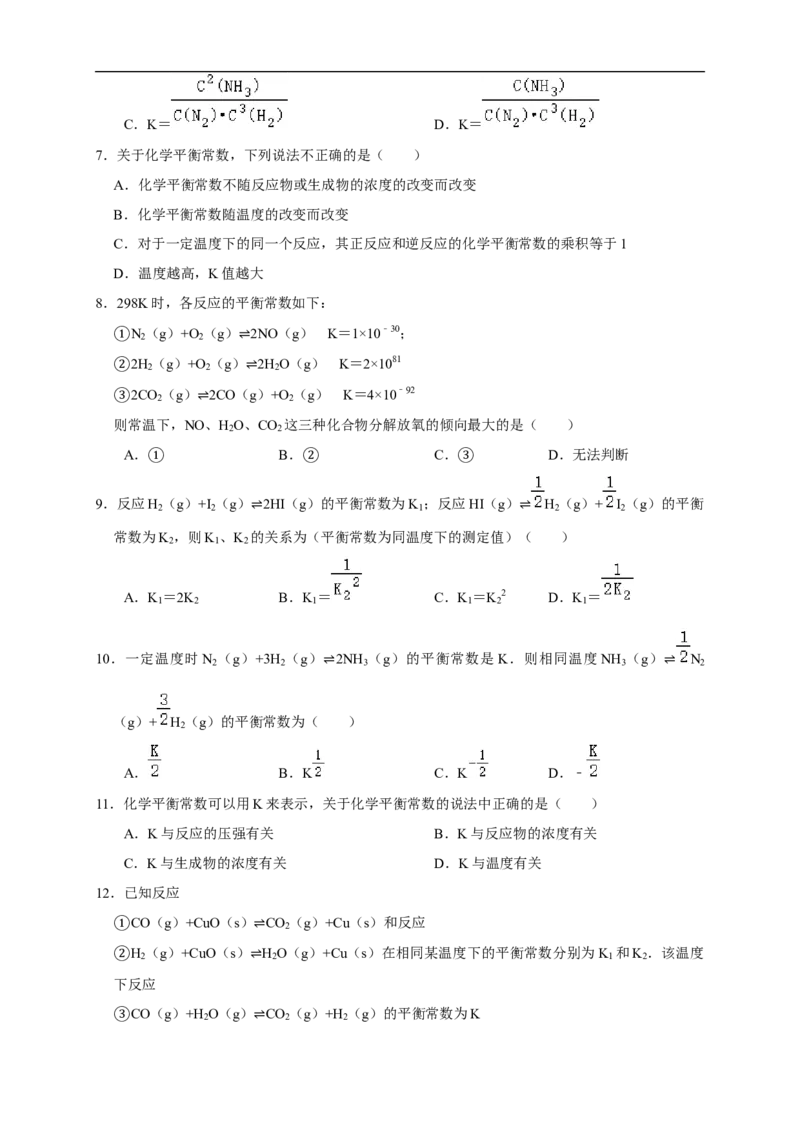
2.观察图:对合成氨反应中,下列叙述错误的是( )
A.开始反应时,正反应速率最大,逆反应速率为零
B.随着反应的进行,正反应速率逐渐减小,逆反应速率逐渐增大
C.反应到达t 时,正反应速率与逆反应速率相等,反应停止
1
D.反应在t 之后,正反应速率与逆反应速率相等,反应达到化学平衡状态
1
3.在一定条件下,使SO 和O 在一密闭容器中进行反应,下列说法中不正确的是( )
2 2
A.反应开始时,正反应速率最大,逆反应速率为零
B.随着反应的进行,正反应速率逐渐减小,最后为零
C.随着反应的进行,逆反应速率逐渐增大,最后不变
D.随着反应的进行,正反应速率逐渐减小,最后不变
4.已知合成氨反应N (g)+3H (g) 2 NH (g)△H=﹣92kJ•mol﹣1,在恒温恒容的密闭容器
2 2 3
中通入2 mol N 和6 mol H ,达平衡⇌时放出热量73.0 kJ,则N 的转化率最接近( )
2 2 2
A.40% B.80% C.30% D.60%
5.对于反应2A(g)+xB(g) 4C(g)达到平衡时 C的浓度为1.5 mol•L﹣1,当其它条件不变,
把体积扩大1倍时,测得C的⇌浓度为0.8 mol•L﹣1,则x的值为( )
A.1 B.2 C.3 D.4
6.已知可逆反应 N (g)+3H (g) 2NH (g)达到平衡时,其平衡常数表达式正确的是
2 2 3
( ) ⇌
A.K= B.K=C.K= D.K=
7.关于化学平衡常数,下列说法不正确的是( )
A.化学平衡常数不随反应物或生成物的浓度的改变而改变
B.化学平衡常数随温度的改变而改变
C.对于一定温度下的同一个反应,其正反应和逆反应的化学平衡常数的乘积等于1
D.温度越高,K值越大
8.298K时,各反应的平衡常数如下:
N (g)+O (g) 2NO(g) K=1×10﹣30;
2 2
①2H
2
(g)+O
2
(g)⇌ 2H
2
O(g) K=2×1081
②2CO (g) 2CO(⇌g)+O (g) K=4×10﹣92
2 2
③则常温下,NO⇌、H
2
O、CO
2
这三种化合物分解放氧的倾向最大的是( )
A. B. C. D.无法判断
① ② ③
9.反应H (g)+I (g) 2HI(g)的平衡常数为K ;反应HI(g) H (g)+ I (g)的平衡
2 2 1 2 2
常数为K ,则K 、K 的⇌关系为(平衡常数为同温度下的测定值)(⇌ )
2 1 2
A.K =2K B.K = C.K =K 2 D.K =
1 2 1 1 2 1
10.一定温度时N (g)+3H (g) 2NH (g)的平衡常数是K.则相同温度NH (g) N
2 2 3 3 2
⇌ ⇌
(g)+ H (g)的平衡常数为( )
2
A. B.K C.K D.﹣
11.化学平衡常数可以用K来表示,关于化学平衡常数的说法中正确的是( )
A.K与反应的压强有关 B.K与反应物的浓度有关
C.K与生成物的浓度有关 D.K与温度有关
12.已知反应
CO(g)+CuO(s) CO (g)+Cu(s)和反应
2
①H
2
(g)+CuO(s)⇌H
2
O(g)+Cu(s)在相同某温度下的平衡常数分别为K
1
和K
2
.该温度
②下反应 ⇌
CO(g)+H O(g) CO (g)+H (g)的平衡常数为K
2 2 2
③ ⇌则下列说法正确的是( )
A.K =
1
B.K=
C.对于反应 ,恒温恒容时,增大压强,c(H )一定减小
2
D.对于反应③,恒容时,温度升高,c(H
2
)减小,则该反应的焓变为正值
13.下列有关平衡③常数的说法中,正确的是( )
A.改变条件,反应物的转化率增大,平衡常数也一定增大
B.反应2NO (g) N O (g)△H<0,升高温度该反应平衡常数增大
2 2 4
C.对于给定可逆反⇌应,温度一定时,其正、逆反应的平衡常数相等
D.CO
2
+H
2
CO+H
2
O的平衡常数表达式为K=
14.关于C (s)+H O (g) CO (g)+H (g)的平衡常数书写形式,正确的是( )
2 2
⇌
A.K= B.K=
C.K= D.K=
15.将固体NH I置于密闭容器中,在某温度下发生下列反应: NH I(s) NH (g)+HI
4 4 3
(g), 2HI(g) H (g)+I (g),当反应达到平衡时①,测得 c(H ⇌)=0.5mol/L,c
2 2 2
(HI)=②4mol/L,则反⇌应 的平衡常数为( )
A.4(mol/L) 2 ① B.16(mol/L) 2
C.20(mol/L) 2 D.25(mol/L) 2
16.将固体NH I置于某体积不变的密闭容器中,在某温度下发生下列反应: NH I(s) NH
4 4 3
(g)+HI(g); 2HI(g) H (g)+I (g),平衡时,c(HI)=6mo①l•L﹣1,c(H⇌)=
2 2 2
1mol•L﹣1,则此温②度下反应 的⇌平衡常数为( )
A.36 B①.49 C.48 D.64
17.将1mol N O 置于2L密闭容器中,在一定温度下发生下列反应:
2 5
2N O (g) 2N O (g)+O (g); N O (g) 2NO (g).达到平衡时,c(O )=
2 5 2 4 2 2 4 2 2
①0.2mol•L﹣1,c(⇌NO )=0.6mol•L﹣1,则②此温度下反应⇌ 的平衡常数为( )
2
①A.3.2 B.0.2 C. D.
18.向2L的密闭容器中充入1mol A和1mol B,反应A(g)+B(g) C(g)+D(g)△H的平
衡常数(K)和温度(T)的关系如下。 800℃时,经5s反应达到平衡⇌状态,此时B的平均反应
速率v(B)=0.04mol/(L•s)。下列说法不正确的是( )
温度/℃ 700 800 900
平衡常数 0.1 X 1
A.平衡时,c(B) 为0.6molL﹣1
B.800℃时平衡常数X=
C.△H>0
D.900℃该反应达到平衡状态时,A的物质的量为0.5mol
19.某温度时,N +3H 2NH 的平衡常数K=16,则此温度下,NH H + N 的平衡常数为(
2 2 3 3 2 2
) ⇌ ⇌
A.0.25 B.4 C.2 D.256
20.已知热化学方程式:aX(g)+3Y(s) bZ(g)△H<0.现在2L的密闭容器中加入0.9mol
的X和1mol的Y,当Y的物质的量减少⇌0.75mol时,达到平衡状态,此时X、Z的浓度分别是
0.2mol/L和0.5mol/L,该温度下的平衡常数为( )
A. B. C.35 D.20
21.一定温度下,某气体反应达到化学平衡,平衡常数K=c(A)•c2(B)/c2(E)•c(F),恒容
时,若温度适当降低,则F的浓度增加,下列说法中正确的是( )
A.降低温度,正反应速率减小、逆反应速率增大
B.增大c(A)、c(B),K增大
C.该反应的化学方程式为2E(g)+F(s) A(g)+2B(g)
D.该反应的焓变△H>0 ⇌
22.将固体NH I置于密闭容器中,在一定温度下发生下列反应:
4
NH I(s) NH (g)+HI(g);
4 3
①2HI(g) ⇌H
2
(g)+I
2
(g)
②达到平衡时,⇌c(H
2
)=0.25mol/L,c(HI)=5mol/L,
则此温度下反应 的平衡常数(单位:mol2•L﹣2)为( )
A.25 ① B.0.025 C.30.25 D.27.523.二甲醚(CH OCH )是一种重要的清洁燃料,可以通过CH OH分子间脱水制得:2CH OH
3 3 3 3
(g) CH OCH (g)+H O(g)△H=﹣23.5J•mol﹣1.在T ℃,恒容密闭容器中建立上述平衡,
3 3 2 1
体系中⇌各组分浓度随时间变化如图所示.
上述由甲醇制二甲醚的反应属于_放热_反应.在T ℃时,反应的平衡常数为_5_;
1
①相同条件下,若改变起始浓度,某时刻各组分浓度依次为 c(CH OH)=0.4mol•L﹣1,c
3
②(H O)=0.6mol•L﹣1、c(CH OCH )=1.2mol•L﹣1,此时正、逆反应速率的大小:v(正)_
2 3 3
>_v(逆)(填“>”、“<”或“=”).
24.化学反应原理在科研和生产中有广泛应用.
Ⅰ、利用“化学蒸气转移法”制备TaS 晶体,发生如下反应:
2
TaS (s)+2I (g)═TaI (g)+S (g)△H>0 ( I)
2 2 4 2
(1)反应( I)的平衡常数表达式K=____________________,
(2)若K=1,向某恒容密闭容器中加入1mol I (g)和足量TaS (s),I (g)的平衡转化率
2 2 2
为______________.
Ⅱ、恒温下,在容积为2L的恒容密闭容器A中通入1mol N 与1mol H 的混合气体,发生如下
2 2
反应:N (g)+3H (g) 2NH (g),△H<0,一段时间后,达到平衡,若平衡时氨气的物
2 2 3
质的量为0.4mol. ⇌
(1)此温度时该反应的K值为___________________.
(2)若在此温度下,向另一容积为1L的恒容容器B中按物质的量分别为2mol、1mol、1mol充
入N 、H 、NH ,此时,该反应是否处于平衡状态___________________(填“是”或“否”),
2 2 3
此时若没有达平衡,反应向___________________方向进行(填“正”或“逆”).
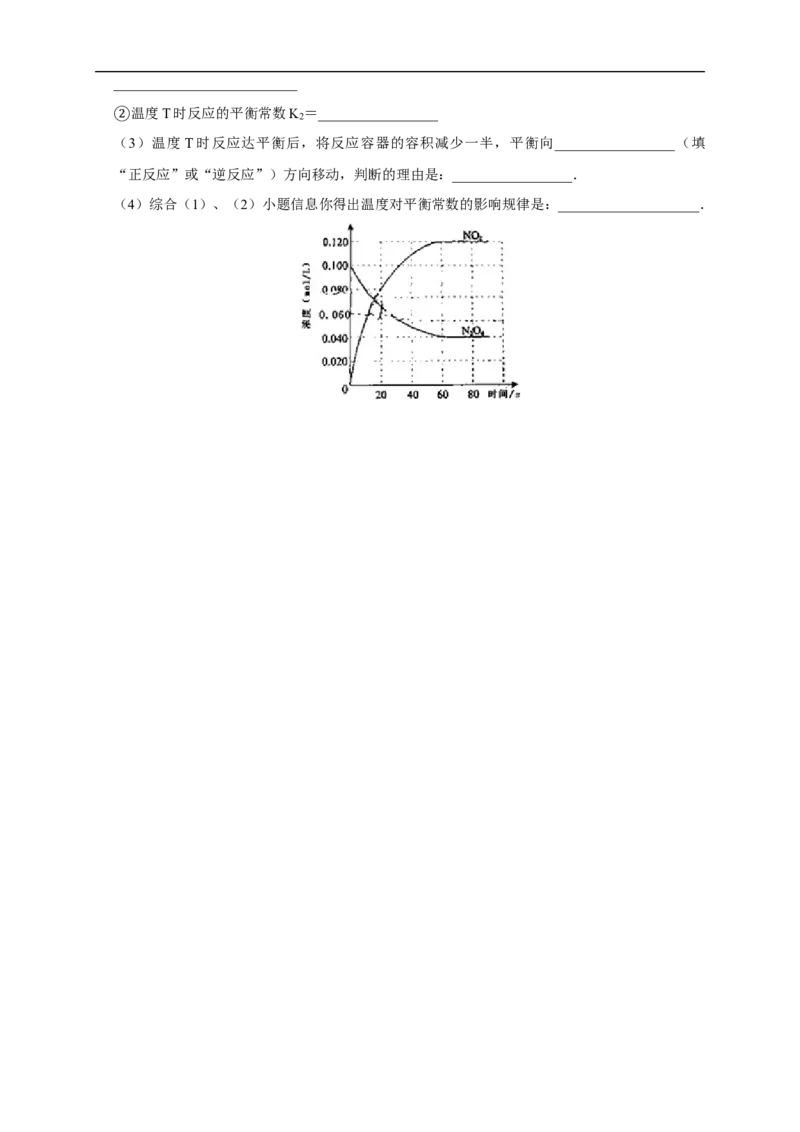
25.在容积为1.00L的容器中,通入一定量的N O ,发生反应N O (g) 2NO (g),随温度升
2 4 2 4 2
高,混合气体的颜色变深.回答下列问题: ⇌
(1)反应的△H__________________0(填“大于”“小于”);100℃时,体系中各物质浓度
随时间变化如上图所示.在0~60s时段,反应速率v(N
2
O
4
)为_________________mol·L﹣1·s
﹣1反应的平衡常数K =_________________.
1
(2)100℃时达到平衡后,改变反应温度为T,c(N
2
O
4
)以0.0020mol·L﹣1·s﹣1的平均速率降
低,经10s又达到平衡.
T___________________100℃ ( 填 “ 大 于 ” “ 小 于 ” ) , 判 断 理 由 是
①__________________________
温度T时反应的平衡常数K =_________________
2
②(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向_________________(填
“正反应”或“逆反应”)方向移动,判断的理由是:_________________.
(4)综合(1)、(2)小题信息你得出温度对平衡常数的影响规律是:____________________.