文档内容
化学
⼀、九省联考命制背景
⼆、����年⾼考各地化学试卷使⽤情况
三、新⾼考化学试卷结构分析
四、�新七省�联考化学试卷考情分析
五、备考策略
⼀、九省联考命制背景
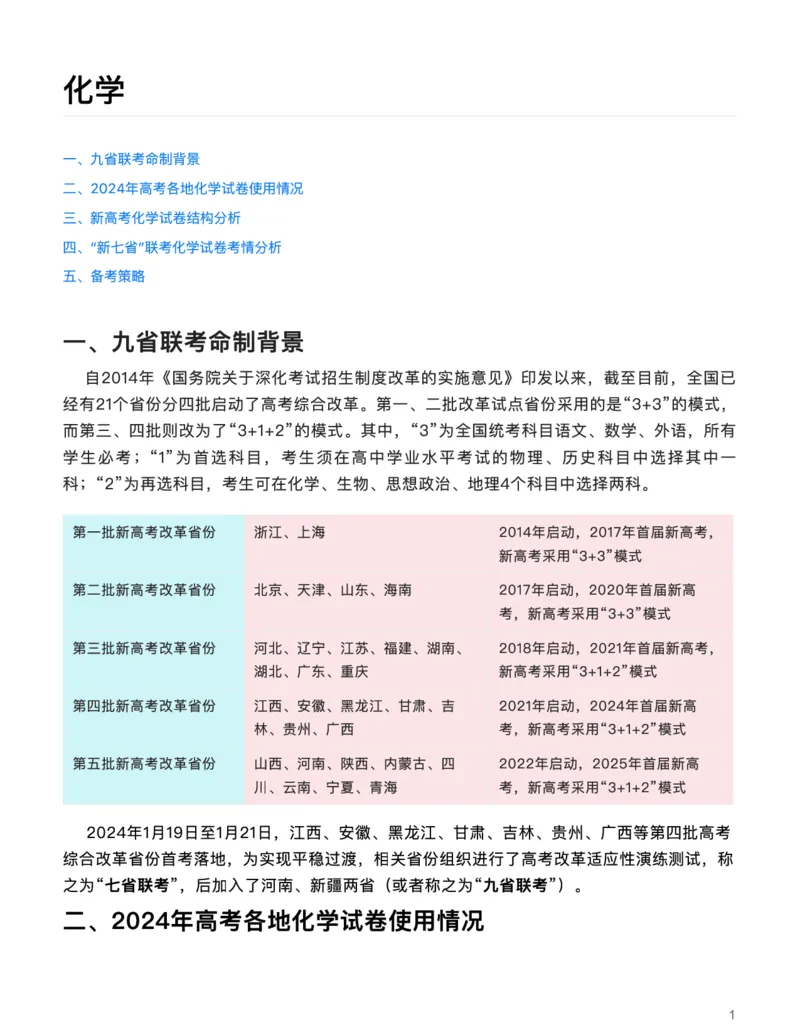
⾃2014年《国务院关于深化考试招⽣制度改⾰的实施意⻅》印发以来,截⾄⽬前,全国已
经有21个省份分四批启动了⾼考综合改⾰。第⼀、⼆批改⾰试点省份采⽤的是“3+3”的模式,
⽽第三、四批则改为了“3+1+2”的模式。其中,“3”为全国统考科⽬语⽂、数学、外语,所有
学⽣必考;“1”为⾸选科⽬,考⽣须在⾼中学业⽔平考试的物理、历史科⽬中选择其中⼀
科;“2”为再选科⽬,考⽣可在化学、⽣物、思想政治、地理4个科⽬中选择两科。
第⼀批新⾼考改⾰省份 浙江、上海 2014年启动,2017年⾸届新⾼考,
新⾼考采⽤“3+3”模式
第⼆批新⾼考改⾰省份 北京、天津、⼭东、海南 2017年启动,2020年⾸届新⾼
考,新⾼考采⽤“3+3”模式
第三批新⾼考改⾰省份 河北、辽宁、江苏、福建、湖南、 2018年启动,2021年⾸届新⾼考,
湖北、⼴东、重庆 新⾼考采⽤“3+1+2”模式
第四批新⾼考改⾰省份 江⻄、安徽、⿊⻰江、⽢肃、吉 2021年启动,2024年⾸届新⾼
林、贵州、⼴⻄ 考,新⾼考采⽤“3+1+2”模式
第五批新⾼考改⾰省份 ⼭⻄、河南、陕⻄、内蒙古、四 2022年启动,2025年⾸届新⾼
川、云南、宁夏、⻘海 考,新⾼考采⽤“3+1+2”模式
2024年1⽉19⽇⾄1⽉21⽇,江⻄、安徽、⿊⻰江、⽢肃、吉林、贵州、⼴⻄等第四批⾼考
综合改⾰省份⾸考落地,为实现平稳过渡,相关省份组织进⾏了⾼考改⾰适应性演练测试,称
之为“七省联考”,后加⼊了河南、新疆两省(或者称之为“九省联考”)。
⼆、2024年⾼考各地化学试卷使⽤情况
1
{#{QQABAY6AggggApBAAAgCAQVQCkOQkBACAAoOABAMoAIASRFABAA=}#}2024年⾸次实⾏新⾼考的7个省份:江⻄、安徽、贵州、⼴⻄、⿊⻰江、吉林、⽢肃(第四批)
已进⼊新⾼考单独命题的省份:浙江、上海(第⼀批)
北京、天津、⼭东、海南(第⼆批)
河北、辽宁、江苏、福建、湖南、湖北、⼴东、重庆(第三
批)
全国⼄卷:内蒙古、⻘海、陕⻄、宁夏(⽼教材)
河南、⼭⻄、新疆(新教材)
全国甲卷:四川、⻄藏(⽼教材)
云南(新教材)
三、新⾼考化学试卷结构分析
卷别 时间 分值 试卷结构(题型、题量及分值)
浙江卷 90min 100 选择题16道(每⼩题3分,共48分),⾮选择题5道(共52分)
分
上海卷 60min 100 5-6道情境综合题(选择题穿插其中,含少数双选题(题上注明)(整卷
分 客观题分值占30%-40%,主观题约占60%-70%,涉及实验分值约占
20%)
天津卷 60min 100 选择题12道(每⼩题3分,共36分),⾮选择题4道(共64分)
分
⼭东卷 90min 100 选择题15道(单项选择题10道,每⼩题2分,共20分;不定项选择题5
分 道,每⼩题4分,共20分),⾮选择题5道(共60分)
海南卷 90min 100 选择题14道(单项选择题8道,每⼩题2分,共16分;不定项选择题6道,
分 每⼩题4分,共24分),⾮选择题5道(共60分)
⼴东卷 75min 100 选择题16道(第1~10⼩题,每⼩题2分;第11~16⼩题,每⼩题4分;共44
分 分。),⾮选择题4道(共56分)
北京卷 90min 100 选择题14道(每⼩题3分,共42分),⾮选择题5道(共58分)
分
江苏卷 75min 100 选择题13道(每⼩题3分,共39分),⾮选择题4道(共61分)
分
福建卷 75min 100 选择题10道(每⼩题4分,共40分),⾮选择题4道(共60分)
分
河北卷 75min 100 选择题14道(每⼩题3分,共42分),⾮选择题4道(共58分)
分
2
{#{QQABAY6AggggApBAAAgCAQVQCkOQkBACAAoOABAMoAIASRFABAA=}#}重庆卷 75min 100 选择题14道(每⼩题3分,共42分),⾮选择题4道(共58分)
分
湖南卷 75min 100 选择题14道(每⼩题3分,共42分),⾮选择题4道(共58分)
分
湖北卷 75min 100 选择题15道(每⼩题3分,共45分),⾮选择题4道(共55分)
分
辽宁卷 75min 100 选择题15道(每⼩题3分,共45分),⾮选择题4道(共55分)
分
⿊⻰ 75min 100 选择题15道(每⼩题3分,共45分),⾮选择题4道(共55分)
江、吉 分
林卷
江⻄卷 75min 100 选择题14道(每⼩题3分,共42分),⾮选择题4道(共58分)
分
安徽卷 75min 100 选择题14道(每⼩题3分,共42分),⾮选择题4道(共58分)
分
贵州卷 75min 100 选择题14道(每⼩题3分,共42分),⾮选择题4道(共58分)
分
⼴⻄卷 75min 100 选择题14道(每⼩题3分,共42分),⾮选择题4道(共58分)
分
⽢肃卷 75min 100 选择题14道(每⼩题3分,共42分),⾮选择题4道(共58分)
分
四、“新七省”联考化学试卷考情分析
试卷结构⽅⾯
安徽、江⻄、贵州、⼴⻄、⽢肃为“14+4”,⿊⻰江、吉林为“15+4”(⿊⻰江吉林卷试题结构
及考察的⼴度和深度贴合辽宁卷新⾼考题型)
整体难度
难度适中,没有偏题、怪题
传递的信息
试卷结构⽐较新,信息给予的⽅式⽐较灵活
情境创设丰富,⽂字表述题较多,阅读量较⼤
对学⽣提取、转化、应⽤信息的能⼒要求较⾼
要关注新旧教材的变化,尤其关注新教材新增的内容,例如适应性试题出现了超分⼦等,
3
{#{QQABAY6AggggApBAAAgCAQVQCkOQkBACAAoOABAMoAIASRFABAA=}#}2022⾼考试题出现了胺类物质(含氮有机物)
相关内容的界定最好以新教材为准,例如官能团的名称等,具体原则由各省份⾃⼰把握
各省份教材不同,⾼考命题依托于课程标准,不完全以各省份教材为依据
⾼考以前出现过的问题应重视,命题专家可能认为“考过即已知”,例如分压平衡等
试卷名称 安徽 江⻄
试卷结构 考试时间:75分钟;满分:100分 考试时间:75分钟;满分:100分
题量:选择题14道(每⼩题3分,共42 题量:选择题14道(每⼩题3分,共42
分),⾮选择题4道(共58分) 分),⾮选择题4道(共58分)
总体分析 难度中等,试卷中考查内容涵盖⾼中化学 难度中等,试题突出对信息摄取、吸收
重要的元素化合物知识、基本概念与理 和整合的能⼒。强调科学思维和⽅法,
论、化学基础实验技能和化学计算,如第1 试题贴近了新⾼考改⾰的趋势,突出对
题以“敦煌壁画传统颜料”为情境考查基本 能⼒和化学学科核⼼素养的综合考查。
概念,涉及的化学物质及其分类作为情境 如第4、6、13题中体现了“宏观辨识与
素材,考查基本概念,意在让学⽣有扎实 微观探析”;第14题体现了“变化观念与
的⽂化积淀。对核⼼主⼲知识不仅仅是体 平 衡 思 想 ” 。 “ 科 学 探 究 与 创 新 意
现在记忆层⾯,还将考查对其在具体问题 识”及“科学态度与社会责任”在第1、
解决过程中的理解和应⽤⽔平。这必将引 6、17题中得到充分体现,考查了学⽣在
导中学化学教学要回归教材、注重基础, 充分理解化学原理的基础上进⾏综合分
紧紧围绕核⼼主⼲知识,强化学⽣应⽤知 析和逻辑思维的能⼒。
识解决实际问题所必备的关键能⼒。
细 选 考点 详细知识点 考点 详细知识点
⽬ 择
第 基本概念 氧化还原反应定义、本质及 化 学 与 ⾦属材料;⾼分⼦材料;新
表 题
1 特征 STSE 型⽆机⾮⾦属材料
分
题
析
第 化 学 与 淀粉、纤维素的⽔解;氨基 物质结构 电⼦式的书写与判断;共价
2 STSE 酸组成、结构共同点 与性质 键的形成及主要类型;利⽤
题 ( 化 学 ⽤ 杂化轨道理论判断分⼦的空
语) 间构型;氢键对物质性质的
影响
第 氧化还原 氧化还原反应的⼏组概念; 常⻅有机 实验室制取⼄炔的装置、操
3 反应 铝;元素、核素、同位素 物的制取 作;仪器使⽤与实验安全;
题 常⽤仪器及使⽤
4
{#{QQABAY6AggggApBAAAgCAQVQCkOQkBACAAoOABAMoAIASRFABAA=}#}第 有机化学 烯烃的顺反异构;油脂的基 阿伏加德 阿伏加德罗常数的应⽤;氧
4 基础 本组成与结构;缩聚反应机 罗常数 化还原反应与NA 相 关 推
题 理及判断 算;原⼦中相关数值及其之
间的相互关系
第 离⼦反应 离⼦⽅程式的正误判断;弱 化学实验 硝酸的强氧化性;⼆氧化硫
5 电解质的电离平衡常数 基础 与其他强氧化剂的反应;⼄
题 醇的消去反应;物质性质的
探究
第 物质结构 共价键的形成及主要类型; 化学反应 原电池正负极判断;原电池
6 与性质 利⽤杂化轨道理论判断分⼦ 原理(电 原理的综合应⽤;新型电池
题 的空间构型;极性分⼦和⾮ 化学)
极性分⼦;弱电解质的电离
平衡常数
第 元素及其 氧化还原反应定义、本质及 物质结构 微粒半径⼤⼩的⽐较⽅法;
7 化合物 特征;硝酸的强氧化性;含 与 性 质 根据原⼦结构进⾏元素种类
题 硫化合物之间的转化 (元素推 推断
断)
第 物质结构 元素周期表结构分析;根据 有机化学 常⻅官能团名称、组成及结
8 与 性 质 原⼦结构进⾏元素种类推 基础 构;烯烃的顺反异构;含碳
题 (元素推 断;电离能变化规律;电负 碳双键物质的性质的推断
断) 性概念
第 化学反应 化学反应速率计算;化学平 物质的制 物质制备的探究;物质性质
9 原理(化 衡的移动及其影响因素;化 备 实验⽅案的设计
题 学反应速 学平衡状态本质及特征
率与化学
平衡)
第 化学基础 影响化学反应速率的因素; 有机物的 有机反应类型;有机官能团
10 实验 盐的⽔解常数;溶度积;分 酸解 的性质及结构;含碳碳双键
题 ⼦的性质 物质的性质的推断
第 化学反应 ⼆次电池;原电池、电解池 化学反应 催化剂对化学反应速率的影
11 原理(电 综合考查 速率与化 响;化学平衡的移动;温度
题 化学) 学平衡 对化学平衡移动的影响;化
学平衡常数的有关计算
5
{#{QQABAY6AggggApBAAAgCAQVQCkOQkBACAAoOABAMoAIASRFABAA=}#}第 化学反应 与物质百分含量变化有关图 酸碱中和 酸碱中和滴定;酸碱中和滴
12 原理(⽔ 像的分析;盐溶液中微粒间 滴定 定的综合考查
题 溶液中的 的电荷守恒、物料守恒、质
离⼦反应 ⼦守恒原理
与平衡)
第 元素化合 电⼦式的书写与判断;利⽤ 物质结构 晶胞;晶胞的有关计算
13 物综合 杂化轨道理论判断化学键杂 与 性 质
题 化类型 (晶胞)
第 反应历程 化学键与化学反应中的能量 化学反应 盐溶液中微粒间的电荷守
14 关系;吸热反应和放热反应 原理(⽔ 恒、物料守恒、质⼦守恒原
题 溶液中的 理;盐溶液中离⼦浓度⼤⼩
离⼦反应 的⽐较
与平衡)
⾮ 第 化学实验 化学平衡常数的影响因素及 化学⼯艺 电解原理;电⼦排布式;常
选 15 综合 应⽤;配合物的结构与性 流程 ⻅⽆机物的制备;常⻅⾦属
择 题 质;常⻅⽆机物的制备 的冶炼
题
第 ⼯艺流程 氧化还原反应⽅程式的书写 化学反应 吸热反应和放热反应;化学
16 综合 与配平;元素周期表提供的 原理综合 平衡常数的有关计算;复合
题 元素信息;常⻅⽆机物的制 判据;利⽤杂化轨道理论判
备 断分⼦的空间构型
第 化学反应 根据△H=反应物的键能之 化学实验 ⼄酸⼄酯制备实验的综合考
17 原理综合 和-⽣成物的键能之和进⾏计 综合 查;常⻅有机物的制备
题 (带晶胞 算;化学平衡常数的有关计
计算) 算;烷烃结构与性质的关
系;晶胞的有关计算
第 有机合成 根据题给物质选择合适合成 有机合成 有机反应类型;根据要求书
18 与推断 路线;有机合成综合考查 与推断 写同分异构体;有机物的推
题 断;根据题给物质选择合适
合成路线
试卷名称 ⿊⻰江、吉林 辽宁(2023年真题卷)
试卷结构 考试时间:75分钟;满分:100分 考试时间:75分钟;满分:100分
题量:选择题15道(每⼩题3分,共45 题量:选择题15道(每⼩题3分,共45
分),⾮选择题4道(共55分) 分),⾮选择题4道(共55分)
6
{#{QQABAY6AggggApBAAAgCAQVQCkOQkBACAAoOABAMoAIASRFABAA=}#}总体分析 难度中等,题型与2023年辽宁⾼考⽐较 难度中等,本试卷试题注重真实情境,将
相似,试题贴近了新⾼考改⾰的趋势,重 知识与⽣产⽣活实际紧密相连,同时,题
视以真实问题情境为测试载体,主要考查 ⽬中的背景信息多与⼯业⽣产有关,体现
教材中的基础实验或者模拟⽣产⽣活实际 了辽宁作为传统⼯业⼤省的地⽅特⾊。试
中的真实实验情境。如第14题以⽣物质电 题创新信息呈现⽅式,设问⻆度独特,要
池为情境,第16题以天⻘⽯(主要成分为 求学⽣多⻆度、多层次、多维度地认识化
硫酸锶)为原料制备碳酸锶,对基础知 学基本规律,在分析和解决化学问题中考
识、反应规律和反应原理进⾏综合考查, 查学科关键能⼒,引导学⽣培育核⼼素
让学⽣运⽤化学知识、运⽤化学原理,提 养。如第17题制备2-噻吩⼄醇,考查有
⾼解决问题的能量,发挥化学⾼考试题的 机物的制备原理,物质分离和提纯,并对
导向作⽤,引导化学教学改⾰ 实验进⾏综合评价,把有机物与化学实验
知识进⾏有机融合,对试题创新进⾏了有
益尝试
细 选 考点 详细知识点 考点 详细知识点
⽬ 择
第 化学与 ⽆机物与有机物;酯化反应; 化学与 ⽆机物与有机物;常⻅能量
表 题
1 STSE 蛋⽩质的变性 STSE 转化形式;⾼分⼦化合物通
分
题 性的概述;合成材料
析
第 传统⽂ 硫与⾦属单质的反应;油脂的 物质结构 ⽴体异构的概念;化学键与
2 化 基本组成与结构;化学科学对 与性质 物质类别关系的判断;电⼦
题 ⼈类⽂明发展的意义 (化学⽤ 排布式;价层电⼦对互斥理
语) 论的应⽤
第 化学⽤ 化学⽤语综合判断;有机物的 常⻅⽆机 氯⽓与⾮⾦属单质的反应;
3 语 结构式、结构简式、⽐例模 物及其应 ⼆氧化硅的化学性质;常⻅
题 型、球棍模型、最简式;电⼦ ⽤ ⾦属的冶炼;氨的合成
式的书写与判断;价层电⼦对
互斥理论的应⽤
第 阿伏加 物质结构基础与NA相关推 化学实验 物质的检验;有机物的检
4 德罗常 算;原⼦中相关数值及其之间 基础 验;常⻅阳离⼦的检验;常
题 数 的相互关系;氢键对物质性质 ⻅阴离⼦的检验
的影响
第 化学实 物质分离、提纯的常⻅化学⽅ 氧化还原 物质的量有关计算;氧化还
5 验基础 法;物质分离、提纯综合应⽤ 反应/阿 原反应有关计算;盐类⽔解
题 伏加德罗 规律;共价键对分⼦构型、
常数 性质的影响
7
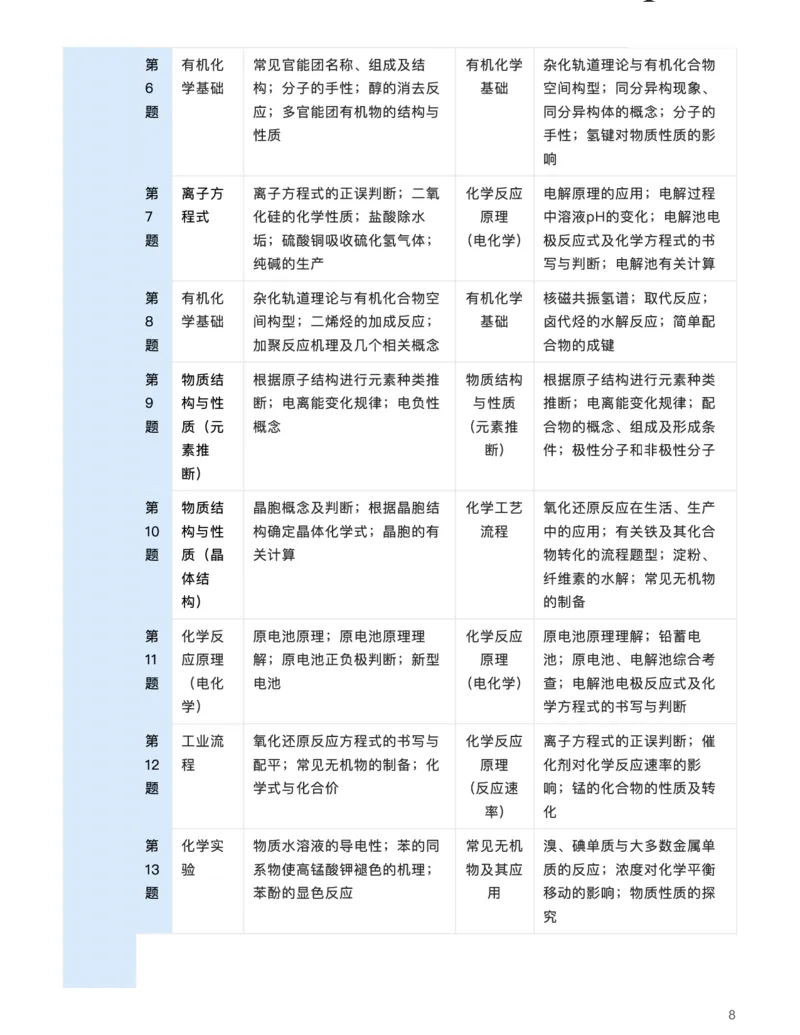
{#{QQABAY6AggggApBAAAgCAQVQCkOQkBACAAoOABAMoAIASRFABAA=}#}第 有机化 常⻅官能团名称、组成及结 有机化学 杂化轨道理论与有机化合物
6 学基础 构;分⼦的⼿性;醇的消去反 基础 空间构型;同分异构现象、
题 应;多官能团有机物的结构与 同分异构体的概念;分⼦的
性质 ⼿性;氢键对物质性质的影
响
第 离⼦⽅ 离⼦⽅程式的正误判断;⼆氧 化学反应 电解原理的应⽤;电解过程
7 程式 化硅的化学性质;盐酸除⽔ 原理 中溶液pH的变化;电解池电
题 垢;硫酸铜吸收硫化氢⽓体; (电化学) 极反应式及化学⽅程式的书
纯碱的⽣产 写与判断;电解池有关计算
第 有机化 杂化轨道理论与有机化合物空 有机化学 核磁共振氢谱;取代反应;
8 学基础 间构型;⼆烯烃的加成反应; 基础 ⻧代烃的⽔解反应;简单配
题 加聚反应机理及⼏个相关概念 合物的成键
第 物质结 根据原⼦结构进⾏元素种类推 物质结构 根据原⼦结构进⾏元素种类
9 构与性 断;电离能变化规律;电负性 与性质 推断;电离能变化规律;配
题 质(元 概念 (元素推 合物的概念、组成及形成条
素推 断) 件;极性分⼦和⾮极性分⼦
断)
第 物质结 晶胞概念及判断;根据晶胞结 化学⼯艺 氧化还原反应在⽣活、⽣产
10 构与性 构确定晶体化学式;晶胞的有 流程 中的应⽤;有关铁及其化合
题 质(晶 关计算 物转化的流程题型;淀粉、
体结 纤维素的⽔解;常⻅⽆机物
构) 的制备
第 化学反 原电池原理;原电池原理理 化学反应 原电池原理理解;铅蓄电
11 应原理 解;原电池正负极判断;新型 原理 池;原电池、电解池综合考
题 (电化 电池 (电化学) 查;电解池电极反应式及化
学) 学⽅程式的书写与判断
第 ⼯业流 氧化还原反应⽅程式的书写与 化学反应 离⼦⽅程式的正误判断;催
12 程 配平;常⻅⽆机物的制备;化 原理 化剂对化学反应速率的影
题 学式与化合价 (反应速 响;锰的化合物的性质及转
率) 化
第 化学实 物质⽔溶液的导电性;苯的同 常⻅⽆机 溴、碘单质与⼤多数⾦属单
13 验 系物使⾼锰酸钾褪⾊的机理; 物及其应 质的反应;浓度对化学平衡
题 苯酚的显⾊反应 ⽤ 移动的影响;物质性质的探
究
8
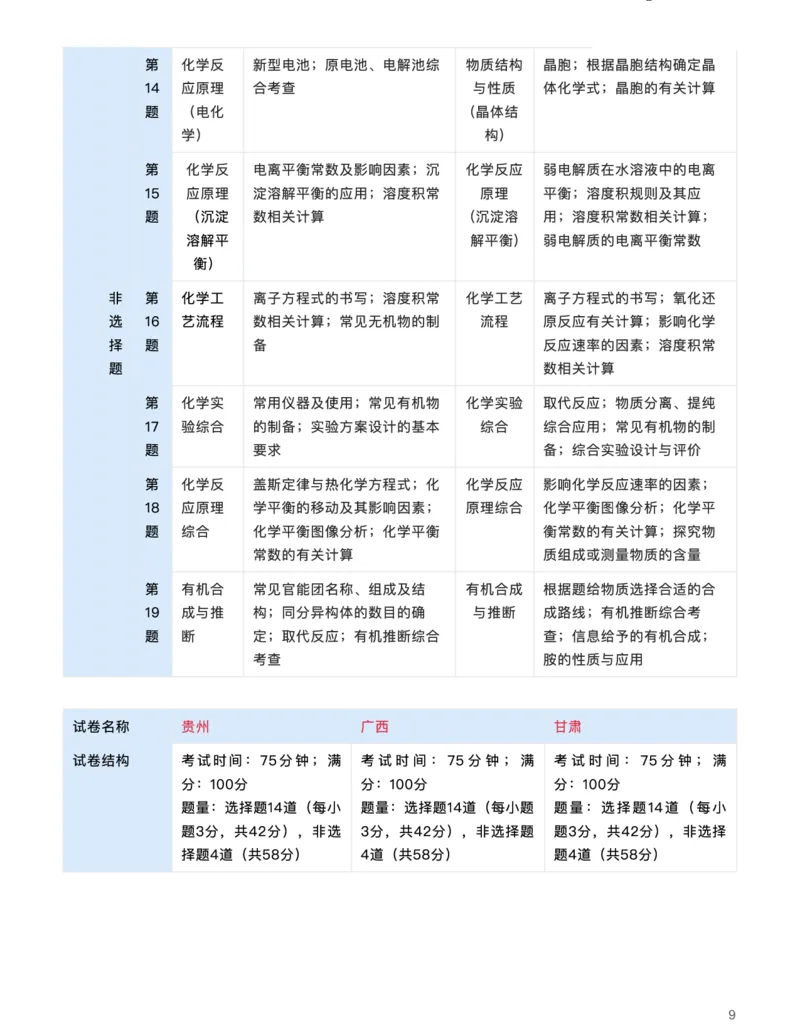
{#{QQABAY6AggggApBAAAgCAQVQCkOQkBACAAoOABAMoAIASRFABAA=}#}第 化学反 新型电池;原电池、电解池综 物质结构 晶胞;根据晶胞结构确定晶
14 应原理 合考查 与性质 体化学式;晶胞的有关计算
题 (电化 (晶体结
学) 构)
第 化学反 电离平衡常数及影响因素;沉 化学反应 弱电解质在⽔溶液中的电离
15 应原理 淀溶解平衡的应⽤;溶度积常 原理 平衡;溶度积规则及其应
题 (沉淀 数相关计算 (沉淀溶 ⽤;溶度积常数相关计算;
溶解平 解平衡) 弱电解质的电离平衡常数
衡)
⾮ 第 化学⼯ 离⼦⽅程式的书写;溶度积常 化学⼯艺 离⼦⽅程式的书写;氧化还
选 16 艺流程 数相关计算;常⻅⽆机物的制 流程 原反应有关计算;影响化学
择 题 备 反应速率的因素;溶度积常
题 数相关计算
第 化学实 常⽤仪器及使⽤;常⻅有机物 化学实验 取代反应;物质分离、提纯
17 验综合 的制备;实验⽅案设计的基本 综合 综合应⽤;常⻅有机物的制
题 要求 备;综合实验设计与评价
第 化学反 盖斯定律与热化学⽅程式;化 化学反应 影响化学反应速率的因素;
18 应原理 学平衡的移动及其影响因素; 原理综合 化学平衡图像分析;化学平
题 综合 化学平衡图像分析;化学平衡 衡常数的有关计算;探究物
常数的有关计算 质组成或测量物质的含量
第 有机合 常⻅官能团名称、组成及结 有机合成 根据题给物质选择合适的合
19 成与推 构;同分异构体的数⽬的确 与推断 成路线;有机推断综合考
题 断 定;取代反应;有机推断综合 查;信息给予的有机合成;
考查 胺的性质与应⽤
试卷名称 贵州 ⼴⻄ ⽢肃
试卷结构 考试时间:75分钟;满 考试时间:75分钟;满 考试时间:75分钟;满
分:100分 分:100分 分:100分
题量:选择题14道(每⼩ 题量:选择题14道(每⼩题 题量:选择题14道(每⼩
题3分,共42分),⾮选 3分,共42分),⾮选择题 题3分,共42分),⾮选择
择题4道(共58分) 4道(共58分) 题4道(共58分)
9
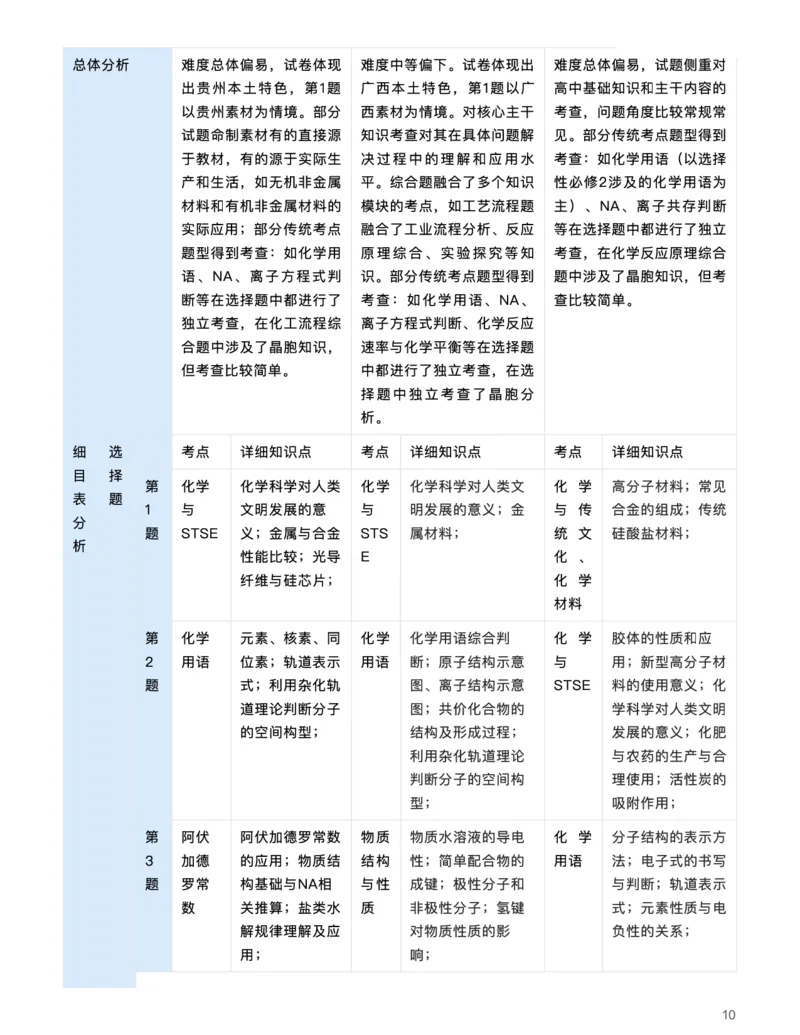
{#{QQABAY6AggggApBAAAgCAQVQCkOQkBACAAoOABAMoAIASRFABAA=}#}总体分析 难度总体偏易,试卷体现 难度中等偏下。试卷体现出 难度总体偏易,试题侧重对
出贵州本⼟特⾊,第1题 ⼴⻄本⼟特⾊,第1题以⼴ ⾼中基础知识和主⼲内容的
以贵州素材为情境。部分 ⻄素材为情境。对核⼼主⼲ 考查,问题⻆度⽐较常规常
试题命制素材有的直接源 知识考查对其在具体问题解 ⻅。部分传统考点题型得到
于教材,有的源于实际⽣ 决过程中的理解和应⽤⽔ 考查:如化学⽤语(以选择
产和⽣活,如⽆机⾮⾦属 平。综合题融合了多个知识 性必修2涉及的化学⽤语为
材料和有机⾮⾦属材料的 模块的考点,如⼯艺流程题 主)、NA、离⼦共存判断
实际应⽤;部分传统考点 融合了⼯业流程分析、反应 等在选择题中都进⾏了独⽴
题型得到考查:如化学⽤ 原理综合、实验探究等知 考查,在化学反应原理综合
语、NA、离⼦⽅程式判 识。部分传统考点题型得到 题中涉及了晶胞知识,但考
断等在选择题中都进⾏了 考查:如化学⽤语、NA、 查⽐较简单。
独⽴考查,在化⼯流程综 离⼦⽅程式判断、化学反应
合题中涉及了晶胞知识, 速率与化学平衡等在选择题
但考查⽐较简单。 中都进⾏了独⽴考查,在选
择题中独⽴考查了晶胞分
析。
细 选 考点 详细知识点 考点 详细知识点 考点 详细知识点
⽬ 择
第 化学 化学科学对⼈类 化学 化学科学对⼈类⽂ 化 学 ⾼分⼦材料;常⻅
表 题
1 与 ⽂明发展的意 与 明发展的意义;⾦ 与 传 合⾦的组成;传统
分
题 STSE 义;⾦属与合⾦ STS 属材料; 统 ⽂ 硅酸盐材料;
析
性能⽐较;光导 E 化 、
纤维与硅芯⽚; 化 学
材料
第 化学 元素、核素、同 化学 化学⽤语综合判 化 学 胶体的性质和应
2 ⽤语 位素;轨道表示 ⽤语 断;原⼦结构示意 与 ⽤;新型⾼分⼦材
题 式;利⽤杂化轨 图、离⼦结构示意 STSE 料的使⽤意义;化
道理论判断分⼦ 图;共价化合物的 学科学对⼈类⽂明
的空间构型; 结构及形成过程; 发展的意义;化肥
利⽤杂化轨道理论 与农药的⽣产与合
判断分⼦的空间构 理使⽤;活性炭的
型; 吸附作⽤;
第 阿伏 阿伏加德罗常数 物质 物质⽔溶液的导电 化 学 分⼦结构的表示⽅
3 加德 的应⽤;物质结 结构 性;简单配合物的 ⽤语 法;电⼦式的书写
题 罗常 构基础与NA相 与性 成键;极性分⼦和 与判断;轨道表示
数 关推算;盐类⽔ 质 ⾮极性分⼦;氢键 式;元素性质与电
解规律理解及应 对物质性质的影 负性的关系;
⽤; 响;
10
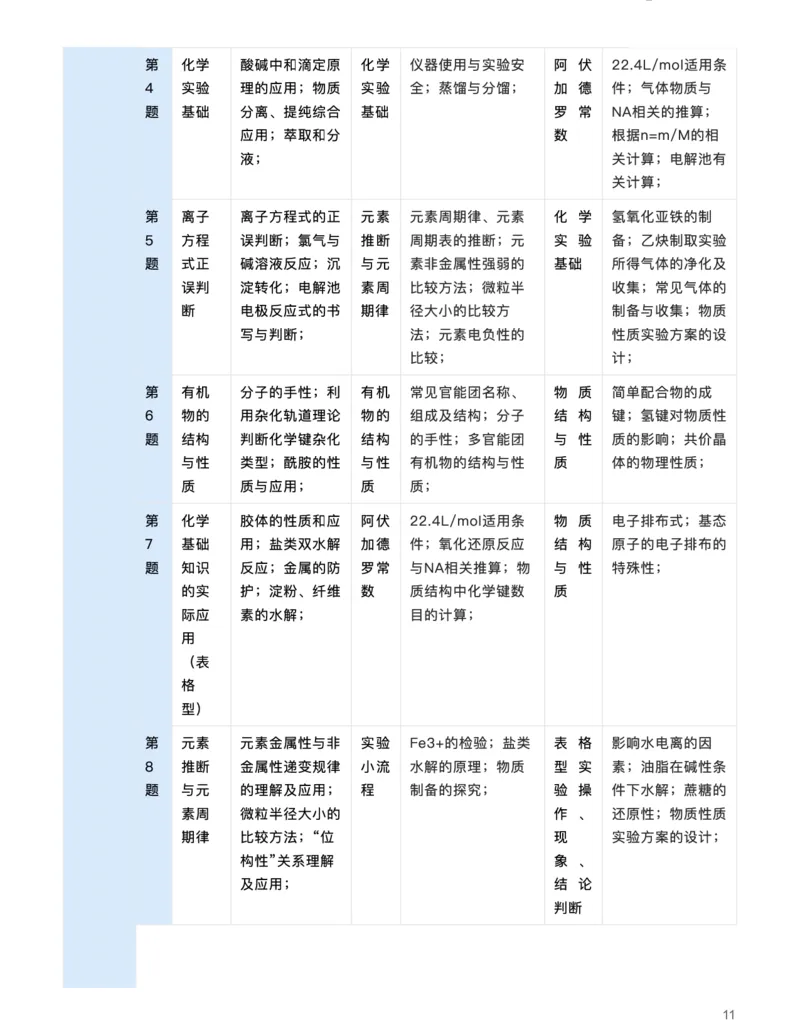
{#{QQABAY6AggggApBAAAgCAQVQCkOQkBACAAoOABAMoAIASRFABAA=}#}第 化学 酸碱中和滴定原 化学 仪器使⽤与实验安 阿 伏 22.4L/mol适⽤条
4 实验 理的应⽤;物质 实验 全;蒸馏与分馏; 加 德 件;⽓体物质与
题 基础 分离、提纯综合 基础 罗 常 NA相关的推算;
应⽤;萃取和分 数 根据n=m/M的相
液; 关计算;电解池有
关计算;
第 离⼦ 离⼦⽅程式的正 元素 元素周期律、元素 化 学 氢氧化亚铁的制
5 ⽅程 误判断;氯⽓与 推断 周期表的推断;元 实 验 备;⼄炔制取实验
题 式正 碱溶液反应;沉 与元 素⾮⾦属性强弱的 基础 所得⽓体的净化及
误判 淀转化;电解池 素周 ⽐较⽅法;微粒半 收集;常⻅⽓体的
断 电极反应式的书 期律 径⼤⼩的⽐较⽅ 制备与收集;物质
写与判断; 法;元素电负性的 性质实验⽅案的设
⽐较; 计;
第 有机 分⼦的⼿性;利 有机 常⻅官能团名称、 物 质 简单配合物的成
6 物的 ⽤杂化轨道理论 物的 组成及结构;分⼦ 结 构 键;氢键对物质性
题 结构 判断化学键杂化 结构 的⼿性;多官能团 与 性 质的影响;共价晶
与性 类型;酰胺的性 与性 有机物的结构与性 质 体的物理性质;
质 质与应⽤; 质 质;
第 化学 胶体的性质和应 阿伏 22.4L/mol适⽤条 物 质 电⼦排布式;基态
7 基础 ⽤;盐类双⽔解 加德 件;氧化还原反应 结 构 原⼦的电⼦排布的
题 知识 反应;⾦属的防 罗常 与NA相关推算;物 与 性 特殊性;
的实 护;淀粉、纤维 数 质结构中化学键数 质
际应 素的⽔解; ⽬的计算;
⽤
(表
格
型)
第 元素 元素⾦属性与⾮ 实验 Fe3+的检验;盐类 表 格 影响⽔电离的因
8 推断 ⾦属性递变规律 ⼩流 ⽔解的原理;物质 型 实 素;油脂在碱性条
题 与元 的理解及应⽤; 程 制备的探究; 验 操 件下⽔解;蔗糖的
素周 微粒半径⼤⼩的 作 、 还原性;物质性质
期律 ⽐较⽅法;“位 现 实验⽅案的设计;
构性”关系理解 象 、
及应⽤; 结 论
判断
11
{#{QQABAY6AggggApBAAAgCAQVQCkOQkBACAAoOABAMoAIASRFABAA=}#}第 物质 键能;元素性质 表格 沉淀转化;元素⾮ 离 ⼦ 限定条件下的离⼦
9 结构 与电负性的关 型实 ⾦属性强弱的⽐较 共 存 共存;
题 与性 系;利⽤杂化轨 验⽬ ⽅法;配制⼀定物 判断
质 道理论判断分⼦ 的、 质的量浓度的溶液
的空间构型; 操作 的步骤、操作;物
质分离、提纯的常
⻅化学⽅法;
第 表格 ⼄醇与钠的反 电化 电解原理的应⽤; 有 机 有机官能团的结构
10 型实 应;铵根离⼦的 学 物 的 及性质;含有酚羟
题 验操 检验;Fe3+的 结 构 基的物质性质的推
作、 检验;葡萄糖与 与 性 断;
现 新制氢氧化铜溶 质
象、 液的反应;化学
结论 实验⽅案的设计
判断 与评价;
第 微型 氧化还原反应在 离⼦ 离⼦⽅程式的正误 电 解 弱电解质在⽔溶液
11 ⼯艺 ⽣活、⽣产中的 ⽅程 判断; 质 溶 中的电离平衡;盐
题 流程 应⽤;铝与强碱 式正 液 曲 溶液中微粒间的电
分析 溶液反应;油脂 误判 线 分 荷守恒、物料守
在碱性条件下⽔ 断 析 恒、质⼦守恒原
解;物质分离、 理;
提纯综合应⽤;
第 电解 弱电解质的电离 晶胞 晶胞的有关计算; 电 化 原电池原理的应
12 质溶 平衡;盐溶液中 分析 化学键类型的判 学 ⽤;新型可充电电
题 液分 微粒间的电荷守 与计 断; 池;
析 恒、物料守恒、 算
质⼦守恒原理;
第 电化 原电池⼯作原理 化学 化学平衡的移动及 有 机 常⻅官能团名称、
13 学 的应⽤; 反应 其影响因素;化学 物 的 组成及结构;多官
题 速率 平衡图像分析; 结 构 能团有机物的结构
与化 与 性 与性质;酰胺的性
学平 质 质与应⽤;
衡
12
{#{QQABAY6AggggApBAAAgCAQVQCkOQkBACAAoOABAMoAIASRFABAA=}#}第 化学 反应历程中的能 电解 酸碱中和滴定原理 元 素 元素⾮⾦属性强弱
14 反应 量变化;活化能 质溶 的应⽤;盐溶液中 推 断 的⽐较⽅法;根据
题 能量 及其对反应速率 液曲 微粒间的电荷守 与 元 原⼦结构进⾏元素
与化 的影响;催化剂 线分 恒、物料守恒、质 素 周 种类推断;电离能
学反 对化学反应速率 析 ⼦守恒原理;弱电 期律 变化规律;利⽤杂
应平 的影响; 解质的电离平衡常 化轨道理论判断分
衡 数; ⼦的空间构型;
⾮ 第 化学 常⽤仪器及使 ⼯艺 ⼆氧化硫的化学性 化 学 酸碱中和滴定原理
选 15 实验 ⽤;蒸发与结 流程 质;原电池电极反 实 验 的应⽤;溶度积常
择 题 综合 晶;探究物质组 综合 应式书写;晶体类 综合 数相关计算;物质
题 成或测量物质的 (涉 型判断;物质的⼯ 分离、提纯综合应
含量; 及晶 业制备流程; ⽤;
体简
单判
断)
第 ⼯艺 氧化还原反应⽅ 化学 盖斯定律及其有关 化 学 盖斯定律与热化学
16 流程 程式的书写与配 反应 计算;催化剂对化 反 应 ⽅程式;化学平衡
题 综合 平;溶度积常数 原理 学反应速率的影 原 理 图像分析;化学平
(涉 相关计算;晶胞 综合 响;化学平衡的移 综 合 衡常数和化学反应
及晶 的有关计算;化 动及其影响因素; ( 涉 速率的有关计算;
胞简 学知识在物质⼯ 化学平衡图像分 及 晶 根据晶胞结构确定
单分 业制备中的应 析; 胞 简 晶体化学式;
析) ⽤; 单 分
析)
第 化学 盖斯定律与热化 化学 物质的制备实验探 ⼯ 艺 盐类⽔解在⽣活、
17 反应 学⽅程式;催化 实验 究;产品的纯度分 流 程 ⽣产中的应⽤;物
题 原理 剂对化学反应速 综合 析; 综合 质分离、提纯综合
综合 率的影响;化学 应⽤;化学知识在
平衡常数的有关 物质的⼯业制备流
计算;反应进⾏ 程中的应⽤;
⽅向判据的应
⽤;
13
{#{QQABAY6AggggApBAAAgCAQVQCkOQkBACAAoOABAMoAIASRFABAA=}#}第 有机 根据要求书写同 有机 根据要求书写同分 有 机 常⻅官能团的名
18 化学 分异构体;同分 化学 异构体;逆合成分 化 学 称、组成及结构;
题 合成 异构体的数⽬的 合成 析法;有机推断综 合 成 根据要求书写同分
与推 确定;多官能团 与推 合考查;杂化轨道 与 推 异构体;有机反应
断 有机物的结构与 断 理论理解; 断 类型的判断;有机
性质;有机推断 推断综合考查;
综合考查;
五、备考策略
1、明确考点,把握⽅向
仔细研读《⾼考评价体系说明》,理解其核⼼理念和指导思想,有助于把握⾼考的⽅向和趋
势,为备考提供指导。分析⾼考试题,探索试题与《⾼考评价体系》之间的联系。通过研究历
年真题,发现试题如何体现“核⼼价值、学科素养、关键能⼒、必备知识”这四个层次,从⽽更
有针对性地备考。
2、回归课本,注重细节
教材是命题的出发点和归宿,考题中通常有相当⼀部分内容是依据课本编制的。复习过程中要
对课本上出现的各种形式的知识做⼀个梳理,包括:基本概念和原理、化学⽅程式、化学式、
演示实验、实验现象、实验基本操作、活动与探究、家庭⼩实验、课本例题、课后习题、教材
插图、单元⼩结等等。化学是理科中的⽂科,许多知识点需要记忆。对于⼀些必知必舍近求远
的细节内容要整理出来,利⽤空暇时间读记。
3、精讲精练,提⾼效率
精讲要做到“三讲”、“三不讲”。
“三讲”即:讲理解不了的问题(难点、疑点),讲归纳不了的问题(规律、⽅法),讲运⽤不了的
问题(知识的迁移、思路的点拨)。
“三不讲”即:学⽣已经会了的不讲,学⽣⾃⼰能学会的不讲,讲了学习仍然不会的不讲。
“精练”在讲练结合,注重实效。恰到好处的“练”能帮助学⽣掌握知识、形成技能、提⾼学习
能⼒,可以说“练”是学⽣⽣学习的主要⼿段。
4、科学诊断 对症下药
备考时,要分析⾃⼰在各次重要模拟考试中的答题情况,建⽴⾃⼰的学情诊断报告。⼀是找必
拿分。如:化学与STSE的考点、阿伏伽德罗常数的考查、化学⽤语、元素周期律、实验基
础、有机基础等;⼆是找弱项。如:如电化学、溶液中的离⼦反应与平衡、信息题、反应原理
⼤题等,注意哪类型的题⽬常错或得分率低;三是分析原因,⽐如:知识漏洞、能⼒不⾜或是
解题模型的缺失导致失分;四是明确需求。要有针对性地进⾏复习。对于不常错的题⽬,要隔
三差五做两道,保持解决这类型题⽬的敏感度;对于常错题,要回顾基础知识点,反复练典型
试题,明确试题的题型特点和解题⽅法,构建试题的答题思维模型。
14
{#{QQABAY6AggggApBAAAgCAQVQCkOQkBACAAoOABAMoAIASRFABAA=}#}5、稳定情绪 树⽴信⼼
备考过程中难免会遇到困难和挫折,但要保持积极的⼼态和信⼼。相信⾃⼰经过努⼒⼀定能够
取得好成绩,遇到困难时要勇敢⾯对并寻求解决⽅法。平和积极的⼼态是成功的关键!
15
{#{QQABAY6AggggApBAAAgCAQVQCkOQkBACAAoOABAMoAIASRFABAA=}#}