文档内容
江门市 2024 年普通高中高一调研测试(二)
化学
本试卷8页,20小题,满分100分。考试时间75分钟。
注意事项:
1.答题前,务必将自己的姓名、准考证号填写在答题卡规定的位置上。
2.做选择题时,必须用2B铅笔将答题卷上对应题目的答案标号涂黑,如需改动,用橡皮擦
干净后,再选涂其它答案标号。
3.答非选择题时,必须用黑色字迹钢笔或签字笔,将答案写在答题卡规定的位置上。
4.所有题目必须在答题卡上作答,在试题卷上作答无效。
5.考试结束后,将答题卡交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Zn 65
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小
题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 中华文物,璨若星河。下列文物主材质属于硅酸盐材料的是
A. 铜鼎 B. 陶马
C. 玛瑙环 D. 竹简
A. A B. B C. C D. D
2. 碳基纳米材料如碳量子点、石墨烯等因具有优异的摩擦学性能,是近年来的研究热点之一,其中碳量子
点通常被定义为尺寸小于10nm的碳纳米粒子,下列叙述正确的是
A. 碳纳米粒子属于胶体 B. 石墨烯属于有机高分子材料
C. 石墨烯与碳量子点互为同位素 D. 石墨烯与碳量子点的化学性质基本相同
3. 化学和生活、科技、社会发展息息相关。下列说法正确的是
第1页/共13页
学科网(北京)股份有限公司A. 高纯度的Si常用于制造光导纤维
B. 常用于抗酸药中,其可与胃酸发生中和反应
C. 常用于漂白毛、丝、纸浆等,是利用了其氧化性
D. 火电厂在燃煤中加适量的石灰石,有利于实现碳中和
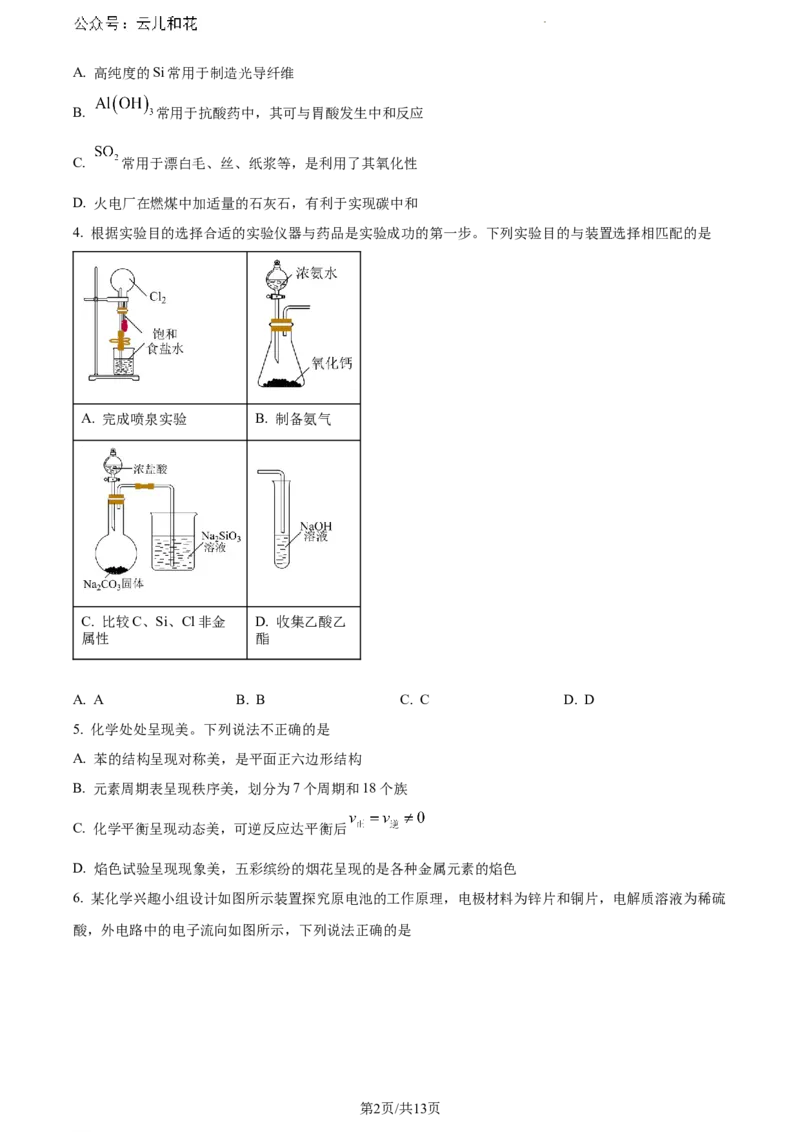
4. 根据实验目的选择合适的实验仪器与药品是实验成功的第一步。下列实验目的与装置选择相匹配的是
A. 完成喷泉实验 B. 制备氨气
C. 比较C、Si、Cl非金 D. 收集乙酸乙
属性 酯
A. A B. B C. C D. D
5. 化学处处呈现美。下列说法不正确的是
A. 苯的结构呈现对称美,是平面正六边形结构
B. 元素周期表呈现秩序美,划分为7个周期和18个族
C. 化学平衡呈现动态美,可逆反应达平衡后
D. 焰色试验呈现现象美,五彩缤纷的烟花呈现的是各种金属元素的焰色
6. 某化学兴趣小组设计如图所示装置探究原电池的工作原理,电极材料为锌片和铜片,电解质溶液为稀硫
酸,外电路中的电子流向如图所示,下列说法正确的是
第2页/共13页
学科网(北京)股份有限公司A. X电极材料为铜,Y电极材料为锌
B. Y电极得电子,发生氧化反应
C. 放电过程中,铜片表面有气泡产生
D. 铜片的电极反应式为
7. “烹饪”出美味,劳动添“趣味”。下列烹饪相关活动中的劳动项目与化学原理均正确的是
选
劳动项目 化学原理
项
A 卤水点豆腐 胶体的聚沉原理
厨房灶具使用燃料从某种主要成分是CO的煤气改为天然 相同体积的煤气和天然气燃烧,煤气
B
气,改小进风口 耗氧量更大
C 为延长腊肉保存时间添加过量亚硝酸钠 亚硝酸钠可以防止腊肉变质
D 制作果酱添加维生素C作抗氧化剂 维生素C具有氧化性
A. A B. B C. C D. D
8. 聚四氟乙烯(如图)可用于制作不粘锅的耐热涂层,关于该有机物的表述不正确的是
A. 属于卤代烃 B. 合成的单体是
C. 可以使溴水褪色 D. 有很高的耐热性和化学稳定性
9. 下列实验操作及对应的现象与结论均正确的是
选
实验操作 现象与结论
项
向盛有待测液的试管中加入NaOH溶液,加热,将湿润
A 试纸未变红,该溶液中不存在
的蓝色石蕊试纸靠近试管口
液面上方出现红棕色气体,铜和稀硝酸
B 将铜丝伸入装有稀硝酸的具支试管中
反应生成
第3页/共13页
学科网(北京)股份有限公司将适量 晶体与 晶体一起放入烧
烧杯与木片黏在一起,该反应吸热,使
C
杯中,并将烧杯放在滴有几滴水的木片上,用玻璃棒快 水凝结成冰
速搅拌
稀硝酸中的铁片溶解并产生气泡,浓硝
D 将质量、大小相同的铁片分别加入浓硝酸和稀硝酸中 酸中的铁片无明显现象,说明稀硝酸的
氧化性比浓硝酸强
A. A B. B C. C D. D
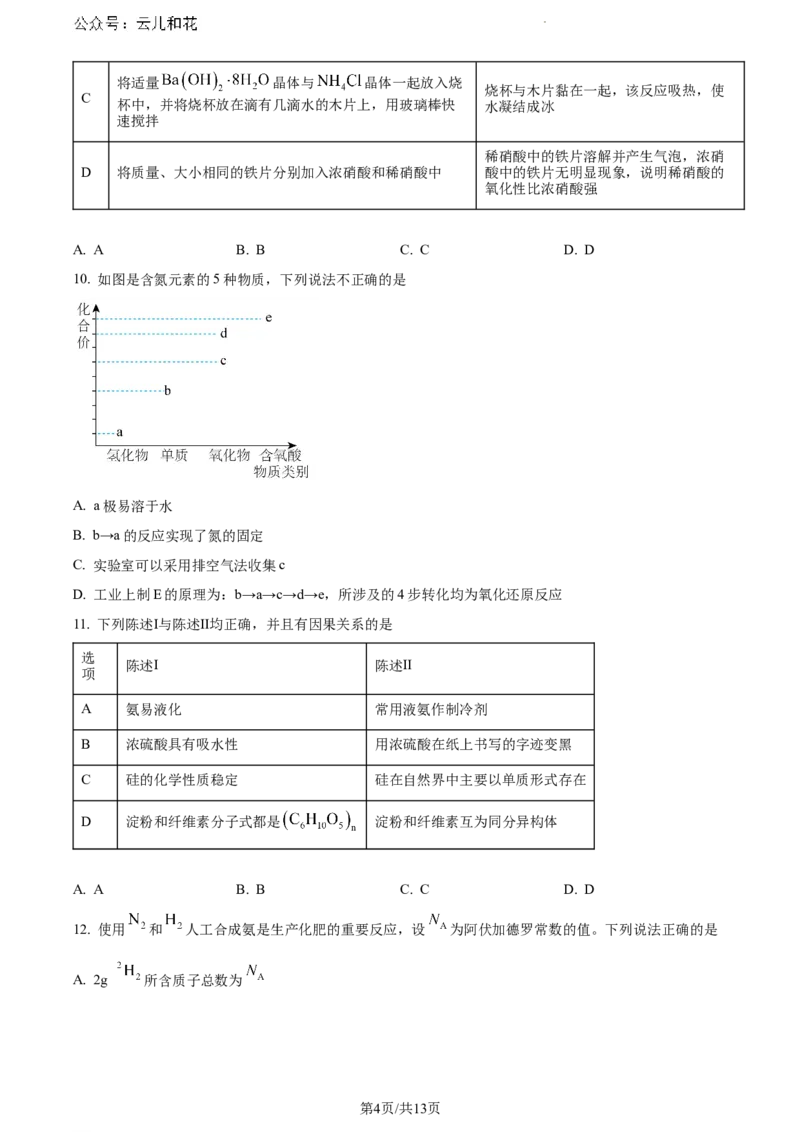
10. 如图是含氮元素的5种物质,下列说法不正确的是
A. a极易溶于水
B. b→a的反应实现了氮的固定
C. 实验室可以采用排空气法收集c
D. 工业上制E的原理为:b→a→c→d→e,所涉及的4步转化均为氧化还原反应
11. 下列陈述Ⅰ与陈述Ⅱ均正确,并且有因果关系的是
选
陈述Ⅰ 陈述Ⅱ
项
A 氨易液化 常用液氨作制冷剂
B 浓硫酸具有吸水性 用浓硫酸在纸上书写的字迹变黑
C 硅的化学性质稳定 硅在自然界中主要以单质形式存在
D 淀粉和纤维素分子式都是 淀粉和纤维素互为同分异构体
A. A B. B C. C D. D
12. 使用 和 人工合成氨是生产化肥的重要反应,设 为阿伏加德罗常数的值。下列说法正确的是
A. 2g 所含质子总数为
第4页/共13页
学科网(北京)股份有限公司B. 每消耗28g ,转移的电子数为
C. 常温常压下,22.4L 中含有的共价键数为
D. 1mol 与足量 充分反应,生成的 分子数为
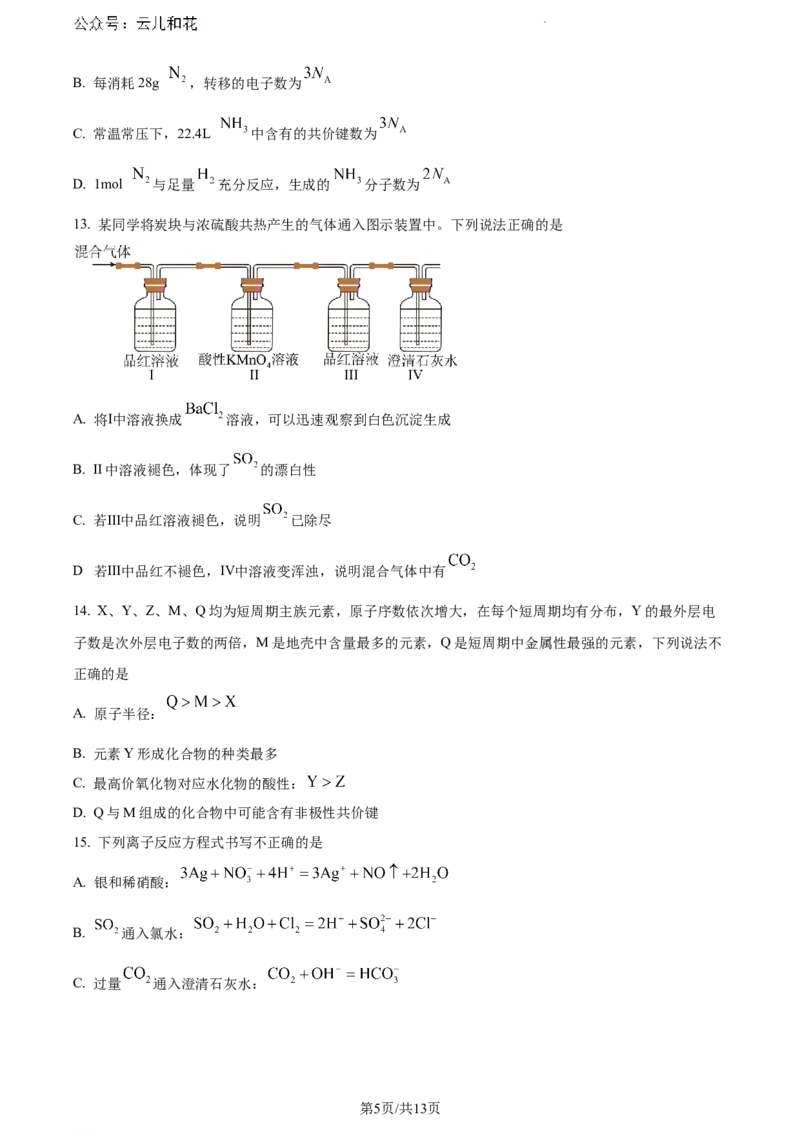
13. 某同学将炭块与浓硫酸共热产生的气体通入图示装置中。下列说法正确的是
A. 将Ⅰ中溶液换成 溶液,可以迅速观察到白色沉淀生成
B. Ⅱ中溶液褪色,体现了 的漂白性
C. 若Ⅲ中品红溶液褪色,说明 已除尽
.
D 若Ⅲ中品红不褪色,Ⅳ中溶液变浑浊,说明混合气体中有
14. X、Y、Z、M、Q均为短周期主族元素,原子序数依次增大,在每个短周期均有分布,Y的最外层电
子数是次外层电子数的两倍,M是地壳中含量最多的元素,Q是短周期中金属性最强的元素,下列说法不
正确的是
A. 原子半径:
B. 元素Y形成化合物的种类最多
C. 最高价氧化物对应水化物的酸性:
D. Q与M组成的化合物中可能含有非极性共价键
15. 下列离子反应方程式书写不正确的是
A. 银和稀硝酸:
B. 通入氯水:
C. 过量 通入澄清石灰水:
第5页/共13页
学科网(北京)股份有限公司D. Al与NaOH溶液反应:
16. 某温度下,在容积为2L的恒容密闭容器中按投料比 通入反应物进行反应,反
应过程中部分物质的物质的量随反应时间的变化如图所示,下列说法正确的是
A. 当 时,该反应达到化学平衡状态
B. 反应达到平衡时充入Ne,生成 的反应速率加快
C. 0~2min内, 反应的平均速率是
D. 通过调控反应条件,可以提高该反应进行的程度
二、非选择题:本题共4小题,共56分。
17. 某实验小组对甲烷与氯气的反应进行了以下探究实验。
(1)查阅资料:甲烷可通过以下反应制取: 。
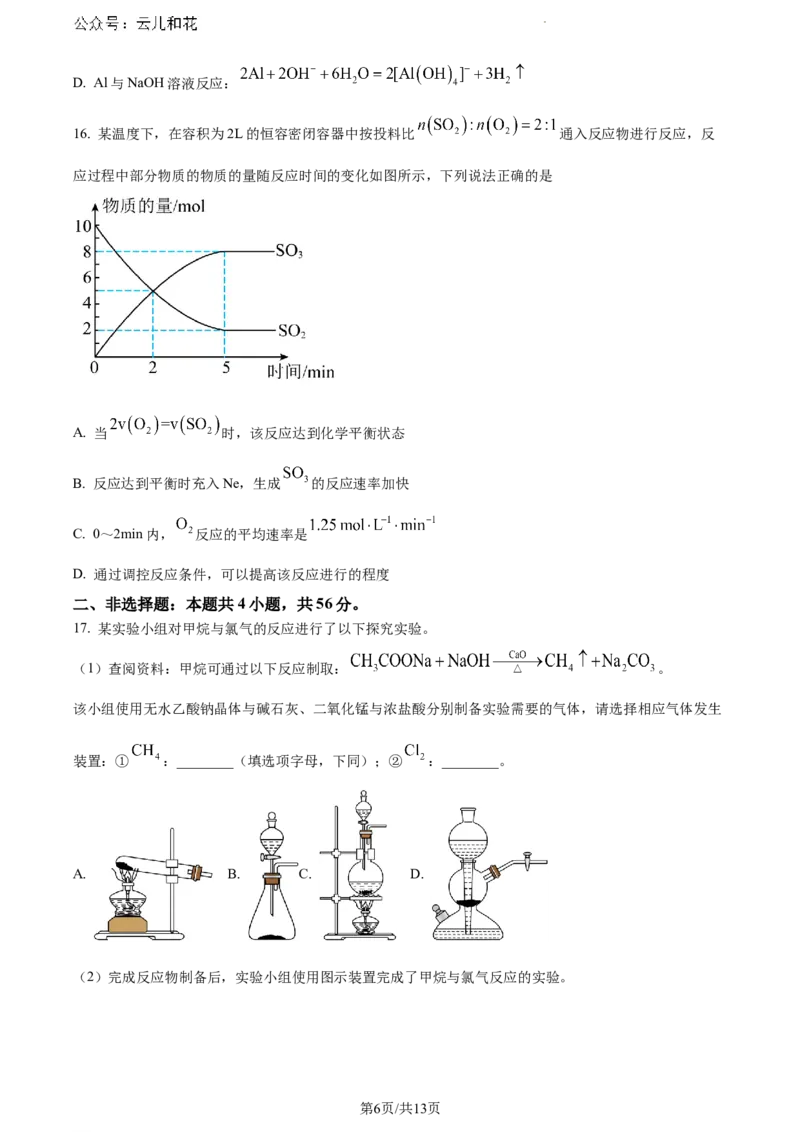
该小组使用无水乙酸钠晶体与碱石灰、二氧化锰与浓盐酸分别制备实验需要的气体,请选择相应气体发生
装置:① :________(填选项字母,下同);② :________。
A. B. C. D.
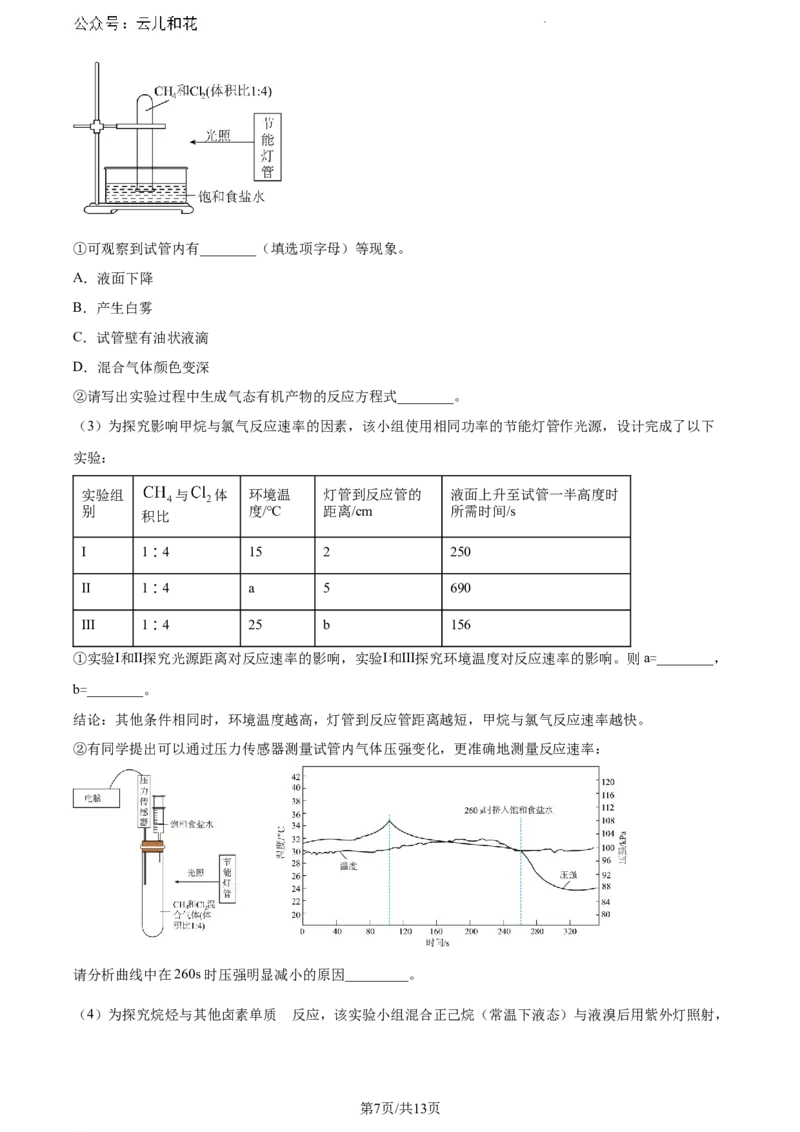
(2)完成反应物制备后,实验小组使用图示装置完成了甲烷与氯气反应的实验。
第6页/共13页
学科网(北京)股份有限公司①可观察到试管内有________(填选项字母)等现象。
A.液面下降
B.产生白雾
C.试管壁有油状液滴
D.混合气体颜色变深
②请写出实验过程中生成气态有机产物的反应方程式________。
(3)为探究影响甲烷与氯气反应速率的因素,该小组使用相同功率的节能灯管作光源,设计完成了以下
实验:
实验组 与 体 环境温 灯管到反应管的 液面上升至试管一半高度时
别 度/℃ 距离/cm 所需时间/s
积比
Ⅰ 1∶4 15 2 250
Ⅱ 1∶4 a 5 690
Ⅲ 1∶4 25 b 156
①实验Ⅰ和Ⅱ探究光源距离对反应速率的影响,实验Ⅰ和Ⅲ探究环境温度对反应速率的影响。则a=________,
b=________。
结论:其他条件相同时,环境温度越高,灯管到反应管距离越短,甲烷与氯气反应速率越快。
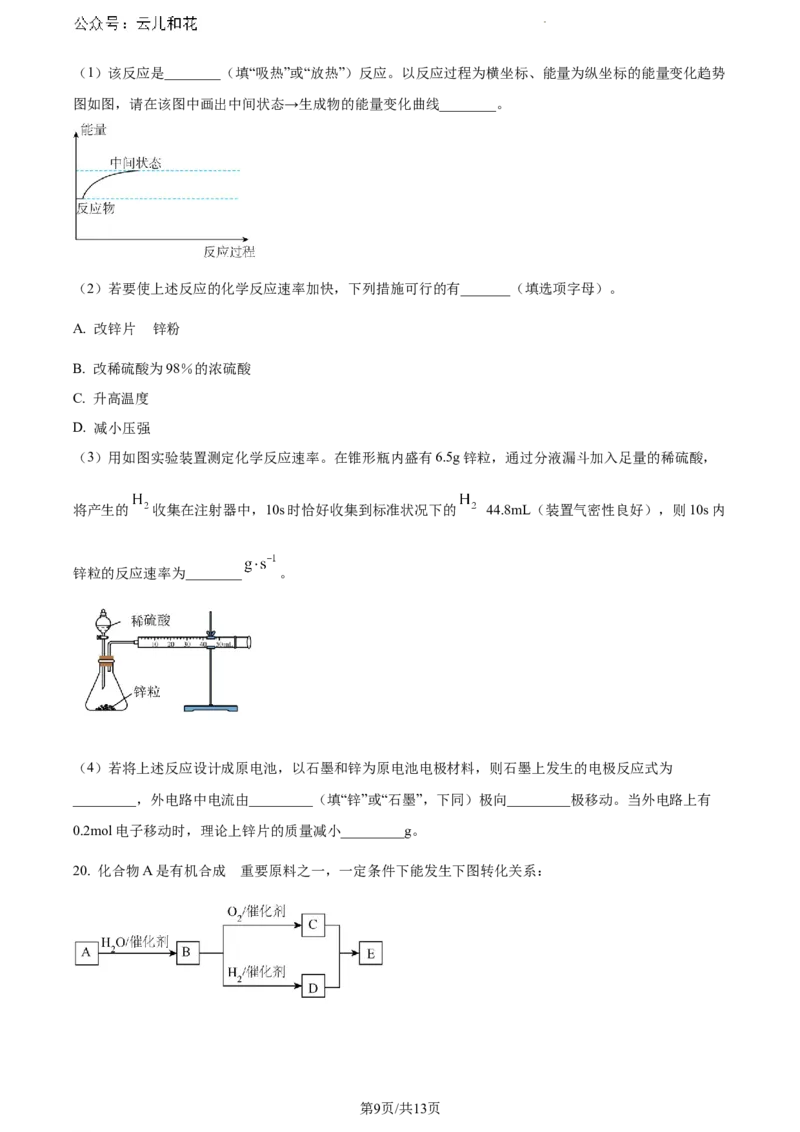
②有同学提出可以通过压力传感器测量试管内气体压强变化,更准确地测量反应速率:
请分析曲线中在260s时压强明显减小的原因_________。
的
(4)为探究烷烃与其他卤素单质 反应,该实验小组混合正己烷(常温下液态)与液溴后用紫外灯照射,
第7页/共13页
学科网(北京)股份有限公司观察到沸腾现象,产生大量气泡。
①同学甲提出猜想:可能是溴单质与正己烷发生了取代反应产生气体,并将产生气体通入 溶液中,
生成淡黄色沉淀,写出在 溶液中发生反应的离子方程式:________。
②同学乙认为该验证方案不严谨,原因是________。
18. 是生产多晶硅的副产物。利用 对废弃的锂电池正极材料 进行氯化处理以回收Li、
Co等金属,工艺路线如下:
回答下列问题:
(1) 中Co元素的化合价为________,Si在元素周期表中的位置是________。
(2)已知烧渣是LiCl、 和 的混合物。
①将“500℃焙烧”后烧渣中剩余的 除去后,再进行水浸、过滤,得到滤饼1,滤饼1的主要成分是
________(填化学式)。
②“500℃焙烧”后剩余的 应先除去,否则水浸 会因剧烈水解生成硅酸( )和另一种酸
而产生大量烟雾,写出 水解的化学方程式________。
(3)已知滤饼2主要为 ,沉钴反应 的离子方程式为________。
(4)鉴别洗净的“滤饼3”和固体 中金属元素常用方法的名称是________。
(5)“850℃煅烧”时发生的反应中氧化剂与还原剂的物质的量之比为________。
19. 化学反应伴随着能量变化,是人类获取能量的重要途径。
某同学以反应 为例,设计了如下实验探究,请按要求回答下列问题。
第8页/共13页
学科网(北京)股份有限公司(1)该反应是________(填“吸热”或“放热”)反应。以反应过程为横坐标、能量为纵坐标的能量变化趋势
图如图,请在该图中画出中间状态→生成物的能量变化曲线________。
(2)若要使上述反应的化学反应速率加快,下列措施可行的有_______(填选项字母)。
为
A. 改锌片 锌粉
B. 改稀硫酸为98%的浓硫酸
C. 升高温度
D. 减小压强
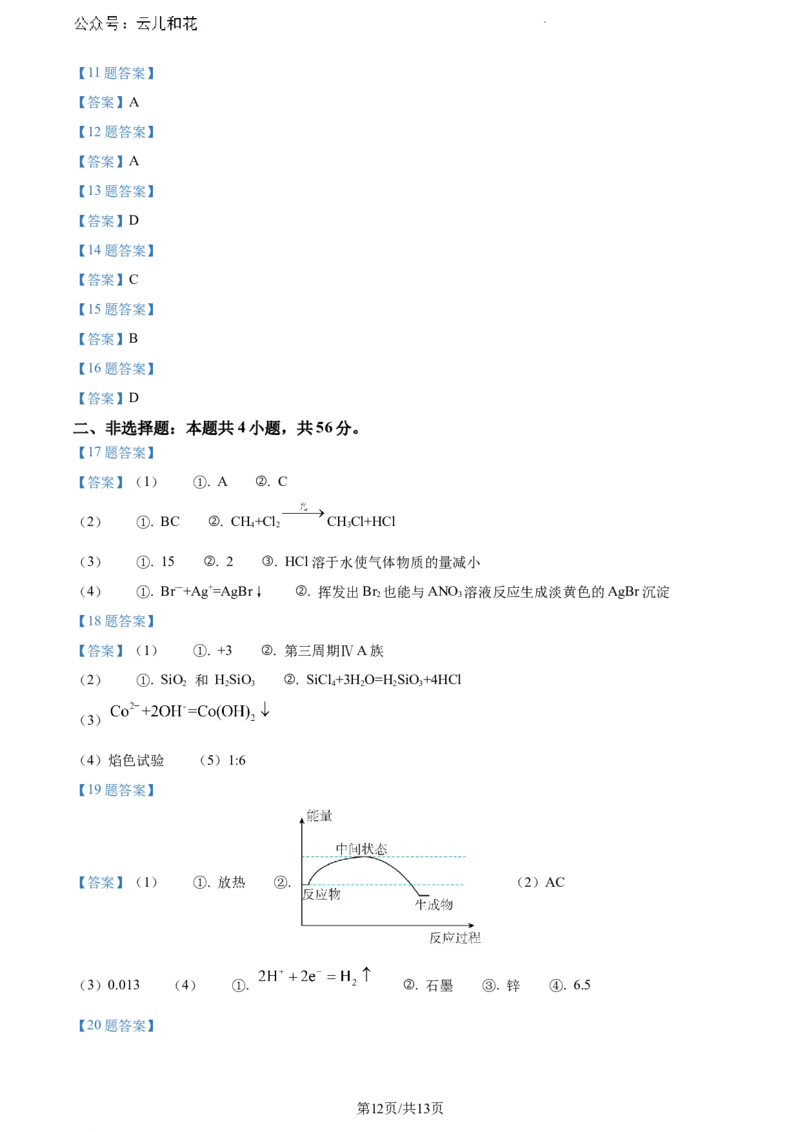
(3)用如图实验装置测定化学反应速率。在锥形瓶内盛有6.5g锌粒,通过分液漏斗加入足量的稀硫酸,
将产生的 收集在注射器中,10s时恰好收集到标准状况下的 44.8mL(装置气密性良好),则10s内
锌粒的反应速率为________ 。
(4)若将上述反应设计成原电池,以石墨和锌为原电池电极材料,则石墨上发生的电极反应式为
_________,外电路中电流由_________(填“锌”或“石墨”,下同)极向_________极移动。当外电路上有
0.2mol电子移动时,理论上锌片的质量减小_________g。
的
20. 化合物A是有机合成 重要原料之一,一定条件下能发生下图转化关系:
第9页/共13页
学科网(北京)股份有限公司已知:B含有醛基,分子式为 ;E是难溶于水的油状液体,有浓郁香味。
(1)A的相对分子质量为26,写出A的结构简式_________。
(2)C中官能团的名称为_________,D的分子式为_________。
(3)已知乙烯的结构及其可能具有的化学性质,参考序号1的示例,完成下表。
序号 化合物 可反应的试剂 反应形成的产物 反应类型
1 加成反应
2 ________ ________
(4)写出B→C的化学方程式:________。
(5)化合物F是E的同分异构体,且F可以与NaOH溶液反应,化合物F为________(任写一种结构简
式)。
第10页/共13页
学科网(北京)股份有限公司江门市 2024 年普通高中高一调研测试(二)
化学
本试卷8页,20小题,满分100分。考试时间75分钟。
注意事项:
1.答题前,务必将自己的姓名、准考证号填写在答题卡规定的位置上。
2.做选择题时,必须用2B铅笔将答题卷上对应题目的答案标号涂黑,如需改动,用橡皮擦
干净后,再选涂其它答案标号。
3.答非选择题时,必须用黑色字迹钢笔或签字笔,将答案写在答题卡规定的位置上。
4.所有题目必须在答题卡上作答,在试题卷上作答无效。
5.考试结束后,将答题卡交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Zn 65
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小
题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
【1题答案】
【答案】B
【2题答案】
【答案】D
【3题答案】
【答案】B
【4题答案】
【答案】B
【5题答案】
【答案】B
【6题答案】
【答案】C
【7题答案】
【答案】A
【8题答案】
【答案】C
【9题答案】
【答案】C
【10题答案】
【答案】C
第11页/共13页
学科网(北京)股份有限公司【11题答案】
【答案】A
【12题答案】
【答案】A
【13题答案】
【答案】D
【14题答案】
【答案】C
【15题答案】
【答案】B
【16题答案】
【答案】D
二、非选择题:本题共4小题,共56分。
【17题答案】
【答案】(1) ①. A ②. C
(2) ①. BC ②. CH+Cl CHCl+HCl
4 2 3
(3) ①. 15 ②. 2 ③. HCl溶于水使气体物质的量减小
(4) ①. Br—+Ag+=AgBr↓ ②. 挥发出Br 也能与ANO 溶液反应生成淡黄色的AgBr沉淀
2 3
【18题答案】
【答案】(1) ①. +3 ②. 第三周期ⅣA族
(2) ①. SiO 和 HSiO ②. SiCl +3H O=HSiO+4HCl
2 2 3 4 2 2 3
(3)
(4)焰色试验 (5)1:6
【19题答案】
【答案】(1) ①. 放热 ②. (2)AC
(3)0.013 (4) ①. ②. 石墨 ③. 锌 ④. 6.5
【20题答案】
第12页/共13页
学科网(北京)股份有限公司【答案】(1)HC≡CH
(2) ①. 羧基 ②. C HO
2 6
(3) ①. O、Cu ②. 氧化反应
2
(4)2CHCHO+O 2CHCOOH
3 2 3
(5)HCOOCH CHCH 或 或CHCHCHCOOH或
2 2 3 3 2 2
第13页/共13页
学科网(北京)股份有限公司