文档内容
张家口市 2025-2026 学年度高一年级第一学期期末考试
化学试卷
班级_______ 姓名_______
注意事项:
1.答卷前,考生务必将自己的学校、班级、姓名及考号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写
在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:O 16 Na 23 Cl 35.5 Fe 56
一、选择题:本题共 20 小题,每小题只有一个正确选项。1~15 小题,每小题 2 分,16~20 小
题每小题 3 分;共 45 分。
1. 张家口市拥有丰富的历史文化与特色物产。下列说法正确的是
A.张家口白庙遗址出土
B 宣化古城墙
的东周时期青铜短剑
C.蔚县打树花
D.怀安豆腐
A. 青铜的主要成分为铜锡合金,其熔点高于纯铜
B. 古城墙青砖呈现的青色,主要是因为含有
C. 蔚县打树花的现象,说明铁的焰色试验为金色
D. “卤水点豆腐”的原理,与胶体的聚沉有关
2. 下列物质中,不属于电解质的是
第 1页/共 14页A. Cu B. HSO C. NaOH D. KNO
2 4 3
3. 下列关于试剂保存或使用的说法正确的是
A. 实验中未用完的 、 不能放回原试剂瓶,防止污染试剂
B. 新制氯水通常保存在棕色细口瓶中
C. 保存 溶液时,通常在溶液中加少量的铁单质
D. 称量 NaOH 固体时,应在两个托盘上各放一张等质量的称量纸
4. 生活离不开化学,下列有关物质用途的说法错误的是
A. :高效、低毒的消毒剂 B. 稀土元素:冶金工业的维生素
C. 硬铝:制造飞机 D. 合金:形状记忆合金
5. 镭( )是一种天然放射性元素,其衰变反应式: 。下列说法错误的是
A. Ra 的质子数为 88 B. 的中子数为 226
C. Rn 的核外电子数为 86 D. X 表示的微粒为
6. 下列化学用语书写正确的是
A. 水合钠离子的示意图:
B. 在熔融状态下的电离方程式:
C. 的结构示意图:
D. 用双线桥表示电子转移的方向和数目:
7. 化学来源于生活,也服务于生活,下列有关生活中的化学知识叙述不正确的是
A. 氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂
B. 氯气和活性炭均可作为漂白剂,若同时使用,漂白效果会明显加强
第 2页/共 14页C. 碳酸氢钠可用于治疗胃酸过多
D. 金属钠着火时,不能用水而需要用干燥的沙土来灭火
8. 下列实验装置及操作正确且能达到实验目的的是
操作
目的 A.观察钠在空气中燃烧的现象 B.配制 NaOH 溶液
操作
D.验证干燥的 没
有 目的 C.验证铁粉与水蒸气反应
漂白性
A. A B. B C. C D. D
9. 化学实验中颜色变化可将化学抽象之美具体为形象之美。下列叙述正确的是
A. 将氯气持续通入稀的酚酞溶液中,溶液先变红后褪色
B. 向氯化亚铁溶液中滴入新制的氯水,溶液由浅绿色变成棕黄色
C. 用玻璃棒将碳酸钠溶液点在 pH 试纸上,试纸变成红色
D. 用洁净的玻璃棒蘸取硝酸钾在酒精灯外焰上灼烧,火焰呈紫色
10. 下列实验操作、现象及结论都正确的是
选项 实验操作和现象 结论
第 3页/共 14页A 将铁锈溶于浓盐酸后滴入酸性 溶液,紫色褪去 铁锈中一定含有
B 向 KBr 溶液中滴入氯水,溶液由无色变 黄色 的氧化性强于
向氢氧化铁胶体中插入碳棒,连接直流电源,连接负极
C 氢氧化铁胶体带正电
的碳棒周围颜色变深
D 向某溶液中滴入 溶液,有白色沉淀生成 该溶液中一定含有
A. A B. B C. C D. D
11. 设 为阿伏加德罗常数的值,下列叙述正确的是
A. 溶液中 数目为
B. 在 298K、101kPa 时,体积相等的 和氦气所含原子数之比约为 3:1
C. 14.2g 与 5.6gFe 反应时,转移的电子数为
D. 7.8g 中含有的离子总数为
12. 25℃时,下列各组离子在指定溶液中一定能大量共存的是
A. 强酸性溶液: 、 、 、
B. 强碱性溶液: 、 、 、
C. 溶液: 、 、 、
D. 与 Al 反应产生 的溶液: 、 、 、
13. 下列离子方程式书写正确的是
A. 与水反应:
B. 与水反应:
C. 氯化铁溶液中加入足量的氨水:
D. Al 与氢氧化钠溶液反应:
14. 类推的思维方法在化学学习和研究中非常重要,以下类推结论正确的是
第 4页/共 14页A. Na 在空气中加热生成 ,则 Li 在空气中加热生成
B. Na 与水反应生成 NaOH 和 ,则 Cs 与水反应生成 CsOH 和
C. 铁和氯气反应生成 ,则铁和碘单质反应生成
D. 卤素单质的熔点从 到 逐渐升高,则碱金属单质的熔点从 Li 到 Cs 也逐渐升高
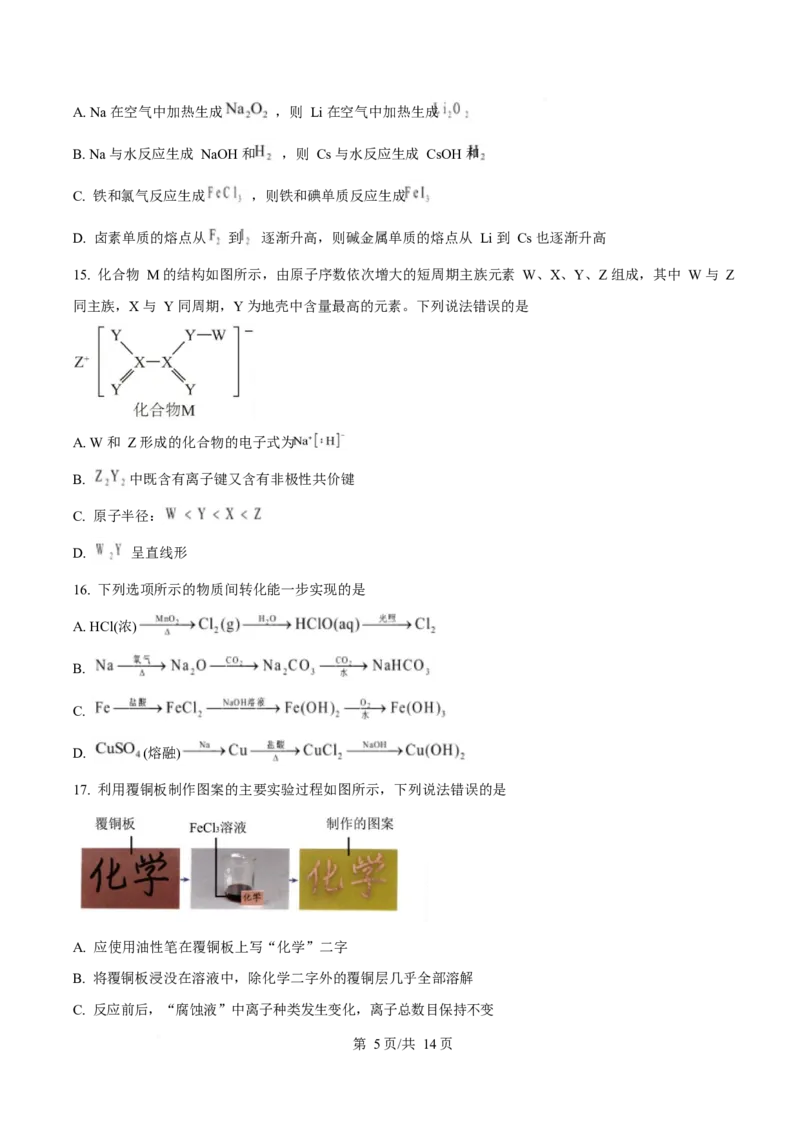
15. 化合物 M 的结构如图所示,由原子序数依次增大的短周期主族元素 W、X、Y、Z 组成,其中 W 与 Z
同主族,X 与 Y 同周期,Y 为地壳中含量最高的元素。下列说法错误的是
A. W 和 Z 形成的化合物的电子式为
B. 中既含有离子键又含有非极性共价键
C. 原子半径:
D. 呈直线形
16. 下列选项所示的物质间转化能一步实现的是
A. HCl(浓)
B.
C.
D. (熔融)
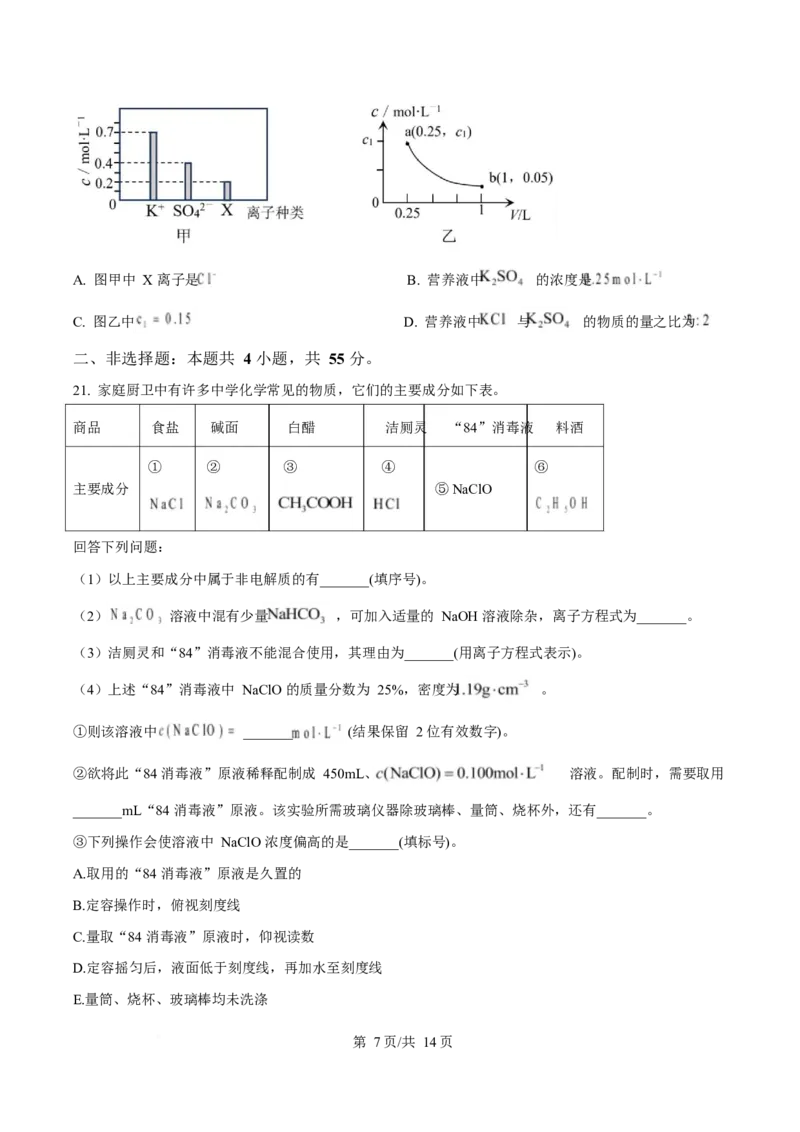
17. 利用覆铜板制作图案的主要实验过程如图所示,下列说法错误的是
A. 应使用油性笔在覆铜板上写“化学”二字
B. 将覆铜板浸没在溶液中,除化学二字外的覆铜层几乎全部溶解
C. 反应前后,“腐蚀液”中离子种类发生变化,离子总数目保持不变
第 5页/共 14页D. 向“腐蚀液”中依次加入过量铁粉和氯水,可实现 Cu 的回收和 溶液再生
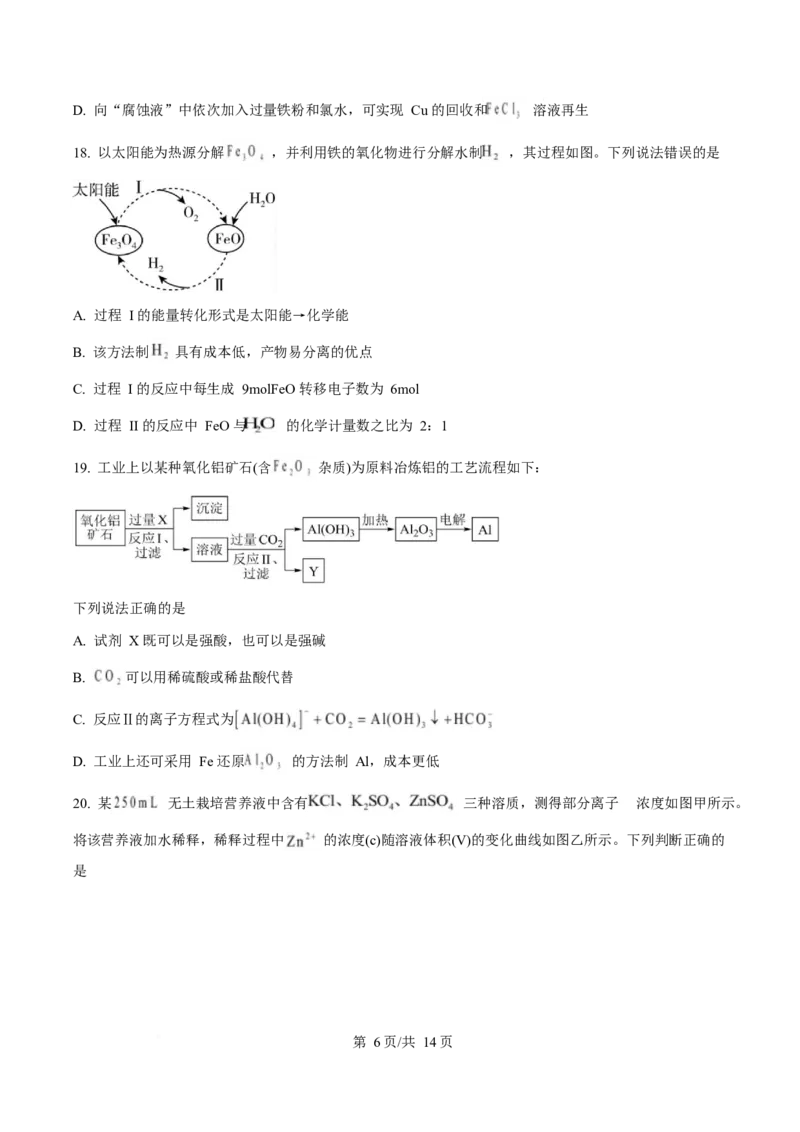
18. 以太阳能为热源分解 ,并利用铁的氧化物进行分解水制 ,其过程如图。下列说法错误的是
A. 过程 I 的能量转化形式是太阳能→化学能
B. 该方法制 具有成本低,产物易分离的优点
C. 过程 I 的反应中每生成 9molFeO 转移电子数为 6mol
D. 过程 II 的反应中 FeO 与 的化学计量数之比为 2:1
19. 工业上以某种氧化铝矿石(含 杂质)为原料冶炼铝的工艺流程如下:
下列说法正确的是
A. 试剂 X 既可以是强酸,也可以是强碱
B. 可以用稀硫酸或稀盐酸代替
C. 反应Ⅱ的离子方程式为
D. 工业上还可采用 Fe 还原 的方法制 Al,成本更低
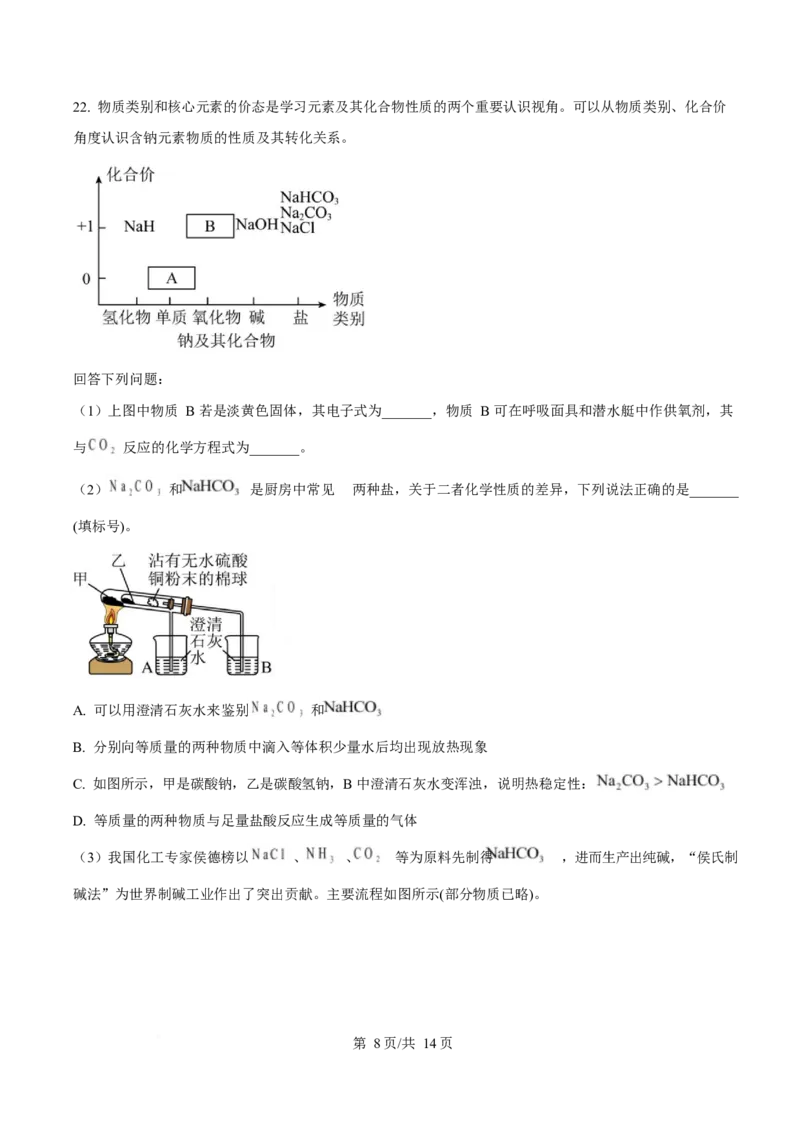
20. 某 无土栽培营养液中含有 三种溶质,测得部分离子 浓度如图甲所示。
将该营养液加水稀释,稀释过程中 的浓度(c)随溶液体积(V)的变化曲线如图乙所示。下列判断正确的
是
第 6页/共 14页A. 图甲中 X 离子是 B. 营养液中 的浓度是
C. 图乙中 D. 营养液中 与 的物质的量之比为
二、非选择题:本题共 4 小题,共 55 分。
21. 家庭厨卫中有许多中学化学常见的物质,它们的主要成分如下表。
商品 食盐 碱面 白醋 洁厕灵 “84”消毒液 料酒
① ② ③ ④ ⑥
主要成分 ⑤NaClO
回答下列问题:
(1)以上主要成分中属于非电解质的有_______(填序号)。
(2) 溶液中混有少量 ,可加入适量的 NaOH 溶液除杂,离子方程式为_______。
(3)洁厕灵和“84”消毒液不能混合使用,其理由为_______(用离子方程式表示)。
(4)上述“84”消毒液中 NaClO 的质量分数为 25%,密度为 。
①则该溶液中 _______ (结果保留 2 位有效数字)。
②欲将此“84 消毒液”原液稀释配制成 450mL、 溶液。配制时,需要取用
_______mL“84 消毒液”原液。该实验所需玻璃仪器除玻璃棒、量筒、烧杯外,还有_______。
③下列操作会使溶液中 NaClO 浓度偏高的是_______(填标号)。
A.取用的“84 消毒液”原液是久置的
B.定容操作时,俯视刻度线
C.量取“84 消毒液”原液时,仰视读数
D.定容摇匀后,液面低于刻度线,再加水至刻度线
E.量筒、烧杯、玻璃棒均未洗涤
第 7页/共 14页22. 物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。可以从物质类别、化合价
角度认识含钠元素物质的性质及其转化关系。
回答下列问题:
(1)上图中物质 B 若是淡黄色固体,其电子式为_______,物质 B 可在呼吸面具和潜水艇中作供氧剂,其
与 反应的化学方程式为_______。
(2) 和 是厨房中常见 两种盐,关于二者化学性质的差异,下列说法正确的是_______
(填标号)。
A. 可以用澄清石灰水来鉴别 和
B. 分别向等质量的两种物质中滴入等体积少量水后均出现放热现象
C. 如图所示,甲是碳酸钠,乙是碳酸氢钠,B 中澄清石灰水变浑浊,说明热稳定性:
D. 等质量的两种物质与足量盐酸反应生成等质量的气体
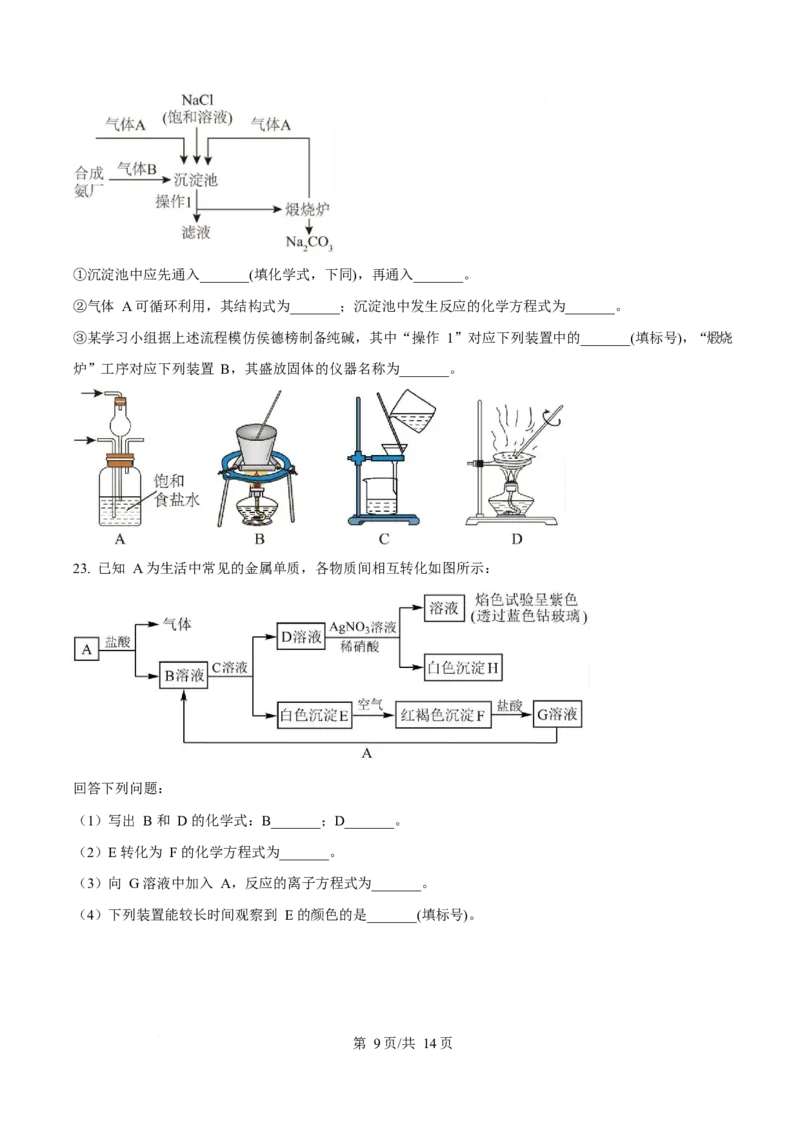
(3)我国化工专家侯德榜以 、 、 等为原料先制得 ,进而生产出纯碱,“侯氏制
碱法”为世界制碱工业作出了突出贡献。主要流程如图所示(部分物质已略)。
第 8页/共 14页①沉淀池中应先通入_______(填化学式,下同),再通入_______。
②气体 A 可循环利用,其结构式为_______;沉淀池中发生反应的化学方程式为_______。
③某学习小组据上述流程模仿侯德榜制备纯碱,其中“操作 1”对应下列装置中的_______(填标号),“煅烧
炉”工序对应下列装置 B,其盛放固体的仪器名称为_______。
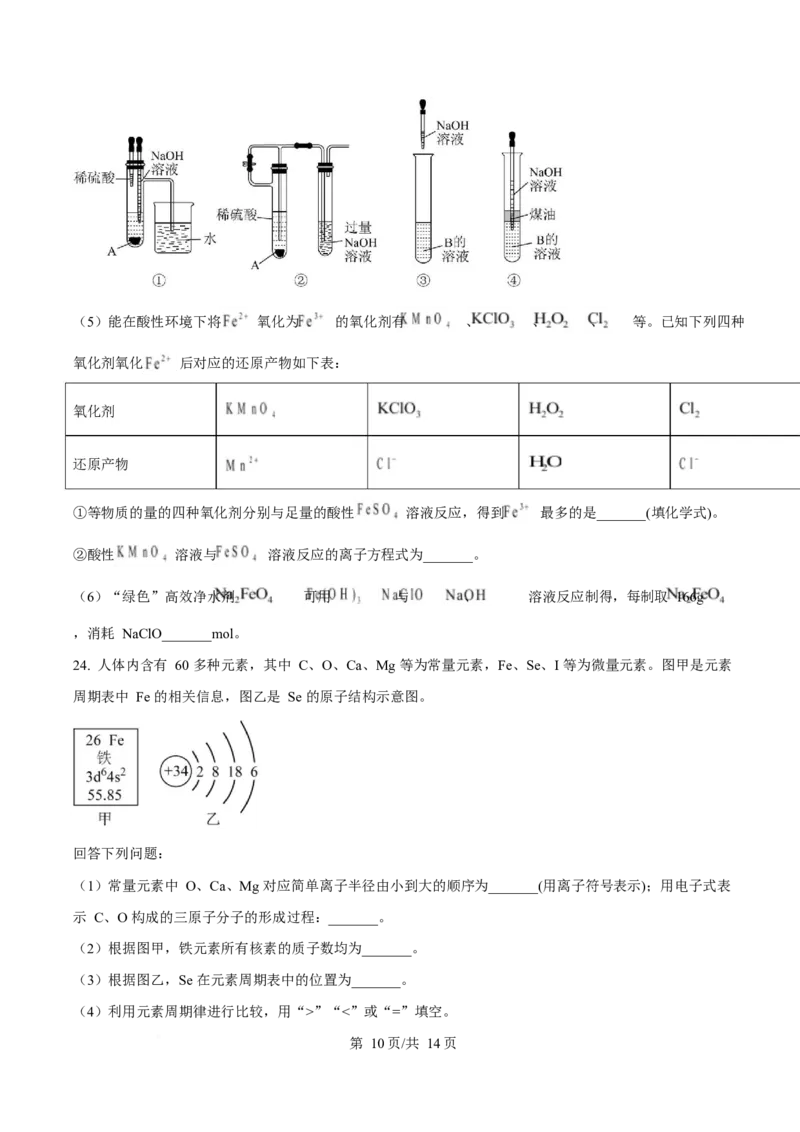
23. 已知 A 为生活中常见的金属单质,各物质间相互转化如图所示:
回答下列问题:
(1)写出 B 和 D 的化学式:B_______;D_______。
(2)E 转化为 F 的化学方程式为_______。
(3)向 G 溶液中加入 A,反应的离子方程式为_______。
(4)下列装置能较长时间观察到 E 的颜色的是_______(填标号)。
第 9页/共 14页(5)能在酸性环境下将 氧化为 的氧化剂有 、 、 、 等。已知下列四种
氧化剂氧化 后对应的还原产物如下表:
氧化剂
还原产物
①等物质的量的四种氧化剂分别与足量的酸性 溶液反应,得到 最多的是_______(填化学式)。
②酸性 溶液与 溶液反应的离子方程式为_______。
(6)“绿色”高效净水剂 可用 与 、 溶液反应制得,每制取 166g
,消耗 NaClO_______mol。
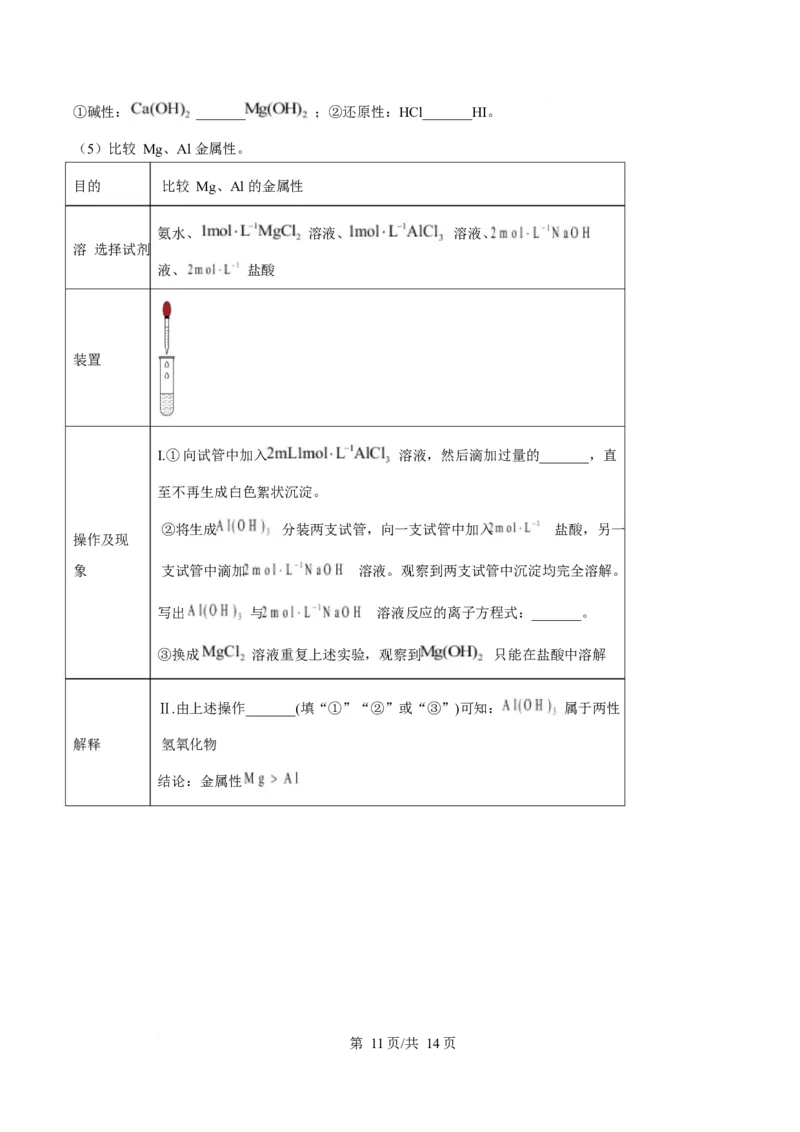
24. 人体内含有 60 多种元素,其中 C、O、Ca、Mg 等为常量元素,Fe、Se、I 等为微量元素。图甲是元素
周期表中 Fe 的相关信息,图乙是 Se 的原子结构示意图。
回答下列问题:
(1)常量元素中 O、Ca、Mg 对应简单离子半径由小到大的顺序为_______(用离子符号表示);用电子式表
示 C、O 构成的三原子分子的形成过程:_______。
(2)根据图甲,铁元素所有核素的质子数均为_______。
(3)根据图乙,Se 在元素周期表中的位置为_______。
(4)利用元素周期律进行比较,用“>”“<”或“=”填空。
第 10页/共 14页①碱性: _______ ;②还原性:HCl_______HI。
(5)比较 Mg、Al 金属性。
目的 比较 Mg、Al 的金属性
氨水、 溶液、 溶液、
溶 选择试剂
液、 盐酸
装置
I.①向试管中加入 溶液,然后滴加过量的_______,直
至不再生成白色絮状沉淀。
②将生成 分装两支试管,向一支试管中加入 盐酸,另一
操作及现
象 支试管中滴加 溶液。观察到两支试管中沉淀均完全溶解。
写出 与 溶液反应的离子方程式:_______。
③换成 溶液重复上述实验,观察到 只能在盐酸中溶解
Ⅱ.由上述操作_______(填“①”“②”或“③”)可知: 属于两性
解释 氢氧化物
结论:金属性
第 11页/共 14页张家口市 2025-2026 学年度高一年级第一学期期末考试
化学试卷
班级_______ 姓名_______
注意事项:
1.答卷前,考生务必将自己的学校、班级、姓名及考号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写
在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:O 16 Na 23 Cl 35.5 Fe 56
一、选择题:本题共 20 小题,每小题只有一个正确选项。1~15 小题,每小题 2 分,16~20 小
题每小题 3 分;共 45 分。
【1 题答案】
【答案】D
【2 题答案】
【答案】A
【3 题答案】
【答案】B
【4 题答案】
【答案】D
【5 题答案】
【答案】B
【6 题答案】
【答案】D
【7 题答案】
【答案】B
【8 题答案】
【答案】C
【9 题答案】
第 12页/共 14页【答案】B
【10 题答案】
【答案】B
【11 题答案】
【答案】C
【12 题答案】
【答案】B
【13 题答案】
【答案】D
【14 题答案】
【答案】B
【15 题答案】
【答案】D
【16 题答案】
【答案】C
【17 题答案】
【答案】C
【18 题答案】
【答案】D
【19 题答案】
【答案】C
【20 题答案】
【答案】D
二、非选择题:本题共 4 小题,共 55 分。
【21 题答案】
【答案】(1)⑥ (2)
(3)
(4) ①. 4.0 ②. 12.5 ③. 胶头滴管、500mL 容量瓶 ④. BC
【22 题答案】
第 13页/共 14页【答案】(1) ①. ②. (2)C
( 3) ① . ② . ③ . ④ .
⑤. C ⑥. 坩埚
【23 题答案】
【答案】(1) ①. ②. KCl
(2)
(3)
(4)①②④ (5) ①. ②.
(6)1.5
【24 题答案】
【答案】(1) ①. ②.
(2)26 (3)第四周期第ⅥA 族
(4) ①. > ②. <
(5) ①. 氨水 ②. ③. ②
第 14页/共 14页