文档内容
2023—2024 学年普通高中高一(下)期末教学质量检测
化学试题
本试卷共6页,18题,满分100分,考试时间75分钟。
★祝考试顺利★
注意事项:
1.答题前,先将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并将准考
证号条形码粘贴在答题卡上的指定位置。
2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,写在
试卷,草稿纸和答题卡上的非答题区域均无效。
3.非选择题的作答:用黑色签字笔直接答在答题卡上对应的答题区域内,写在试卷、草稿纸
和答题卡的非答题区域均无效。
4.考试结束后,请将本试卷和答题卡一并上交。
可能用到相对原子质量:
一、选择题(本大题共14小题,每小题只有一个选项符合题意,每小题3分,共42分。)
1. 文房四宝是中华传统文化的瑰宝。下列有关叙述错误的是
A. 羊毛可用于制毛笔,主要成分为蛋白质
B. 松木可用于制墨,墨的主要成分是单质碳
C. 竹子可用于造纸,纸的主要成分是纤维素
D. 大理石可用于制砚台,主要成分为硅酸盐
2. 下列化学事实不符合“事物的双方既相互对立又相互统一”的哲学观点的是
A. 氯气与强碱反应时,氯气既是氧化剂又是还原剂
B. 铜锌原电池在工作时,正极和负极同时发生反应
C. 的金属性随核外电子层数的增多而增强
D. 工业上合成氨的过程中同时存在氨气的生成与分解
3. 下列说法正确的是
A. 和 互为同素异形体 B. 和 互为同系物
第1页/共13页
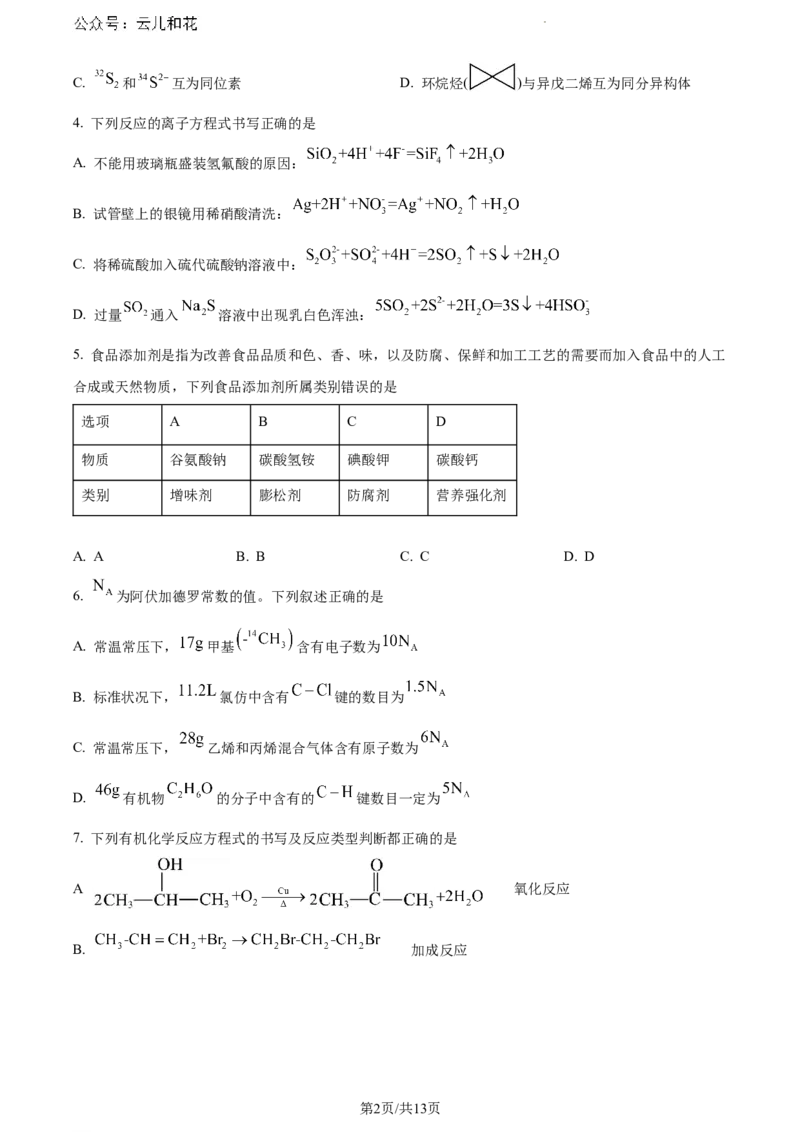
学科网(北京)股份有限公司C. 和 互为同位素 D. 环烷烃( )与异戊二烯互为同分异构体
4. 下列反应的离子方程式书写正确的是
A. 不能用玻璃瓶盛装氢氟酸的原因:
B. 试管壁上的银镜用稀硝酸清洗:
C. 将稀硫酸加入硫代硫酸钠溶液中:
D. 过量 通入 溶液中出现乳白色浑浊:
5. 食品添加剂是指为改善食品品质和色、香、味,以及防腐、保鲜和加工工艺的需要而加入食品中的人工
合成或天然物质,下列食品添加剂所属类别错误的是
选项 A B C D
物质 谷氨酸钠 碳酸氢铵 碘酸钾 碳酸钙
类别 增味剂 膨松剂 防腐剂 营养强化剂
A. A B. B C. C D. D
6. 为阿伏加德罗常数的值。下列叙述正确的是
A. 常温常压下, 甲基 含有电子数为
B. 标准状况下, 氯仿中含有 键的数目为
C. 常温常压下, 乙烯和丙烯混合气体含有原子数为
D. 有机物 的分子中含有的 键数目一定为
7. 下列有机化学反应方程式的书写及反应类型判断都正确的是
A. 氧化反应
B. 加成反应
第2页/共13页
学科网(北京)股份有限公司C. 酯化反应
D. 加聚反应
8. 利用如图所示装置进行下列实验,能得到相应实验结论的是
选
① ② ③ 实验结论
项
A 硝酸 溶液 非金属性:
浓 硫 浓硫酸具有脱水性和强氧
B 蔗糖 溴水褪色
酸 化性
加有酚酞的 溶液
C 硫酸 具有漂白性
褪色
浓 盐
D 溶液变为黄色 氧化性:
酸
A. A B. B C. C D. D
9. 下列资源利用中,在给定工艺条件下转化关系正确的是
A. 煤 煤油 B. 石油 乙烯
C. 油脂 甘油 D. 淀粉 乙醇
10. 下列关于化学反应与能量的说法中,正确的是
A. 能量变化必然伴随发生化学反应
B. 化学反应中的能量变化主要是由化学键变化引起的
C. 可以用右图表示Ba(OH) ·8H O与NH Cl的反应
2 2 4
D. 已知右图可以表示白磷转化为黑磷的能量变化,则说明白磷比黑磷稳定
第3页/共13页
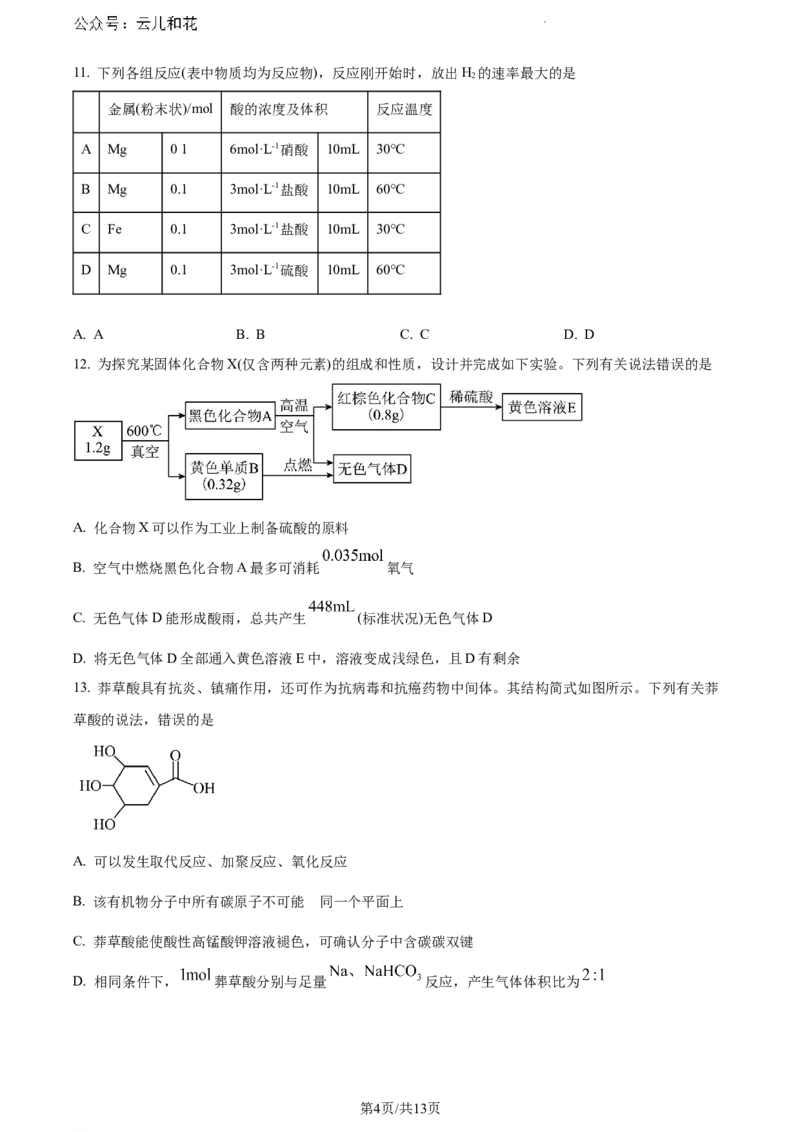
学科网(北京)股份有限公司11. 下列各组反应(表中物质均为反应物),反应刚开始时,放出H 的速率最大的是
2
金属(粉末状)/mol 酸的浓度及体积 反应温度
.
A Mg 01 6mol·L-1硝酸 10mL 30℃
B Mg 0.1 3mol·L-1盐酸 10mL 60℃
C Fe 0.1 3mol·L-1盐酸 10mL 30℃
D Mg 0.1 3mol·L-1硫酸 10mL 60℃
A. A B. B C. C D. D
12. 为探究某固体化合物X(仅含两种元素)的组成和性质,设计并完成如下实验。下列有关说法错误的是
A. 化合物X可以作为工业上制备硫酸的原料
B. 空气中燃烧黑色化合物A最多可消耗 氧气
C. 无色气体D能形成酸雨,总共产生 (标准状况)无色气体D
D. 将无色气体D全部通入黄色溶液E中,溶液变成浅绿色,且D有剩余
13. 莽草酸具有抗炎、镇痛作用,还可作为抗病毒和抗癌药物中间体。其结构简式如图所示。下列有关莽
草酸的说法,错误的是
A. 可以发生取代反应、加聚反应、氧化反应
在
B. 该有机物分子中所有碳原子不可能 同一个平面上
C. 莽草酸能使酸性高锰酸钾溶液褪色,可确认分子中含碳碳双键
D. 相同条件下, 葬草酸分别与足量 反应,产生气体体积比为
第4页/共13页
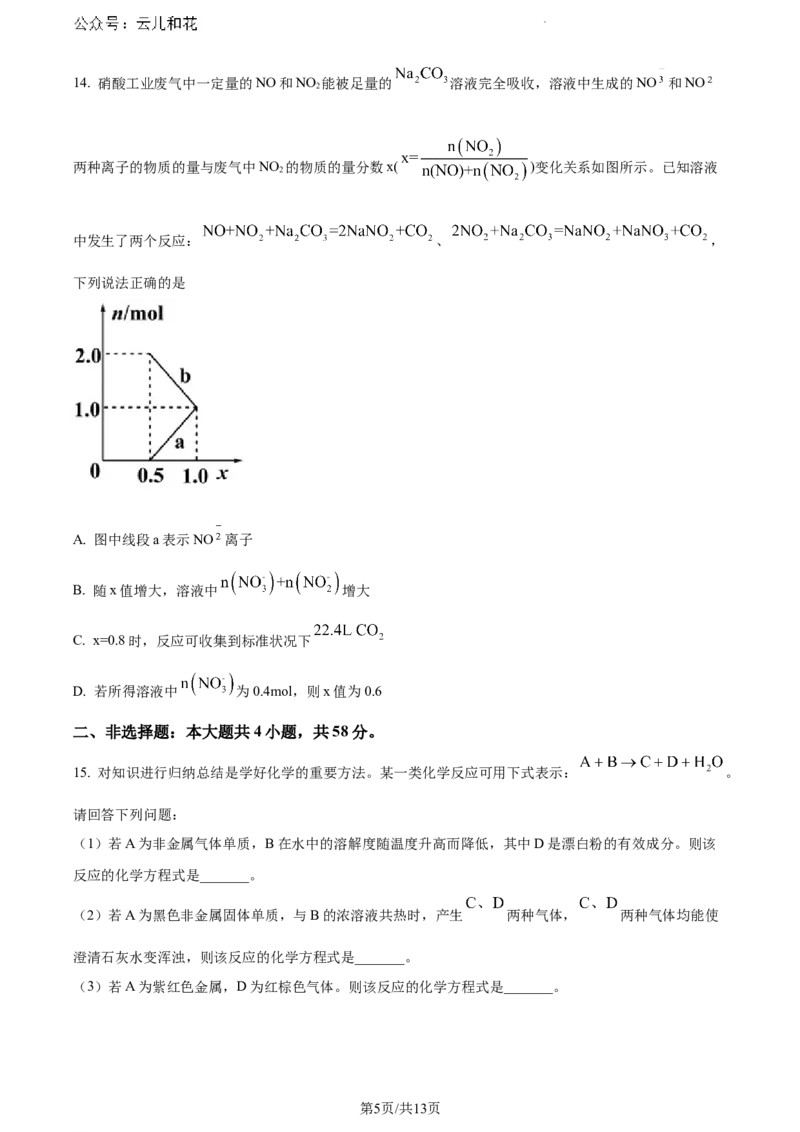
学科网(北京)股份有限公司14. 硝酸工业废气中一定量的NO和NO 能被足量的 溶液完全吸收,溶液中生成的NO 和NO
2
两种离子的物质的量与废气中NO 的物质的量分数x( )变化关系如图所示。已知溶液
2
中发生了两个反应: 、 ,
下列说法正确的是
A. 图中线段a表示NO 离子
B. 随x值增大,溶液中 增大
C. x=0.8时,反应可收集到标准状况下
D. 若所得溶液中 为0.4mol,则x值为0.6
二、非选择题:本大题共4小题,共58分。
15. 对知识进行归纳总结是学好化学的重要方法。某一类化学反应可用下式表示: 。
请回答下列问题:
(1)若A为非金属气体单质,B在水中的溶解度随温度升高而降低,其中D是漂白粉的有效成分。则该
反应的化学方程式是_______。
(2)若A为黑色非金属固体单质,与B的浓溶液共热时,产生 两种气体, 两种气体均能使
澄清石灰水变浑浊,则该反应的化学方程式是_______。
(3)若A为紫红色金属,D为红棕色气体。则该反应的化学方程式是_______。
第5页/共13页
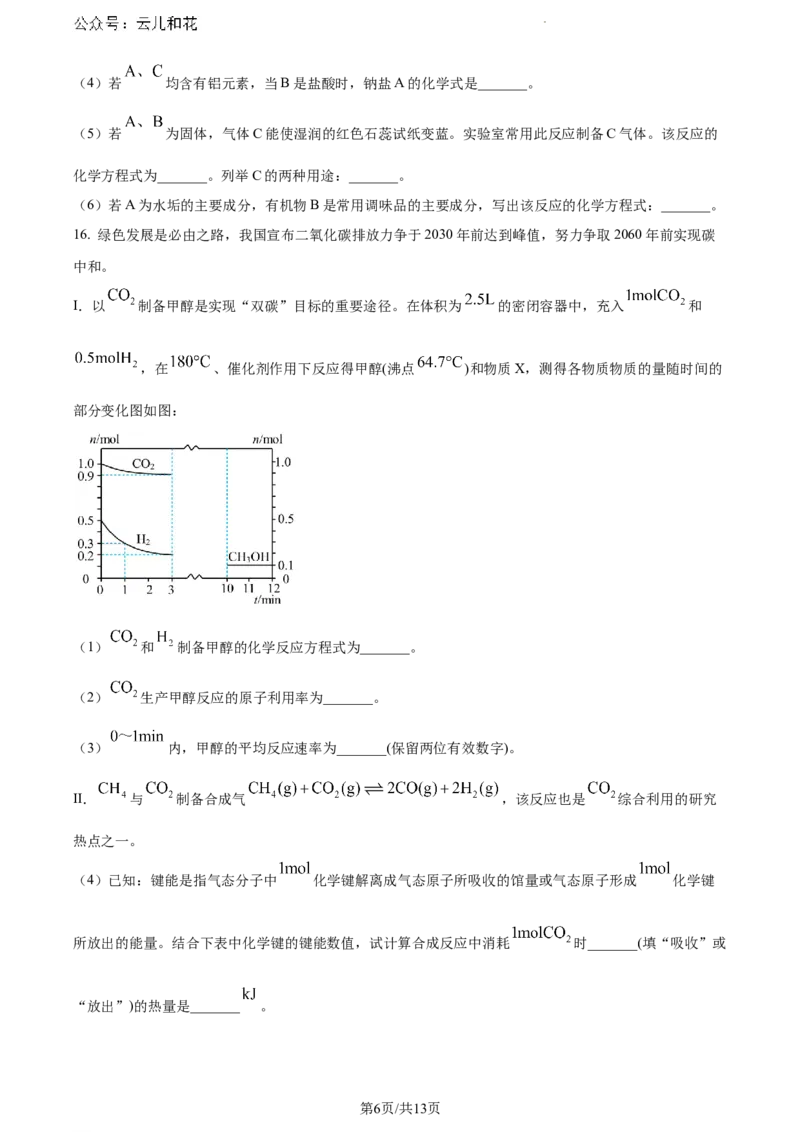
学科网(北京)股份有限公司(4)若 均含有铝元素,当B是盐酸时,钠盐A的化学式是_______。
(5)若 为固体,气体C能使湿润的红色石蕊试纸变蓝。实验室常用此反应制备C气体。该反应的
化学方程式为_______。列举C的两种用途:_______。
(6)若A为水垢的主要成分,有机物B是常用调味品的主要成分,写出该反应的化学方程式:_______。
16. 绿色发展是必由之路,我国宣布二氧化碳排放力争于2030年前达到峰值,努力争取2060年前实现碳
中和。
I.以 制备甲醇是实现“双碳”目标的重要途径。在体积为 的密闭容器中,充入 和
,在 、催化剂作用下反应得甲醇(沸点 )和物质X,测得各物质物质的量随时间的
部分变化图如图:
(1) 和 制备甲醇的化学反应方程式为_______。
(2) 生产甲醇反应的原子利用率为_______。
(3) 内,甲醇的平均反应速率为_______(保留两位有效数字)。
Ⅱ. 与 制备合成气 ,该反应也是 综合利用的研究
热点之一。
(4)已知:键能是指气态分子中 化学键解离成气态原子所吸收的馆量或气态原子形成 化学键
所放出的能量。结合下表中化学键的键能数值,试计算合成反应中消耗 时_______(填“吸收”或
“放出”)的热量是_______ 。
第6页/共13页
学科网(北京)股份有限公司化学键
键能 413 745 436 1075
(5)恒容条件下,下列描述能证明该反应达到平衡的是_______(填字母)。
A. 容器中气体密度不再改变 B. 不再改变
C. 断裂 同时断裂 D. 的体积分数不再改变
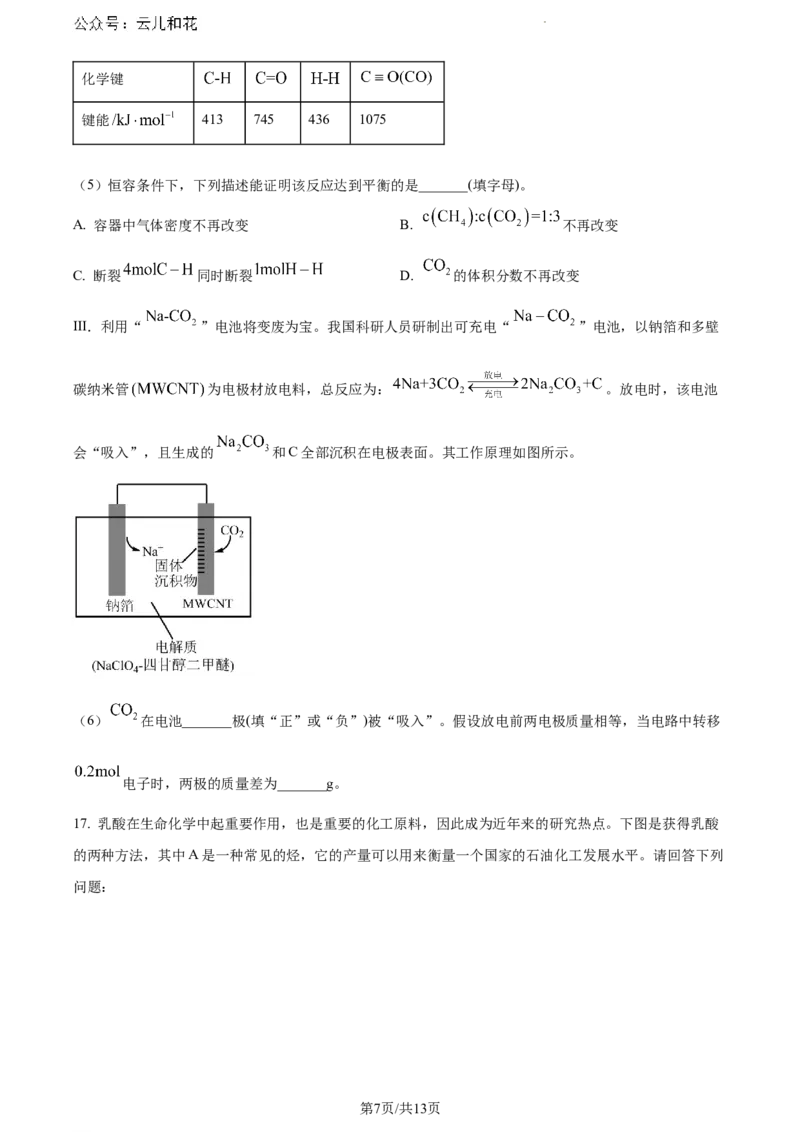
Ⅲ.利用“ ”电池将变废为宝。我国科研人员研制出可充电“ ”电池,以钠箔和多壁
碳纳米管 为电极材放电料,总反应为: 。放电时,该电池
会“吸入”,且生成的 和C全部沉积在电极表面。其工作原理如图所示。
(6) 在电池_______极(填“正”或“负”)被“吸入”。假设放电前两电极质量相等,当电路中转移
电子时,两极的质量差为_______g。
17. 乳酸在生命化学中起重要作用,也是重要的化工原料,因此成为近年来的研究热点。下图是获得乳酸
的两种方法,其中A是一种常见的烃,它的产量可以用来衡量一个国家的石油化工发展水平。请回答下列
问题:
第7页/共13页
学科网(北京)股份有限公司(1)上述有机物中有一种可作为水果的催熟剂,其所含官能团结构简式:_______。
(2)向C中加入新制氢氧化铜悬浊液加热后的实验现象是_______。
(3)淀粉完全水解得到 的结构简式是_______。为检验淀粉水解产物D,某同学向淀粉溶液中加入稀
硫酸并加热一段时间,冷却后的溶液中直接加入银氨溶液,水浴加热,无银镜出现。你认为该同学实验失
败的主要原因是_______。
(4)两分子乳酸在一定条件下通过酯化反应可生成一分子六元环酯 和两分子水,该环酯的结
构简式是_______。
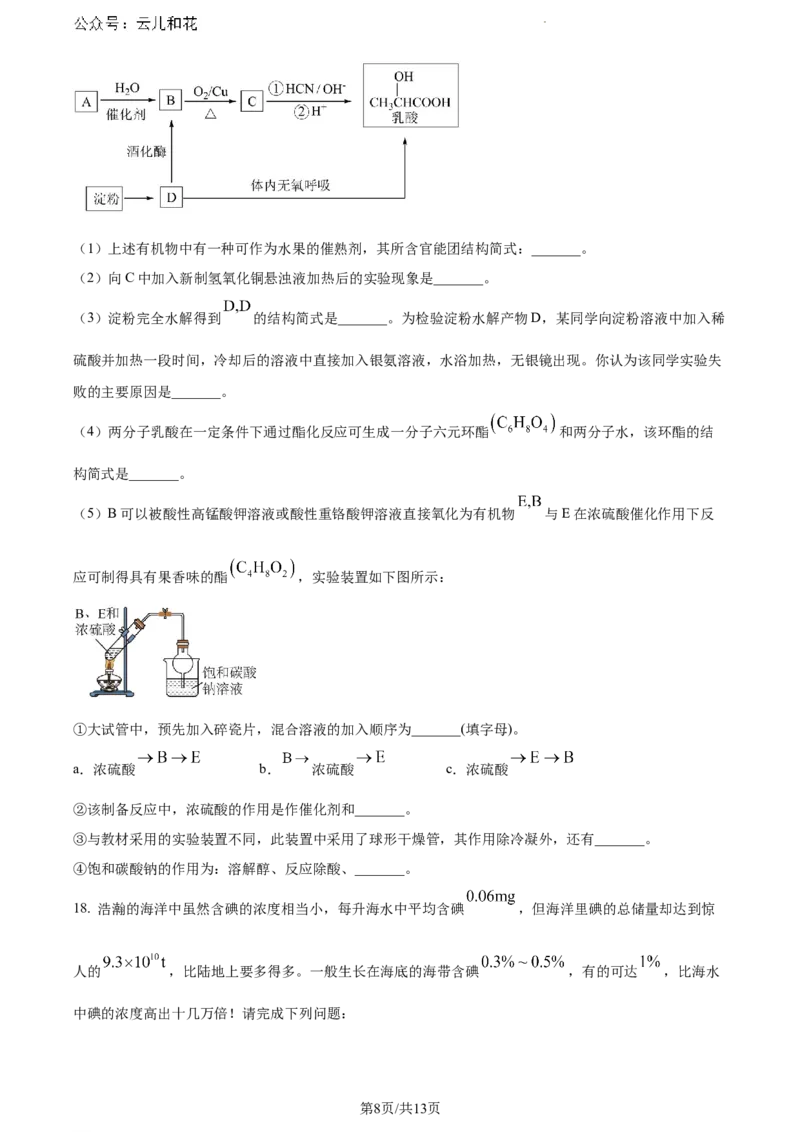
(5)B可以被酸性高锰酸钾溶液或酸性重铬酸钾溶液直接氧化为有机物 与E在浓硫酸催化作用下反
应可制得具有果香味的酯 ,实验装置如下图所示:
①大试管中,预先加入碎瓷片,混合溶液的加入顺序为_______(填字母)。
a.浓硫酸 b. 浓硫酸 c.浓硫酸
②该制备反应中,浓硫酸的作用是作催化剂和_______。
③与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用除冷凝外,还有_______。
④饱和碳酸钠的作用为:溶解醇、反应除酸、_______。
18. 浩瀚的海洋中虽然含碘的浓度相当小,每升海水中平均含碘 ,但海洋里碘的总储量却达到惊
人的 ,比陆地上要多得多。一般生长在海底的海带含碘 ,有的可达 ,比海水
中碘的浓度高出十几万倍!请完成下列问题:
第8页/共13页
学科网(北京)股份有限公司I.海水制盐所得的卤水中可提取碘。活性炭吸附法是工业提碘的方法之一,其流程如下:
资料显示:a. 时, 溶液只能将 氧化为 ,同时生成 。b.
,氧化性: 。
(1)反应①的离子方程式是_______。
(2)方案甲中,根据 的特性,分离操作X应为_______、冷凝结晶。
(3)已知:反应②中每吸收 转移 电子,离子方程式是_______。
(4) 、酸性 等都是常用的强氧化剂,但该工艺中氧化卤水中的 却选择了价格较高的
,原因是_______。
(5)方案乙中,已知反应③过滤后,滤液中仍存在少量的 。为了检验滤液中的 ,某小组同学设
计如下实验方案,请将实验步骤补充完整。
实验中可供选择的试剂:稀 、淀粉溶液、 溶液、 。
a.将滤液用 多次萃取、分液,直到水层用淀粉溶液检验不出碘单质存在。
b.从水层取少量溶液于试管中,_______。
Ⅱ.海带中含有丰富的碘。从海带中提取碘的实验过程如下图所示:
(6)实验步骤①不需要下列仪器中的_______(填字母)。
a.酒精灯 b.漏斗 c.坩埚 d.泥三角
第9页/共13页
学科网(北京)股份有限公司(7)步骤④中反应的离子方程式是_______。
(8)海带灰中含有的硫酸盐,碳酸盐等,在实验步骤_______(填序号)中实现与碘分离。
第10页/共13页
学科网(北京)股份有限公司2023—2024 学年普通高中高一(下)期末教学质量检测
化学试题
本试卷共6页,18题,满分100分,考试时间75分钟。
★祝考试顺利★
注意事项:
1.答题前,先将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并将准考
证号条形码粘贴在答题卡上的指定位置。
2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,写在
试卷,草稿纸和答题卡上的非答题区域均无效。
3.非选择题的作答:用黑色签字笔直接答在答题卡上对应的答题区域内,写在试卷、草稿纸
和答题卡的非答题区域均无效。
4.考试结束后,请将本试卷和答题卡一并上交。
可能用到相对原子质量:
一、选择题(本大题共14小题,每小题只有一个选项符合题意,每小题3分,共42分。)
【1题答案】
【答案】D
【2题答案】
【答案】C
【3题答案】
【答案】D
【4题答案】
【答案】D
【5题答案】
【答案】C
【6题答案】
【答案】C
【7题答案】
【答案】A
第11页/共13页
学科网(北京)股份有限公司【8题答案】
【答案】B
【9题答案】
【答案】C
【10题答案】
【答案】B
【11题答案】
【答案】D
【12题答案】
【答案】B
【13题答案】
【答案】C
【14题答案】
【答案】C
二、非选择题:本大题共4小题,共58分。
【15题答案】
【答案】(1)2Ca(OH) +2Cl=CaCl +Ca(ClO) +2H O
2 2 2 2 2
(2)C+2H SO (浓) CO↑+2SO↑+2H O
2 4 2 2 2
(3)Cu+4HNO (浓)=Cu(NO)+2NO↑+2H O
3 3 2 2 2
(4)Na[Al(OH)]
4
.
(5) ① Ca(OH) +2NHCl CaCl +2NH↑+2H O ②. 用于制造氮肥,也可以用作制冷剂
2 4 2 3 2
(6)CaCO +2CH COOH=(CH COO) Ca+H O+CO↑
3 3 3 2 2 2
【16题答案】
【答案】(1)CO+3H CHOH+H O
2 2 3 2
(2)64% (3)0.027mol·L-1·min-1
(4) ①. 吸收 ②. 120 (5)BD
(6) ①. 正 ②. 15.8
【17题答案】
第12页/共13页
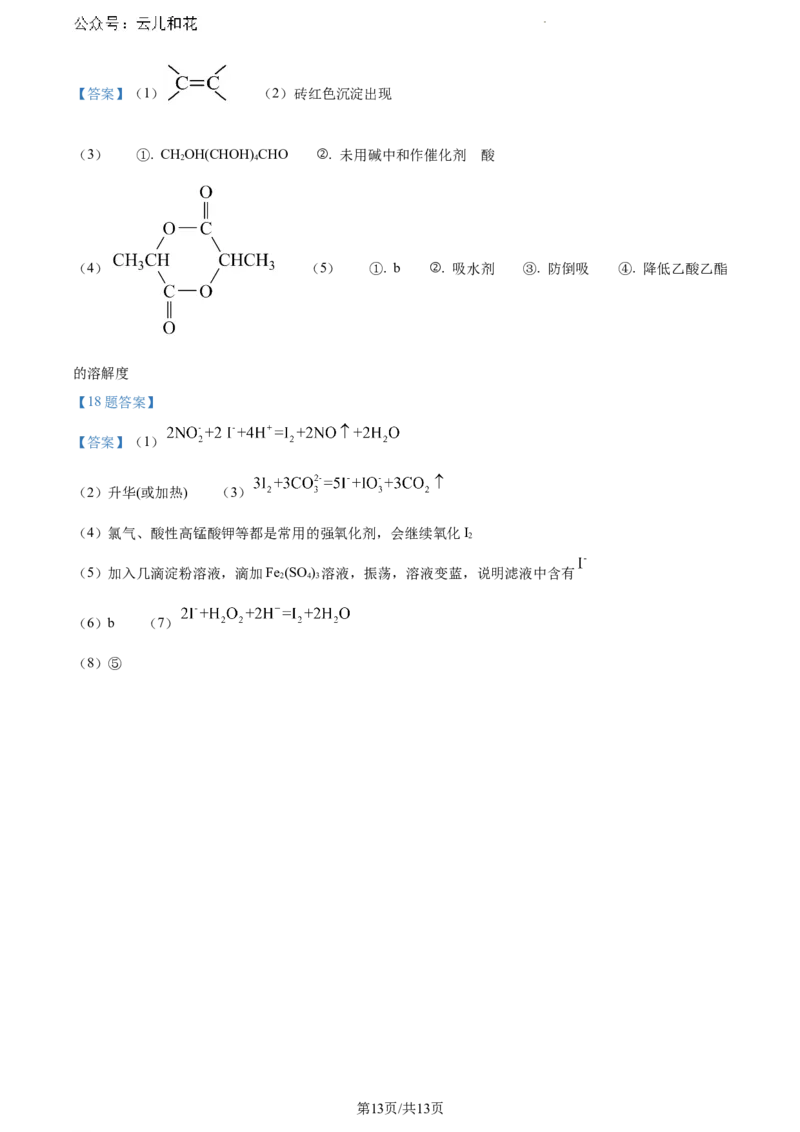
学科网(北京)股份有限公司【答案】(1) (2)砖红色沉淀出现
的
(3) ①. CHOH(CHOH) CHO ②. 未用碱中和作催化剂 酸
2 4
(4) (5) ①. b ②. 吸水剂 ③. 防倒吸 ④. 降低乙酸乙酯
的溶解度
【18题答案】
【答案】(1)
(2)升华(或加热) (3)
(4)氯气、酸性高锰酸钾等都是常用的强氧化剂,会继续氧化I
2
(5)加入几滴淀粉溶液,滴加Fe (SO ) 溶液,振荡,溶液变蓝,说明滤液中含有
2 4 3
(6)b (7)
(8)⑤
第13页/共13页
学科网(北京)股份有限公司