文档内容
武汉市部分重点中学 学年度下学期期末联考
2024—2025
高一化学
命题单位:武汉三中化学学科组 审题单位:圆创教育研究中心 武汉市第一中学
本试卷共8页,19题。满分100分。考试用时75分钟。 考试时间:2025年6月25日上午11 00—12 15
祝考试顺利
★ ★
注意事项:
答题前,先将自己的姓名、准考证号填写在试卷和答题卡上,并将准考证号条形码贴在答题卡上的
1.
指定位置。
选择题的作答:每小题选出答案后,用 铅笔把答题卡上对应题目的答案标号涂黑。 写在试卷、
2. 2B
草稿纸和答题卡上的非答题区域均无效。
非选择题的作答:用黑色签字笔直接答在答题卡上对应的答题区域内。 写在试卷、草稿纸和答题
3.
卡上的非答题区域均无效。
考试结束后,请将本试卷和答题卡一并上交。
4.
可能用到的相对原子质量:
H 1 C 12 N 14 O 16 Na 21 S 32 Cl 35.5 Ag 108
一、选择题:本题共15小题,每小题3分,共45分。 在每小题给出的四个选项中,只有一项是符合题目要
求的。
我国有许多手工创作物件 承载着历史文明 下列说法正确的是
1. , 。
孔明灯的燃料是蜡烛 蜡烛可通过石油的常压分馏获得
A. ,
皮影的原料主要采用羊皮 羊皮的主要成分是蛋白质
B. ,
吹糖画的原料是麦芽糖 麦芽糖在酸或碱性条件下均能水解
C. ,
文房四宝中纸的主要成分是纤维素 可在人体内水解为葡萄糖
D. ,
下列化学用语或图示表达正确的是
2.
丙烷的球棍模型 乙烯的结构简式
A. : B. :CH2CH2
四氯化碳的空间填充模型 聚丙烯的结构简式
C. : D. :CH2—CH—CH3
青少年帮厨既可培养劳动习惯 也能将化学知识应用于实践 下列说法错误的是
3. , 。
将白糖熬成焦糖汁 是因为蔗糖高温下充分炭化为食物增色
A. ,
食用油久置有 哈喇 味 是因为不饱和高级脂肪酸甘油酯被氧化
B. “ ” ,
用盐卤 主要成分 点豆腐 是因为豆浆中的蛋白质胶体聚沉
C. ( MgCl2) ,
制作面包时加入碳酸氢钠等膨松剂 是因为其受热分解并中和酸
D. ,
高一化学试卷 第 页 共 页
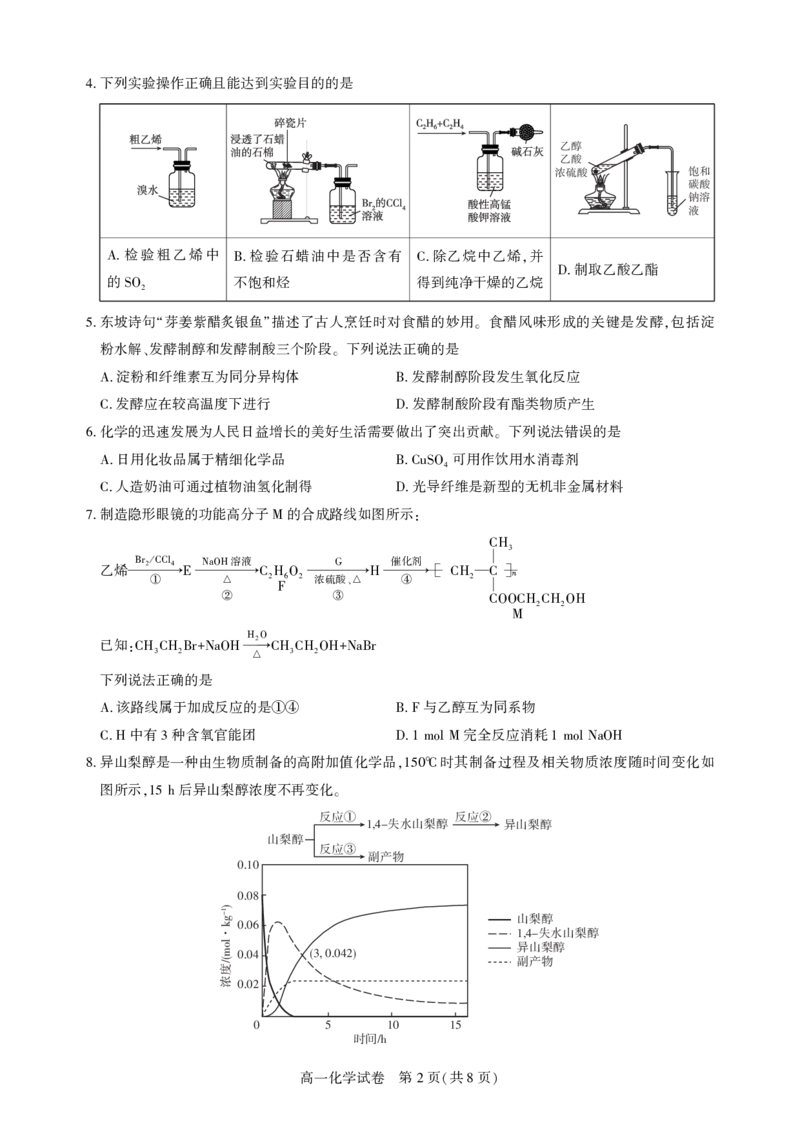
1 ( 8 )下列实验操作正确且能达到实验目的的是
4.
检验粗乙烯中 检验石蜡油中是否含有 除乙烷中乙烯 并
A. B. C. , 制取乙酸乙酯
的 不饱和烃 得到纯净干燥的乙烷 D.
SO2
东坡诗句 芽姜紫醋炙银鱼 描述了古人烹饪时对食醋的妙用 食醋风味形成的关键是发酵 包括淀
5. “ ” 。 ,
粉水解 发酵制醇和发酵制酸三个阶段 下列说法正确的是
、 。
淀粉和纤维素互为同分异构体 发酵制醇阶段发生氧化反应
A. B.
发酵应在较高温度下进行 发酵制酸阶段有酯类物质产生
C. D.
化学的迅速发展为人民日益增长的美好生活需要做出了突出贡献 下列说法错误的是
6. 。
日用化妆品属于精细化学品 可用作饮用水消毒剂
A. B.CuSO4
人造奶油可通过植物油氢化制得 光导纤维是新型的无机非金属材料
C. D.
制造隐形眼镜的功能高分子 的合成路线如图所示
7. M :
CH3
溶液 催化剂
乙烯 Br2/CCl4 NaOH G
→E →C2H6O2 浓硫酸 →H → CH2 C
① △ 、△ ④
F
② ③
COOCH2CH2OH
M
已知 H2O
:CH3CH2Br+NaOH →CH3CH2OH+NaBr
△
下列说法正确的是
该路线属于加成反应的是 与乙醇互为同系物
A. ①④ B.F
中有 种含氧官能团 完全反应消耗
C.H 3 D.1 mol M 1 mol NaOH
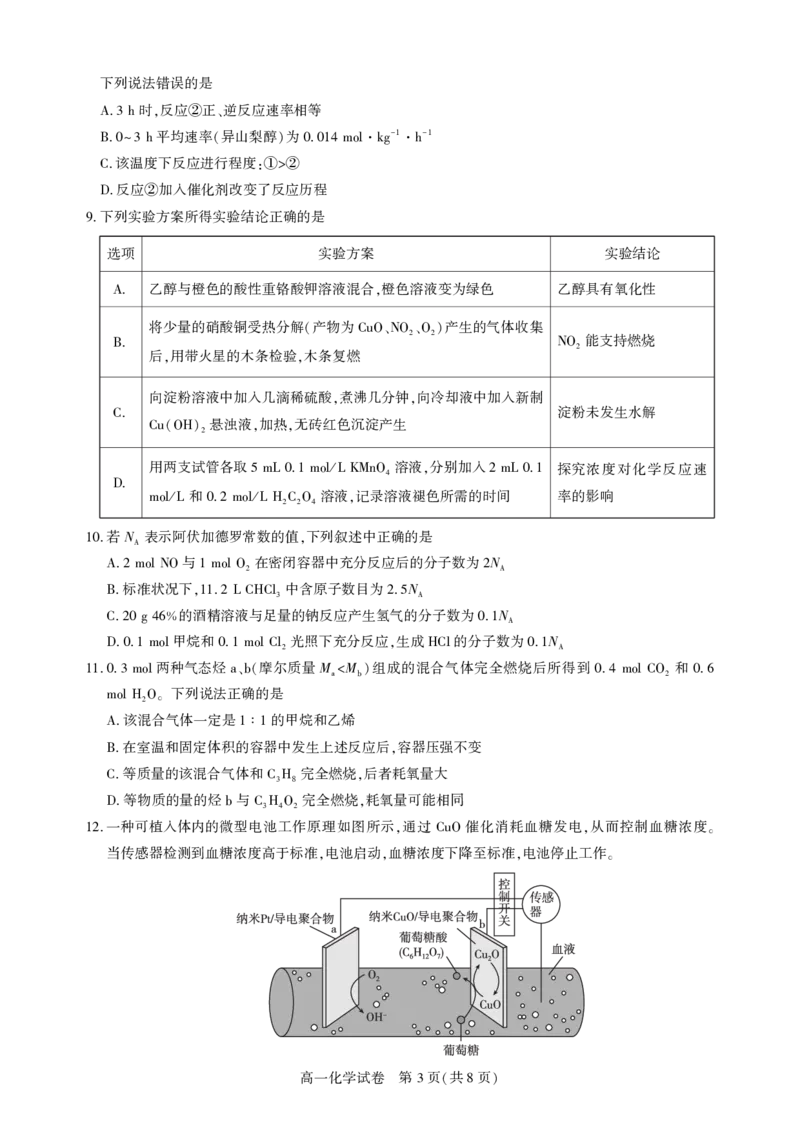
异山梨醇是一种由生物质制备的高附加值化学品 时其制备过程及相关物质浓度随时间变化如
8. ,150℃
图所示 后异山梨醇浓度不再变化
,15 h 。
高一化学试卷 第 页 共 页
2 ( 8 )
HLeMPN
I下列说法错误的是
时 反应 正 逆反应速率相等
A.3 h , ② 、
平均速率 异山梨醇 为 -1 -1
B.0~3 h ( ) 0.014 mol·kg ·h
该温度下反应进行程度
C. :①>②
反应 加入催化剂改变了反应历程
D. ②
下列实验方案所得实验结论正确的是
9.
选项 实验方案 实验结论
乙醇与橙色的酸性重铬酸钾溶液混合 橙色溶液变为绿色 乙醇具有氧化性
A. ,
将少量的硝酸铜受热分解 产物为 产生的气体收集
( CuO、NO2、O2) 能支持燃烧
B.
后 用带火星的木条检验 木条复燃
NO2
, ,
向淀粉溶液中加入几滴稀硫酸 煮沸几分钟 向冷却液中加入新制
, ,
淀粉未发生水解
C. 悬浊液 加热 无砖红色沉淀产生
Cu(OH)2 , ,
用两支试管各取 溶液 分别加入 探究浓度对化学反应速
5 mL 0.1 mol/L KMnO4 , 2 mL 0.1
D. 和 溶液 记录溶液褪色所需的时间 率的影响
mol/L 0.2 mol/L H2C2O4 ,
若N 表示阿伏加德罗常数的值 下列叙述中正确的是
10. A ,
与 在密闭容器中充分反应后的分子数为 N
A.2 mol NO 1 mol O2 2 A
标准状况下 中含原子数目为 N
B. ,11.2 L CHCl3 2.5 A
%的酒精溶液与足量的钠反应产生氢气的分子数为 N
C.20 g 46 0.1 A
甲烷和 光照下充分反应 生成 的分子数为 N
D.0.1 mol 0.1 mol Cl2 , HCl 0.1 A
两种气态烃 摩尔质量 M M 组成的混合气体完全燃烧后所得到 和
11.0.3 mol a、b( a< b) 0.4 mol CO2 0.6
下列说法正确的是
mol H2O。
该混合气体一定是 的甲烷和乙烯
A. 1 ∶ 1
在室温和固定体积的容器中发生上述反应后 容器压强不变
B. ,
等质量的该混合气体和 完全燃烧 后者耗氧量大
C. C3H8 ,
等物质的量的烃 与 完全燃烧 耗氧量可能相同
D. b C3H4O2 ,
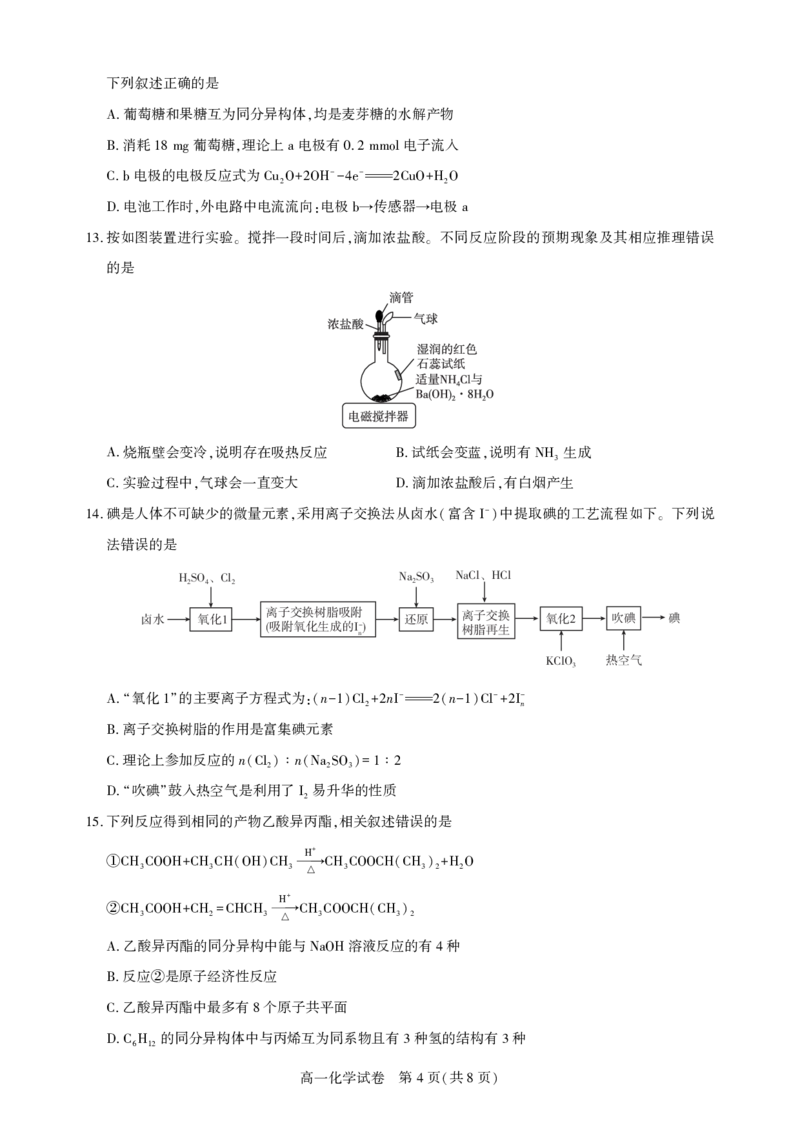
一种可植入体内的微型电池工作原理如图所示 通过 催化消耗血糖发电 从而控制血糖浓度
12. , CuO , 。
当传感器检测到血糖浓度高于标准 电池启动 血糖浓度下降至标准 电池停止工作
, , , 。
高一化学试卷 第 页 共 页
3 ( 8 )下列叙述正确的是
葡萄糖和果糖互为同分异构体 均是麦芽糖的水解产物
A. ,
消耗 葡萄糖 理论上 电极有 电子流入
B. 18 mg , a 0.2 mmol
电极的电极反应式为 - -
C.b Cu2O+2OH -4e 2CuO+H2O
电池工作时 外电路中电流流向 电极 传感器 电极
D. , : b→ → a
按如图装置进行实验 搅拌一段时间后 滴加浓盐酸 不同反应阶段的预期现象及其相应推理错误
13. 。 , 。
的是
烧瓶壁会变冷 说明存在吸热反应 试纸会变蓝 说明有 生成
A. , B. , NH3
实验过程中 气球会一直变大 滴加浓盐酸后 有白烟产生
C. , D. ,
碘是人体不可缺少的微量元素 采用离子交换法从卤水 富含 - 中提取碘的工艺流程如下 下列说
14. , ( I ) 。
法错误的是
)40$M /B40 /B$M)$M
*
O
,$M0
氧化 的主要离子方程式为 n n - n - -
A.“ 1” :( -1)Cl2+2 I 2( -1)Cl +2In
离子交换树脂的作用是富集碘元素
B.
理论上参加反应的n n
C. (Cl2) ∶ (Na2SO3)= 1 ∶ 2
吹碘 鼓入热空气是利用了 易升华的性质
D.“ ” I2
下列反应得到相同的产物乙酸异丙酯 相关叙述错误的是
15. ,
+
H
①CH3COOH+CH3CH(OH)CH3 →CH3COOCH(CH3)2+H2O
△
+
H
②CH3COOH+CH2=CHCH3 →CH3COOCH(CH3)2
△
乙酸异丙酯的同分异构中能与 溶液反应的有 种
A. NaOH 4
反应 是原子经济性反应
B. ②
乙酸异丙酯中最多有 个原子共平面
C. 8
的同分异构体中与丙烯互为同系物且有 种氢的结构有 种
D.C6H12 3 3
高一化学试卷 第 页 共 页
4 ( 8 )二、非选择题:本题共4小题,共55分。
分
16.(14 )
近年来 科学家致力于将二氧化碳和氢气转化为甲醇 的技术研究 某温度下 加氢制
, (CH3OH) 。 CO2
甲醇的总反应为 已知该反应是放热反应 回答下列问题
:CO2(g)+3H2(g)CH3OH(g)+H2O(g), 。 :
在 下 纯物质完全燃烧生成指定产物时所放出的热量 叫做该物质的燃烧
(1) 25℃、101 kPa ,1 mol ,
热 已知 完全燃烧生成 和液态水时 放热 则 的燃烧热为
。 1g CH3OH(l) CO2(g) , 22. 68 kJ, CH3OH(l)
-1
kJ·mol 。
有关 加氢制甲醇的反应 下列说法正确的是
(2) CO2 , 。
反应物的化学键断裂要吸收的能量大于生成物的化学键形成要放出的能量
A.
恒压条件下 向容器中充入一定量的 反应速率不变
B. , Ar,
分离出 后 正 逆反应速率减小
C. CH3OH , 、
煤的间接液化可生成甲醇
D.
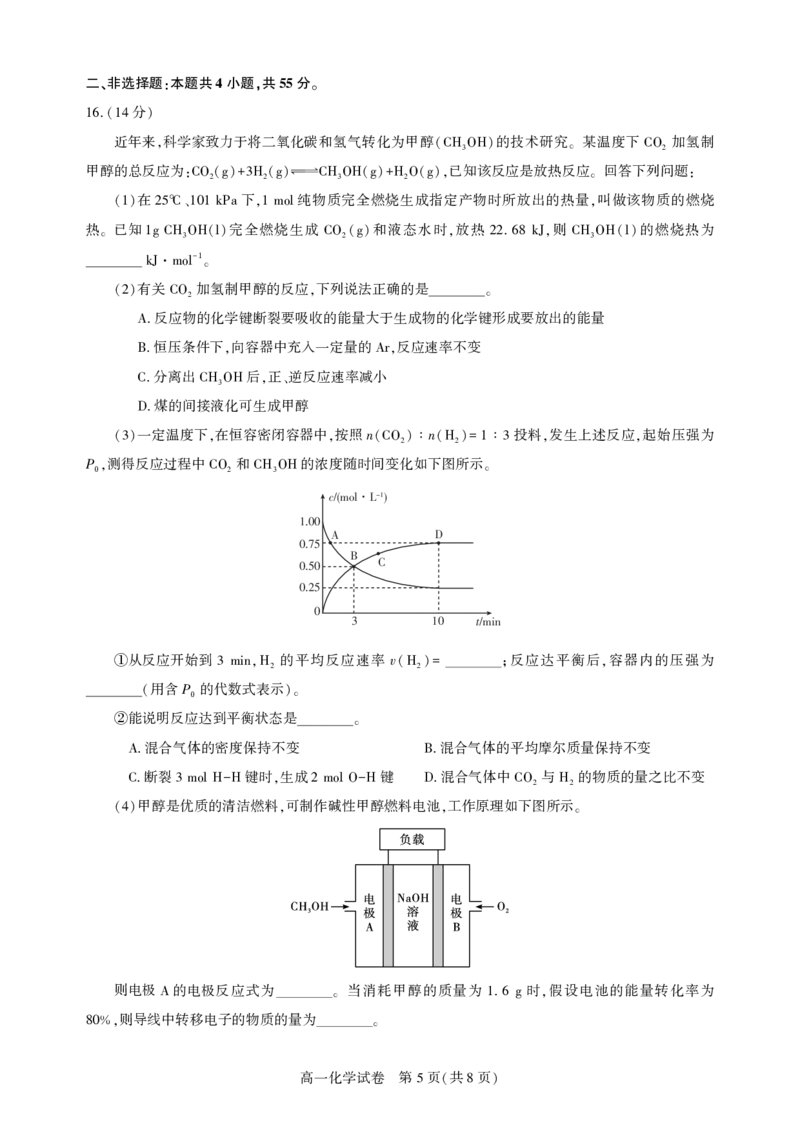
一定温度下 在恒容密闭容器中 按照n n 投料 发生上述反应 起始压强为
(3) , , (CO2) ∶ (H2)= 1 ∶ 3 , ,
P 测得反应过程中 和 的浓度随时间变化如下图所示
0, CO2 CH3OH 。
D NPMe-
" %
#
$
UNJO
从反应开始到 的平均反应速率 v 反应达平衡后 容器内的压强为
① 3 min,H2 (H2)= ; ,
用含P 的代数式表示
( 0 )。
能说明反应达到平衡状态是
② 。
混合气体的密度保持不变 混合气体的平均摩尔质量保持不变
A. B.
断裂 键时 生成 键 混合气体中 与 的物质的量之比不变
C. 3 mol H-H , 2 mol O-H D. CO2 H2
甲醇是优质的清洁燃料 可制作碱性甲醇燃料电池 工作原理如下图所示
(4) , , 。
则电极 的电极反应式为 当消耗甲醇的质量为 时 假设电池的能量转化率为
A 。 1. 6 g ,
% 则导线中转移电子的物质的量为
80 , 。
高一化学试卷 第 页 共 页
5 ( 8 )分
17.(14 )
二氯乙烷是杀菌剂稻瘟灵和植物生长调节剂矮壮素的中间体 不溶于水 易溶于有机溶剂 沸点
1,2- , , ,
化学家们提出乙烯液相直接氯化法制备 二氯乙烷 相关反应原理和实验装置图如图
83.6℃。 1,2- , 。
已知 P2O5 甘油的沸点为
:C2H5OH 高温→CH2=CH2↑+H2O; 290℃。
.O0
10
$)$M$)$M
回答以下问题
:
装置甲中反应的离子方程式为
(1) 。
装置乙中的试剂名称为
(2) 。
装置己中水的作用是
(3) 。
装置丁中发生反应的反应类型为 多孔球泡的作用是
(4) ; 。
丁中反应前先加入少量 二氯乙烷液体 其作用是
(5) 1,2— , 。
作催化剂 溶解 和乙烯 促进气体反应物间的接触
a. b. Cl2 c.
已知 液相直接氯化法可生成 二氯乙烷的同系物 满足分子式 的同
(6) C4H8 1,2— C4H8Cl2, C4H8Cl2
分异构体有 种
。
高一化学试卷 第 页 共 页
6 ( 8 )分
18.(13 )
连二亚硫酸钠 俗称保险粉 广泛应用于有机合成 实验室常用 还原法制备连二亚硫酸
(Na2S2O4) , , SO2
钠 回答下列问题
。 :
硫的不同存在形态结构不同 下列含硫物质的说法正确的是
(1) , 。
固体中含有的阴离子个数为N
A.110 g Na2S2 A
常温常压下 气体含有的分子数大于N
B. ,22.4 L SO2 A
硫在足量的氧气中充分燃烧转移的电子数为 N
C.32 g 6 A
试管壁上残留的硫粉可选择乙醇洗涤
D.
实验室选用下图所示装置制取纯净干燥的
(2) SO2。
C D E F G
B
/B0)
" # $ % &
按气流方向连接各仪器接口 顺序为
① , a→ →f。
装置 中反应的化学方程式为
② A 。
连二亚硫酸钠的制备
(3)
/B0)
40
/B0)
将锌粉悬浊液加入三口烧瓶中并将烧瓶温度维持 向其中先通入 一段时间后 改通
Ⅰ. 35~45℃, N2 ,
充分反应后生成 固体
SO2, ZnS2O4 。
向烧瓶中加入 溶液 在 条件下生成 和
Ⅱ. NaOH , 28~55℃ Na2S2O4 Zn(OH)2。
过滤 将滤液冷却至室温 待 析出后 滤出晶体用无水乙醇洗涤即得产品
Ⅲ. , , Na2S2O4 , 。
步骤 中的加热方式是
① Ⅰ 。
向三颈烧瓶中先通入 的目的是
② N2 。
加入无水乙醇洗涤的作用是
③ 。
连二亚硫酸钠的纯度测定
(4)
准确称取产品m 于烧杯中 加入 中性甲醛溶液 搅拌至产品完全溶解 加水配成
g , 20.00 mL , , 250 mL
溶液 取 于锥形瓶中 酸化后用c -1 标准溶液滴定 消耗 标准溶液V
, 25.00 mL , mol·L I2 , I2 mL。
溶解反应
:Na2S2O4+2HCHO+H2ONaHSO3·CH2O+NaHSO2·CH2O
滴定反应
:NaHSO2·CH2O+2I2+2H2ONaHSO4+4HI+HCHO
则产品中 质量分数为 列出含m c V的最简表达式
Na2S2O4 ( 、 、 )。
高一化学试卷 第 页 共 页
7 ( 8 )分
19.(14 )
随着科技和社会的发展 生物质资源替代以煤 石油 天然气为原料的化工生产路线将是一条绿色的
, 、 、
可持续发展途径 秸秆是一种具有多用途的可再生的生物资源 秸秆主要成分是纤维素 工业上利用生
。 , 。
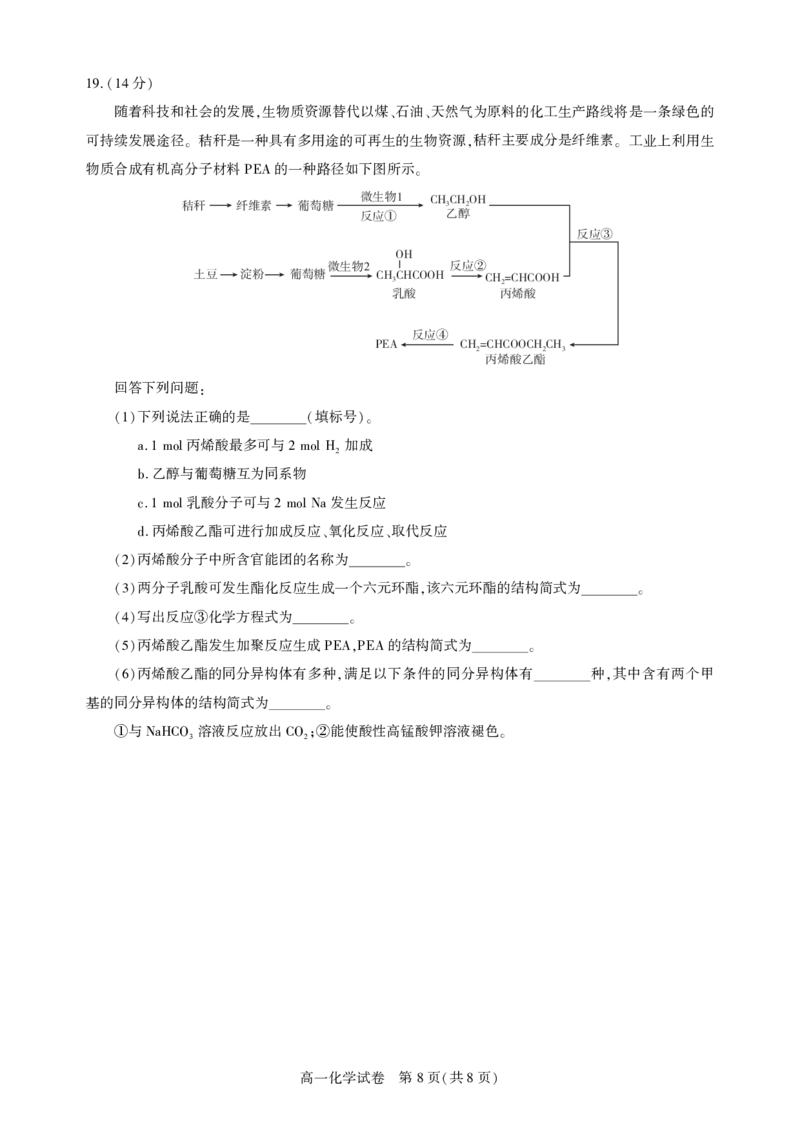
物质合成有机高分子材料 的一种路径如下图所示
PEA 。
$)$)0)
0)
$) $)$00) $) $)$00)
1&" $) $)$00$)$)
回答下列问题
:
下列说法正确的是 填标号
(1) ( )。
丙烯酸最多可与 加成
a.1 mol 2 mol H2
乙醇与葡萄糖互为同系物
b.
乳酸分子可与 发生反应
c.1 mol 2 mol Na
丙烯酸乙酯可进行加成反应 氧化反应 取代反应
d. 、 、
丙烯酸分子中所含官能团的名称为
(2) 。
两分子乳酸可发生酯化反应生成一个六元环酯 该六元环酯的结构简式为
(3) , 。
写出反应 化学方程式为
(4) ③ 。
丙烯酸乙酯发生加聚反应生成 的结构简式为
(5) PEA,PEA 。
丙烯酸乙酯的同分异构体有多种 满足以下条件的同分异构体有 种 其中含有两个甲
(6) , ,
基的同分异构体的结构简式为
。
与 溶液反应放出 能使酸性高锰酸钾溶液褪色
① NaHCO3 CO2;② 。
高一化学试卷 第 页 共 页
8 ( 8 )