文档内容
人教版(2019)必修第二册第七章 第三节 乙醇与乙酸
课时训练一
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.植物木质素中含有芥子醇,结构简式如下图所示。下列有关芥子醇的说法正确的是
A.分子式是C H O
11 16 4
B.属于芳香烃
C.含有两种官能团
D.可发生加成、取代、氧化等反应
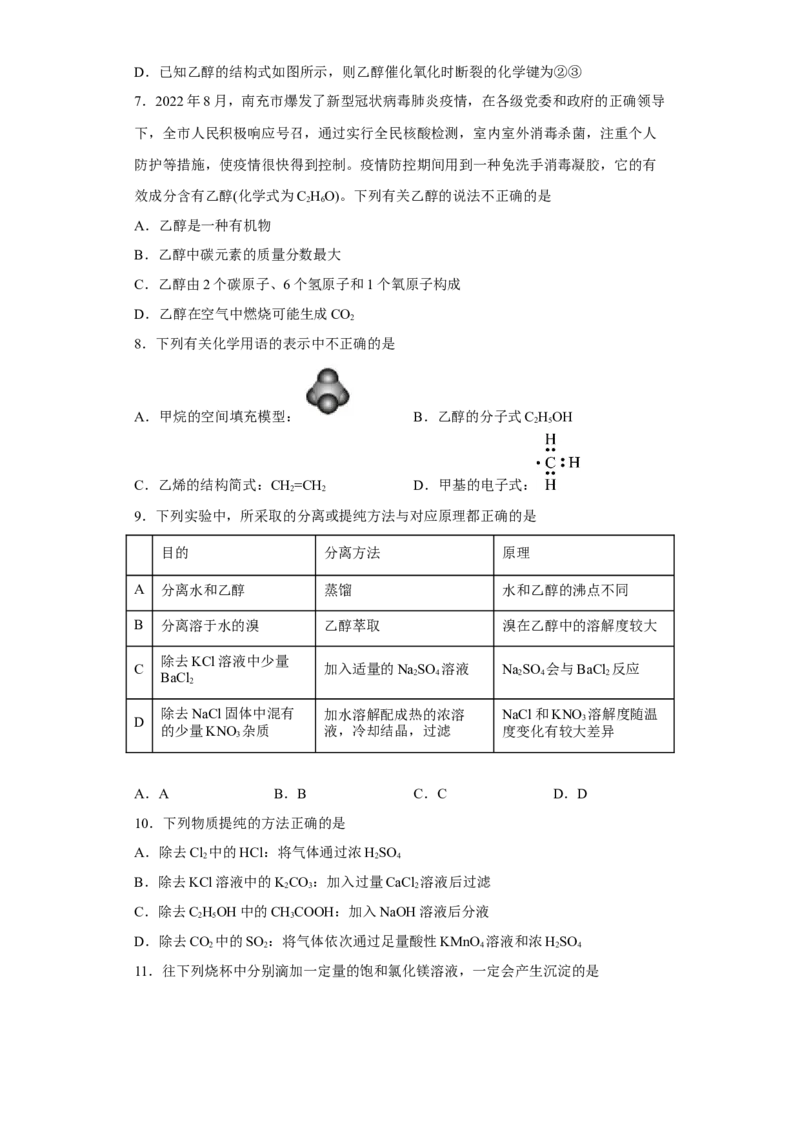
2.聚维酮碘的水溶液是一种常见的碘伏类缓释消毒剂,聚维酮通过氢键与HI 形成聚
3
维酮碘,其结构表示如图(图中虚线表示氢键)下列说法不正确的是
A.聚维酮的单体是
B.聚维酮分子由(2m+n)个单体聚合而成
C.聚维酮碘是一种水溶性物质
D.聚维酮的单体能发生水解反应,也能发生加聚、消去、加成、取代反应
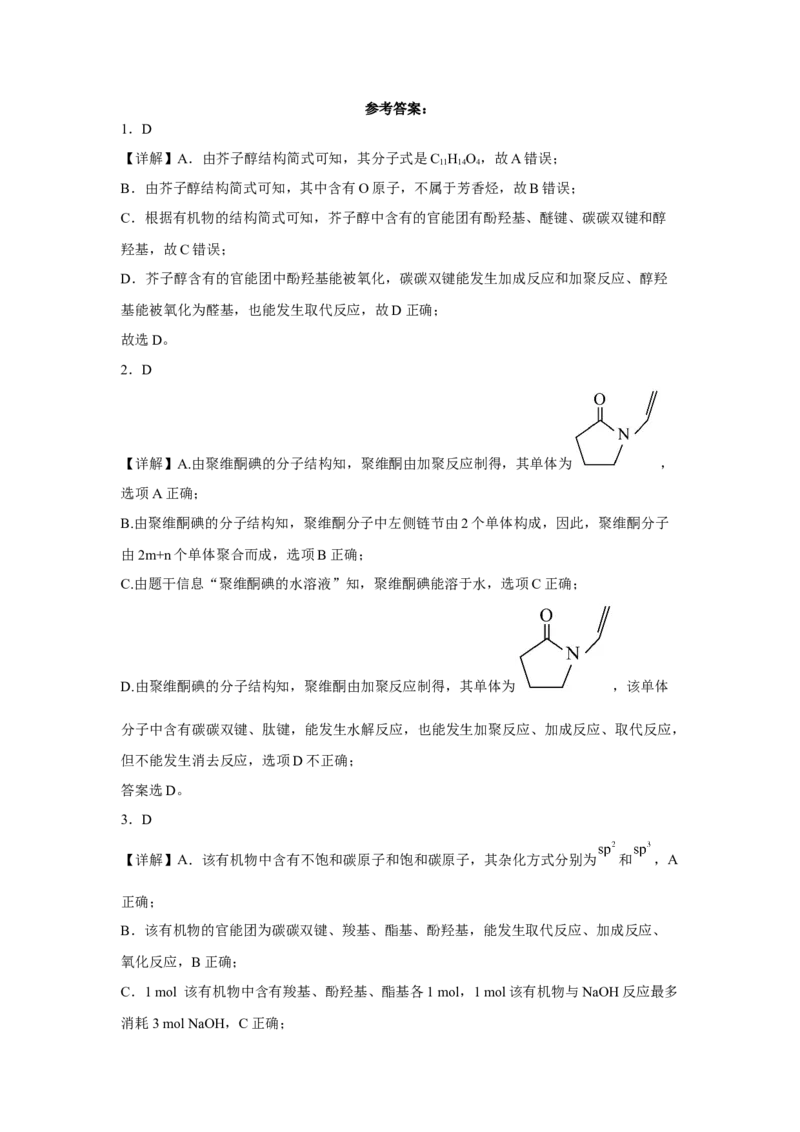
3.我国中草药文化源远流长,通过临床试验,从某中草药中提取的有机物具有较好的
治疗癌症的作用,该有机物的结构如图所示。下列说法中错误的是A.该有机物中碳原子的杂化方式为 和
B.该有机物能发生取代反应、加成反应、氧化反应
C.1 mol 该有机物与NaOH反应最多消耗3 molNaOH
D.1 mol 该有机物与溴水反应最多消耗2 mol
4.下列实验,预测的实验现象正确的是
选
实验内容 预测的实验现象
项
检验氯化铵溶液中含有
A 滴加NaOH溶液,试管口湿润的蓝色石蕊试纸变红
NH
检验铁锈中是否含有二 将铁锈溶于稀盐酸,滴入KSCN溶液,溶液变为血
B
价铁 红色
向NaSO 溶液中加入BaCl 和稀盐酸,观察是否产
C 检验NaSO 是否变质 2 3 2
2 3 生白色沉淀
D 检验乙醇中是否含有水 向乙醇中加入一小粒金属钠,产生无色气体
A.A B.B C.C D.D
5.下列有关化学用语表示不正确的是
A.中子数为20的氯原子: B.乙醇的结构简式:C HOH
2 5
C.NaClO的电子式: D.CO 的比例模型:
2
6.下列说法正确的是
A.羟基与氢氧根有相同的化学式
B.1mol-OH中含有9mol电子
C.常温下,1mol乙醇可与足量的Na反应生成11.2LH
2
试卷第2页,共3页D.已知乙醇的结构式如图所示,则乙醇催化氧化时断裂的化学键为②③
7.2022年8月,南充市爆发了新型冠状病毒肺炎疫情,在各级党委和政府的正确领导
下,全市人民积极响应号召,通过实行全民核酸检测,室内室外消毒杀菌,注重个人
防护等措施,使疫情很快得到控制。疫情防控期间用到一种免洗手消毒凝胶,它的有
效成分含有乙醇(化学式为C HO)。下列有关乙醇的说法不正确的是
2 6
A.乙醇是一种有机物
B.乙醇中碳元素的质量分数最大
C.乙醇由2个碳原子、6个氢原子和1个氧原子构成
D.乙醇在空气中燃烧可能生成CO
2
8.下列有关化学用语的表示中不正确的是
A.甲烷的空间填充模型: B.乙醇的分子式C HOH
2 5
C.乙烯的结构简式:CH=CH D.甲基的电子式:
2 2
9.下列实验中,所采取的分离或提纯方法与对应原理都正确的是
目的 分离方法 原理
A 分离水和乙醇 蒸馏 水和乙醇的沸点不同
B 分离溶于水的溴 乙醇萃取 溴在乙醇中的溶解度较大
除去KCl溶液中少量
C 加入适量的NaSO 溶液 NaSO 会与BaCl 反应
BaCl 2 4 2 4 2
2
除去NaCl固体中混有 加水溶解配成热的浓溶 NaCl和KNO 溶解度随温
D 3
的少量KNO 杂质 液,冷却结晶,过滤 度变化有较大差异
3
A.A B.B C.C D.D
10.下列物质提纯的方法正确的是
A.除去Cl 中的HCl:将气体通过浓HSO
2 2 4
B.除去KCl溶液中的KCO:加入过量CaCl 溶液后过滤
2 3 2
C.除去C HOH中的CHCOOH:加入NaOH溶液后分液
2 5 3
D.除去CO 中的SO :将气体依次通过足量酸性KMnO 溶液和浓HSO
2 2 4 2 4
11.往下列烧杯中分别滴加一定量的饱和氯化镁溶液,一定会产生沉淀的是化学试
剂
选项 A B C D
A.A B.B C.C D.D
12.下列说法正确的是
A.乙醇与金属钠能反应,且在相同条件下比水与金属钠的反应更剧烈
B.苯都能与 发生加成反应,说明苯的分子中含碳碳双键
C.新戊烷有一种一氯取代物
D.金属钠在加热条件下生成氧化钠
13.有关乙醇 说法正确的是
A.与钠反应产生H,说明乙醇属于酸
2
B.分子中含有-OH,所以乙醇是碱
C.发生酯化反应,断裂②键
D.发生氧化反应生成乙醛,断裂①、③键
14.下列有机反应中,有一种反应类型与其他三种反应类型不同的是
A.
B.
C.
D.
二、多选题
15.下列说法正确的是
试卷第4页,共3页A.金属钠分别与乙醇、水反应时,钠均浮在液面上
B.除去乙醇中的少量水可加生石灰,然后蒸馏
C.乙醇与金属钠反应时,乙醇分子中的C—H键断裂
D.在催化剂存在和加热条件下,乙醇可被氧化为乙醛
三、填空题
16.生活中的有机物种类丰富,在衣食住行等多方面应用广泛,其中乙醇是比较常见
的有机物。
(1)乙醇是无色有特殊香味的液体,密度比水的___________。
(2)工业上用乙烯与水反应可制得乙醇,该反应的反应类型是___________。
(3)下列属于乙醇的同系物的是___________,属于乙醇的同分异构体的是
___________(填编号)。
A. B. C.乙醚(CHCHOCH CH) D.甲
3 2 2 3
醇 E.CH-O-CH F.HO-CHCH-OH
3 3 2 2
(4)乙醇能够发生氧化反应:
①46 g乙醇完全燃烧消耗___________mol氧气。
②乙醇在铜作催化剂的条件下可被氧气氧化为乙醛,反应的化学方程式为___________。
17.甲烷、乙醇均为重要的化工原料和燃料。请回答下列问题:
(1)甲烷在催化剂作用下可被氧化为甲醇(CHOH),其化学方程式为: 2CH + O
3 4 2
___________
(2)光照条件下,甲烷与足量的氯气反应可得到CCl ,其反应类型为_______。
4
(3)乙醇在氧气不足的环境中燃烧,其产物除CO、HO和C外还可能有_____。
2 2
18.合成乙酸乙酯的路线如图:
CH=CH C HOH CHCHO
2 2 2 5 3
CHCOOH CHCOOCH CH,请回答下列问题:
3 3 2 3
(1)乙烯能发生聚合反应,其产物的结构简式为_______。
(2)写出下列反应②的化学方程式:_______。
(3)写出下列反应④的化学方程式:_______。
(4)反应④的实验装置如图所示,试管B中在反应前加入的是_______。(5)交警常使用酒精检测仪来检验机动车司机是否酒驾,其原理是:司机口中呼出的乙
醇可以使检测仪中的橙色重铬酸钾(K Cr O)转变为绿色的硫酸铬[Cr(SO )],上述反应
2 2 2 4 3
涉及的乙醇性质有_______。
A.无色液体 B.密度比水的小 C.易挥发 D.具有还原性
19.已知A的产量通常用来衡量一个国家的石油化工水平,现以A为主要原料合成一
种具有果香味的物质E,其合成路线如图所示。
请回答下列问题:
(1)写出A的结构简式____。
(2)B、D分子中的官能团名称分别是____、____。
(3)写出下列反应的化学方程式,并注明反应类型:①____,____。
20.辛烷值是车用汽油最重要的指标,辛烷值越高,其防爆震的能力越强。已知不同
烃的辛烷值:芳香烃(含苯环的烃)>异构烷烃(支链烷烃)>正构烷烃(直链烷烃)
(1)汽油的主要成分为C ~C 的烷烃混合物,如 、CH-CH-
5 11 3 2
CH-CH-CH-CH-CH-CH 等。
2 2 2 2 2 3
①两者的分子式均为 _______。
②比较辛烷值:前者 _______(填“>”“<”或“=”)后者。
(2)向汽油中添加高辛烷值物质是提高汽油辛烷值的途径之一,甲基叔丁基醚(MTBE)是
一种常用的添加剂,可通过下面反应制得:
①CHOH中所含官能团的名称为 _______。
3
试卷第6页,共3页②该反应类型为 _______。
(3)乙醇是另一种高辛烷值添加剂。使用添加乙醇的汽油,可降低汽车尾气排放、改善
能源结构。乙醇在燃烧过程中会产生乙酸,对汽车金属有腐蚀作用,所以乙醇汽油需
要添加金属腐蚀抑制剂。乙醇产生乙酸的化学方程式是 _______。
(4)增加高辛烷值组分的比例是提高汽油辛烷值的另一种途径。中科院设计了一种新型
多功能复合催化剂,实现了CO 直接加氢制取高辛烷值汽油,其过程如图。
2
①过程Ⅰ除了CO,还生成了 _______。
②写出物质a的所有同分异构体的结构简式 _______。
③中间产物(CH) 为烯烃,可以用 _______(填试剂)鉴别a和(CH)。
2 n 2 n
④该方法生产的汽油辛烷值较高的原因是 _______。
四、实验题
21. 用途广泛,某兴趣小组探究其性质。
(1)装置B的名称是_______,该装置内制取 的化学方程式为_______。
(2)欲用以上装置验证 的氧化性、还原性和漂白性,F中应盛放的试剂是_______。
A.碘水 B.石蕊溶液 C. 溶液 D.饱和NaCl溶液
(3)NaOH溶液的作用是_______。
(4)该小组同学对品红溶液褪色的原因进一步探究。
提出猜想:导致品红溶液褪色的原因是 、 、 、 中的一种或几种粒
子与品红发生了反应。
实验设计及测定数据:
编
操作 品红褪色需要的时间
号
1 向品红的乙醇溶液中通入 30min仍未褪色
向5mL饱和 溶液( 约为 )中加入 2min开始褪色,4min完
2
2mL品红溶液 全褪色
3
向 的 溶液中加入2mL品红溶
约2min完全褪色
液
4 ①
相同条件下, 与品红反应的速率比 快得多,则①的操作为_______。
实验结论:通过以上实验,证明了品红溶液褪色_______ 直接所致(填“是”、“不
是”),亚硫酸电离产生的 、 能使品红溶液褪色。
(5)国家规定葡萄酒中 的最大含量为 。该兴趣小组测某白葡萄酒中 含量:
测得100mL白葡萄酒,与 碘水恰好反应,则该葡萄酒中 的含量为
_______g/L(已知 )。若用酸性 溶液测定,测量结
果会明显偏大,原因是 溶液除了与 反应,还会与葡萄酒中的_______发生
反应。
22.如图,在左试管中先加入2 mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再
加入2mL乙酸,充分摇匀。在右试管中加入5 mL A.按图连接好装置,用酒精灯对左
试管小火加热3~5min后,改用大火加热,当观察到右试管中有明显现象时停止实验。
试卷第8页,共3页(1)实验生成的乙酸乙酯___________(填“属于”或“不属于”)烃类;写出酯化反应的
化学方程式:___________。
(2)官能团决定有机物的性质。乙酸中含有的官能团名称是___________。
(3)乙醇能使酸性高锰酸钾溶液褪色,说明乙醇具有___________性。
(4)A为___________;分离右试管中所得乙酸乙酯和A所需主要仪器为___________。参考答案:
1.D
【详解】A.由芥子醇结构简式可知,其分子式是C H O,故A错误;
11 14 4
B.由芥子醇结构简式可知,其中含有O原子,不属于芳香烃,故B错误;
C.根据有机物的结构简式可知,芥子醇中含有的官能团有酚羟基、醚键、碳碳双键和醇
羟基,故C错误;
D.芥子醇含有的官能团中酚羟基能被氧化,碳碳双键能发生加成反应和加聚反应、醇羟
基能被氧化为醛基,也能发生取代反应,故D正确;
故选D。
2.D
【详解】A.由聚维酮碘的分子结构知,聚维酮由加聚反应制得,其单体为 ,
选项A正确;
B.由聚维酮碘的分子结构知,聚维酮分子中左侧链节由2个单体构成,因此,聚维酮分子
由2m+n个单体聚合而成,选项B正确;
C.由题干信息“聚维酮碘的水溶液”知,聚维酮碘能溶于水,选项C正确;
D.由聚维酮碘的分子结构知,聚维酮由加聚反应制得,其单体为 ,该单体
分子中含有碳碳双键、肽键,能发生水解反应,也能发生加聚反应、加成反应、取代反应,
但不能发生消去反应,选项D不正确;
答案选D。
3.D
【详解】A.该有机物中含有不饱和碳原子和饱和碳原子,其杂化方式分别为 和 ,A
正确;
B.该有机物的官能团为碳碳双键、羧基、酯基、酚羟基,能发生取代反应、加成反应、
氧化反应,B正确;
C.1 mol 该有机物中含有羧基、酚羟基、酯基各1 mol,1 mol该有机物与NaOH反应最多
消耗3 mol NaOH,C正确;D.1 mol 该有机物的酚羟基的邻对位氢原子与溴水发生取代反应消耗2 mol ,一个碳
碳双键与溴水加成消耗1 mol ,最多消耗3 mol ,D错误;
故选D。
4.C
【详解】A.检验氯化铵溶液中含有NH ,滴加NaOH溶液并加热,试管口湿润的红色石
蕊试纸变蓝,说明含有NH ,故A错误;
B.将铁锈溶于稀盐酸,滴入KSCN溶液,溶液变为血红色,说明含有Fe3+,不能判断是否
含有二价铁,故B错误;
C.向NaSO 溶液中加入BaCl 和稀盐酸,若产生白色沉淀,沉淀是硫酸钡,说明溶液中
2 3 2
含有 ,说明NaSO 已变质,故C正确;
2 3
D.乙醇、水电暖与钠反应放出氢气,向乙醇中加入一小粒金属钠,产生无色气体,不能
证明乙醇中含有水,故D错误;
选C。
5.D
【详解】A.中子数为20的氯原子质量数为20+17=37,符号为 ,A正确;
B.乙醇由乙基和羟基构成,结构简式为C HOH,B正确;
2 5
C.NaClO由钠离子和次氯酸根构成,电子式为 ,C正确;
D.中心为C原子,C原子的半径应大于O原子半径,D错误;
综上所述答案为D。
6.B
【详解】A.羟基的化学式是-OH,电子式是 ,氢氧根的化学式是OH-,电子式是
,故A错误;
B.1mol-OH中含有9mol电子,故B正确;
答案第2页,共2页C.1mol乙醇与足量的Na反应生成0.5molH,常温下气体摩尔体积不是22.4L/mol,体积
2
不是11.2L,故C错误;
D.乙醇催化氧化生成乙醛,断裂化学键为:①③,故D错误;
故选:B。
7.C
【详解】A.乙醇(化学式为(C HO)是一种含碳元素的化合物,属于有机物,A正确;
2 6
B.乙醇中碳、氢、氧元素的质量比为12:3:8,乙醇中碳元素的质量分数最大,B正确;
C.乙醇是由乙醇分子构成的,1个乙醇分子由2个碳原子、6个氢原子和1个氧原子构成,
C错误;
D.乙醇中含有碳元素,由质量守恒定律可知,乙醇在空气中燃烧可能生成CO,D正确;
2
故本题选C。
8.B
【详解】A.甲烷分子为正四面体结构,其空间填充模型为: ,A正确;
B.乙醇的结构简式为C HOH,分子式为C HO,B错误;
2 5 2 6
C.乙烯中所含官能团的名称为碳碳双键,所以其结构简式为:CH=CH ,C正确;
2 2
D.甲基的结构简式为-CH,其电子式为: ,D正确;
3
故选B。
9.A
【详解】A.水和乙醇的沸点不同,分离水和乙醇的混合液,可以采用蒸馏的方法,A正
确;
B.溴和水都能溶于乙醇中,不能用乙醇萃取水中的溴,B错误;
C.向含有少量 的 溶液中加入适量的 溶液,
,产生新的杂质 ,C错误;
D.除去 固体中混有的少量 杂质,加水溶解配成热的浓溶液,冷却结晶,过滤,
用重结晶的方法,是因为 的溶解度受温度的影响很大, 的溶解度几乎不受温度的影响,D错误;
故选A。
10.D
【详解】A.HCl极易溶于水,为减少氯气的溶解损失,应将气体通过饱和食盐水除去Cl
2
中的HCl,故A错误;
B.加入过量CaCl 溶液后过滤,会引入新的杂质CaCl ,故B错误;
2 2
C.CHCOOH与NaOH溶液反应生成醋酸钠溶液,乙醇与水互溶,不会分层,不能分液,
3
故C错误;
D.SO 与酸性KMnO 溶液发生氧化还原反应,从而除去SO ,再通过浓硫酸,干燥CO,
2 4 2 2
故D正确;
故选D。
11.D
【详解】A.饱和食盐水中加入饱和氯化镁溶液,水的质量增大,溶质变得不饱和,没有
沉淀生成,A不符合题意;
B.75%乙醇溶液中加入饱和氯化镁溶液,生成乙醇合氯化镁溶解在水中,没有沉淀生成,
B不符合题意;
C.饱和硫酸钾溶液中加入一定量饱和氯化镁,水的质量增大,溶液变得不饱和,没有沉
淀生成,C不符合题意;
D.饱和苛性钠溶液中加入一定量的饱和氯化镁,发生反应生成Mg(OH) 沉淀,D符合题
2
意;
故选D。
12.C
【详解】A.乙醇与Na反应比水与Na反应更缓和,因乙醇中羟基H不如水中H活泼,故
A错误;
B.苯分子中的碳碳键是介于碳碳单键和碳碳双键之间的特殊的键,故B错误;
C.新戊烷(C(CH))中有1种H原子,其一氯代物有1种,故C正确;
3 4
D.金属钠在加热条件下生成过氧化钠,故D错误;
故选C。
13.D
【详解】A.与钠反应产生H,说明乙醇含有活泼氢原子,并不表示一定显酸性,如钠与
2
水反应也能生成H,A不正确;
2
答案第4页,共2页B.分子中含有-OH,不是OH-,所以乙醇不是碱,B不正确;
C.发生酯化反应时,羧酸脱羟基、醇脱氢,断裂①键,C不正确;
D.乙醇发生催化氧化反应时,生成 ,脱掉羟基上的1个H原子和羟基所连
碳原子上的1个H原子,即断裂①、③键,D正确;
故选D。
14.D
【详解】A中三氯甲烷和氯气光照下发生取代反应;B中钠和乙醇发生取代反应;C中甲
烷和氯气光照下发生取代反应;D中乙醇和氧气在催化剂加热条件下发生催化氧化反应;
故选D。
15.BD
【详解】A.钠的密度大于乙醇小于水,所以钠与水反应时浮在水面,但与乙醇反应时钠
会沉在乙醇底部,故A错误;
B.CaO与水反应生成氢氧化钙,增大与乙醇的沸点差异,然后通过蒸馏可分离提纯,故B
正确;
C.乙醇与Na反应生成氢气,-OH上O-H键断裂,而C-H键不发生变化,故C错误;
D.乙醇具有还原性,在铜催化并加热条件下,乙醇可被O 氧化为乙醛,故D正确;
2
故选:BD。
16. 小 加成反应 D E 3 2CHCHOH+O
3 2 2
2CHCHO+2H O
3 2
【详解】(1)乙醇的密度比水的密度小。故答案为:小;
(2)乙烯与水发生加成反应生成乙醇,方程式为:CH=CH + H O
2 2 2
CHCHOH。故答案为:加成;
3 2
(3)同系物满足两个条件:结构相似,组成相差n个CH 原子团,故甲醇与乙醇互为同系物;
2
同分异构体满足两个条件:分子式相同,不同的空间结构,故CH—O—CH 与乙醇互为同
3 3
分异构体。故答案为:D;E;
(4)①乙醇燃烧方程式:C HOH + 3O 2CO + 3H O,46g乙醇的物质的量是1 mol,故1
2 5 2 2 2
mol乙醇完全燃烧消耗3 mol O 。
2②乙醇催化氧化生成乙醛和水,方程式为2CHCHOH + O 2CHCHO+2H O。故答
3 2 2 3 2
案为:3;2CHCHOH + O 2CHCHO+2H O。
3 2 2 3 2
17. 2CHOH 取代反应 CO(或一氧化碳)
3
【详解】(1)甲烷(CH)在催化剂作用下可被氧化为甲醇(CHOH),根据元素守恒,
4 3
生成的CHOH系数应为2,即2CH + O 2CHOH;
3 4 2 3
(2)甲烷与氯气反应可生成氯代甲烷和HCl,属于取代反应;
(3)乙醇在氧气不足的环境中燃烧,乙醇中的C燃烧不充分,可能会生成C和CO;
18.(1)
(2)2CH CHOH+O 2CHCHO+2H O
3 2 2 3 2
(3)CH COOH+CH CHOH CHCOOCH CH+H O
3 3 2 3 2 3 2
(4)饱和碳酸钠溶液
(5)CD
【分析】乙烯和水在催化剂条件下反应生成乙醇,乙醇在催化剂条件下氧化生成乙醛,乙
醛和氧气反应生成乙酸,乙酸和乙醇在浓硫酸加热条件下反应生成乙酸乙酯。据此解答。
【详解】(1)乙烯发生聚合反应生成聚乙烯,结构简式为: 。
(2)乙醇的催化氧化方程式为:2CHCHOH+O 2CHCHO+2H O。
3 2 2 3 2
(3)乙醇和乙酸的酯化方程式为:CHCOOH+CH CHOH
3 3 2
CHCOOCH CH+H O。
3 2 3 2
(4)酯化反应的实验中试管B中加入的是饱和碳酸钠溶液。
(5)。乙醇具有挥发性,所以人喝酒后呼出的气体有酒精。酒精检测仪是利用轨道乙醇的
还原性,与氧化性的物质重铬酸钾反应生成绿色的硫酸铬。
19.(1)CH =CH
2 2
(2) 羟基 羧基
答案第6页,共2页(3) CH=CH +H O CHCHOH 加成反应
2 2 2 3 2
【分析】题中合成路线为 ,C HOH
2 5
和CHCOOH发生酯化反应生成CHCOOC H,据此分析。
3 3 2 5
(1)
由分析可知,A为乙烯,其结构简式为CH=CH 。
2 2
(2)
B为乙醇,官能团名称为羟基;D为乙酸,官能团名称为羧基。
(3)
反应为乙烯与水发生加成反应,化学方程式为CH=CH +H O CHCHOH。
2 2 2 3 2
20.(1) C H >
8 18
(2) 羟基 取代反应
(3)CH CHOH+O CHCOOH+H O
3 2 2 3 2
(4) HO CHCHCHCHCH、(CH)C 溴水或酸性高锰酸钾溶液 烯烃的异
2 3 2 2 2 3 3 4
构化和芳香化
【解析】(1)
①二者都属于饱和烷烃,且互为同分异构体,分子中都含有8个C原子、18个H原子,分
子式为C H ,故答案为:C H ;
8 18 8 18
②辛烷值:异构烷烃(支链烷烃)>正构烷烃(直链烷烃),前者含有3个支链、后者不含支链,
则辛烷值:前者>后者,故答案为:>;
(2)
①CHOH中所含官能团的名称为羟基,故答案为:羟基;
3
②甲醇中醇羟基上的H原子被取代生成MTBE,所以该反应属于取代反应,故答案为:取
代反应;
(3)
乙醇被催化氧化生成乙酸和水,反应方程式为CHCHOH+O CHCOOH+H O,故
3 2 2 3 2答案为:CHCHOH+O CHCOOH+H O;
3 2 2 3 2
(4)
①过程I中二氧化碳和氢气反应生成CO和水,则过程I中除了生成CO还生成HO,故答
2
案为:HO;
2
②a的同分异构体还有CHCHCHCHCH、(CH)C,故答案为:CHCHCHCHCH、
3 2 2 2 3 3 4 3 2 2 2 3
(CH)C;
3 4
③(CH) 为烯烃、a为烷烃,烯烃能和溴水发生加成反应而使溴水褪色,能被酸性高锰酸钾
2 n
溶液氧化而使酸性高锰酸钾溶液褪色,烷烃和溴水、高锰酸钾溶液不反应,所以可以用溴
水或酸性高锰酸钾溶液鉴别a和(CH),故答案为:溴水或酸性高锰酸钾溶液;
2 n
④根据图知,烯烃能发生异构化和芳香化,则该方法生产的汽油辛烷值较高的原因是烯烃
的异构化和芳香化,故答案为:烯烃的异构化和芳香化。
21.(1) 圆底烧瓶
(2)C
(3)吸收尾气防止污染环境
(4) 向 的 溶液中加入2mL品红溶液 不是
(5) 0.32 乙醇
【分析】由实验装置图可知,装置A中的浓硫酸与装置B中的铜共热反应制得二氧化硫,
装置C中盛有的品红溶液用于验证二氧化硫的漂白性,装置D中盛有的酸性高锰酸钾溶液
用于验证二氧化硫的还原性,装置F中盛有的硫化钠溶液用于验证二氧化硫的氧化性,装
置G中盛有的氢氧化钠溶液用于吸收未反应的二氧化硫,防止污染空气。
(1)
由实验装置图可知,装置B为圆底烧瓶;圆底烧瓶中发生的反应为铜与浓硫酸共热反应生
成硫酸铜、二氧化硫和水,反应的化学方程式为 ,
答案第8页,共2页故答案为:圆底烧瓶; ;
(2)
由分析可知,装置F中盛有的硫化钠溶液用于验证二氧化硫的氧化性,故选C;
(3)
由分析可知,装置G中盛有的氢氧化钠溶液用于吸收未反应的二氧化硫,防止污染空气,
故答案为:吸收尾气防止污染环境;
(4)
由相同条件下,亚硫酸根离子与品红反应的速率比亚硫酸氢根离子快得多可知,①的操作
为向5ml0.1mol/L的亚硫酸钠溶液中加入2mL品红溶液,观察、记录品红褪色需要的时间;
由品红褪色需要的时间可知,品红溶液褪色不是二氧化硫所致,应是亚硫酸电离产生的亚
硫酸氢根和亚硫酸根所致,故答案为:向 的 溶液中加入2mL品红溶
液;不是;
(5)
由100mL白葡萄酒与50ml0.01mol/L碘水恰好反应可知,100mL白葡萄酒中二氧化硫的质
量为0.01mol/L×0.05L×64g/mol=0.032g,葡萄酒中二氧化硫的含量为0.32g/L;由于白葡萄
酒中的乙醇也能与酸性高锰酸钾溶液发生氧化反应,所以用酸性高锰酸钾溶液测定二氧化
硫含量时,消耗酸性高锰酸钾溶液的体积会偏大,导致测量结果会明显偏大,故答案为:
0.32;乙醇。
22.(1) 不属于 CHCOOH+CH CHOH CHCOOCH CH+H O
3 3 2 3 2 3 2
(2)羧基
(3)还原
(4) 饱和碳酸钠溶液 分液漏斗
【解析】(1)
乙酸乙酯除了C、H元素外,还含有O元素,不属于烃类;乙酸和乙醇在浓硫酸催化作用
下发生酯化反应,生成乙酸乙酯和水,反应的化学方程式为CHCOOH+CH CHOH
3 3 2
CHCOOCH CH+H O;
3 2 3 2(2)
乙酸中含有的官能团是-COOH,名称是羧基;
(3)
酸性高锰酸钾具有强氧化性,乙醇能与酸性高锰酸钾溶液发生氧化还原反应生成乙酸,乙
醇被氧化,说明乙醇具有还原性;
(4)
A为饱和碳酸钠溶液,其作用为吸取乙醇、除去乙酸,降低乙酸乙酯的溶解度,乙酸乙酯
和NaCO 溶液分层,分液法分离,主要仪器为分液漏斗。
2 3
答案第10页,共2页