文档内容
安徽省 2024 年高考适应性联考
高三化学试卷
可能用到的相对原子质量:H 1 Li 7 C 12 O 16 P 31 Cl 35.5 Br 80 Sn 119 Ba 137
一、选择题(本题共14小题,每小题3分,共计42分。在每小题列出的四个选项中,只有一
项是符合题目要求的)
1. 我国著名化学家徐光宪曾指出:“化学是不断发明和制造对人类更有用的新物质的科学。化学科学是现
代科学技术发展的重要基础科学。”下列说法正确的是
A. 5G时代某三维存储器能储存海量数据,其半导体衬底材料是SiO
2
的
B. 铁磁流体液态机器人中驱动机器人运动 磁铁的主要成分是Fe O
2 3
C. 三苯基铋在石墨烯中加热得到铋纳米球胶体,铋纳米球的直径在1nm以下
D. 氨硼烷(BHNH )作为一种储氢材料备受关注,氨硼烷分子中只存在极性共价键
3 3
2. 在473K、12159kPa下处理白磷(结构如图所示)得到斜方黑磷,继续增大压力,斜方黑磷还能转化为菱形
黑磷(每层由曲折的磷原子链组成),设 为阿伏加德罗常数的值。下列说法中错误的是
A. 白磷与黑磷属于磷元素的同素异形体
B. 中含有的中子数为
C. 12.4g白磷与0.6 mol H 在密闭容器中充分反应,生成的PH 分子数为
2 3
D. 0.11mol白磷发生反应: ,转移的电子数为
3. 根据实验操作和现象,得出相应结论正确的是
选
实验操作 现象 结论
项
A 向溴水中加入苯,振荡后静置 水层颜色变浅 溴与苯发生了加成反应
第1页/共11页
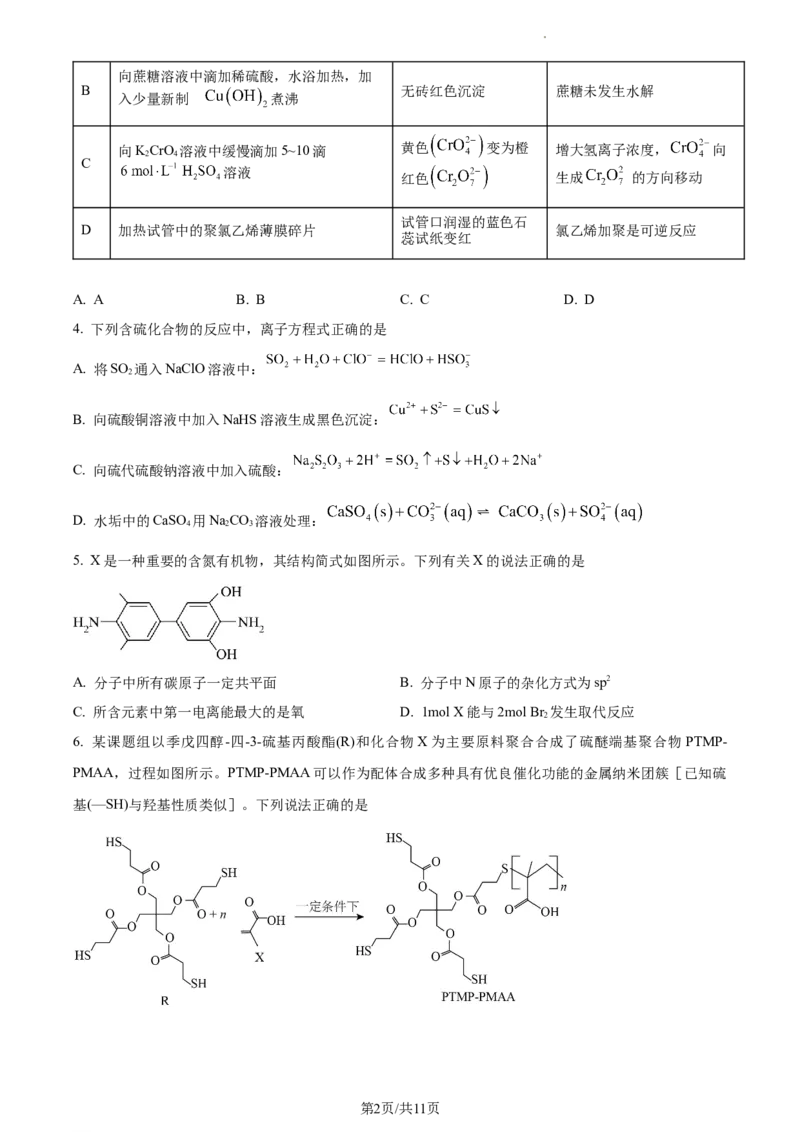
学科网(北京)股份有限公司向蔗糖溶液中滴加稀硫酸,水浴加热,加
B 无砖红色沉淀 蔗糖未发生水解
入少量新制 的煮沸
向KCrO 溶液中缓慢滴加5~10滴 黄色 变为橙 增大氢离子浓度, 向
2 4
C
溶液
红色 生成 的方向移动
试管口润湿的蓝色石
D 加热试管中的聚氯乙烯薄膜碎片 氯乙烯加聚是可逆反应
蕊试纸变红
A. A B. B C. C D. D
4. 下列含硫化合物的反应中,离子方程式正确的是
A. 将SO 通入NaClO溶液中:
2
B. 向硫酸铜溶液中加入NaHS溶液生成黑色沉淀:
C. 向硫代硫酸钠溶液中加入硫酸:
D. 水垢中的CaSO 用NaCO 溶液处理:
4 2 3
5. X是一种重要的含氮有机物,其结构简式如图所示。下列有关X的说法正确的是
A. 分子中所有碳原子一定共平面 B. 分子中N原子的杂化方式为sp2
C. 所含元素中第一电离能最大的是氧 D. 1mol X能与2mol Br 发生取代反应
2
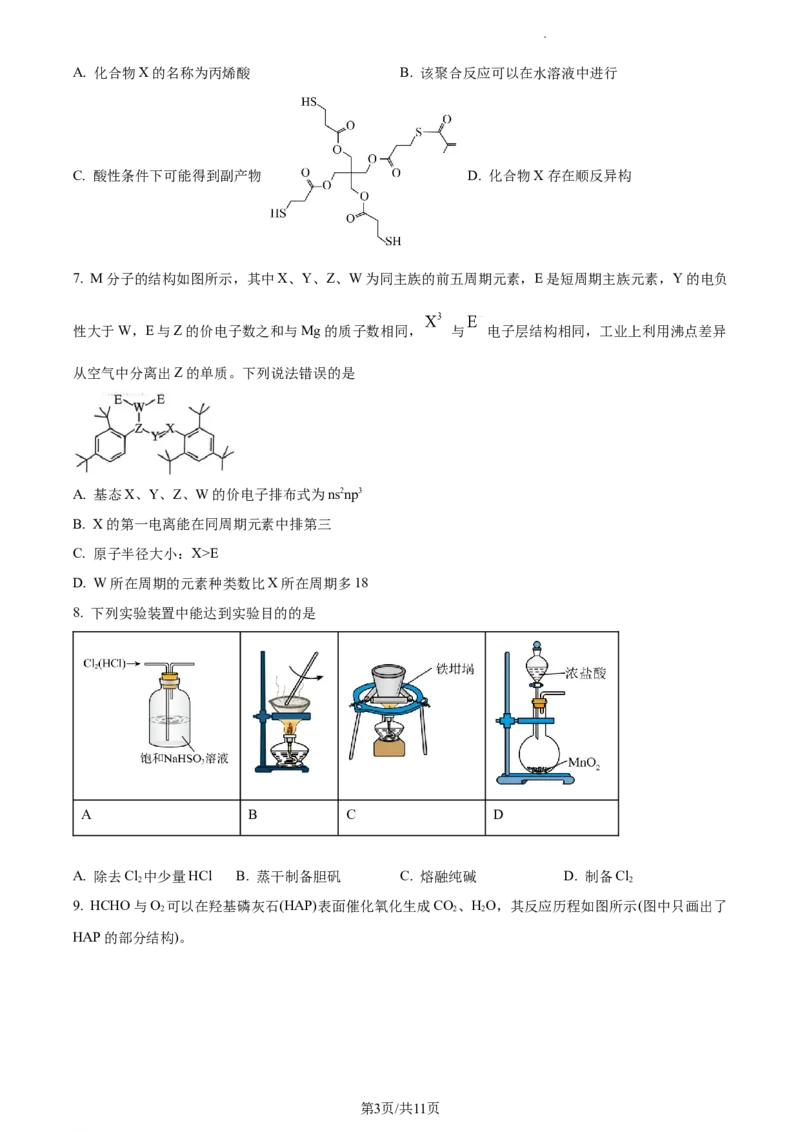
6. 某课题组以季戊四醇-四-3-硫基丙酸酯(R)和化合物X为主要原料聚合合成了硫醚端基聚合物PTMP-
PMAA,过程如图所示。PTMP-PMAA可以作为配体合成多种具有优良催化功能的金属纳米团簇[已知硫
基(—SH)与羟基性质类似]。下列说法正确的是
第2页/共11页
学科网(北京)股份有限公司A. 化合物X的名称为丙烯酸 B. 该聚合反应可以在水溶液中进行
C. 酸性条件下可能得到副产物 D. 化合物X存在顺反异构
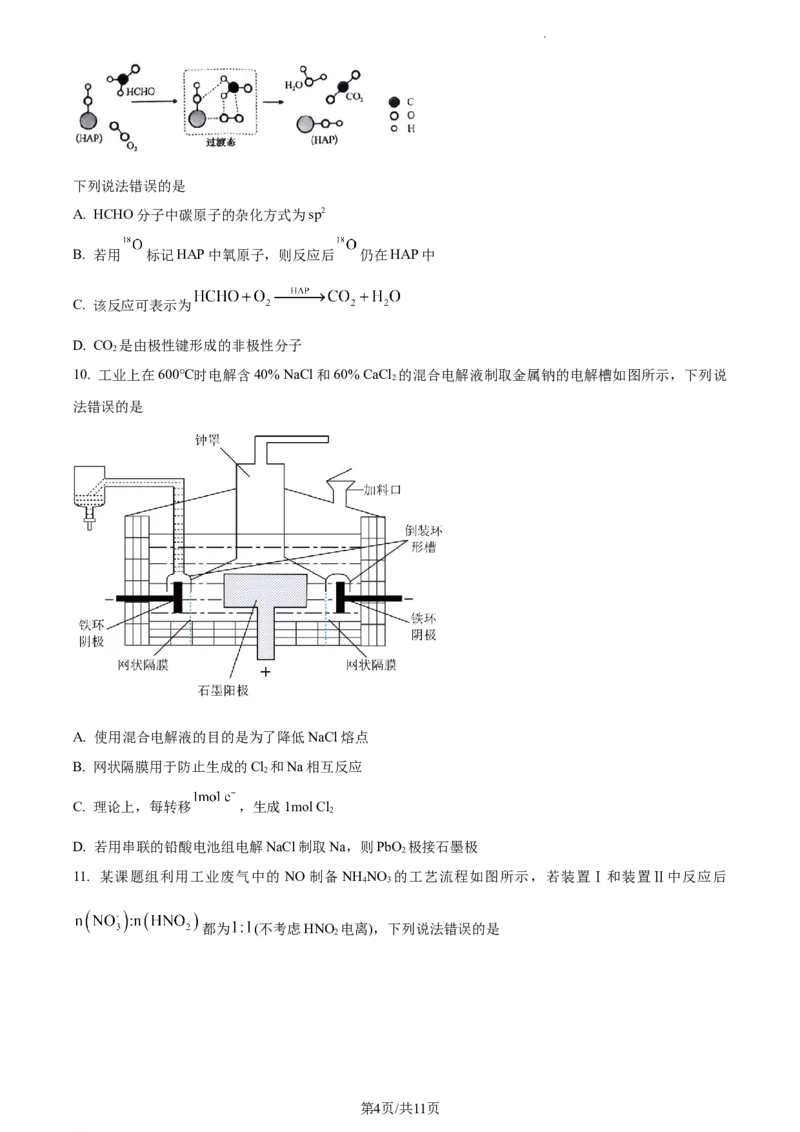
7. M分子的结构如图所示,其中X、Y、Z、W为同主族的前五周期元素,E是短周期主族元素,Y的电负
性大于W,E与Z的价电子数之和与Mg的质子数相同, 与 电子层结构相同,工业上利用沸点差异
从空气中分离出Z的单质。下列说法错误的是
A. 基态X、Y、Z、W的价电子排布式为ns2np3
B. X的第一电离能在同周期元素中排第三
C. 原子半径大小:X>E
D. W所在周期的元素种类数比X所在周期多18
8. 下列实验装置中能达到实验目的的是
A B C D
A. 除去Cl 中少量HCl B. 蒸干制备胆矾 C. 熔融纯碱 D. 制备Cl
2 2
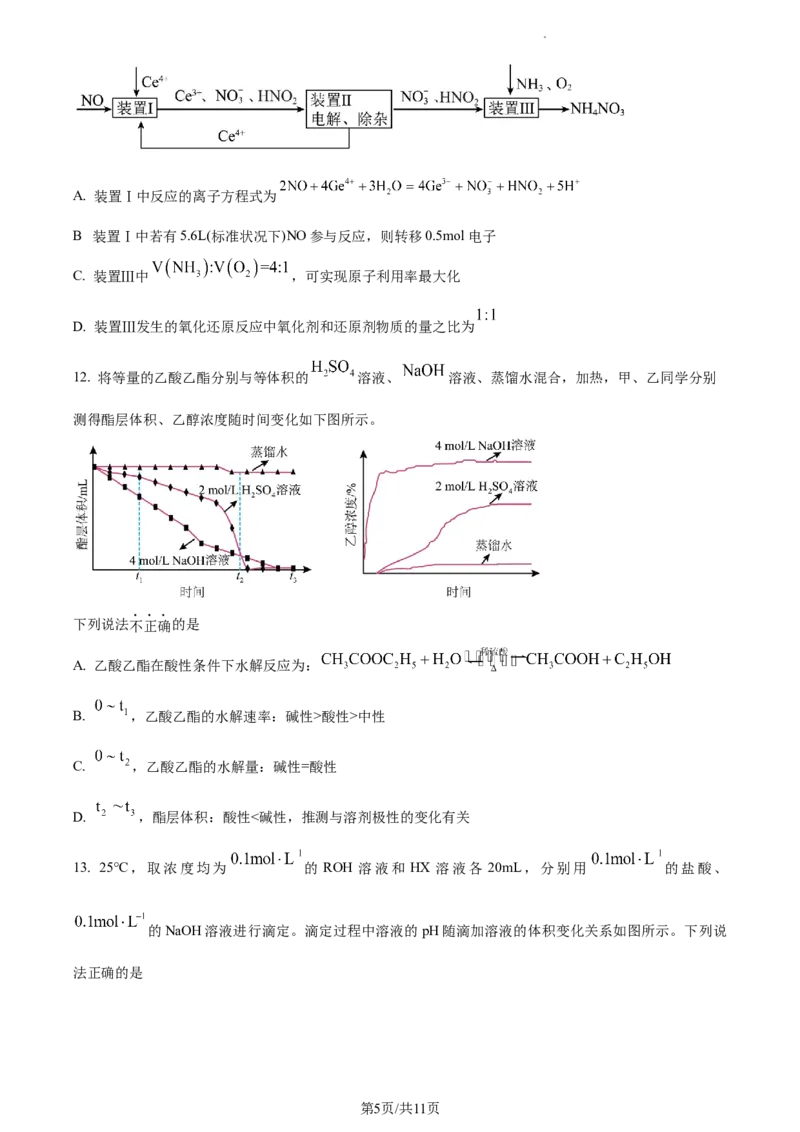
9. HCHO与O 可以在羟基磷灰石(HAP)表面催化氧化生成CO 、HO,其反应历程如图所示(图中只画出了
2 2 2
HAP的部分结构)。
第3页/共11页
学科网(北京)股份有限公司下列说法错误的是
A. HCHO分子中碳原子的杂化方式为sp2
B. 若用 标记HAP中氧原子,则反应后 仍在HAP中
C. 该反应可表示为
D. CO 是由极性键形成的非极性分子
2
10. 工业上在600℃时电解含40% NaCl和60% CaCl 的混合电解液制取金属钠的电解槽如图所示,下列说
2
法错误的是
A. 使用混合电解液的目的是为了降低NaCl熔点
B. 网状隔膜用于防止生成的Cl 和Na相互反应
2
C. 理论上,每转移 ,生成1mol Cl
2
D. 若用串联的铅酸电池组电解NaCl制取Na,则PbO 极接石墨极
2
11. 某课题组利用工业废气中的 NO制备NH NO 的工艺流程如图所示,若装置Ⅰ和装置Ⅱ中反应后
4 3
都为 (不考虑HNO 电离),下列说法错误的是
2
第4页/共11页
学科网(北京)股份有限公司A. 装置Ⅰ中反应的离子方程式为
.
B 装置Ⅰ中若有5.6L(标准状况下)NO参与反应,则转移0.5mol电子
C. 装置Ⅲ中 ,可实现原子利用率最大化
D. 装置Ⅲ发生的氧化还原反应中氧化剂和还原剂物质的量之比为
12. 将等量的乙酸乙酯分别与等体积的 溶液、 溶液、蒸馏水混合,加热,甲、乙同学分别
测得酯层体积、乙醇浓度随时间变化如下图所示。
下列说法不正确的是
A. 乙酸乙酯在酸性条件下水解反应为:
B. ,乙酸乙酯的水解速率:碱性>酸性>中性
C. ,乙酸乙酯的水解量:碱性=酸性
D. ,酯层体积:酸性<碱性,推测与溶剂极性的变化有关
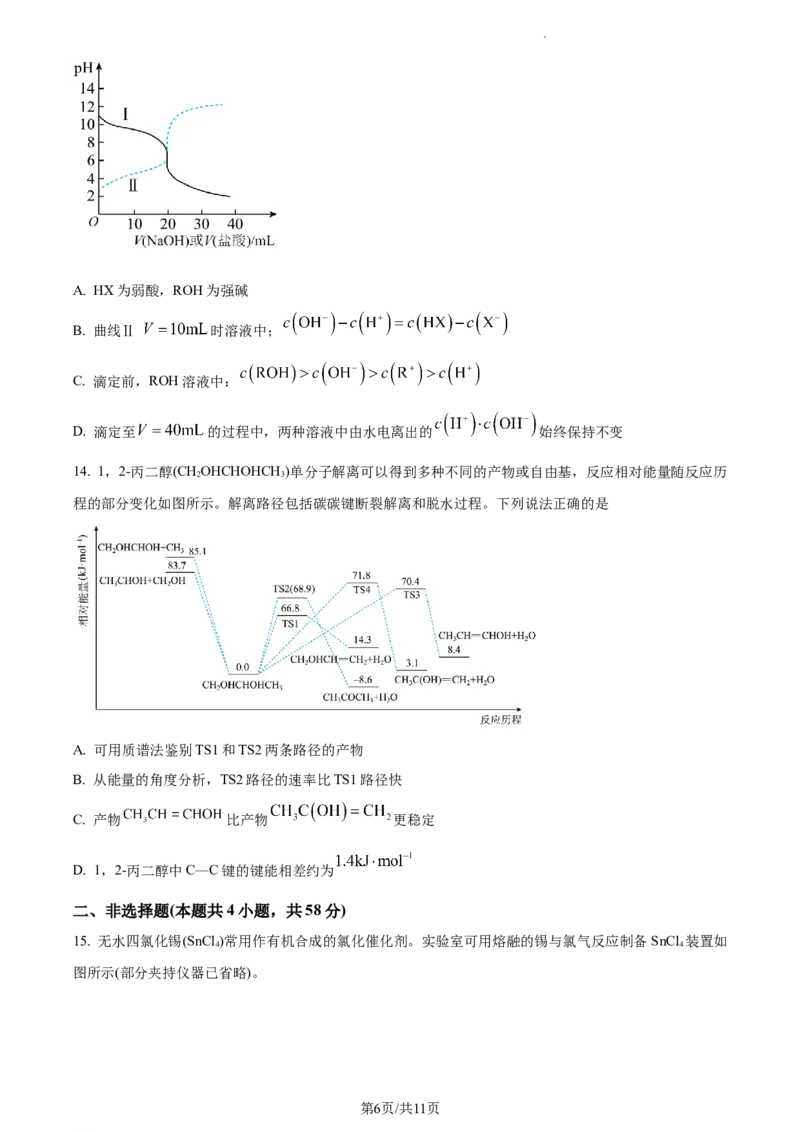
13. 25℃,取浓度均为 的 ROH 溶液和 HX 溶液各 20mL,分别用 的盐酸、
的NaOH溶液进行滴定。滴定过程中溶液的pH随滴加溶液的体积变化关系如图所示。下列说
法正确的是
第5页/共11页
学科网(北京)股份有限公司A. HX为弱酸,ROH为强碱
B. 曲线Ⅱ 时溶液中;
C. 滴定前,ROH溶液中:
D. 滴定至 的过程中,两种溶液中由水电离出的 始终保持不变
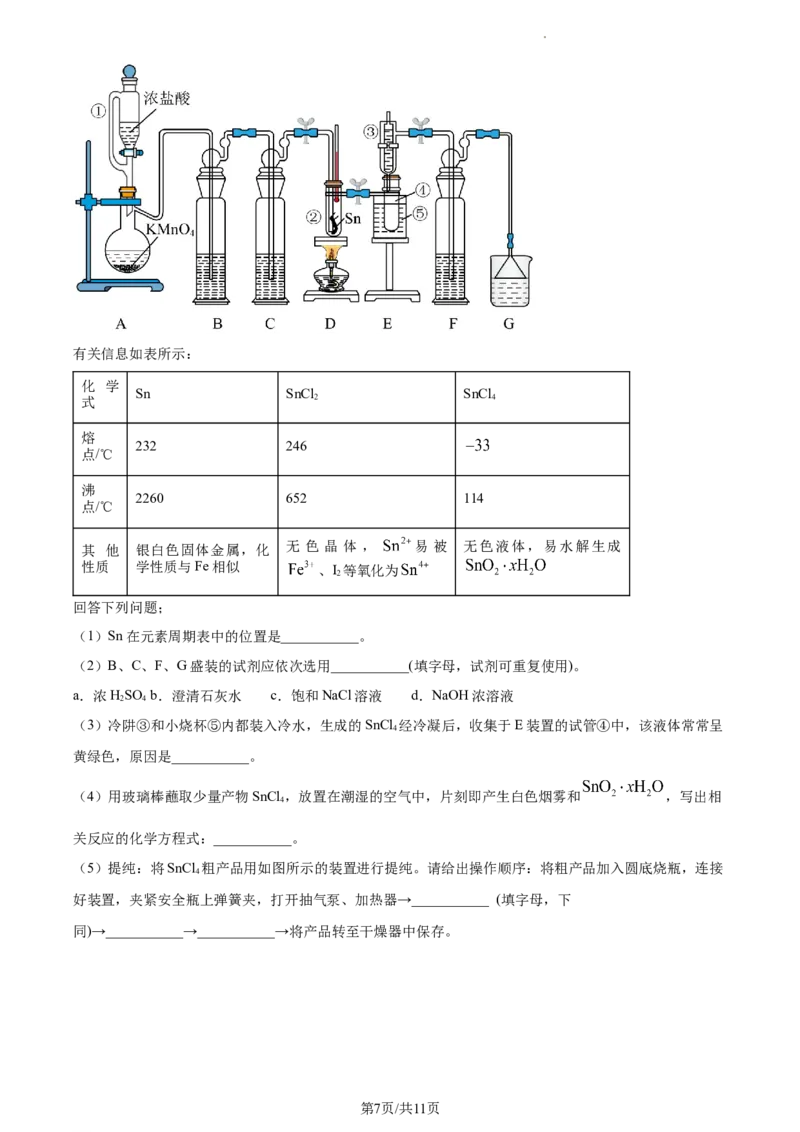
14. 1,2-丙二醇(CHOHCHOHCH )单分子解离可以得到多种不同的产物或自由基,反应相对能量随反应历
2 3
程的部分变化如图所示。解离路径包括碳碳键断裂解离和脱水过程。下列说法正确的是
A. 可用质谱法鉴别TS1和TS2两条路径的产物
B. 从能量的角度分析,TS2路径的速率比TS1路径快
C. 产物 比产物 更稳定
D. 1,2-丙二醇中C—C键的键能相差约为
二、非选择题(本题共4小题,共58分)
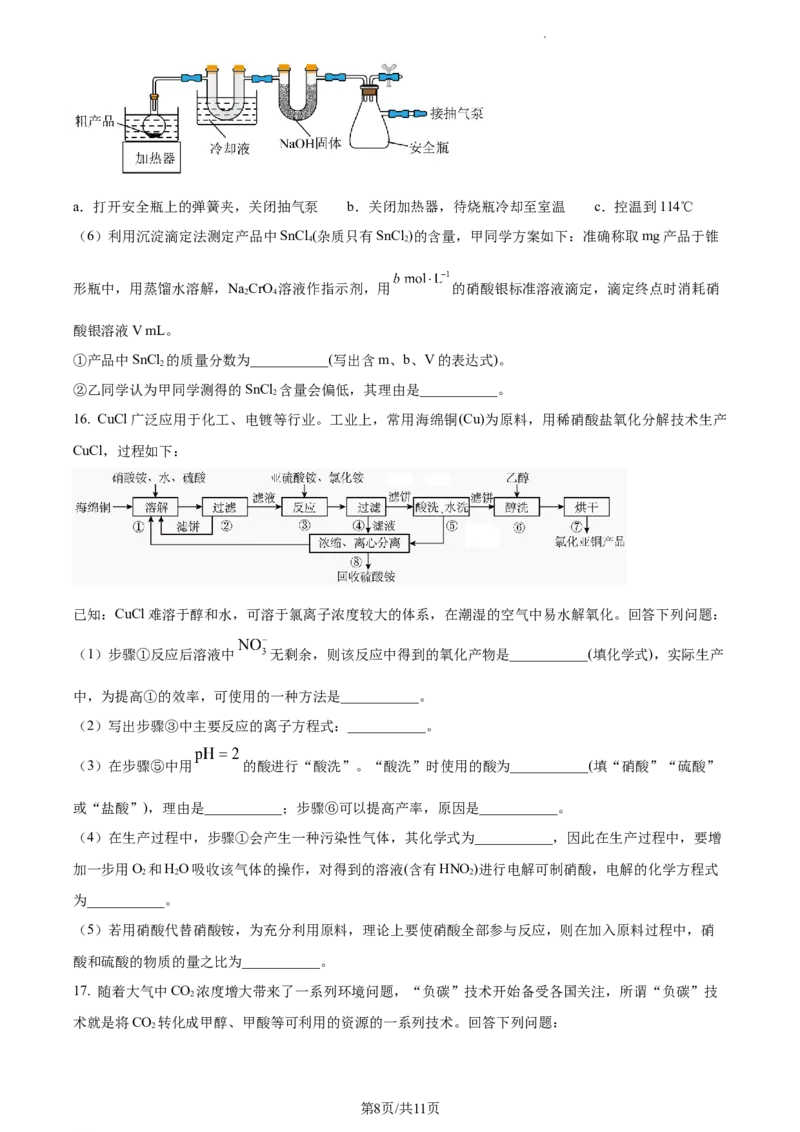
15. 无水四氯化锡(SnCl )常用作有机合成的氯化催化剂。实验室可用熔融的锡与氯气反应制备SnCl 装置如
4 4
图所示(部分夹持仪器已省略)。
第6页/共11页
学科网(北京)股份有限公司有关信息如表所示:
化 学
Sn SnCl SnCl
式 2 4
熔
232 246
点/℃
沸
2260 652 114
点/℃
其 他 银白色固体金属,化 无 色 晶 体 , 易 被 无色液体,易水解生成
性质 学性质与Fe相似 、I 等氧化为
2
回答下列问题;
(1)Sn在元素周期表中的位置是___________。
(2)B、C、F、G盛装的试剂应依次选用___________(填字母,试剂可重复使用)。
a.浓HSO b.澄清石灰水 c.饱和NaCl溶液 d.NaOH浓溶液
2 4
(3)冷阱③和小烧杯⑤内都装入冷水,生成的SnCl 经冷凝后,收集于E装置的试管④中,该液体常常呈
4
黄绿色,原因是___________。
(4)用玻璃棒蘸取少量产物SnCl ,放置在潮湿的空气中,片刻即产生白色烟雾和 ,写出相
4
关反应的化学方程式:___________。
(5)提纯:将SnCl 粗产品用如图所示的装置进行提纯。请给出操作顺序:将粗产品加入圆底烧瓶,连接
4
好装置,夹紧安全瓶上弹簧夹,打开抽气泵、加热器→___________ (填字母,下
同)→___________→___________→将产品转至干燥器中保存。
第7页/共11页
学科网(北京)股份有限公司a.打开安全瓶上的弹簧夹,关闭抽气泵 b.关闭加热器,待烧瓶冷却至室温 c.控温到114℃
(6)利用沉淀滴定法测定产品中SnCl (杂质只有SnCl )的含量,甲同学方案如下:准确称取mg产品于锥
4 2
形瓶中,用蒸馏水溶解,NaCrO 溶液作指示剂,用 的硝酸银标准溶液滴定,滴定终点时消耗硝
2 4
酸银溶液V mL。
①产品中SnCl 的质量分数为___________(写出含m、b、V的表达式)。
2
②乙同学认为甲同学测得的SnCl 含量会偏低,其理由是___________。
2
16. CuCl广泛应用于化工、电镀等行业。工业上,常用海绵铜(Cu)为原料,用稀硝酸盐氧化分解技术生产
CuCl,过程如下:
已知:CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿的空气中易水解氧化。回答下列问题:
(1)步骤①反应后溶液中 无剩余,则该反应中得到的氧化产物是___________(填化学式),实际生产
中,为提高①的效率,可使用的一种方法是___________。
(2)写出步骤③中主要反应的离子方程式:___________。
(3)在步骤⑤中用 的酸进行“酸洗”。“酸洗”时使用的酸为___________(填“硝酸”“硫酸”
或“盐酸”),理由是___________;步骤⑥可以提高产率,原因是___________。
(4)在生产过程中,步骤①会产生一种污染性气体,其化学式为___________,因此在生产过程中,要增
加一步用O 和HO吸收该气体的操作,对得到的溶液(含有HNO)进行电解可制硝酸,电解的化学方程式
2 2 2
为___________。
(5)若用硝酸代替硝酸铵,为充分利用原料,理论上要使硝酸全部参与反应,则在加入原料过程中,硝
酸和硫酸的物质的量之比为___________。
17. 随着大气中CO 浓度增大带来了一系列环境问题,“负碳”技术开始备受各国关注,所谓“负碳”技
2
术就是将CO 转化成甲醇、甲酸等可利用的资源的一系列技术。回答下列问题:
2
第8页/共11页
学科网(北京)股份有限公司Ⅰ.CO 催化加氢制甲醇
2
以CO、H 为原料合成CHOH涉及的反应如下:
2 2 3
反应i: ;
反应ii: ;
反应iii: 。
(1)反应i的 ___________。
(2)一定温度和催化剂条件下,0.73mol H 、0.24mol CO 和0.03 mol N(已知N 不参与反应)在密闭容器中
2 2 2 2
进行上述反应,平衡时CO 的转化率、CHOH和CO的选择性随温度的变化曲线如图所示。
2 3
①图中曲线b表示物质___________(填“CO”“CHOH”或“CO”)的变化。
2 3
②上述反应体系在一定条件下建立平衡后,下列说法错误的有___________(填字母)。
A.降低温度,反应i~iii的正、逆反应速率都减小
B.恒压条件下,向容器中再通入少量N,CO 的平衡转化率下降
2 2
C.移去部分HO(g),反应iii平衡不移动
2
D.选择合适的催化剂能减小反应iii的焓变
③某温度下(大于180℃), 反应到达平衡,测得容器中CHOH的体积分数为12.5%,容器内气体总
3
压强为8.0MPa.此时用CHOH的分压表示 时间内的反应速率 ___________
3
。设此时 ,计算该温度下反应ii的压强平衡常数 ___________(用含有n
的代数式表示,分压=总压×该组分物质的量分数)。
Ⅱ.CO 催化加氢制低碳烯烃(2~4个C的烯烃)
2
某研究小组使用Zn—Ga—O/SAPO—34双功能催化剂实现了CO 直接合成低碳烯烃,并给出了其可能的反
2
第9页/共11页
学科网(北京)股份有限公司应历程(如图所示)。H 首先在Zn—Ga—O表面解离成2个H*,随后参与到CO 的还原过程;SAPO—34则
2 2
催化生成的甲醇转化为低碳烯怪。
注:□表示氧原子空位,*表示吸附在催化剂上的微粒。
(3)理论上,反应历程中消耗的H*与生成的甲醇的物质的量之比为___________。
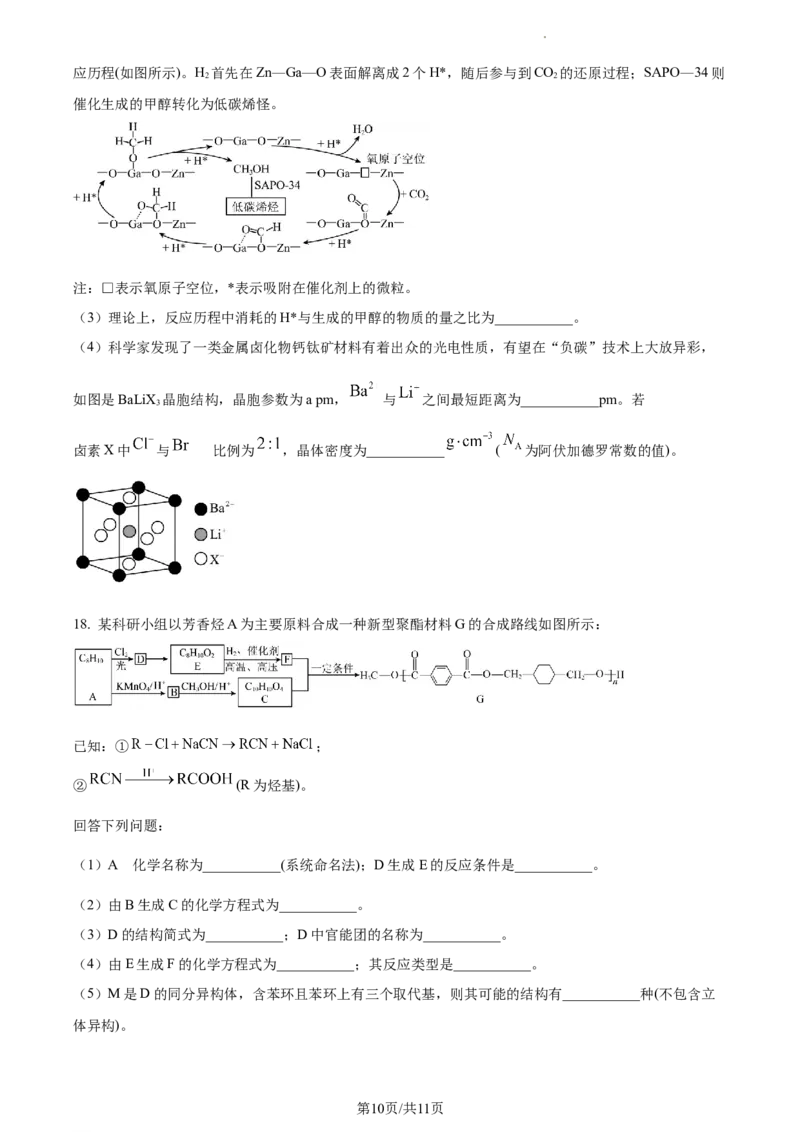
(4)科学家发现了一类金属卤化物钙钛矿材料有着出众的光电性质,有望在“负碳”技术上大放异彩,
如图是BaLiX 晶胞结构,晶胞参数为a pm, 与 之间最短距离为___________pm。若
3
的
卤素X中 与 比例为 ,晶体密度为___________ ( 为阿伏加德罗常数的值)。
18. 某科研小组以芳香烃A为主要原料合成一种新型聚酯材料G的合成路线如图所示:
已知:① ;
② (R为烃基)。
回答下列问题:
的
(1)A 化学名称为___________(系统命名法);D生成E的反应条件是___________。
(2)由B生成C的化学方程式为___________。
(3)D的结构简式为___________;D中官能团的名称为___________。
(4)由E生成F的化学方程式为___________;其反应类型是___________。
(5)M是D的同分异构体,含苯环且苯环上有三个取代基,则其可能的结构有___________种(不包含立
体异构)。
第10页/共11页
学科网(北京)股份有限公司(6)苯乙酸苄酯( )是花香型香料,设计以苯甲醇为起始原料制备苯乙酸苄酯的合成路线:
___________(无机试剂任选)。
第11页/共11页
学科网(北京)股份有限公司